8 травня, 2026
Постменопаузальний остеопороз у сучасних рекомендаціях: від оцінки ризику до персоналізованої терапії
 У межах вебінару «Менеджмент захворювань кісток та суглобів: сучасні стандарти та можливості індивідуального підходу», який відбувся 25 березня на онлайн-платформі OsteoHub, Єлизавета Давидівна Єгудіна, д.мед.н., професорка, керівниця навчального центру Інституту ревматології, лікарка-ревматологиня Клініки сучасної ревматології (м. Київ), представила сучасний погляд на ведення осіб з остеопорозом, зокрема із постменопаузальним. У доповіді були розглянуті питання діагностики, стратифікації ризику переломів та вибору оптимальної фармакотерапії відповідно до рекомендацій. Особливу увагу приділено індивідуалізації лікування з урахуванням категорії ризику та необхідності довготривалого ведення хворих. Окремо висвітлено роль базової підтримки кальцієм і вітаміном D як невід’ємної складової ефективної терапії остеопорозу.
У межах вебінару «Менеджмент захворювань кісток та суглобів: сучасні стандарти та можливості індивідуального підходу», який відбувся 25 березня на онлайн-платформі OsteoHub, Єлизавета Давидівна Єгудіна, д.мед.н., професорка, керівниця навчального центру Інституту ревматології, лікарка-ревматологиня Клініки сучасної ревматології (м. Київ), представила сучасний погляд на ведення осіб з остеопорозом, зокрема із постменопаузальним. У доповіді були розглянуті питання діагностики, стратифікації ризику переломів та вибору оптимальної фармакотерапії відповідно до рекомендацій. Особливу увагу приділено індивідуалізації лікування з урахуванням категорії ризику та необхідності довготривалого ведення хворих. Окремо висвітлено роль базової підтримки кальцієм і вітаміном D як невід’ємної складової ефективної терапії остеопорозу.
Епідеміологія та клінічне значення
Пані Єгудіна зазначила, що постменопаузальний остеопороз є первинним системним метаболічним захворюванням скелета, що розвивається у жінок після настання менопаузи внаслідок дефіциту естрогенів. Цей стан характеризується зниженням мінеральної щільності кісткової тканини (МЩКТ) та порушенням її мікроархітектури, що призводить до суттєвого підвищення ризику переломів. Ключові патофізіологічні зміни включають зниження рівня естрогенів, підвищення активності остеокластів, посилення кісткової резорбції та швидку втрату трабекулярної кісткової тканини, особливо на рівні хребта.
За даними Міжнародного фонду остеопорозу (IOF), остеопороз і пов’язані з ним переломи становлять значне глобальне навантаження. Станом на сьогодні близько 158 млн людей мають високий ризик переломів, і очікується, що до 2040 р. ця цифра зросте до 319 млн. Таким чином, кількість осіб із високим ризиком переломів фактично подвоїться протягом кількох десятиліть. Особливе занепокоєння викликає прогнозоване зростання частоти переломів стегнової кістки. За період із 1990 до 2050 рр. очікується збільшення їх кількості на 240% у жінок і на 310% у чоловіків, що відображає старіння населення та недостатню ефективність профілактичних стратегій на сьогодні.
Важливим клінічним аспектом є те, що ризик повторних переломів суттєво підвищується вже протягом першого року після первинного перелому і залишається суттєвим упродовж наступних років. Зокрема, переломи хребців, незалежно від того, є вони клінічно маніфестними чи ні, асоційовані з п’ятикратним зростанням ризику наступних переломів хребців і 2‑3-разовим збільшенням імовірності переломів в інших локалізаціях (Tang et al., 2024).
Попри це, значна частка пацієнтів залишається поза увагою системи охорони здоров’я: до 80% осіб із малотравматичними переломами не проходять належного обстеження та не отримують лікування, відповідно, профілактика подальших епізодів у них не проводиться. Клінічна значущість проблеми підтверджується також збільшенням імовірності летальних випадків після переломів. Найбільш несприятливі наслідки спостерігаються після переломів стегна та хребців, але підвищений ризик смерті відзначається і при інших типах остеопоротичних переломів (Cayley et al., 2000).
Згідно із сучасними підходами, остеопоротичним вважається перелом, який виникає внаслідок падіння з висоти власного зросту або при дії сили, недостатньої для пошкодження здорової кістки. До основних (великих) остеопоротичних переломів належать переломи шийки стегнової кістки, хребців, плечової кістки та дистального відділу передпліччя. До малих відносять переломи ребер, таза (за відсутності перелому шийки стегна), великогомілкової кістки, а також кісточок гомілково-ступневого суглоба. Водночас переломи кистей, стоп, кісток черепа та лицевого скелета зазвичай не класифікуються як остеопоротичні.
Таким чином, постменопаузальний остеопороз є не лише поширеним, але й клінічно значущим захворюванням із високим ризиком інвалідизації та смертності. Недостатня діагностика та лікування, разом зі зростаючим тягарем переломів, підкреслюють необхідність своєчасної оцінки ризику та впровадження ефективних персоналізованих терапевтичних стратегій.
Діагностика і стратифікація ризику
Діагностика остеопорозу базується насамперед на оцінюванні МЩКТ за допомогою двоенергетичної рентгенівської абсорбціометрії. Згідно з рекомендаціями Американської академії сімейних лікарів (AAFP, 2009) та Національного фонду остеопорозу США (NOF, 2014), денситометричне обстеження слід проводити жінкам віком ≥65 років і чоловікам ≥70 років. Окрім того, воно показане жінкам у постменопаузі віком до 65 років та чоловікам до 70 років за наявності клінічних факторів ризику. Окрему групу становлять пацієнти після 50 років, які вже перенесли переломи будь-якої локалізації, оскільки в них імовірність повторних переломів значно зростає. До ключових факторів ризику належать сімейний анамнез переломів, куріння, низька вага, тривале застосування глюкокортикоїдів (понад три місяці), а також наявність хронічних захворювань, що впливають на кісткову тканину.
Відповідно до критеріїв Всесвітньо організації охорони здоров’я (ВООЗ), для жінок у постменопаузі та чоловіків віком від 50 років перевага надається оцінюванню показника T-score, що дозволяє класифікувати стан кісткової тканини як норму (-1,0 або вище), остеопенію (від -1,0 до -2,5) або остеопороз (-2,5 чи нижче). Тяжкий (маніфестний) остеопороз встановлюється за наявності значення -2,5 чи нижче у поєднанні з низькоенергетичним переломом (Kanis, 2002). Вимірювання МЩКТ рекомендовано проводити в поперековому відділі хребта, шийці стегнової кістки, проксимальному відділі стегна та у дистальній третині променевої кістки (1/3 radius) – ці зони є найбільш інформативними для оцінювання ризику переломів.
Водночас за даними Міжнародного товариства із клінічної денситометрії (ISCD, 2023), нині термін «остеопенія» поступово замінюється на більш коректні формулювання – «низька кісткова маса» або «низька щільність кісткової тканини», оскільки не всі пацієнти із такими показниками мають високий ризик переломів. Своєю чергою у молодших осіб (жінки до менопаузи та чоловіки <50 років) інформативнішим є Z-score. Значення -2,0 або нижче інтерпретується як «нижче очікуваного для віку», тоді як показники вище -2,0 – «у межах очікуваного». При цьому діагноз остеопорозу в цій групі не може базуватися виключно на показниках МЩКТ.
Сучасні рекомендації Американської асоціації клінічних ендокринологів (AACE, 2016, 2020) розширюють діагностичні підходи, підкреслюючи, що остеопороз може бути встановлений не лише за показниками МЩКТ. Діагноз підтверджується за наявності будь-якого з таких критеріїв: T-score -2,5 чи нижче у ключових анатомічних ділянках; низькоенергетичний перелом хребта або стегна незалежно від рівня МЩКТ; T-score у межах остеопенії (від -1,0 до -2,5) у поєднанні з переломами проксимального відділу плечової кістки, таза чи дистального відділу передпліччя; або ж наявність високого 10-річного ризику переломів за інструментом FRAX відповідно до національних порогів втручання.
Модель FRAX може застосовуватися у жінок у постменопаузі та чоловіків віком від 40 років, особливо у пацієнтів з остеопенією. FRAX враховує низку клінічних факторів, зокрема вік, стать, масу тіла, зріст, наявність попередніх переломів, сімейний анамнез перелому шийки стегна, куріння, вживання алкоголю, приймання глюкокортикоїдів, наявність ревматоїдного артриту та інших причин вторинного остеопорозу. За наявності даних денситометрії до розрахунку може додаватися показник МЩКТ шийки стегнової кістки. Використання FRAX дозволяє визначити доцільність призначення лікування, особливо у випадках остеопенії, коли лише показники МЩКТ не дають повної клінічної картини.
Важливим етапом ведення пацієнтів є проведення початкового лабораторного обстеження, яке дозволяє як підтвердити дефіцитні стани, так і виключити вторинні причини остеопорозу. Обов’язковим є визначення рівня 25(OH) вітаміну D для виявлення його дефіциту. Вимірювання концентрації паратгормону допомагає виявити порушення кальцієвого обміну та гіперпаратиреоз. Електрофорез білків сироватки крові й сечі застосовується для виключення множинної мієломи та моноклональної гаммапатії невизначеного значення. Оцінювання функції щитоподібної залози є важливим для виявлення тиреотоксикозу, який може призводити до посиленого кісткового ремоделювання. Розширена біохімічна панель (кальцій, магній, фосфор, лужна фосфатаза, креатинін, розрахункова швидкість клубочкової фільтрації) дозволяє оцінити функцію печінки, нирок і нутритивний статус пацієнта.
Додатково можуть здійснюватися вимірювання рівня фосфору, скринінг на целіакію для виявлення мальабсорбції, а також аналіз добової сечі для оцінки гіперкальціурії. Маркери кісткового обміну (BSAP, CTX, P1NP) іноді використовують для оцінювання інтенсивності ремоделювання кісткової тканини, але їх не рекомендовано визначати протягом перших 2‑3 місяців після гострого перелому.
Згідно із рекомендаціями Ендокринного товариства (2019), пацієнтів доцільно розподіляти за категоріями ризику переломів. До групи низького ризику належать особи без переломів в анамнезі з T-score вище ніж -1,0 та низьким 10-річним ризиком за FRAX. Помірний ризик визначається за відсутності переломів в анамнезі, але з T-score вище за -2,5 або низьким 10-річним ризиком за FRAX. Високий ризик встановлюється за наявності переломів хребта чи стегна в анамнезі, T-score -2,5 чи нижче або ризиком за FRAX вище порогів втручання. Окремо виділяють категорію дуже високого ризику, до якої, за критеріями різних товариств, належать пацієнти із множинними чи нещодавніми переломами, переломами на тлі терапії остеопорозу, дуже низькими показниками МЩКТ або високим ризиком падінь (AACЕ/ACE, 2020; BHOF, 2022).
Загальні принципи ведення пацієнтів, профілактика й терапія
Загальні принципи менеджменту пацієнтів передбачають, що, незалежно від ступеня ризику, важливо враховувати модифіковані фактори, що призводять до падінь, зокрема застосування седативних препаратів, поліпрагмазію, порушення зору, гіпотонію, порушення ходи тощо. Пацієнтам слід рекомендувати програми тренування рівноваги та зміцнення м’язів, що доведено зменшують імовірність падінь і переломів. Відповідно до канадських рекомендацій (2023), регулярна фізична активність, як-от функціональні вправи, тренування балансу та силові навантаження, сприяють зниженню ризику падінь, поліпшенню якості життя та фізичного функціонування. Додатково доцільно радити відмовитися від куріння та обмежити вживання алкоголю.
Харчування має бути збагачене білком і кальцієм, а також слід обов’язково включити адекватне забезпечення вітаміном D3 із досягненням цільового рівня 25(OH)D у межах 30‑50 нг/мл. Зокрема, раціон із достатнім вмістом кальцію є ключовим компонентом профілактики остеопорозу. Основними його джерелами є молоко та молочні продукти, зелені листові овочі, риба з м’якими кістками, а також горіхи й насіння. Рекомендоване добове споживання кальцію становить 1000 мг для чоловіків віком 50‑70 років і 1200 мг для жінок ≥51 року та чоловіків ≥71 року. За недостатнього надходження кальцію з їжею доцільно розглядати застосування добавок (Leboff et al., 2022).
Доповідачка підкреслила, що з урахуванням сучасних рекомендацій, лікування постменопаузального остеопорозу має базуватися на стратифікації ризику переломів із подальшим індивідуалізованим вибором терапії. У пацієнток із високим ризиком переломів препаратами першої лінії залишаються антирезорбтивні засоби, зокрема бісфосфонати (алендронат, ризедронат, золедронова кислота) або деносумаб як альтернатива. У групі дуже високого ризику доцільним є застосування анаболічної терапії (як-от терипаратид, абалопаратид або ромозозумаб) із подальшим переходом на антирезорбтивні препарати для підтримання досягнутого ефекту (Leboff et al., 2022).
Водночас остеопороз є хронічним захворюванням, що потребує тривалого лікування з періодичною повторною оцінкою ризику переломів. Так, ефективність терапії визначають через 3‑6 років, залежно від рекомендацій провідних товариств, із можливістю продовження лікування або переходу на іншу терапевтичну стратегію (AACЕ/ACE, 2020; ESCEO/IOF, 2019‑2020; Osteoporosis Canada, 2023). У частини хворих можливе застосування так званих медикаментозних канікул після тривалого приймання бісфосфонатів, але цей підхід потребує ретельного моніторингу. Під час таких періодів особливого значення набуває контроль стану кісткової тканини: регулярне оцінювання МЩКТ, аналіз клінічних факторів ризику та, за необхідності, визначення маркерів кісткового метаболізму. Відновлення терапії показане при зниженні МЩКТ, появі нових переломів або формуванні додаткових факторів ризику (Eastell et al., 2019).
Незалежно від обраного фармакологічного лікування, базовим компонентом ведення пацієнток із постменопаузальним остеопорозом залишається адекватне забезпечення організму кальцієм і вітаміном D. Ця складова визначає ефективність як антирезорбтивної, так і анаболічної терапії та є обов’язковою на всіх етапах лікування, включно з періодами «медикаментозних канікул».
Важливо, що кістковий метаболізм є складним багаторівневим процесом, який включає проліферацію та диференціацію остеобластів, синтез органічного матриксу та подальшу мінералізацію. У цьому контексті принципове значення має не лише кількість кальцію, але й його форма, біодоступність та вплив на його рівень у сироватці крові. Як свідчать епідеміологічні дані, високі пікові концентрації кальцію після приймання традиційних солей можуть асоціюватися із підвищеним серцево-судинним ризиком, що обґрунтовує доцільність застосування форм кальцію з більш фізіологічним, контрольованим профілем абсорбції (Li et al., 2012).
Із цих позицій привертає увагу мікрокристалічний гідроксиапатитний комплекс StimuCal™ (Остіверон®), який поєднує органічну (осеїн) та мінеральну (гідроксиапатит) складові. Така структура забезпечує фізіологічну мінералізацію кісткової тканини та сприяє синтезу колагену й остеокальцину, що формує повноцінний кістковий матрикс.
Зокрема, доведено, що мікрокристалічний гідроксиапатитний комплекс Остіверон® стимулює проліферацію та диференціацію остеобластів із формуванням тканинноспецифічних структур регенерату. В експериментальному дослідженні додавання цього комплексу до культур остеобластів супроводжувалося достовірним збільшенням площі мінералізованої кістки вже на 14-ту добу із подальшим ефектом на 21-шу добу порівняно з контролем (Musson et al., 2012).
Важливою клінічною перевагою StimuCal™ (Остіверон®) є його здатність забезпечувати більш контрольований профіль кальціємії. За даними клінічного дослідження, пікові рівні кальцію у крові після його застосування були на 45‑49% нижчими порівняно із карбонатом і цитратом кальцію, що свідчить про відсутність різких коливань концентрації та потенційно кращий профіль безпеки. При цьому ефективність щодо впливу на кістковий метаболізм залишається порівнянною із традиційними солями кальцію (Reid et al., 2012).
Таким чином, Остіверон® забезпечує комплексний вплив на всі етапи остеогенезу, як-от:
- стимуляція остеобластичної активності;
- підтримання синтезу органічного матриксу;
- фізіологічна мінералізація;
- контрольоване надходження кальцію без пікових навантажень.
З огляду на необхідність адекватного забезпечення організму кальцієм і вітаміном D у жінок із постменопаузальним остеопорозом, доцільне використання комбінації засобів Остіверон® як джерела кальцію та Солемакс® як джерела вітаміну D. Завдяки своїй структурі, Остіверон® зумовлює поступове та рівномірніше надходження кальцію в організм, що асоційовано зі сприятливим профілем безпеки, та при цьому демонструє ефективність щодо впливу на маркери ремоделювання кісткової тканини. Додавання вітаміну D (Солемакс®) є важливим для адекватної абсорбції кальцію та реалізації його біологічних ефектів у кістковій тканині, що особливо актуально для жінок у постменопаузі (Reid et al., 2012).
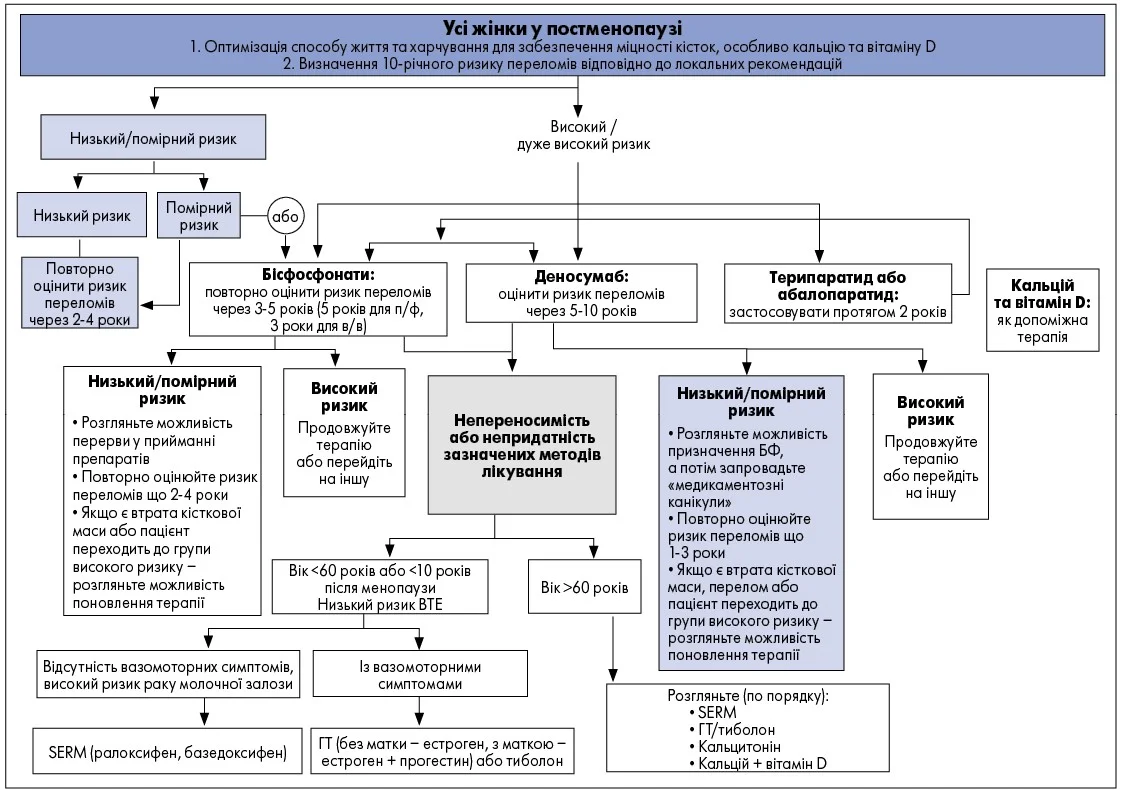
Алгоритм ведення пацієнток із постменопаузальним остеопорозом залежно від індивідуального ризику переломів, відповідно до рекомендацій Ендокринного товариства (2019), наведено на рисунку.
Рисунок. Алгоритм ведення пацієнток із постменопаузальним остеопорозом залежно від індивідуального ризику переломів
Примітки: БФ – бісфосфонати, п/ф – пероральна форма, в/в – внутрішньовенно, ВТЕ – венозна тромбоемболія, SERM – селективні модулятори естрогенових рецепторів, ГТ – гормональна терапія.
Адаптовано за R. Eastell et al. (2019)
Завершуючи виступ, Є.Д. Єгудіна підсумувала, що сучасна стратегія ведення пацієнток із постменопаузальним остеопорозом передбачає стратифікацію ризику переломів і вибір відповідної фармакотерапії з регулярним повторним оцінюванням її ефективності, індивідуалізований підхід до тривалості лікування та можливості «медикаментозних канікул», а також обов’язкову базову підтримку кальцієм і вітаміном D.
Підготувала Олена Коробка
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 2 (105) 2026 р.