10 березня, 2026
Розлад адаптації в умовах тривалого стресу: сучасні підходи до ведення і місце фенібуту
Повномасштабна війна, поза сумнівом, має надпотужний несприятливий вплив на психічне здоров’я за рахунок тривалого стресу та значної кількості психотравматичних подій. За даними 2024 р., кожен 5-й українець втратив знайому людину, 12,7% втратили рідних і близьких, 2,1% повідомили про руйнування або втрату будинку, 6,0% стали вимушено переміщеними особами в Україні чи за її межами (Info Sapiens, 2024). Війна, як надзвичайна та екстремальна ситуація, є тривалим деструктивним чинником зовнішнього впливу, протистояти якому людина не має достатніх душевних ресурсів. Отже, спричинений війною стрес значно відрізняється від повсякденного, оскільки суттєво перевищує спроможність людини адаптуватися (Павленко Г.В., Звєрєва А.М., 2024). Ця ситуація може стати причиною розладу адаптації (РА) – вагомої медичної та соціальної проблеми, поширеність якої становить від 0,2 до 40% залежно від стресової ситуації, яку переживає пацієнт (Geer K. et al., 2023).
За визначенням 5-го видання Діагностичного та статистичного посібника з психічних розладів (DSM-5), РА – це мальадаптивна реакція на стресову подію, яка зумовлює дистрес, що перевищує очікуваний. Ця реакція виникає упродовж 3 місяців після початку дії стресора та зазвичай зникає протягом 6 місяців після припинення дії стресора або її наслідків. Цікаво, що РА може виникати під впливом як негативних, так і позитивних життєвих подій. Виокремлюють 6 підтипів РА: з депресією, із тривожністю, з поєднанням депресії та тривожності, з розладом поведінки, зі змішаним розладом поведінки й емоцій, а також невизначений підтип (DSM‑5, 2022).
Схожим є і визначення, яке надає Міжнародна класифікація хвороб 11-го перегляду (МКХ‑11). Згідно з ним, РА – мальадаптивна реакція на стресову життєву подію, наявні в цей момент психосоціальні стресові обставини або поєднання стресових ситуацій, яка зазвичай виникає упродовж 1 місяця після впливу стресора та зникає протягом 6 місяців, якщо дія стресора завершується. МКХ‑11 характеризує РА двома кластерами симптомів: занепокоєністю – стресором, який передбачає нав’язливі неприємні думки (румінацію) щодо стресора чи його наслідків, а також нездатністю до адаптації, що охоплює труднощі з концентрацією уваги, порушення сну та нездатність до емоційного відновлення. Для встановлення діагнозу РА симптоми мають бути пов’язані зі значущим порушенням функціонування (Levin Y. et al., 2022).
Типовими причинами РА в економічно розвинених країнах є розлучення або розрив близьких стосунків, втрата роботи, виявлена хвороба, початок інвалідизуючого стану та конфлікти вдома чи на роботі. Із глобального погляду частими стресорами є економічні труднощі, примусова міграція чи адаптація до нової культури (Maercker A., Lorenz L., 2018). Фактори ризику РА: жіноча стать, молодий вік, безробіття, часті/хронічні стреси, соматичні захворювання та травми, низький рівень соціальної підтримки й анамнез психічних захворювань (Kelber M. et al., 2022).
Патофізіологічні механізми РА вивчені недостатньо, однак вважається, що при тривалому стійкому хронічному стресі виникають зміни нейротрансмітерних функцій та нейропластичної відповіді, що може сприяти депресії. Важливу роль у завершенні стресової відповіді організму, тобто протидії хронізації стрес-реакції, відіграють ГАМК-ергічні нейрони, трансмітером для яких є γ-аміномасляна кислота (ГАМК). В експериментальних моделях депресії та тривожності в лабораторних тварин спостерігається зниження вмісту ГАМК у фронтальній корі головного мозку та кортикальних синаптонейросомах. І навпаки, нормалізація вмісту ГАМК спричиняє ремісію депресивних симптомів та ознак підвищеної тривожності (Fogaça M.V., Duman R.S., 2019; Arora I. et al., 2024). Незважаючи на певний успіх наявних на фармацевтичному ринку антидепресантів, кількість ефективних медикаментів, спрямованих на збільшення вмісту ГАМК у тканинах нервової системи, обмежена (Shao Q. et al., 2025). Імовірно, порушення ГАМК-ергічної регуляції лежить і в основі РА.
Хоча РА вважають самообмежувальним процесом, його тривалість може зростати в разі продовження впливу стресора, зумовлюючи значне погіршення якості життя та підвищення ризику суїциду (Levin Y. et al., 2022).
Для діагностики РА в умовах первинної практики застосовують опитувальник ADNM (Adjustment Disorder – New Module) у формі 29, 20, 8 або 4 запитань (Levin Y. et al., 2022). Також цей опитувальник існує у формах структурованого клінічного інтерв’ю та анкети для самооцінки. В першій частині опитувальника респондент має вибрати зі списку стресори (гострі та хронічні), які були наявні в його житті протягом останнього року, та виокремити найвиразніші. Друга частина містить запитання, пов’язані з надмірною занепокоєністю, неспроможністю адаптуватися, униканням впливу стресора, депресивним настроєм, тривожністю та порушенням контролю імпульсів (O’Donnell M. et al., 2019).
У веденні пацієнтів із РА використовуються нефармакологічні заходи (когнітивно-поведінкова терапія, соціальна підтримка, стратегії стрес-менеджменту, модифікація способу життя), а також фармакотерапія (Zelviene P., Kazlauskas E., 2018; O’Donnell M. et al., 2019; DSM‑5, 2022), проте більшість препаратів діють лише на окремі симптоми, мають побічні ефекти та не враховують патофізіології РА. Зокрема, призначаються антидепресанти, анксіолітики, бензодіазепіни, рослинні засоби (гінкго білоба, кава-кава). З огляду на відсутність однозначно схвалених для лікування РА фармакопрепаратів клініцистам доцільно дотримуватися ключового принципу primum non nocere, тобто «насамперед не нашкодь». Саме тому бензодіазепіни, що асоціюються із широким спектром побічних реакцій та формуванням звикання, не слід призначати ні при РА, ні при посттравматичному стресовому розладі. Крім того, з огляду на особливості діагностики РА (зокрема, обмеженість у часі) методологія більшості наявних клінічних досліджень не відповідає цьому стану, а досліджувані препарати не показали переваг над плацебо (Stein D., 2018).
Фенібут – патофізіологічно обґрунтоване лікування РА; за хімічною будовою він є фенільним похідним основного гальмівного нейротрансмітера – ГАМК, тому цій речовині притаманні як ноотропні, так і анксіолітичні (заспокійливі) властивості. Фенібут знижує тривожність, збудження й страхи, покращує сон, а також достовірно зменшує вираженість симптомів астенії та вазовегетативних розладів (головного болю, відчуття тяжкості в голові, дратівливості, емоційної лабільності), водночас збільшуючи ментальну працездатність і покращуючи увагу, пам’ять, швидкість та точність сенсомоторних реакцій. Як агоніст В-рецепторів ГАМК фенібут підвищує зацікавленість, ініціативність та мотивацію в пацієнтів з астенією, не зумовлюючи таких небажаних ефектів, як седація чи збудження (Tērauds E. et al., 2025).
У дослідженні Е. Tērauds і співавт. (2025) взяли участь пацієнти з РА, які отримували фенібут у дозі 250 мг 3 р/добу протягом 3 тижнів.
Перед початком лікування та через 7 днів після прийому останньої дози фенібуту проводили оцінку за ADNM‑20. Було виявлено достовірне зменшення сумарної оцінки та оцінки за кожною з окремих субшкал (табл.).
|
Таблиця. Зміна оцінки за ADNM‑20 порівняно з початковим показником |
|||
|
|
Початковий показник |
Після лікування |
Відмінність |
|
Загалом |
60,3±10,5 |
45,5±12,3 |
14,8±11,3 |
|
Основні симптоми |
24,0±4,9 |
17,4±5,2 |
6,6±4,9 |
|
Додаткові симптоми |
36,3±6,1 |
28,1±7,4 |
8,2±6,9 |
|
Субшкали |
|||
|
Надмірна занепокоєність стресором |
12,5±2,7 |
9,2±2,8 |
3,4±2,7 |
|
Неспроможність адаптуватися |
11,5±2,9 |
8,3±2,7 |
3,2±2,7 |
|
Уникання впливу стресора |
12,0±2,5 |
9,8±2,8 |
2,2±2,8 |
|
Депресивний настрій |
8,8±2,1 |
6,7±2,0 |
2,1±2,2 |
|
Тривожність |
5,8±1,4 |
4,4±1,4 |
1,4±1,5 |
|
Порушення контролю імпульсів |
9,7±2,0 |
7,1±2,3 |
2,6±2,2 |
|
Тяжкість симптомів |
|||
|
Низька |
12,2% |
7,8% |
<0,19 |
|
Помірна |
31,1% |
55,6% |
<0,001 |
|
Висока |
56,7% |
22,2% |
<0,001 |
|
Нижче нижнього порогового значення |
Не виявлено |
14,4% |
– |
|
Примітка: * дані подані як середнє значення ± стандартне відхилення. |
|||
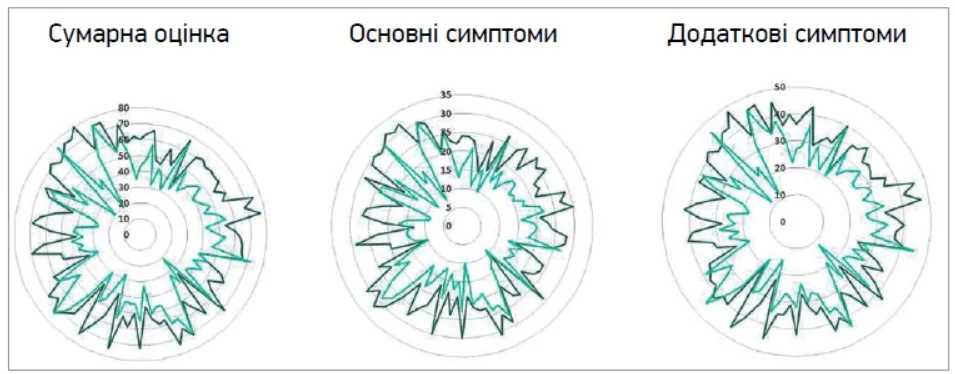
Частка пацієнтів із тяжким РА зменшилася в 2,5 раза, а в 14% пацієнтів РА було ліквідовано. Цікаво, що в хворих із тяжчим РА спостерігалося вираженіше покращення (рис.). Сприятливий вплив фенібуту не залежав від віку та статі.
Рис. Оцінка за ADNM‑20 по кожному пацієнту до (зовнішня крива) та після (внутрішня крива) лікування фенібутом упродовж 3 тижнів
Під час оцінки окремих складових за ADNM‑20 виявлено, що вираженість кожного компонента РА знизилася щонайменше на 15%. Найпотужніше зниження спостерігалося для розладів сну (теза на кшталт «з моменту стресової ситуації я більше не можу нормально спати») та нав’язливих думок про стресову ситуацію («змушена (-ий) продовжувати думати про стресову ситуацію, і це мене дуже пригнічує»).
Зіставлення оцінок динаміки РА пацієнтом і лікарем співпало, а це підтверджує отриманий результат щодо позитивного впливу лікування. Профіль безпеки фенібуту був сприятливим, і жоден пацієнт не припинив лікування через побічні ефекти, що відповідає наявним даним літератури (Tērauds E. et al., 2025).
Висновки
Через тривалий вплив повномасштабної війни як стійкого та потужного стресового фактора серед населення України спостерігається зростання поширеності клінічних і субклінічних психічних розладів, зокрема РА. Критерії діагностики цього стану представлені в DSM‑5 та МКХ‑11 і передбачають часовий зв’язок із впливом стресора й наявність мальадаптивної реакції на життєві обставини. Лікування РА залишається маловивченим питанням, однак, за даними літератури, ефективним і безпечним є застосування фенібуту в дозі 250 мг 3 р/добу протягом 3 тижнів.
Довідка «ЗУ»
Біфрен® (Acino, part of Arcera, міжнародна фармацевтична група компаній зі штаб-квартирою в Цюриху, Швейцарія; https://acino.ua/) є відомим серед українських лікарів препаратом фенібуту. Відповідно до інструкції для медичного застосування, показаннями до застосування Біфрену є астенічні та тривожно-невротичні стани (неспокій, страх, тривожність; безсоння, нічний неспокій у людей літнього віку; передопераційні стресові стани); хвороба Меньєра і запаморочення, пов’язані з дисфункцією вестибулярного аналізатора різного походження; кінетоз (захитування) – як профілактичний засіб; заїкання, тики в дітей віком 8-14 років; абстинентний синдром при алкоголізмі (як допоміжний засіб). З огляду на здатність проникати через гематоенцефалічний бар’єр і ГАМК-агоністичні властивості Біфрен® має потужний терапевтичний потенціал щодо РА.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 3 (614), 2026 р