4 червня, 2022
Больовий синдром у неврології: ефективний старт терапії
 М’язово-скелетні болі різної локалізації (біль у шиї, кінцівках, спині, суглобах, а також розлитий біль) є однією з провідних причин звернення пацієнтів до лікаря первинної ланки (Main C. J., Williams A. C.C., 2002). Біль у нижній частині спини (БНЧС) є патологічним станом опорно-рухового апарату, який чинить значний несприятливий вплив на якість життя. За визначенням, БНЧС являє собою біль, задубілість чи м’язове напруження, локалізоване між нижнім краєм нижніх ребер і сідничними складками (Vlaeyen J. W.S. et al., 2018; Urits A. et al., 2019).
М’язово-скелетні болі різної локалізації (біль у шиї, кінцівках, спині, суглобах, а також розлитий біль) є однією з провідних причин звернення пацієнтів до лікаря первинної ланки (Main C. J., Williams A. C.C., 2002). Біль у нижній частині спини (БНЧС) є патологічним станом опорно-рухового апарату, який чинить значний несприятливий вплив на якість життя. За визначенням, БНЧС являє собою біль, задубілість чи м’язове напруження, локалізоване між нижнім краєм нижніх ребер і сідничними складками (Vlaeyen J. W.S. et al., 2018; Urits A. et al., 2019).
БНЧС поширений у всьому світі та є однією із провідних причин інвалідності (Safiri S. et al., 2021). Аналіз даних Глобального тягаря хвороб (Global Burden of Disease), опублікований у січні 2022 р., свідчить про те, що стандартизована за віком поширеність БНЧС становить 6972,5 випадку на 100 000 населення. Цікаво, що найвищими є показники поширеності БНЧС в індустріалізованих країнах із високим рівнем достатку (США, Данія, Швейцарія) (Chen S. et al., 2022). За даними популяційного дослідження J. K. Freburger та співавт. (2009), у світі спостерігається як зростання поширеності БНЧС, так і збільшення витрат на його лікування. У той чи інший період свого життя на БНЧС страждає ≈⅔ дорослого населення планети (Deyo R. A., Weinstein J. N., 2001).
Причинами БНЧС можуть бути різнопланові чинники, однак ≈97% випадків мають механічну етіологію, тобто є наслідками різноманітних мікротравм поперекового відділу хребта й асоційованих із віком дегенеративних процесів у міжхребцевих дисках, рідше – кил дисків та остеопоротичних компресійних переломів (Deyo R. A., Weinstein J. N., 2001). Немеханічні причини (новоутворення, інфекційні та запальні артрити, захворювання вісцеральних органів) спричиняють БНЧС набагато рідше (Zippel H., Wagenitz A., 2007). Загалом пацієнтів із БНЧС можна розподілити на осіб із неспецифічним болем (≈85%), осіб зі специфічним болем або тяжкою спінальною патологією та осіб із радикулярним болем. У зв’язку із цим діагностичні заходи при БНЧС здебільшого спрямовані на виявлення «червоних прапорців» – ознак пухлини, перелому чи інфекції, а також на виключення хвороб, які спричиняють специфічний біль (Koes B. W. et al., 2001).
Нерідко БНЧС хронізується і турбує пацієнтів протягом тривалого часу (Dunn K. M. et al., 2013; Meucci R. D. et al., 2015). Персистуючий БНЧС асоціюється з низкою додаткових вторинних проблем і хвороб, у т. ч. із розладами сну, тривожністю, депресією, м’язово-скелетними болями іншої локалізації (Duffield S. J. et al., 2017; Gore M. et al., 2012; Scarpsno E. S. et al., 2020; Hartvigsen J. et al., 2013).
Основною групою препаратів, яка застосовується в лікуванні БНЧС, є нестероїдні протизапальні препарати (НПЗП), причому, відповідно до рекомендацій Північноамериканського товариства хребта (North American Spine Society, 2020), саме неселективні НПЗП, як-от декскетопрофен.
Декскетопрофен являє собою НПЗП, який належить до підгрупи похідних арилпропіонової кислоти та є S‑ізомером, ізольованим із рацемічного кетопрофену (Brzezinski K., Wordliczek J., 2013). Дослідження продемонстрували, що S‑ізомер є у декілька разів потужнішим інгібітором циклооксигенази 1 і 2 типу, ніж рацемічний кетопрофен (Carabaza A. et al., 1997; Cabre F. et al., 1998). Крім того, декскетопрофену притаманна уп’ятеро нижча ульцерогенна активність, ніж рацемічній суміші (Gich I. et al., 1996). Створення декскетопрофену як хірально чистого S‑ізомеру кетопрофену дозволило досягти таких переваг, як потреба в низьких дозах препарату, зниження метаболічного навантаження, уникнення лікарських взаємодій та різке зменшення імовірності побічних реакцій (Hardikar M. S., 2008). Це підтверджується даними J. R. Laporte та співавт. (2004), які проаналізували >4000 випадків гастроінтестинальних кровотеч, з’ясувавши, що найбільший відносний ризик цього ускладнення притаманний кеторолаку (24,7; 95% довірчий інтервал (ДІ) 8,0-77,0). Для декскетопрофену цей показник становить 4,9 (95% ДІ 1,7-13,9), для мелоксикаму – 5,7 (95% ДІ 2,2-15,0), а для рофекоксибу – 7,2 (95% ДІ 2,3-23,0).
До рандомізованого подвійного сліпого багатоцентрового дослідження H. Zippel та A. Wagenitz (2007) було залучено 370 амбулаторних пацієнтів із гострим БНЧС, яких рандомізували до груп внутрішньом’язового застосування декскетопрофену (50 мг 2 р/добу) та диклофенаку (75 мг 2 р/добу) протягом 2 днів. Виявилося, що зниження інтенсивності болю за візуальною аналоговою шкалою (ВАШ) через 6 год після введення першої дози декскетопрофену становило 117,3 мм/год, а після введення диклофенаку – 114,7 мм/год. В обох групах спостерігалася однакова потреба в препаратах порятунку, а також необхідність у покращенні функціональних можливостей; частота побічних ефектів також приблизно була зіставною. Автори дійшли висновку, що декскетопрофен забезпечує клінічно вагомий аналгетичний ефект при БНЧС і має хорошу переносимість як при однократному, так і при повторному застосуванні.
Згідно з наказом МОЗ України від 29.12.2012 № 751, універсальним джерелом клінічних настанов є Кокранівська база даних систематичних оглядів. Висновки Кокранівських метааналізів рекомендовано використовувати для впровадження в практику ефективних методів лікування. Проспективне рандомізоване подвійне сліпе дослідження Е. Demirozogul і співавт. (2019), яке входить до Кокранівського центрального реєстру контрольованих досліджень, включало 200 пацієнтів із різними видами гострого нетравматичного м’язового болю. Пацієнтів було рандомізовано в групи внутрішньовенного застосування декскетопрофену (50 мг) і парацетамолу (1000 мг). Виявилося, що декскетопрофен був достовірно ефективнішим за ВАШ і чисельною шкалою оцінки болю в усіх проаналізованих локалізаціях больових відчуттів (р=0,001).
Метааналіз R. A. Moore та J. Barden (2008) виявив, що в лікуванні гострого і хронічного болю всі можливі дози декскетопрофену мають перевагу над плацебо та (щонайменше) зіставну ефективність з кетопрофеном у дозі 100 мг, трамадолом у дозі 100 мг, диклофенаком у дозі 75 мг 2 р/день. Декскетопрофен має відмінні показники ефективності та безпеки не лише при БНЧС, а й за низки інших нозологій. Так, ін’єкційне застосування декскетопрофену забезпечувало відсутність / низьку інтенсивність болю в 93,3% випадків ударнохвильової літотрипсії щодо сечокам’яної хвороби, а ін’єкційне застосування диклофенаку – лише у 85% (Tokgoz H. et al., 2010).
Декскетопрофен ефективний також при мігрені. Метааналіз B. Yang і співавт. (2019), який включав 5 рандомізованих контрольованих досліджень за участю 749 пацієнтів, виявив, що порівняно з контрольною групою застосування декскетопрофену асоціювалося з достовірно більшою імовірністю відсутності болю через 2 години (відношення ризиків (ВР) 1,90; 95%ДІ 1,43-2,53; р<0,0001) та 48 годин (ВР 1,63; 95% ДІ 1,07-2,49; р=0,02) після введення, а також оцінкою ефекту лікування як хорошого/відмінного (ВР 1,48; 95% ДІ 1,24-1,78). Застосування декскетопрофену супроводжувалося меншою потребою в препаратах порятунку (ВР 0,64; 95% ДІ 0,43-0,94; р=0,02). Що важливо, всі переваги декскетопрофену спостерігалися на тлі відсутності достовірного зростання частоти розвитку побічних ефектів. Загалом декскетопрофен належить до НПЗП із помірним ризиком кровотеч із верхніх відділів шлунково-кишкового тракту, на відміну від кеторолаку, піроксикаму, індометацину, кетопрофену, напроксену та аспірину, яким притаманний високий ризик (Aranguren I. et al., 2016).
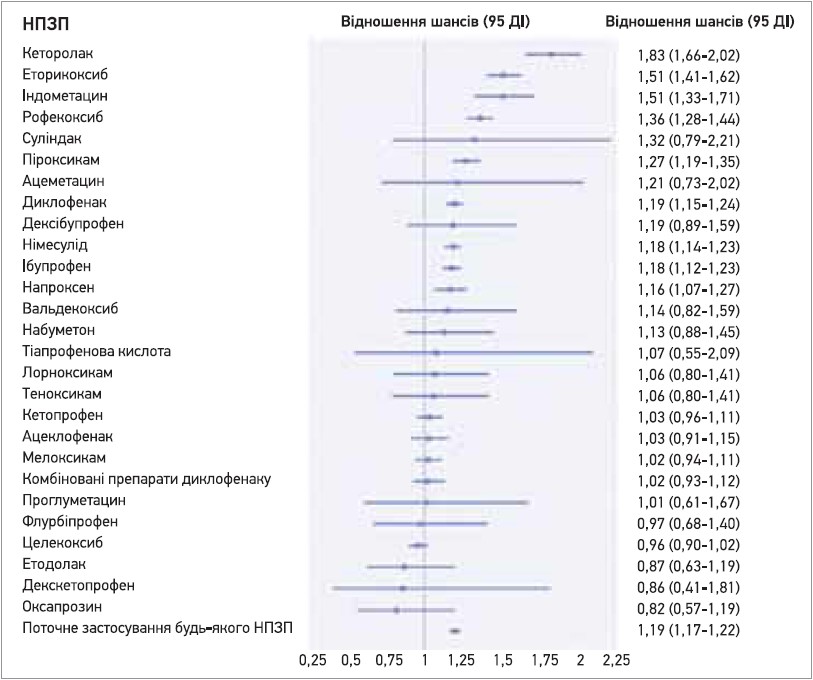
Щодо кардіоваскулярної безпеки декскетопрофену дослідження, яке включало дані близько 10 млн пацієнтів з європейських країн, показало, що застосування цього препарату, на відміну від низки неселективних НПЗП і коксибів, не збільшує частоту госпіталізацій з приводу серцевої недостатності (рис.) (Arfe А. et al., 2016).
Рис. Узагальнені асоціації між поточним вживанням окремих НПЗП та ризиком госпіталізації з приводу серцевої недостатності
Вагомою проблемою комплексного лікування хворих є міжлікарська взаємодія, особливо у випадках, коли побічні ефекти призначених препаратів можуть підсилювати один одного. Встановлено, що декскетопрофен можна безпечно застосовувати в сполученні з низькомолекулярними гепаринами (НМГ). У багатоцентровому рандомізованому подвійному сліпому дослідженні H. Zippel та A. Wagenitz (2007) взяли участь 252 пацієнти з болем помірної та високої інтенсивності після ортопедичних хірургічних втручань, 94,4% з них отримували НМГ. Було продемонстровано, що внутрішньовенне застосування декскетопрофену в сполученні з НМГ не супроводжувалося зростанням кількості геморагічних подій. В іншому дослідженні декскетопрофен призначався з НМГ у профілактичних дозах пацієнтам із травмами та особам після ортопедичних хірургічних втручань. Автори виявили, що між НМГ і декскетопрофеном відсутні будь-які взаємодії, котрі можуть суттєво вплинути на параметри згортання крові. Хоча було зафіксовано певне збільшення кількості невеликих кровотеч, кількість великих і клінічно значущих кровотеч у післяопераційному періоді залишилася незмінною. Комбінація НМГ та декскетопрофену не збільшувала імовірність кровотечі з післяопераційної рани та крововтрат через дренажі, а також не підвищувала потребу в переливаннях крові (Кучин Ю., 2014).
Додатковою перевагою декскетопрофену є те, що хемореактомний аналіз цього препарату виявив потенційні вазодилатувальні, антиагрегантні, протидіабетичні та протипухлинні властивості цієї молекули (Торшин И. Ю. и соавт., 2018).
Препарат Кейдекс Ін’єкт є ін’єкційною формою декскетопрофену для внутрішньом’язового та внутрішньовенного введення. Виявлені переваги над іншими НПЗП, зокрема диклофенаком, дозволяють вважати Кейдекс Ін’єкт новим золотим стандартом аналгезії. Кейдекс Ін’єкт містить декскетопрофен у формі водорозчинної солі декскетопрофену трометамолу, що забезпечує швидке досягнення максимальної концентрації діючої речовини (через 20 (10-45) хвилин), а отже, швидке настання знеболювального ефекту. Важливо також те, що декскетопрофен швидко елімінується з організму та не накопичується в тканинах навіть у разі застосування 3 р/день (Barbanoj M. J. et al., 2001; Walczak J. S., 2011). Показання до застосування препарату Кейдекс Ін’єкт – симптоматичне лікування гострого болю середньої та високої інтенсивності у випадках, коли пероральне використання препарату є недоцільним, наприклад, при післяопераційних болях, ниркових кольках, болю в попереку (БНЧС). На тлі короткотривалого застосування препарату Кейдекс Ін’єкт відповідно до інструкції для медичного використання (не більше 2 діб) профіль побічних ефектів цього препарату відповідає профілю плацебо (Walczak J. S., 2011).
Таким чином, Кейдекс Ін’єкт є оптимальним стартовим препаратом для знеболення, оскільки має такі переваги, як ефективність, відмінний профіль гастроінтестинальної та кардіоваскулярної безпеки, висока швидкість настання ефекту.