26 лютого, 2023
Складнощі діагностики спадкового ангіоневротичного набряку в разі клінічного поліморфізму його проявів
 Спадковий ангіоневротичний набряк (САН) – рідкісне генетично-детерміноване захворювання з автосомно-домінантним типом успадкування. Клінічна картина САН характеризується періодичними епізодами набряку підшкірної або підслизової клітковини з будь-якою локалізацією (найчастіше кінцівок), а також нападами інтенсивного болю в животі. В основі захворювання лежить мутація гена SERPING1 (serine protease inhibitor), який кодує інгібітор С1-естерази (C1-INH). Недостатність білка C1-INH призводить до вивільнення надмірної кількості прозапального медіатора брадикініну, отже, й до суттєвого збільшення проникності судин із розвитком епізодів ангіоневротичного набряку. Клінічна картина САН часто нагадує таку при алергічних реакціях, тим самим дезорієнтуючи лікарів тоді, коли застосування антигістамінних препаратів (АГП), глюкокортикоїдів та адреналіну не має жодного ефекту. Аналогічно гострий біль у животі – ще один характерний симптом САН – може імітувати гостру хірургічну патологію та спричиняти непотрібні оперативні втручання. Через низьку специфічність симптомів і недостатню обізнаність щодо цієї патології діагностика захворювання може затримуватися на десятки років. Разом із тим сьогодні є надійні та доступні діагностичні тести, які надають можливість з високою імовірністю підтвердити або виключити це захворювання, а також вчасно розпочати лікування.
Спадковий ангіоневротичний набряк (САН) – рідкісне генетично-детерміноване захворювання з автосомно-домінантним типом успадкування. Клінічна картина САН характеризується періодичними епізодами набряку підшкірної або підслизової клітковини з будь-якою локалізацією (найчастіше кінцівок), а також нападами інтенсивного болю в животі. В основі захворювання лежить мутація гена SERPING1 (serine protease inhibitor), який кодує інгібітор С1-естерази (C1-INH). Недостатність білка C1-INH призводить до вивільнення надмірної кількості прозапального медіатора брадикініну, отже, й до суттєвого збільшення проникності судин із розвитком епізодів ангіоневротичного набряку. Клінічна картина САН часто нагадує таку при алергічних реакціях, тим самим дезорієнтуючи лікарів тоді, коли застосування антигістамінних препаратів (АГП), глюкокортикоїдів та адреналіну не має жодного ефекту. Аналогічно гострий біль у животі – ще один характерний симптом САН – може імітувати гостру хірургічну патологію та спричиняти непотрібні оперативні втручання. Через низьку специфічність симптомів і недостатню обізнаність щодо цієї патології діагностика захворювання може затримуватися на десятки років. Разом із тим сьогодні є надійні та доступні діагностичні тести, які надають можливість з високою імовірністю підтвердити або виключити це захворювання, а також вчасно розпочати лікування.
САН уражає ≈1 особу на кожні 50 тис. популяції планети і з однаковою частотою зустрічається в чоловіків та жінок, хоча вираженість загострень є більшою серед жіночого населення. САН розподіляється на два типи: І тип, що спостерігається в ≈85% хворих, характеризується низьким рівнем C1-INH, а ІІ типу (15% випадків) притаманна дисфункція цього білка. Обидва типи САН викликані мутацією гена SERPING1.
Розпочавшись у дитинстві, в підлітковому віці (найчастіший вік дебюту САН) або в дорослого пацієнта, періодичні набряки супроводжуватимуть його все подальше життя.
Частота набряків може змінюватися від кількох разів на тиждень до декількох разів на рік. Так само можуть змінюватися їхня інтенсивність та локалізація, а за високої частоти в пацієнта може виникати відчуття, що набряк не закінчується, а перетікає з однієї частини тіла до іншої.
Причиною виникнення набряку є підвищення рівня брадикініну, зумовлене порушеннями в калікреїн-кініновій системі. САН належить до первинних імунодефіцитів, а отже, ведення пацієнтів із діагностованим САН здійснюють імунологи. Частота і тривалість нападів залежать від рівня С1-інгібітора і частково – від віку початку розвитку симптомів; в ≈⅓ випадків симптоми САН маніфестують у віці до 5 років. У такому разі зазвичай спостерігається тяжчий перебіг захворювання. В більшості випадків перші прояви САН розвиваються у віці до 20 років і дуже рідко – у віці >40 років.
Тригерами загострень можуть бути стрес, травма, втома, інфекційні процеси, гормональні розлади, застосування медикаментів (інгібітори АПФ, бета-блокатори, естрогени тощо), однак у багатьох випадках визначити тригер неможливо.
Клінічно в хворих із САН спостерігаються непередбачувані набряки шкіри та слизових оболонок, які найчастіше уражають живіт і кінцівки, обличчя, гортань, статеві органи. Значно рідше зустрічаються «невидимі» набряки черевної порожнини або інших слизових.
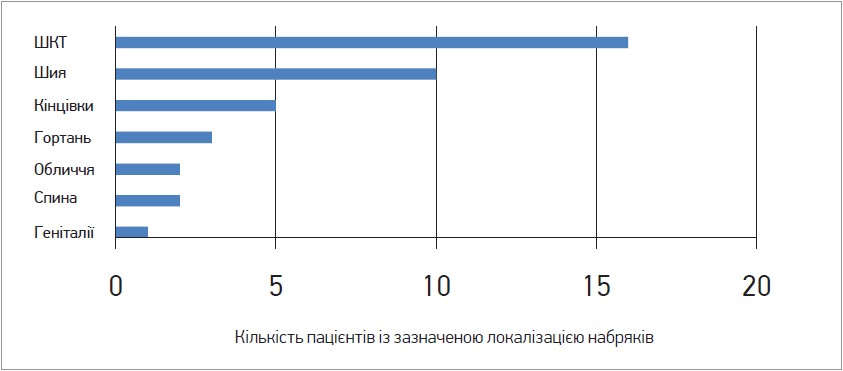
За даними опитування 27 українських пацієнтів із САН, ≈45% усіх набряків – це набряки черевної порожнини (за 3 міс набряк ШКТ спостерігали 16 пацієнтів (рис. 1).
Рис. 1. Частота локалізації набряків у 27 українських пацієнтів із САН протягом 3 міс
(за даними паперового щоденника)
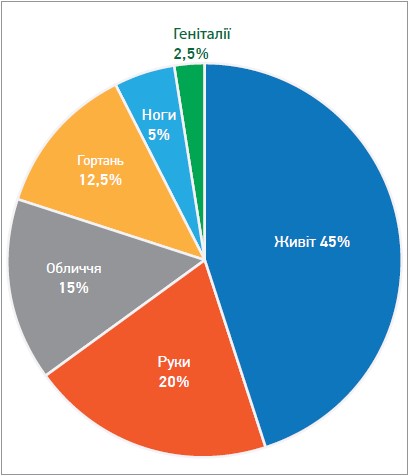
Наші спостереження зіставні з даними польських колег, які показали таку частоту локалізації набряків: живіт – 45%, 20% – руки, 15% – обличчя, 12,5% – гортань, 5% – ноги, 2,5% – геніталії при реєстрації набряків протягом року в 40 пацієнтів із САН І та ІІ типів (рис. 2).
Рис. 2. Локалізація набряків у 40 пацієнтів за 1 рік (за даними професора Обтулович, Польща)
Перед розвитком ангіоедеми хворий може відчувати продромальні симптоми, як-от сильна втома, біль у суглобах і м’язах, нудота, гастроінтестинальні розлади, головний біль, грипоподібні симптоми, відчуття оніміння/поколювання в ділянці майбутнього формування набряку. Багато пацієнтів із САН перебувають у депресії та відчувають тривогу, що, своєю чергою, погіршує перебіг захворювання.
Однією з найважливіших проблем, асоційованих із САН, є напади набряку гортані. Хоча епізоди набряку гортані становлять лише ≈1% від усіх нападів, близько половини пацієнтів із САН протягом життя щонайменше 1 раз мали епізод набряку цієї локалізації. Оскільки епізоди набряку гортані несуть реальну загрозу життю пацієнта, вони потребують негайного лікування. Тоді як гострі алергічні реакції або анафілаксія мають тенденцію до досягнення піку клінічних проявів протягом декількох хвилин після впливу алергену, набряк гортані в пацієнтів із САН розвивається в середньому протягом декількох годин (хоча інколи може розвиватися протягом коротшого часового проміжку), впродовж яких і необхідно ввести препарат для патогномонічної терапії (наприклад, уже доступний в Україні С1-інгібітор або свіжозаморожену плазму в разі відсутності С1-інгібітора).
Слід зазначити, що впродовж останніх років діагностика САН в Україні стала доступнішою. Сьогодні в низці приватних лабораторій проводять визначення концентрації й активності С1-INH, а також концентрації C4 компонента комплементу в сироватці/плазмі крові, що потрібно для встановлення діагнозу САН. Окрім того, ГО «Всеукраїнська асоціація дитячої імунології» було розпочато проєкт «Поширеність САН в Україні», в рамках якого проводяться обстеження осіб із підозрою на САН, лабораторний скринінг батьків, дітей і родичів пацієнтів із САН. Як наслідок, кількість діагностованих випадків САН в Україні за останні 2 роки зросла майже вдвічі. Проте частота виявлення нових випадків САН в Україні все ще залишається вкрай низькою: станом на 2022 рік лише 80 осіб в Україні мають підтверджений діагноз, хоча орієнтовно кількість таких пацієнтів має становити не менше ніж 800.
Лікарю необхідно вміти відрізняти ангіоневротичний набряк при САН від набряків іншої етіології (анафілаксія, алергічна реакція, інфекційні ураження шкіри тощо), що особливо стосується набряку гортані й абдомінального набряку.
В разі набряку гортані внаслідок анафілактичної реакції в анамнезі є алергія, а сам набряк супроводжують інші клінічні ознаки анафілаксії (зниження тиску, бронхообструктивний синдром, риніт, кон’юнктивіт). При алергічному ангіонабряку клінічні прояви розвиваються швидко (відсутнє повільне прогресування набряку протягом 3-4 год, як при САН).
Алергічний ангіонабряк, оскільки є гістамінозалежним, часто супроводжується зудом, еритемою, уртикарією.
Інфекційні та автоімунні захворювання, якщо і проявляються ангіонабряком, мають відповідну супутню клінічну картину. Для бешихи і флегмони є характерним напруження шкіри, біль, лихоманка. У випадку системного червоного вовчака й інших колагенозів пацієнт може мати обтяжений анамнез системного захворювання зміни відповідних лабораторних показників. Гострий контактний дерматит пов’язаний із впливом на шкіру подразнювального агента, характеризується інтенсивним зудом. Ідіопатичний набряк калитки в дітей має невідому етіологію, втім, набряк обмежується винятково ділянкою калитки. Синдром Мелькерсона – Розенталя: рецидивуючий набряк обличчя (і тільки обличчя), рецидивуючий периферичний парез N. facialis і тріщини на язиці; при САН клінічні прояви різноманітні.
Алгоритм обстеження пацієнта з ангіоневротичним набряком:
- молекулярна алергодіагностика;
- бактеріальні посіви, особливо за наявності лихоманки і болю в горлі;
- визначення концентрації тиреоїдних гормонів;
- визначення концентрації та функції інгібітора С1-естерази і C3 та C4 компонентів комплементу;
- дослідження калу на яйця гельмінтів і паразитів;
- загальний аналіз крові з формулою, визначенням ШОЕ, АНА (особливо якщо в пацієнта є артрит або інші ознаки дифузних захворювань сполучної тканини).
Рецидивуючі набряки, що свідчать про високу імовірність САН, мають типові характеристики: асиметричність, відсутність свербежу, дефігурація набряклої частини тіла (найчастіше спотворення обличчя), висока щільність набряку, відсутність кропив’янки, чіткого зв’язку з алергеном, сімейна історія схожого захворювання, набряки повільно проходять (набряки підшкірної клітковини регресують упродовж 2-5 днів, у разі локалізації набряку в черевній порожнині характерні абдомінальні симптоми, які регресують впродовж 12-24 год), відсутня або сумнівна відповідь на АГП й кортикостероїди, наявність періодичних безпричинних нападів абдомінального болю з дитячого віку.
У випадку абдомінальної локалізації набряк дуже болісний, розпираючий зсередини. У зв’язку з накопиченням великої кількості рідини у черевній порожнині живіт може збільшуватися в декілька разів, що загрожує розвитком гіповолемічного шоку. Пацієнти спостерігають виражений біль у ділянці серця, за грудиною, в черевній порожнині, внизу живота (залежно від локалізації набряку). Набряки черевної порожнини належать до тяжких через значний вплив на якість життя пацієнтів. Через сильний розпираючий біль пацієнти не йдуть на роботу чи на навчання, ледь пересуваються квартирою та часто не можуть зробити навіть кількох кроків.
Інтенсивний біль у животі, який розвивається в ≈93% пацієнтів із САН, може імітувати гостру хірургічну патологію та навіть стати причиною проведення оперативних втручань; близько 25% хворих до моменту встановлення діагнозу САН переносять оперативні втручання, пов’язані із сильним абдомінальним болем. Окрім вираженого абдомінального болю, напад може зумовити нудоту, блювання, діарею. Тривалість болю зазвичай становить від 2 до 4 днів. При таких нападах клінічно важко диференціювати САН із гострою хірургічною патологією, адже патогномонічні зміни органів ШКТ при цьому захворюванні відсутні. Утім, деякі автори описують такі зміни в черевній порожнині під час абдомінального нападу САН: наявність вільної рідини та потовщення стінок кишечнику за даними УЗД та КТ. Також слід звернути увагу на відсутність істотних відхилень у стандартних лабораторних аналізах під час нападу САН і, що дуже важливо, сімейний анамнез подібних рецидивуючих клінічних симптомів із появою періодичних набряків іншої локалізації.
Клінічний випадок
Представлений клінічний випадок чоловіка віком 40 років (військовослужбовець) відрізняється нетиповими проявами САН. Через те що «видимі» набряки шкіри (кінцівок, обличчя і навіть гортані) в хворого виникали вкрай рідко (1-2 набряки на рік, після фізичної роботи, перевтоми, на тлі ГРВІ чи гострого тонзиліту), щодо них пацієнт не звертався по медичну допомогу, а інколи звертався до лікаря через періодичні болі в животі ріжучого характеру, інтенсивні, що часто супроводжувалися блюванням і нудотою, метеоризмом, деформацією стінки черевної порожнини та турбували його з пубертатного віку (13 років). Такі болі непокоїли пацієнта досить часто (2-4 р/міс) і дуже заважали нести військову службу. Пацієнт неодноразово мусив звертатися по допомогу до гастроентеролога, адже прийом знеболювальних, АГП, спазмолітичних препаратів не був ефективним. Під час детальнішого обстеження спостерігався позитивний тест на Helicobacter pylori, на основі якого було встановлено діагноз еритематозної гастродуоденопатії. Згодом була проведена відповідна ерадикаційна терапія. Частота загострень дещо знизилася, втім, це мало вплинуло на перебіг та інтенсивність больового синдрому.
Під час фіброгастродуоденоскопії (ФГДС) щодо подальшого нападу гострого болю в животі, шлунку було виявлено набряк слизової, зменшення перистальтики та значну кількість рідини у шлунку – 500 мл (за норми натще – 50-100 мл), що згодом наштовхнуло лікаря-гастроентеролога на думку провести спрямовану діагностику САН.
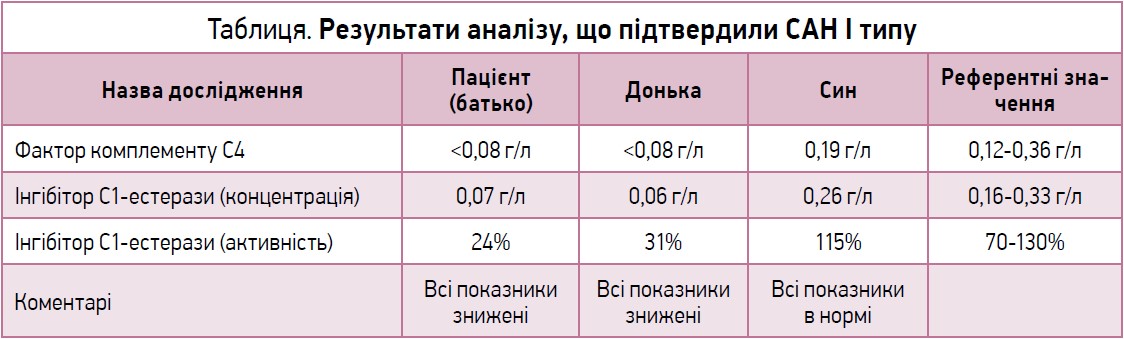
Отримані результати підтвердили САН І типу (табл.).
Порівнюючи локалізацію і частоту набряків у цього пацієнта протягом року зі статистичними даними, можемо відмітити суттєву різницю. У хворого превалюють (виникають майже на 50% частіше) набряки черевної порожнини (85%), які супроводжують тяжкий перебіг САН. Набряки рук, ніг та обличчя мають місце значно рідше – в 5% випадків кожної із цих локалізацій, тому встановити діагноз було надто складно.
Дуже важливе спостереження провели наші польські колеги в 40 пацієнтів із САН під час абдомінального нападу. Пацієнтам проводили ультразвукову діагностику (УЗД) органів черевної порожнини та малого таза протягом перших 6 год після від початку нападу та повторювали ці дослідження під час ремісії.
Крім того, за наявності гострих абдомінальних симптомів вони виконували комп’ютерну томографію (КТ) органів черевної порожнини та малого таза (23 випадки). Отримані результати УЗД та КТ свідчать про транзиторну наявність значної кількості вільної рідини в черевній порожнині та набряк кишечнику під час прогресування абдомінальних симптомів і спонтанне зникнення набряку після покращення стану пацієнтів.
Схожу картину набряку ШКТ ми спостерігали і при виконанні УЗД, ФГДС під час розвитку больового синдрому, блювання: «Шлунок містить натще до 500 мл секреторної рідини. Слизова оболонка шлунка і дванадцятипалої кишки вогнищево-гіперемована. Перистальтика зменшена. Складки виражені».
Слід зазначити, що антихелікобактерна терапія сприяла певному покращенню самопочуття пацієнта і зменшення частоти та інтенсивності нападів. Це збігається з дослідженням 65 хворих із САН угорського центру Земмельвейського університету. Науковці продемонстрували, що успішна ерадикація Helicobacter pylori супроводжується значним зменшенням кількості нападів у пацієнтів із САН. Отже, скринінг хворих із САН на інфекцію Helicobacter pylori є виправданим, оскільки ерадикація Helicobacter pylori може спричинити помітне зменшення тяжкості перебігу захворювання.
Напади абдомінального болю в нашого пацієнта здебільшого були високої інтенсивності та змушували проводити в ліжку декілька днів. Описана тяжкість проявів симптомів корелює з дослідженням німецького Центру із САН, де ретроспективно спостерігали загалом 33 671 абдомінальний напад у 153 пацієнтів із САН. Під час аналізу симптомів, перебігу, частоти нападів та ускладнень було виявлено, що співвідношення легких, середніх, тяжких нападів становило 1:1,4:5,6. Отже, більшість абдомінальних нападів при САН мають тяжкий перебіг, призводять до тимчасової втрати працездатності та суттєво знижують якість життя. Розуміння того, що набряки ШКТ у більшості випадків тяжкі, може допомогти в ранньому розпізнаванні нападу та покращити клінічне лікування.
Після встановлення діагнозу САН були обстежені діти пацієнта; в старшої доньки (17 років) підтверджено діагноз спадкового ангіонабряку І типу, хоча її турбують періодично тільки болі ШКТ, які родина пов’язувала з періодичними болями перед менструацією; набряків шкіри ще не було.
Саме з набряків черевної порожнини може розпочинатися захворювання в дітей, супроводжуючись болями протягом декількох днів. Імітуючи клініку гострого живота, пацієнти можуть потрапити на операційний стіл із діагнозом апендициту, непрохідності кишечнику та іншими захворюваннями, що потребують невідкладної хірургічної допомоги. Також часто встановлюють помилкові діагнози таких гастроентерологічних захворювань, як непереносимість глютену, лактозна недостатність, гельмінтози, хелікобактерна інфекція, що призводить до подальшого тривалого й неефективного лікування.
Пацієнти можуть роками приймати непотрібні їм лікарські засоби майже без жодного ефекту (частіше знеболювальні, спазмолітичні, АГП та глюкокортикоїди).
Багато років консультуючи, підтримуючи, опікуючись пацієнтами із САН, доводилося часто мати справу з, так би мовити, байдужістю пацієнта до свого стану, своєї хвороби, яка робить людину замкненою у своєму середовищі, часто – без належного розуміння та підтримки з боку родини й оточення. Серед хворих є багато самотніх людей, які пережили смерть найближчих родичів (батька, матері, брата, сестри або навіть власної дитини).
Тривалий час у світі не існувало ефективних препаратів для лікування САН. І єдиною можливістю допомогти пацієнтам було застосування свіжозамороженої плазми, однак такий підхід асоціюється з ризком вірусної контамінації та посиленням тяжкості нападу. Першим препаратом, схваленим Управлінням з контролю за якістю продуктів харчування та лікарських засобів (FDA) для лікування САН, став інгібітор С1-естерази плазмового походження для внутрішньовенного введення. Сьогодні цей препарат доступний і для українських пацієнтів із САН, що у випадку вчасної діагностики може суттєво змінити якість життя та долю таких людей. Препарат дозволяє хворим жити без постійного очікування нового нападу, надає можливість вільно планувати своє переміщення або знаходитися (за потреби) в довготривалій ізоляції, що в часи війни з кожним днем стає актуальнішим.
Висновки
- Через різну локалізацію набряку під час нападу САН є значні труднощі в диференційній діагностиці цього захворювання.
- Рецидивуючі набряки різної локалізації, що не реагують на АГП та глюкокортикоїди, можуть бути проявом САН і приводом для обстеження стану системи комплементу (рівень С4, рівень й функція С1-інгібітора).
- Абдомінальні напади САН відрізняє від інших гострих станів наявність вільної рідини в черевній порожнині та потовщення стінок кишечнику на тлі відсутності виражених змін у стандартних лабораторних аналізах.
- В Україні існує та розвивається система діагностики і забезпечення лікуванням пацієнтів із САН.
- САН за етіологією є первинним імунодефіцитом з ураженням системи комплементу. Тому у випадку підозри на САН проконсультуйте пацієнта в імунолога.
Література
1. Richard G. Gower WAO Journal 2011; 4: S9-S21.
2. Maurer M. et al. Allergy. 2018: doi:10.1111/all.1338.
3. Хавнюков О.О., Гашинова К. Ю., Євстігнєєв І. В., Дитятковська Є. М., Єгудіна Є. Д., Кравченко О. І., Хмель О. С. Імунодефіцитні стани у клінічній практиці: Навчальний посібник для практичних занять та самостійної роботи. – Дніпро: 2019 р. ISBN.
4. Клінічна оцінка, діагностичне та прогностичне значення результатів лабораторних досліджень, Катеренчук І. П., 2019 р.
5. Abdominal and pelvic imaging in the diagnosis of acute abdominal attacks in patients with hereditary angioedema due to C1-inhibitor deficiency Piotr Obtułowicz 1, Marcin Stobiecki 2 3, Wojciech Dyga 2 3, Aldona Juchacz 4, Tadeusz Popiela 1 5, Krystyna Obtułowicz 2 3 2022 Aug; 39 (4): 749-756.doi: 10.5114/ada.2021.108438. Epub 2021 Aug 1.
6. Helicobacter pylori infection as a triggering factor of attacks in patients with hereditary angioedema. Beata Visy, George Fust, Anette Bygum. PMID:17493006DOI: 10.1111/j.1523-5378.2007.00501.x.
7. Bork K., Staubach P., Eckardt A. J., Hardt J. Симптоми, перебіг та ускладнення абдомінальних нападів при спадковому ангіоневротичному набряку внаслідок дефіциту інгібітора С1. Am J Gastroenterol. 2006 рік; 101:619-627.
За підтримки ТОВ «Такеда Україна».
VV-MEDMAT-80023
Медична газета «Здоров’я України 21 сторіччя» № 18-19 (535-536), 2022 р.