24 грудня, 2021
Питання стабільності лікарських препаратів: фокус на таблетовану форму левотироксину
Всесвітня організація охорони здоров’я (ВООЗ) визначила забезпечення якості як широку концепцію, що охоплює всі питання, які окремо або разом впливають на якість продукту. Його стабільність під час дистрибуції до моменту, коли він потрапить до користувача, є одним із параметрів якості. Фармакопея США (United States Pharmacopeia, USP) стабільність лікарських засобів (ЛЗ) визначає як здатність продукту зберігати у встановлених межах і впродовж усього періоду зберігання і використання (тобто терміну придатності) ті самі властивості і характеристики, які він мав на момент виробництва.
Ключові слова: левотироксин; стабільність; фотостабільність; ефективність і безпека; фармакопея; USP.
Стабільність ЛЗ
Стабільність продукту пов’язана з його стійкістю до різних хімічних, фізичних і мікробіологічних реакцій, які можуть змінити вихідні властивості препарату під час транспортування, зберігання й використання. Іншими критеріями стабільності є вплив згаданих змін на придатність продукту до використання як ЛЗ. Стабільність часто виражається кількісно у вигляді терміну придатності, тобто часу, протягом якого ЛЗ, як передбачається, залишається придатним для використання за призначенням за певних умов зберігання.
Термін придатності
Термін придатності ЛЗ, які зберігаються в закритій тарі відповідно до зазначених умов, зазвичай визначають від дати виробництва або приготування до моменту, коли первинна активність або вміст активного фармацевтичного інгредієнта зменшується на 10%. Цей показник відомий як t10% або (t90%). Хоч визначати термін придатності виключно з точки зору хімічної стабільності активної складової видається доцільним, важливо, щоб під час зберігання продукту не порушувалися й інші бажані властивості ЛЗ.
Фактори, що впливають на стабільність продукту
Кожен інгредієнт, як терапевтично активний, так і фармацевтично необхідний, може впливати на стабільність лікарської субстанції та лікарських форм. Розглянемо, які саме чинники впливають на стабільність ЛЗ:
- фактори довкілля, які можуть зменшувати стабільність ЛЗ: несприятливі для зберігання температура, світло, вологість, вміст кисню і вуглекислого газу;
- фактори, пов’язані з лікарською формою: у лікарських формах реакції призводять до нестабільності ЛЗ і зменшення вмісту активного фармацевтичного інгредієнта. Зазвичай це відбувається без явних змін зовнішнього вигляду чи запаху продукту.
Хімічні властивості левотироксину натрію
Левотироксин натрію (раніше у Великій Британії називався тироксин натрію) – це натрію (2S)-2-аміно‑3-[4-(4-гідрокси‑3,5-дийодфенокси)-3,5-дийодфеніл] пропаноат. Діапазон оптичного обертання левотироксину натрію становить +16-20.
Стабільність левотироксину натрію
Тироксин стабільний при сухому повітрі, але руйнується під впливом світла, тепла й вологості. У деяких країнах траплялися випадки, коли таблетки тироксину виявлялися нестабільними навіть за кімнатної температури і для збереження питомої активності потрібна була температура зберігання 8-15 °C. У США FDA виявило проблему, пов’язану зі стабільністю і терапевтичною активністю тироксину для перорального застосування. Тому дуже важливо, щоб таблетки тироксину зберігалися в оригінальній упаковці та в сухому прохолодному місці.
Термін придатності таблеток тироксину, наприклад, австралійського виробництва становить 1 рік із дати виробництва. З огляду на те що флакон містить 200 таблеток, цілком можливо, що термін придатності може закінчитися до завершення курсу лікування. Незабаром стане доступною нова упаковка з терміном зберігання 18 міс; ця форма випуску потребує постійного зберігання в холодильнику.
Цілі дослідження
Левотироксин натрію має вузький терапевтичний індекс. Тому особливо важливо, щоб кількість активного фармацевтичного інгредієнта в таблетованій формі відповідала вказаній, оскільки необхідно ретельно титрувати дозу. Завданнями наведеного дослідження є вивчення таблетованої форми левотироксину натрію, а саме:
1. Оцінка стабільності в реальному часі.
2. Вивчення фотостабільності.
Матеріали і методи
У дослідженні порівнювали стабільність лікарських форм левотироксину натрію різних виробників між собою та зі стандартними зразками.
Стандартні зразки
- Стандартний зразок левотироксину натрію; партія № A010445003, питома активність становила 99,99%, виготовлено Acros Organic (Бельгія).
- Стандартний зразок ліотироніну; партія № A010434001, питома активність становила 99,95%, виготовлено Acros Organic (Бельгія).
Калібрувальна крива
Концентрації 10-100 мкг/мл отримували зі свіжоприготованого розчину (А) шляхом серійного розведення, використовуючи як розчинник розчин метанол:вода (1:1). Кількісний аналіз цих розчинів проводили за допомогою ВЕРХ, описаної раніше. Кожен зразок вводили двічі та отримували площу під піком, що відповідала кожному введенню для кожної концентрації. Процедуру повторювали тричі.
Було проведено аналіз та оцінку однорідності вмісту таблеток левотироксину натрію з використанням методу ВЕРХ, описаного в Британській фармакопеї (ВР).
Дослідження стабільності – було здійснено два типи досліджень стабільності таблетованої форми левотироксину натрію:
фотостабільність таблеток левотироксину натрію оцінювали за допомогою таблеток L-тироксин натрію. Таблетки зберігали в закритому скляному посуді на прямому сонячному світлі протягом 10 днів. Після цього проводили аналіз: виміряли точну вагу і подрібнили 10 таблеток (використовуючи ступку і товкач). Масу порошку, еквівалентну приблизно 100 мкг левотироксину натрію, перенесли в кількісному співвідношенні в колбу об’ємом 10 мл зі скляного бурштину, за допомогою ультразвуку розчинили в розчиннику, що містить метанол і 0,1 М гідроксиду натрію (1:1), а потім струшували протягом 15 хвилин. Об’єм довели до необхідного за допомогою того самого розчинника, що й контрольний розчин, так само приготували розчин, використовуючи 10 таблеток із тієї самої партії, що зберігалися за кімнатної температури; потім провели порівняльний аналіз зі стандартним розчином левотироксину натрію.
Результати дослідження та їх обговорення
Аналіз і визначення однорідності вмісту таблеток левотироксину натрію. Було проведено аналіз трьох лікарських засобів і визначення однорідності їхнього вмісту за допомогою методу ВЕРХ ВР; кількісне визначення проводили тричі в різні дні, відносне стандартне відхилення (СВ) для всіх результатів становило <2%.
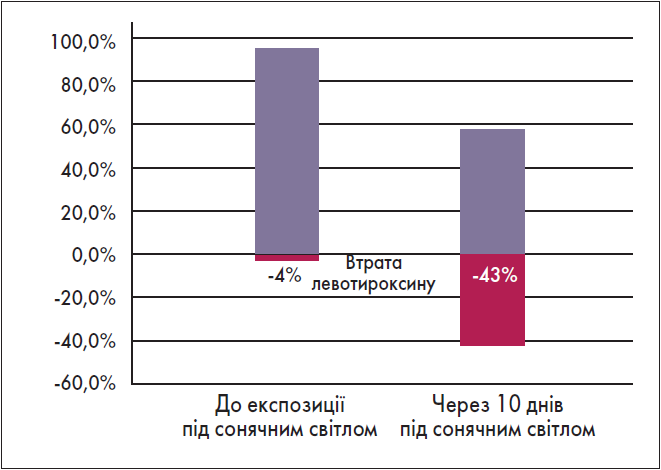
Рис. Аналіз таблеток левотироксину при зберіганні під прямим сонячним світлом протягом 10 днів, отриманий методом ВЕРХ
Фотостабільність таблеток левотироксину натрію. Аналіз таблеток левотироксину натрію, які зберігали в закритому скляному посуді під прямими сонячними променями впродовж 10 днів, виявив значущий вплив сонця на стабільність левотироксину навіть у твердій лікарській формі (рис.); результати, отримані методом ВЕРХ, наведені в таблиці.
Ці результати підтверджують рекомендації BP і USP щодо зберігання таблеток левотироксину натрію в щільному контейнері, захищеному від світла. Тироксин натрію залишається стабільним в умовах сухого повітря, але під впливом світла він може набувати рожевого кольору. Світлове і гамма-опромінення тироксину, розведеного у водному розчині, спричинює його дейодування і перетворення на інші йодовані органічні молекули.
Результати, отримані після екстракції тироксину з натрію (під час аналізу стабільності за допомогою ВЕРХ), показали, що рожеві таблетки в дозі 200 мкг одного виробника містять допоміжну речовину або допоміжні речовини, які прискорюють розпад тироксину. Цей каталітичний ефект, імовірно, відбувається за наявності світла.
Висновки
Левотироксин натрію не рекомендується поставляти у великих упаковках. Також необхідно обирати тип контейнера, аби забезпечити захист від сонячного світла, що має виражений вплив на стабільність навіть твердих лікарських форм левотироксину натрію.
На сьогодні в Україні єдиним препаратом левотироксину, що має захищене від світла пакування, є L-Тироксин від компанії «Берлін-Хемі». Завдяки світлозахисному блістеру фотодеградація не призводить до зменшення вмісту діючої речовини в таблетках, а це – гарантія стабільності дози L-Тироксину, яку отримує пацієнт. Таким чином, стабільність дозування дає можливість досягнути кращого контролю гіпотиреозу.
Реферативний огляд статті Ishraqa Mohamed et al. Stability of Levothyroxine Sodium Tablets Marketed in Sudan, J Pharm Biomed Sci, Vol. 06, № 05.
Підготувала Ганна Кирпач
Повну версію див.: http://lawarencepress.com/