26 жовтня, 2021
Клінічна ефективність та безпека цефоперазону/сульбактаму в лікуванні інтраабдомінальних інфекцій: систематичний огляд і метааналіз
Згідно з даними Всесвітньої організації охорони здоров’я, швидке зростання стійкості мікроорганізмів до антибактеріальних засобів є однією із ключових проблем охорони здоров’я. Так, відповідно до даних аналізу британських експертів (O’Neill J. et al., 2014), якщо ефективність антибіотиків (АБ) знижуватиметься так стрімко, до 2050 р. річна смертність унаслідок антибіотикорезистентності сягне 10 млн осіб. Для порівняння: станом на 2019 р. у США ≈35 тис. хворих померли унаслідок резистентних інфекцій (Centers for Disease Control and Prevention). У Європі, за оцінками експертів, невтішна статистика є схожою.
Інтраабдомінальні інфекції (ІАІ) – це тяжкі інфекційні захворювання, асоційовані з порушенням функцій багатьох органів і високою смертністю, яка складає, за різними даними, від 23 до 38% (Barie P. S. et al., 2004; Volakli E. et al., 2010; De Waele J. et al., 2014). Крім своєчасного й адекватного контролю джерел інфекції, обрання ефективних протимікробних засобів має важливе значення для лікування ІАІ. Відомо, що ІАІ можуть спричиняти, зокрема, деякі антибіотикорезистентні штами бактерій, що синтезують β-лактамазу розширеного спектра (ESBL) та штами Enterobacteriaceae, стійкі до карбапенему (Canto’n R. et al., 2018; Canto’n R. et al., 2019; Zhang H. et al., 2019; Lob S. H. et al., 2018; Lob S. H. et al., 2020).
Цефоперазон/сульбактам in vitro проявив потужну активність проти поширених грампозитивних бактерій, як-от Streptococcus spp. і золотистий стафілокок, чутливий до метициліну; грамнегативних бактерій, зокрема, Escherichia coli, Enterobacter cloacae та Klebsiella pneumoniae; декількох анаеробів (Sader H. S. et al., 2020; Appelbaum P. C. et al., 1993; Pfaller M. A. et al., 2017; Jean S. S. et al., 2017; Chiang T-T. et al., 2016; Wang F. D. et al., 2014). З додаванням сульбактаму цефоперазон in vitro продемонстрував посилену активність проти ESBL‑продукувальних Escherichia coli та Klebsiella pneumoniae і стійких до карбапенему Enterobacteriaceae й Acinetobacter baumannii (Lai C. C. et al., 2018; Lai C. C. et al., 2019).
Дослідники провели цей систематичний огляд і метааналіз з метою оцінки клінічної ефективності та безпеки застосування цефоперазону/сульбактаму порівняно з іншими АБ при лікуванні ІАІ.
Пацієнти та методи
Пошук робіт відбувався в базах даних PubMed, Cochrane, Web of Science, Ovid Medline та CKNI. Були включені лише клінічні дослідження, які порівнювали клінічну ефективність та безпеку цефоперазону/сульбактаму з іншими протимікробними препаратами при лікуванні пацієнтів з ІАІ.
Дослідження включали до метааналізу, якщо вони відповідали таким критеріям:
- у випробуванні брали участь пацієнти з ІАІ;
- в схемах терапії застосовувався цефоперазон/сульбактам;
- наявне порівняння з іншими схемами антибіотикотерапії;
- наявні результати ефективності, в т. ч. клінічні та мікробіологічні відповіді на терапію.
Критерії виключення:
- звіти про випадки;
- дослідження, в яких не повідомлялося про результати застосування цефоперазону/сульбактаму при лікуванні ІАІ;
- дослідження, в яких не порівнювалися результати застосування цефоперазону/сульбактаму з результатами інших схем антибіотикотерапії;
- фармакокінетичні дослідження;
- дослідження in vitro.
В метааналізі вивчали й узагальнювали такі дані:
- рік публікації;
- дизайн дослідження;
- схеми антибіотикотерапії (цефоперазон/сульбактам, цефтріаксон, кліндаміцин + гентаміцин, цефтазидим, амікацин, метронідазол, ципрофлоксацин, цефотаксим, моксифлоксацин, левофлоксацин, тинідазол);
- клінічні та мікробіологічні результати;
- розвиток побічних ефектів на тлі антибіотикотерапії.
Кінцевими точками визначено:
- клінічну ефективність, що передбачала клінічне покращення та/або одужання;
- клінічний успіх лікування, критеріями якого були терапія ІАІ лише передбаченими в дослідженні АБ без додавання інших антимікробних препаратів, відсутність рецидивів інфекції упродовж періоду спостереження;
- клінічну невдачу, яку фіксували за таких обставин:
а) необхідність призначення додаткових антибактеріальних засобів для контролю ІАІ;
б) наявність показань до хірургічного втручання;
в) смерть, пов’язана з інфекцією;
- мікробіологічну ефективність: усунення джерела інфекції або відсутність росту в культурах залишкових вогнищ інфекції;
- розвиток побічних ефектів.
Результати
Серед результатів пошуку, що налічували загалом 2974 публікації, відповідно до критеріїв було відібрано 12 робіт – 10 рандомізованих клінічних досліджень (РКД) і 2 ретроспективних дослідження. 5 випробувань були багатоцентровими, решта 7 – одноцентровими. 8 досліджень проведено в Китаї, 2 – в США, по 1 випробуванню – в Японії та Індії (Yura et al., 1985; Janregni et al., 1990; Greenberg et al., 1994; Zhou et al., 2004; Long et al., 2006; Chandra et al., 2008; Yang et al., 2010; Geng et al., 2012; Gao et al., 2013; Wang et al., 2013; Jiao et al., 2017; He et al., 2020) (табл.).
До метааналізу залучили 1674 пацієнтів, з яких 781 особа отримувала цефоперазон/сульбактам.
Загалом коефіцієнт клінічної ефективності цефоперазону/сульбактаму і порівнюваних АБ становив 87,7 та 81,7% відповідно. Цефоперазон/сульбактам асоціювався з вищою клінічною ефективністю, ніж контрольні препарати (ВР 1,98; 95% ДІ 1,31-3,00). Перевага цефоперазону/сульбактаму над препаратами порівняння залишалася незмінною в об’єднаному аналізі 10 РКД (ВР 1,89; 95% ДІ 1,18-3,03).
В об’єднаному аналізі досліджень, опублікованих до 2000 р., показник клінічної ефективності застосування цефоперазону/сульбактаму був зіставним з таким при використанні контрольних препаратів (ВР 1,69; 95% ДІ 0,44-6,52), після 2000 р. клінічна ефективність цефоперазону/сульбактаму була вищою, ніж у групі порівняння (ВР 2,03; 95% ДІ 1,43-2,88).
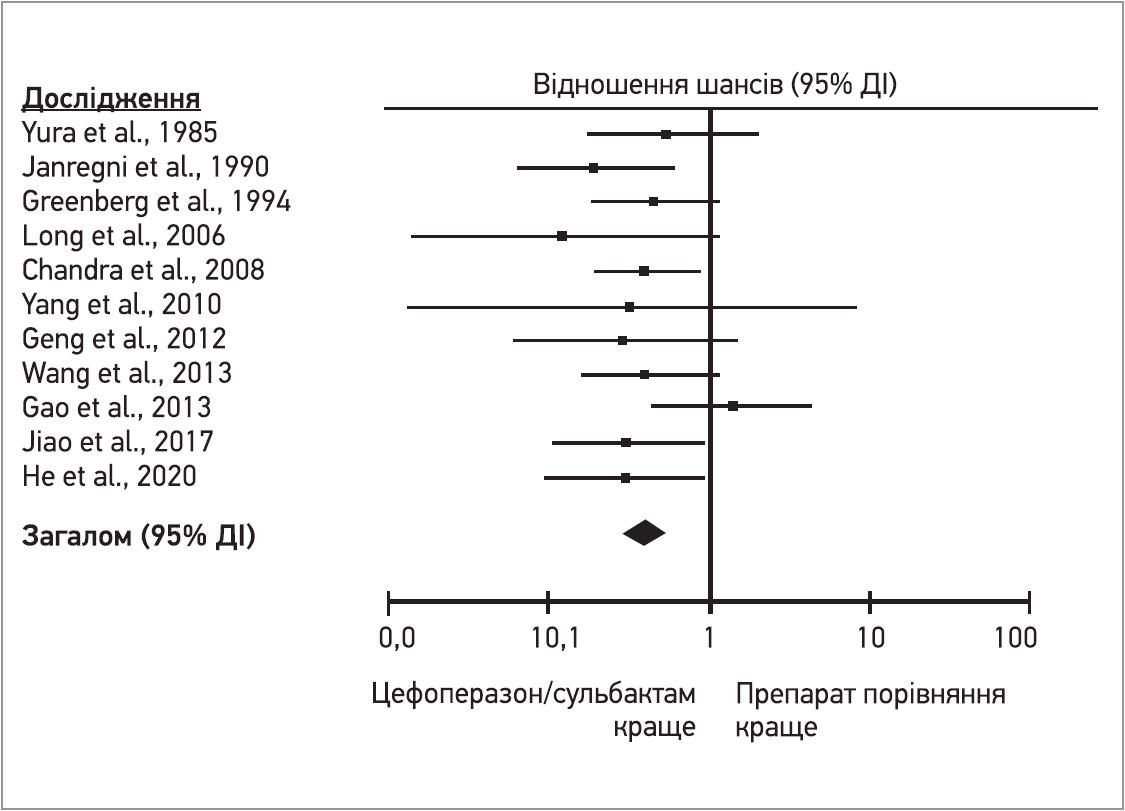
Згідно з локалізацією патологічного процесу, клінічна ефективність цефоперазону/сульбактаму була схожою з аналогічними показниками контрольної групи препаратів у пацієнтів з інфекцією жовчовивідних шляхів (ВР 1,76; 95% ДІ 0,83-3,75), спонтанними бактеріальними інфекціями (ВР 3,97; 95% ДІ 1,44-10,93) або іншими ІАІ (ВР 1,82; 95% ДІ 0,99-3,35; I2 = 51%). Слід зазначити, що клінічна ефективність цефоперазону/сульбактаму була зіставною з такою в терапевтичних схемах, що включали цефалоспорини III покоління, у підгрупі пацієнтів з інфекцією жовчовивідних шляхів (ВР 1,58; 95% ДІ 0,86-2,90) (рис. 1).
Рис. 1. Частота клінічної невдачі при застосуванні цефоперазону/сульбактаму та препаратів порівняння у лікуванні інтраабдомінальної інфекції
В 11 дослідженнях повідомлялося про клінічні невдачі; об’єднаний аналіз цих робіт продемонстрував, що схеми лікування із призначенням цефоперазону/сульбактаму асоціювалися з меншою частотою останніх порівняно з препаратами порівняння (ВР 0,40; 95% ДІ 0,28-0,57).
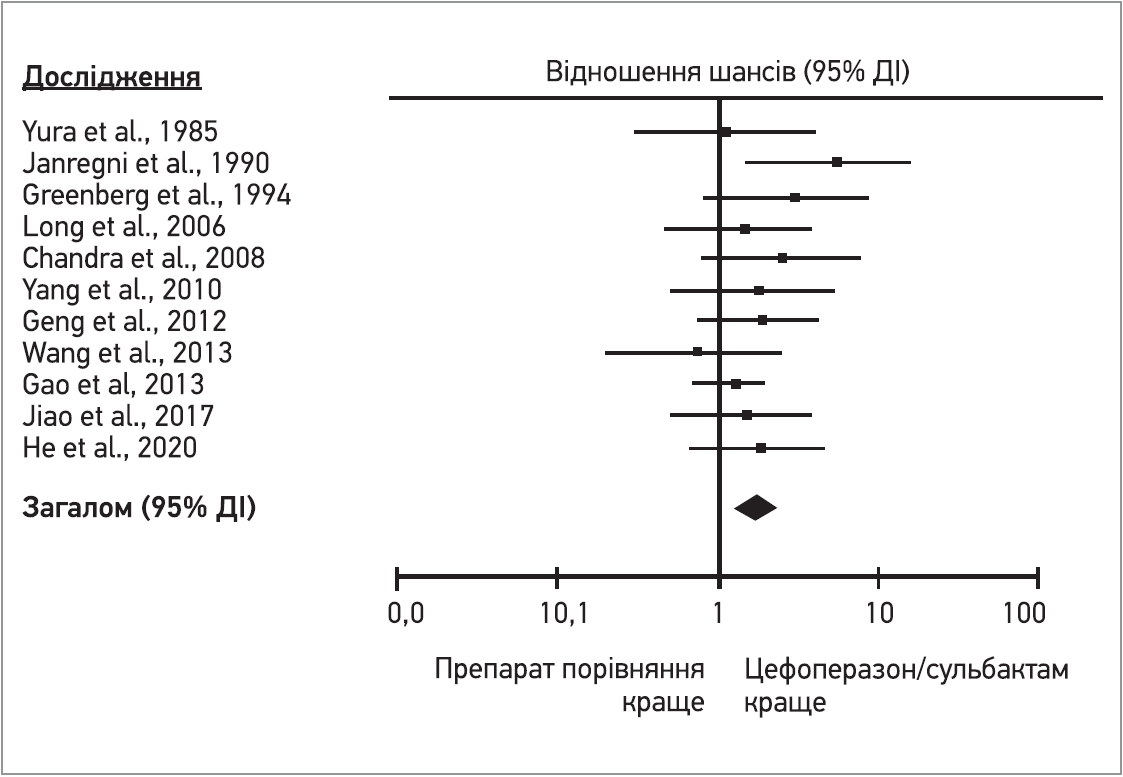
У 9 роботах вивчали, зокрема, терміни клінічного одужання. Згідно з об’єднаними результатами цих випробувань, лікування цефоперазоном/сульбактамом мало переконливі переваги щодо цієї кінцевої точки порівняно з іншими схемами антибіотикотерапії (ВР 1,54; 95% ДІ 1,17-2,03) (рис. 2)
Рис. 2. Частота клінічного одужання при застосуванні цефоперазону/сульбактаму та препаратів порівняння у лікуванні інтраабдомінальної інфекції
При узагальненні даних 7 РКД визначено, що в групі застосування цефоперазону/сульбактаму спостерігався вищий показник клінічного одужання (ВР 1,78; 95% ДІ 1,22-2,59) незалежно від популяції хворих.
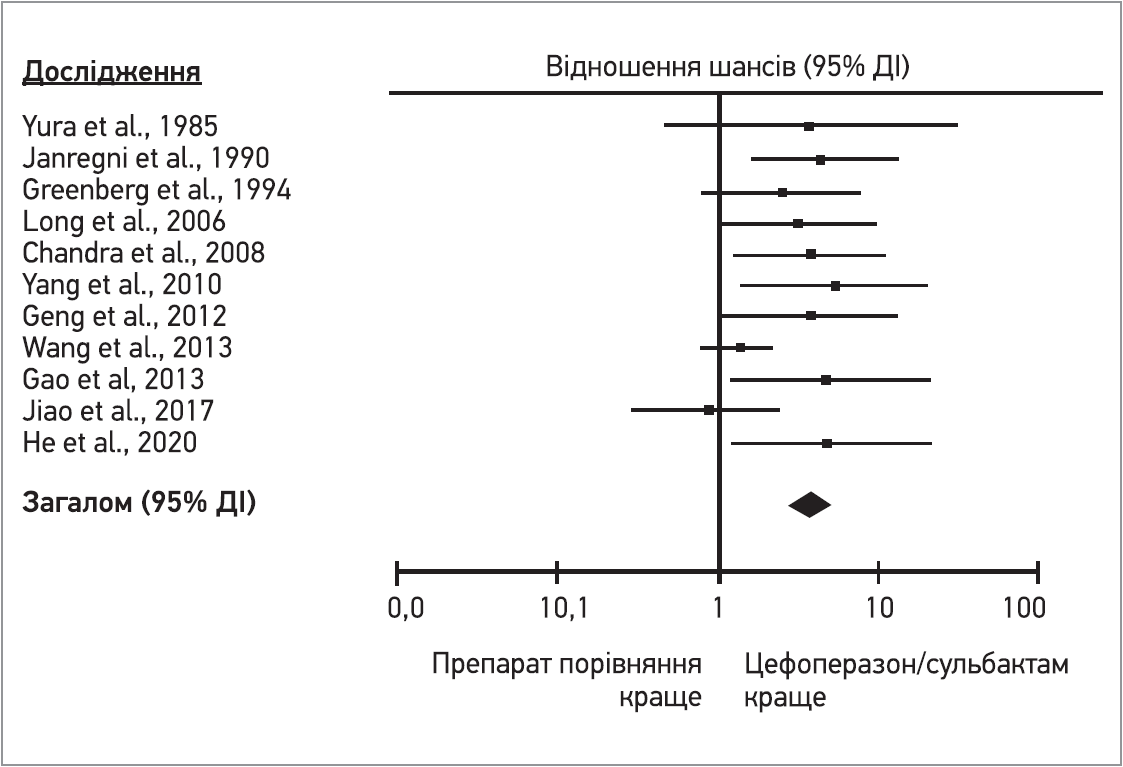
У 8 випробуваннях повідомлялося про ефективність досліджуваних препаратів щодо мікробіологічної ерадикації. Відповідно до даних об’єднаного аналізу результатів цих робіт при застосуванні цефоперазону/сульбактаму спостерігається швидша ерадикація збудника порівняно із препаратами порівняння (ВР 2,54; 95% ДІ 1,72-3,76) (рис. 3).
Рис. 3. Частота мікробіологічної ерадикації при застосуванні цефоперазону/сульбактаму та препаратів порівняння у лікуванні інтраабдомінальної інфекції
Після узагальнення даних щодо летальності пацієнтів з ІАІ та виникнення побічних ефектів на тлі застосування цефоперазону/сульбактаму і препаратів порівняння не виявлено суттєвої різниці для цих кінцевих точок (ВР 0,90; 95% ДІ 0,38-2,16 та ВР 1,07; 95% ДІ 0,74-1,55 відповідно).
Обговорення
У представленому метааналізі 12 клінічних досліджень за участю 1674 пацієнтів досліджували клінічну ефективність та безпеку цефоперазону/сульбактаму в лікуванні ІАІ. Результати об’єднаного аналізу продемонстрували вищу клінічну ефективність цефоперазону/сульбактаму по відношенню до антибіотиків порівняння. Крім того, свідчення вищої клінічної ефективності цефоперазону/сульбактаму були отримані в підгруповому аналізі 10 рандомізованих контрольованих досліджень, проведених у Китаї.
Частота клінічної ефективності в разі застосування цефоперазону/сульбактаму залишалася зіставною з відповідними показниками в контрольній групі (загальноприйнятий режим антибіотикотерапії, що включав цефалоспорин ІІІ покоління) як у дослідженнях, виконаних до 2000 року, так і в більш свіжих роботах.
Дослідники зазначають, що цефоперазон/сульбактам асоціювався з вищою частотою клінічного одужання, ніж терапія препаратами порівняння. Імовірність клінічної невдачі при застосуванні цефоперазону/сульбактаму, згідно з даними об’єднаного аналізу 12 досліджень та аналізів у підгрупах, виявилася нижчою за відповідні показники для препаратів порівняння. Подібна закономірність спостерігалася й щодо смертності, але ця різниця не досягла рівня статистичної значимості. Таким чином, цефоперазон/сульбактам за ефективністю не поступається альтернативним антибіотикам, які зазвичай використовуються в лікуванні ІАІ.
Посилаючись на отримані докази, автори метааналізу рекомендують застосовувати цефоперазон/сульбактам як один із варіантів терапії ІАІ [13].
У представленому метааналізі також оцінювали швидкість мікробіологічної ерадикації збудників у пацієнтів з ІАІ. Виявилося, що цефоперазон/сульбактам асоціюється зі значно вищою швидкістю ерадикації, ніж антибіотики порівняння. Отримані результати підтверджуються даними кількох інших досліджень, які також продемонстрували ефективність цефоперазону/сульбактаму щодо поширених збудників ІАІ [5, 6, 38].
Хоча в представленому метааналізі не оцінювали окремо ефективність цефоперазону/сульбактаму проти мікроорганізмів, які продукують β-лактамази розширеного спектра, низка досліджень in vitro (20,38) продемонструвала його високу активність щодо таких бактерій. Lai та співавт. [20] виявили, що 75,9% штамів К. pneumoniae та 91,4% штамів E. coli, які продукують β-лактамази розширеного спектра, залишаються чутливими до цефоперазону/сульбактаму. Shi та співавт. показали, що понад 50% штамів E. coli та K. pneumoniae були стійкими до цефалоспоринів ІІІ покоління або хінолонів, однак цефоперазон/сульбактам виявився активним in vitro проти цих двох поширених патогенів незалежно від наявності генів ESBL [38]. Ці результати зайвий раз переконують у доцільності застосування цефоперазону/сульбактаму в пацієнтів з ІАІ. Нарешті, дослідники оцінили безпеку застосування цефоперазону/сульбактаму для лікування пацієнтів з ІАІ. З’ясувалося, що цефоперазон/сульбактам не збільшує ризик виникнення побічних ефектів порівняно з альтернативними антибіотиками. Отже, цефоперазон/сульбактам можна вважати безпечним засобом для лікування пацієнтів з ІАІ.
Висновки
Цефоперазон/сульбактам асоціювався із кращою або порівнюваною клінічною ефективністю та вищими чи порівнюваними показниками клінічного одужання порівняно з іншими АБ, які застосовували в рамках 12 досліджень, включених до метааналізу. Частота клінічних невдач, летальних випадків і розвитку побічних ефектів при застосуванні цефоперазону/сульбактаму була схожою з такою при прийомі препаратів порівняння. Цефоперазон/сульбактам можна рекомендувати як ефективний (із прийнятним профілем безпеки) терапевтичний варіант для лікування ІАІ.
Довідка «ЗУ»
На вітчизняному фармацевтичному ринку комбінація цефоперазону та сульбактаму представлена у вигляді препарату Гепацеф Комбі виробництва АТ «Київмедпрепарат» (корпорація «Артеріум»). Цефоперазон належить до цефалоспоринів ІІІ покоління, дія якого пов’язана з пригніченням біосинтезу мукопептиду клітинної стінки. Сульбактам є незворотним інгібітором найважливіших β-лактамаз, які продукуються пеніцилін-резистентними мікроорганізмами.
Гепацеф Комбі випускається у флаконах; 1 флакон містить стерильної суміші цефоперазону натрієвої солі та сульбактаму натрієвої солі (1:1) у перерахуванні на цефоперазон – 1,0 г та сульбактам – 1,0 г. Звичайна доза препарату Гепацеф Комбі для дорослих становить 2-4 г/добу (тобто 1-2 г цефоперазону на добу) внутрішньовенно або внутрішньом’язово в рівномірно розподілених дозах кожні 12 годин.
Shao-Huan Lan, Chien-Ming Chao, Shen-Peng Chang, Li-Chin Lu, Chih-Cheng Lai. Clinical Efficacy and Safety of Cefoperazone–Sulbactam in Treatment of Intra-Abdominal Infections: A Systematic Review and Meta-Analysis. Surgical Infections.http://doi.org/10.1089/sur.2020.468. Online Ahead of Print:February 23, 2021
Підготувала Наталія Нечипорук