8 січня, 2024
Безпека застосування тестостерон-замісної терапії по відношенню до серцево-судинної системи

У статті представлено коментарі до дослідження TRAVERSE* , яке оцінювало ризик виникнення довгострокових серцево-судинних подій у чоловіків із гіпогонадизмом, що застосовують тестостерон-замісну терапію.
Ключові слова: гіпогонадизм, тестостерон, тестостерон-замісна терапія, основні несприятливі серцево-судинні події.
На сьогодні відсутні дані потужних рандомізованих досліджень щодо довгострокової ефективності та безпеки тестостерон-замісної терапії (ТЗТ) у чоловіків середнього і старшого віку, які мають вікове зниження рівня тестостерону.
У березні 2015 року Управління із санітарного нагляду за якістю харчових продуктів і медикаментів США (FDA) дійшло висновку про можливе підвищення ризику серцево-судинних ускладнень, пов’язаних із застосуванням ТЗТ. Це призвело до змін маркування у США всіх препаратів тестостерону, що відпускаються за рецептом, щоб звернути увагу на ймовірне підвищення ризику серцевих нападів та інсультів, пов’язаних із використанням зазначених лікарських засобів. Від виробників схвалених продуктів тестостерону вимагалося провести добре сплановане клінічне дослідження для вирішення питання про довгострокову безпеку ТЗТ.
У відповідь на вимогу FDA було розроблено дослідження з оцінювання тривалої ефективності й безпеки ТЗТ щодо серцево-судинних подій у чоловіків із гіпогонадизмом (TRAVERSE), профінансоване консорціумом виробників препаратів для TЗT на чолі з AbbVie у США.
Дизайн дослідження
Дослідження IV фази, багатоцентрове рандомізоване подвійне сліпе плацебоконтрольоване, дослідження не меншої ефективності в паралельних групах.
Пацієнти
Чоловіки середнього та старшого віку, від 45 до 80 років, із наявними серцевосудинними захворюваннями або високим ризиком їх виникнення.
Критерії включення
Повідомлення пацієнта про один або більше симптомів гіпогонадизму (зниження сексуального потягу, або лібідо; послаблення спонтанної ерекції; зниження енергії або втома; низький або депресивний настрій; втрата пахвового чи лобкового волосся або зменшення кількості процедур гоління; припливи).
Симптоми гіпогонадизму в учасників дослідження були лабораторно підтверджені: рівень тестостерону в сироватці крові натще серце становив ˂300 нг/дл (10,4 нмоль/л) на основі двох надійних вимірювань.
Критерії виключення
• Вроджений або тяжкий гіпогонадизм – рівень тестостерону ˂ 100 нг/дл (3,5 нмоль/л)
• Рак передміхурової залози або вузли у тканині передміхурової залози в анамнезі
• Підвищений рівень простатспецифічного антигену ˃3,0 нг/мл
• Тромбофілія, неспровокований тромбоз глибоких вен або емболія легеневої артерії в анамнезі
• Поліцитемія (гематокрит ≥54%)
• Неконтрольована серцева недостатність, гіпертонія або діабет
• Неконтрольований серйозний психічний розлад або ризик суїциду
• Гострий коронарний синдром, інсульт або коронарна чи периферична реваскуляризація за останні 4 місяці
• Лікування препаратами тестостерону або андрогенними стероїдами протягом останніх 6 місяців
Рандомізацію проводили у співвідношенні 1:1 для щоденного застосування 1,62% тестостерон-вмісного гелю Андрожель (n=2596) або відповідного плацебо (n=2602). Первинною серцево-судинною кінцевою точкою був час від рандомізації до першої появи будь-якого компонента основних несприятливих серцево-судинних подій (ОНСП), який визначався як комбінація наступного: (1) смерть від серцево-судинних причин, (2) нефатальний інфаркт міокарда, (3) нефатальний інсульт. Критерій не меншої ефективності вимагав верхньої межі відношення ризиків (ВР) ˂1,5 для 95% довірчого інтервалу (ДІ) серед пацієнтів, які отримували щонайменше одну дозу тестостерону або плацебо.
Результати
• Пацієнти отримували лікування протягом 21,7±14,1 місяця і знаходилися під спостереженням протягом 33,0±12,1 місяця (середнє значення ± стандартне відхилення).
• Загалом 61,4 і 61,7% пацієнтів припинили лікування в групах ТЗТ і плацебо відповідно.
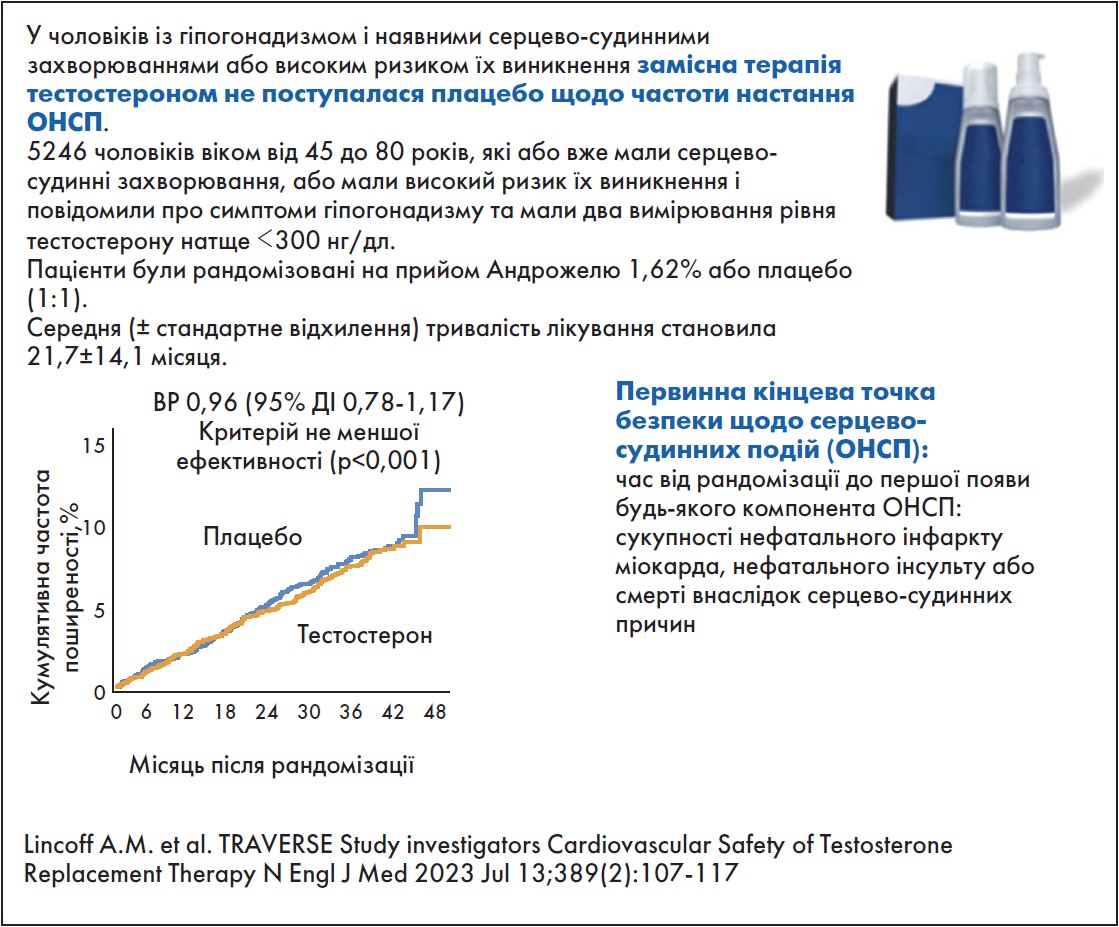
• Первинна серцево-судинна кінцева точка спостерігалася у 182 (7,0%) пацієнтів у групі, яка отримувала тестостерон, та у 190 (7,3%) чоловіків у групі плацебо (ВР 0,96; 95% ДІ 0,78-1,17; p˂0,001 для не меншої ефективності) (рисунок).
• Згідно з аналізом, у чоловіків із гіпогонадизмом і наявними серцево-судинними захворюваннями або високим ризиком їх виникнення ТЗТ не поступалася плацебо у частоті настання ОНСП.
• Не було виявлено жодних клінічно значущих відмінностей між групами лікування щодо частоти настання вторинних серцево-судинних подій, пов’язаних із безпекою, або окремих компонентів ОНСП.
Рис. Результати дослідження TRAVERSE: порівняння показників первинної кінцевої точки щодо виникнення ОНСП між групами лікування
Значення для клінічної практики
• Результати дослідження TRAVERSE надають переконливі докази кардіоваскулярної безпеки ТЗТ у чоловіків середнього та старшого віку із гіпогонадизмом, навіть з установленими серцево-судинними захворюваннями або кількома факторами ризику виникнення несприятливих серцево-судинних подій.
* Детальна інформація представлена в оригіналі: LincoffA.M. et al. TRAVERSE Study Investigators. Cardiovascular Safety of Testosterone-Replacement Therapy. N Engl J Med. 2023 Jul 13;389(2):107-117.
Тематичний номер «Урологія. Нефрологія. Андрологія» № 4 (31), 2023 р.