16 січня, 2019
Тиреоїдити: питання діагностики та лікування
За матеріалами Школи ендокринолога, 13-14 вересня, Львів
У рамках освітнього проекту «Школа ендокринолога» 13-14 вересня у Львові провідні фахівці галузі представили доповіді з найактуальніших питань, що стосуються хвороб залоз внутрішньої секреції.
Доцент кафедри ендокринології з курсом післядипломної освіти Вінницького національного медичного університету ім. М. І. Пирогова, кандидат медичних наук Анатолій Васильович Паламарчук присвятив свій виступ діагностиці та лікуванню тиреоїдитів.
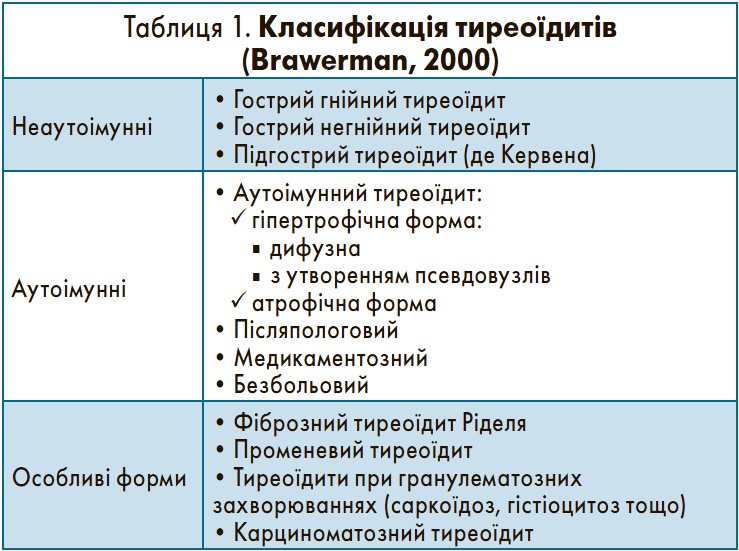
 – Термін «тиреоїдити» охоплює захворювання щитоподібної залози (ЩЗ), які відрізняються за етіологією та патогенезом, характеризуються різними змінами розмірів, структури і функції ЩЗ, але об’єднані таким патогенетичним компонентом, як запалення. Класифікація тиреоїдитів за Brawerman представлена в таблиці 1.
– Термін «тиреоїдити» охоплює захворювання щитоподібної залози (ЩЗ), які відрізняються за етіологією та патогенезом, характеризуються різними змінами розмірів, структури і функції ЩЗ, але об’єднані таким патогенетичним компонентом, як запалення. Класифікація тиреоїдитів за Brawerman представлена в таблиці 1.
Підгострий гранулематозний тиреоїдит де Кервена
Підгострий гранулематозний тиреоїдит де Кервена (ПГТ) – негнійне запалення ЩЗ, описане в 1904 р. французьким патологоанатомом де Кервеном. Частка ПГТ в структурі захворювань ЩЗ дорівнює 1-2%. Жінки хворіють у 4-6 раз частіше за чоловіків, зазвичай хвороба розвивається у віковому періоді 30-50 років. Найімовірнішою причиною ПГТ вважається вірусна інфекція. Підтвердженням вірусної етіології захворювання можуть бути такі факти, як анамнестичний зв’язок з вірусною інфекцією, що передувала хворобі (грип, аденовірусна інфекція, кір тощо), збільшення кількості випадків хвороби на тлі спалахів вірусної інфекції в осінньо-зимовий період, наявність у хворих високих титрів антитіл (АТ) до вірусу Коксакі, аденовірусів, вірусів грипу, піковірусів. Утім, специфічних вірусів, що зумовлюють ПГТ, не виявлено.
У ролі фактора ризику розвитку ПГТ можуть розглядатися вогнища хронічної інфекції в ділянці носоглоткового лімфатичного кільця. Слід зазначити, що схильність до ПГТ генетично детермінована (в осіб, які перехворіли на ПГТ, виявляють антигени гістосумісності HLA BW35 та DR35).
 Початок захворювання зазвичай є гострим: через 3-6 тиж після перенесеної вірусної інфекції з’являється біль у ділянці шиї, який іррадіює в нижню щелепу, вуха, потиличну поверхню шиї; посилюється при повертанні голови, ковтанні, кашлі. Іншими симптомами є слабкість, пітливість, головний біль, нервовість, підвищення температури тіла до 38-39 °С. Пальпаторно ЩЗ або одна з її часток збільшена, щільна та болюча; спостерігається міграція болю з однієї частки в іншу. Шкіра над ЩЗ або не змінена, або гіперемійована внаслідок рефлекторного розширення судин. Периферійні лімфатичні вузли здебільшого не змінені. Близько 50% пацієнтів з ПГТ мають початкову тиреотоксичну фазу через вивільнення тиреоїдних гормонів з ушкоджених фолікулярних клітин ЩЗ.
Початок захворювання зазвичай є гострим: через 3-6 тиж після перенесеної вірусної інфекції з’являється біль у ділянці шиї, який іррадіює в нижню щелепу, вуха, потиличну поверхню шиї; посилюється при повертанні голови, ковтанні, кашлі. Іншими симптомами є слабкість, пітливість, головний біль, нервовість, підвищення температури тіла до 38-39 °С. Пальпаторно ЩЗ або одна з її часток збільшена, щільна та болюча; спостерігається міграція болю з однієї частки в іншу. Шкіра над ЩЗ або не змінена, або гіперемійована внаслідок рефлекторного розширення судин. Периферійні лімфатичні вузли здебільшого не змінені. Близько 50% пацієнтів з ПГТ мають початкову тиреотоксичну фазу через вивільнення тиреоїдних гормонів з ушкоджених фолікулярних клітин ЩЗ.
Клінічні форми ПГТ, за de Luca і співавт., включають фульмінантну (різко виражені прояви запалення, швидкий перебіг), пролонговану (повільний розвиток симптомів, субфебрилітет, відсутність симптомів інтоксикації, незначна болючість в ділянці шиї), псевдотиреотоксичну (ознаки підвищеної функції ЩЗ), псевдонеопластичну (виражене ущільнення, швидке збільшення ЩЗ).
Стадії зміни функції ЩЗ в разі ПГТ можна розподілити на:
- ранню тиреотоксичну – триває 2-3 тиж, супроводжується клінікою тиреотоксикозу при низьких цифрах захоплення залозою I131;
- перехідну – триває 2-3 тиж, перебіг на еутиреоїдному фоні;
- стадію тимчасового гіпотиреозу;
- стадію відновлення з нормалізацією функції ЩЗ – триває 2-4 тиж, характеризується загибеллю вірусів, поступовим зниженням титру АТ.
У 5-15% випадків формується стійкий гіпотиреоз, в 1-4% пацієнтів виникають рецидиви.
Лабораторна діагностика ПГТ передбачає загальний аналіз крові (швидкість осідання еритроцитів (ШОЕ) до 30-60 мм/год при нормальному або незначному збільшенні лейкоцитів, можливий лімфоцитоз), біохімічний аналіз крові (підвищення вмісту α2-глобулінів, фібриногену, сіалових кислот; зниження рівня альбумінів, позитивний якісний аналіз на С-реактивний білок, підвищення вмісту Т3 та Т4 на тлі зниження рівня тиреотропного гормона (ТТГ); АТ до тиреоглобуліну з’являються лише через 2-3 тиж від початку захворювання).
При ультразвуковому дослідженні (УЗД) у пацієнтів з ПГТ можна побачити хмароподібні зони зниженої ехогенності, нечіткість контурів збільшеної ЩЗ або однієї з її часток на тлі нормальної ехоструктури й ехогенності іншої (неураженої) частки. Біопсія ЩЗ при ПГТ не потрібна. Проте, якщо проводити біопсію через невизначеність діагнозу, її результат демонструє картину (гранулематозний інфільтрат, гігантські клітини), що відповідає вірусній інфекції.
Диференційну діагностику ПГТ слід проводити із захворюваннями, які супроводжуються болем у ділянці шиї: гострим тиреоїдитом, крововиливом у ЩЗ, медіастинітом, хондроперихондритом, ангіною, тонзилітом, фарингітом, ларингітом, патологічними станами хребта, шийним міозитом. Враховуючи стадійність захворювання, варто диференціювати ПГТ з неврозом і дифузним токсичним зобом (у тиреотоксичну фазу).
Діагноз ПГТ підтверджує позитивний тест Крайля: клінічна ремісія (зменшення больових відчуттів у ділянці шиї, зниження температури тіла і зниження ШОЕ в загальному аналізі крові) через 24-72 год від початку прийому преднізолону в дозі 30-40 мг/добу.
Згідно з рекомендаціями Американської тиреоїдної асоціації (2016), пацієнтам з легкими симптомами ПГТ на етапі початкової терапії показано призначення β-блокаторів (для ліквідації тиреотоксикозу) та нестероїдних протизапальних препаратів (НПЗП). Глюкокортикоїди слід застосовувати в ситуації недостатньої ефективності та збереження виражених больових відчуттів і симптомів тиреотоксикозу на тлі прийому НПЗП. Препаратом вибору є преднізолон, який приймають у дозі 30-40 мг/добу (за умов важкого перебігу – 40-60 мг/добу) до усунення болю в ділянці ЩЗ і нормалізації ШОЕ. Через 2-3 тиж дозу преднізолону поступово зменшують на 5 мг кожні 5-7 днів до повної відміни. При гіпотиреоїдній фазі призначають L-тироксин по 50-100 мкг/добу протягом 3-6 міс з повною відміною при відновленні функції ЩЗ.
Аутоімунний тиреоїдит
Аутоімунний тиреоїдит (АІТ) – це хронічне органоспецифічне аутоімунне захворювання, морфологічним проявом якого є лімфоїдна та плазмоцитарна інфільтрація тканини ЩЗ з поступовим руйнуванням тиреоцитів і фолікулів та заміщенням їх сполучною тканиною під впливом імунних/цитотоксичних комплексів. Ця хвороба вперше була описана в 1912 р. японським хірургом Хашимото. АІТ зазвичай виникає у віковому періоді 25-35 років, хоча може з’являтися в будь-якому віці. Жінки хворіють частіше за чоловіків, що пояснюють можливим зв’язком між генами Х-хромосоми та розвитком аутоімунного процесу, а також впливом естрогенів на функцію Т-лімфоцитів.
В основі патогенезу АІТ лежить взаємодія генетичної схильності та несприятливих факторів навколишнього середовища. Генетична обумовленість виникнення АІТ підтверджується його асоціацією з антигенами системи HLA (гіпертрофічна форма поєднується з HLA DR5, атрофічна – з HLA DR3); сімейними формами хвороби та частим поєднанням з іншими хворобами з елементами аутоімунного патогенезу (аутоімунна офтальмопатія, гіпокортицизм, цукровий діабет 1 типу, ревматоїдний артрит, перніціозна анемія, вітіліго, вогнищева алопеція, системний червоний вовчак, гемолітична анемія, аутоімунні тромбоцитопатії, целіакія, синдром Шегрена тощо), обтяженим алергологічним анамнезом, наявністю АТ до тканини ЩЗ у родичів хворого.
Фактором зовнішнього середовища, який може запустити аутоімунний процес у ЩЗ в генетично схильних осіб, є тривалий прийом надлишкової кількості йоду. Йдеться про дуже високі дози йоду (десятки і сотні міліграмів), що містяться, зокрема, в рентгеноконтрастних препаратах і деяких антисептиках. Особливо активізується окисна дія йоду в умовах дефіциту селену. Забезпечення нормальної потреби в йоді (добова доза – 100-200 мкг) не збільшує частоту аутоімунної патології ЩЗ у здорових осіб.
Також причиною розвитку АІТ може бути рентгенівське опромінення голови, шиї та верхньої частини грудної клітки (з лікувальною метою) та/або низькоінтенсивне опромінення ЩЗ радіойодом і всього тіла радіоцезієм (унаслідок проживання з 1986 р. у регіонах, що постраждали внаслідок аварії на ЧАЕС); вплив різноманітних бактерій і вірусів; прийом інтерферону та препаратів літію; дія відходів промислових підприємств, сільськогосподарських отрутохімікатів; стресові фактори.
Класифікація АІТ за нозологічною формою передбачає розподіл на АІТ як самостійне захворювання, АІТ у поєднанні з іншими захворюваннями ЩЗ (підгострий тиреоїдит, вузловий зоб, дифузний токсичний зоб), АІТ як компонент аутоімунного поліендокринного синдрому; за розмірами ЩЗ – на гіпертрофічну й атрофічну форми; за функціональним станом залози – на АІТ з гіпо- чи еутиреозом, тиреотоксикозом; за клінічним перебігом – на латентний і клінічно виражений.
Захворювання зазвичай розвивається поступово, протягом декількох років, без виражених клінічних проявів. Розрізняють дві основні форми АІТ: гіпертрофічна (власне тиреоїдит Хашимото), що проявляється дифузним або вогнищевим збільшенням ЩЗ з нерівномірним ущільненням її тканини, та атрофічна, для якої характерно зменшення розмірів ЩЗ і клінічно виражене зниження її функції. Основною ознакою гіпертрофічної форми на початковій стадії хвороби є наявність зоба, який випадково може виявити сам хворий або оточуючі. Інколи ще до виявлення збільшення ЩЗ можуть виникати скарги на слабкість, легку втому, невизначені відчуття в ділянці шиї (тиск, дискомфорт при застібанні комірця, утруднене дихання при нахилі тулуба, лежачи на спині).
Клінічним еквівалентом імуноморфологічних змін при АІТ є ущільнення ЩЗ, яке виявляється під час пальпації більш ніж у 80% випадків. Однак за невеликої давності патологічного процесу ЩЗ може мати м’яку консистенцію. Збільшення ЩЗ може бути як рівномірним, так і асиметричним, причому зазвичай асиметрія спостерігається за рахунок правої частки. Поверхня залози може бути гладенькою, проте частіше вона нерівна, горбиста. Іноді відзначається нерівномірна щільність в одній частці або (частіше) у верхніх полюсах обох часток, що створює хибне уявлення про вузлову або змішану форму зоба. В усіх випадках шкіра та лімфатичні вузли шиї є інтактними, а залоза – рухомою.
Перебіг захворювання тривалий час відбувається на еутиреоїдному фоні, рідко – з короткочасною клінікою тиреотоксикозу (так званий хашитоксикоз), який виникає внаслідок деструкції тканини ЩЗ через аутоагресію, вивільнення великої кількості раніше синтезованих гормонів у кров і наявність АТ, що стимулюють продукцію тиреоїдних гормонів. Тиреотоксикоз при АІТ характеризується відносно неважким перебігом, помірним підвищенням рівнів Т3, Т4, схильністю до спонтанної ремісії та швидкого переходу в гіпотиреоз. Іноді АІТ має хвилеподібний перебіг з чергуванням гіпо- та гіпертиреозу, причому гіпотиреоз може передувати гіпертиреозу. Варто відмітити, що тиреотоксикоз може бути також зумовлений дифузним токсичним зобом, оскільки зустрічаються випадки поєднання АІТ із цим станом. У разі загибелі більшої частини тканини ЩЗ внаслідок АІТ виникає спочатку субклінічний, а в подальшому явний гіпотиреоз, який розглядається як незворотний стан.
Атрофічна форма АІТ характеризується масивною деструкцією фолікулярного епітелію ЩЗ, різким розвитком лімфоїдної та фіброзної тканини. ЩЗ зменшується в об’ємі і пальпаторно не визначається. У більшості випадків розвивається субклінічний або явний гіпотиреоз, що і дозволяє діагностувати цю форму. Зустрічається ще атрофічна асимптоматична форма, що діагностується при комплексному вивченні ЩЗ (титр АТ, УЗД), яка, імовірно, є початковою формою гіпотиреозу.
Поруч із традиційними аутоімунними захворюваннями ЩЗ – дифузним токсичним зобом, АІТ – у клінічній практиці трапляються випадки синдрому аутоімунного перехресту (overlap-синдром), що характеризується комбінацією клінічних, біохімічних і серологічних проявів, властивих декільком захворюванням цієї залози. На сьогодні етіологія аутоімунних захворювань ЩЗ залишається недостатньо з’ясованою, тому неможливо однозначно вирішити, чи є overlap-синдром самостійним захворюванням або ж це варіант перебігу того чи іншого аутоімунного захворювання ЩЗ.
Діагностика АІТ ґрунтується на таких клінічних, лабораторних та інструментальних методах обстеження: клінічний огляд і пальпація ЩЗ; визначення рівня тиреоїдних гормонів та ТТГ; виявлення АТ до тиреоїдної пероксидази (АТ ТПО); УЗД ЩЗ; тонкоголкова біопсія ЩЗ (у випадку проведення диференційної діагностики з вузловим зобом).
Діагноз АІТ не може бути встановленим лише на підставі даних пальпації ЩЗ, а також збільшення або зменшення її об’єму. Великими діагностичними ознаками, поєднання яких дозволяє встановити діагноз АІТ, вважають первинний гіпотиреоз (маніфестний або стійкий субклінічний); наявність АТ ТПО у високих титрах (≥250 од/мл); ультразвукові ознаки аутоімунної патології (дифузна гетерогенність і на тлі дифузного зниження ехогенності – розмиті ізо- та гіперехогенні ділянки, неоднорідність структури). За відсутності принаймні однієї з великих діагностичних ознак АІТ носить лише імовірний характер. Останнє положення особливо важливе, оскільки досить часто виявлення АТ проти тканин ЩЗ або ж діагностика практично будь-яких змін ехогенності залози розглядається як патогномонічна ознака АІТ.
Пункційна біопсія ЩЗ для підтвердження діагнозу АІТ не показана. Вона здебільшого проводиться в рамках діагностичного пошуку при вузловому зобі, виступаючи невід’ємною частиною комплексного обстеження. Однак у разі її виконання можна виявити такі цитоморфологічні ознаки АІТ: облігатну ознаку (лімфоплазмоцитарна інфільтрація: незрілі лімфоїдні елементи аж до зародкових центрів, плазмоцити) і факультативні (сполучнотканинні елементи, войлокоподібні структури, онкоцитарна інфільтрація β-клітинами Ашкеназі-Гюртля). Варто зауважити, що цитологія АІТ і дифузного токсичного зоба не відрізняється.
Важливо наголосити, що дослідження динаміки рівня циркулюючих АТ до ЩЗ з метою оцінки розвитку та прогресування АІТ не має діагностичного і прогностичного значення. Це слід запам’ятати, оскільки в клінічній практиці трапляються хворі з досить тяжкими ятрогеніями, що розвинулися на тлі змін лікування після непотрібного дослідження показника, який не піддається корекції.
Специфічне лікування АІТ дотепер не розроблене, ефективні та безпечні методи впливу на аутоімунний процес у ЩЗ відсутні, тому ведення АІТ зводиться до терапії порушень функціонального стану ЩЗ. При гіпертиреоїдній фазі АІТ застосовують симптоматичне лікування (β-адреноблокатори – анаприлін 40-80-120 мг/добу, атенолол – 50-100 мг/добу; седативні препарати), у разі значних проявів – мерказоліл 20-30 мг/добу (оскільки не виключена можливість короткочасної продукції тиреостимулюючих АТ). При явному (підвищення рівня ТТГ та зниження рівня вільного Т4) і субклінічному гіпотиреозі (нормальні рівні вільного Т4 і підвищені рівні ТТГ, підтверджені дворазовим дослідженням) показана також терапія левотироксином (1,6-1,8 мкг/кг під контролем ТТГ), критерієм адекватності якої є досягнення нормального рівня ТТГ і стійке збереження його в оптимальних межах (0,5-2,0 мОД/л).
Настанови Американської тиреоїдної асоціації (2017) вказують, що у вагітних слід перевіряти титр АТ ТПО при рівні ТТГ >2,5 мОд/л. Застосування левотироксину передбачено при позитивних АТ ТПО і ТТГ >2,5 мОд/л; при негативних АТ ТПО і ТТГ понад триместрспецифічне референтне значення. Застосування левотироксину рекомендовано при позитивних АТ ТПО і ТТГ понад триместрспецифічне референтне значення; при негативних АТ ТПО і ТТГ >10,0 мОд/л. Терапія левотироксином не рекомендована при негативних АТ ТПО і ТТГ у межах триместрспецифічного референтного значення (або <4,0 мОд/л). За умов АІТ з еутиреозом слід спостерігати за хворими. Показаннями до оперативного лікування є великий зоб з об’єктивними ознаками стискання ним органів шиї, загрудинно розміщений зоб великих розмірів, поєднання АІТ з неопластичними процесами в ЩЗ.
Перспективним в комплексному лікуванні АІТ можна вважати використання препаратів селену (враховуючи роль його дефіциту в розвитку АІТ), а також кальцитріолу (активний метаболіт вітаміну D3), який пригнічує проліферацію активованих Т-лімфоцитів, гальмує секрецію інтерлейкіну‑2, фактора некрозу пухлини, інтерферону γ і регулює процес апоптозу.
Селен та ЩЗ
ЩЗ має особливо високу потребу в селені і належить до органів, у тканинах яких відзначається найвищий рівень вмісту цього мікроелемента. Селен необхідний для формування, активації і метаболізму гормонів ЩЗ, тому вирішальним фактором нормального функціонування залози є достатнє постачання селену. Фармакологічні властивості селену включають антиоксидантну й імуномодулюючу дію, профілактику пухлинних захворювань, гальмування метаболізму ракових клітин, стимулювання механізмів відновлення ДНК, активацію апоптозу, протизапальний вплив, кардіопротекторний та антигіпотиреоїдний ефекти, детоксикацію в разі впливу важких металів.
Селензалежні ферменти відіграють важливу роль у функціонуванні ЩЗ. До цих ферментів належать дейодинази та глутатіонпероксидази. Дейодинази (D1, D2, D3) – це група ферментів, що здійснюють метаболізм тиреоїдних гормонів і входять до складу йодтироніно-селено-дейодиназної системи. Ці ферменти відповідають за перетворення Т4 у більш активний Т3. Своєю чергою, група ферментів-глутатіонпероксидаз (GPx) захищає організм від окислювального ушкодження. Глутатіонпероксидази каталізують відновлення перекисів ліпідів у відповідні спирти і відновлення пероксиду водню до води.
Препарат Цефасель (компанія Сefak KG, Німеччина) є результатом ретельних науково-технічних пошуків, розпочатих у 1984 р. Цефасель містить селен у вигляді неорганічної солі – селеніту натрію. Завдяки високій біодоступності селеніт натрію демонструє явні терапевтичні переваги в порівнянні з органічними харчовими добавками селену (рис.).
Рис. Метаболізм органічних і неорганічних форм селену in vivo
Препарати, що містять селеніт натрію, характеризуються високим і точно визначеним вмістом селену. У зв’язку зі специфічними метаболічними механізмами засоби на основі селеніту натрію потужно активують біосинтез селенопротеїнів. Цефасель чудово підходить для компенсування станів гострого дефіциту селену, а також для специфічної терапії аутоімунних захворювань ЩЗ.
У разі застосування в ролі етіотропної терапії АІТ, як і при спільному застосуванні з гормонами ЩЗ (левотироксином), селен слід призначати в дозі 200 мкг/день (1 таблетка (100 мкг) препарату Цефасель 2 р/день). Тривалість етіотропного лікування має становити 3-9 міс. Важливо, що супутня терапія Цефаселем дозволяє приймати L-тироксин у мінімальній ефективній дозі.
Нещодавно в Україні з’явилося нове дозування препарату Цефасель – 300 мкг. Теоретично зрозуміло, що велика доза селену сприятиме підвищенню активності селенопротеїнів, тим самим запобігаючи накопиченню перекисних продуктів обміну речовин у ЩЗ. Велика доза селену також збільшить вміст дейодиназ, що активують тиреоїдні гормони. Водночас виникає запитання щодо безпеки більш високої дози. Цей аспект селенотерапії є добре дослідженим. У Великій Британії група зі 103 осіб отримувала селен у дозі 300 мкг/добу протягом 6 міс. Було зафіксовано підвищення рівня селену плазми з 92,0±20,0 до 233,0 ±54,0 мкг/л. У датському дослідженні (n=49) вивчалися рівні селену в плазмі крові при призначенні його в дозі 100, 200 та 300 мкг/добу протягом 2 років. Концентрація селену виявилася пропорційною загальній добовій дозі: за умов отримання дози 300 мкг/добу цей показник стійко відзначався на рівні 241,0±132 мкг/л. Таким чином, довготривалий прийом селену в стабільній дозі та застосування високодозових препаратів сприяють більш активному насиченню організму цим мікроелементом. Доза селену 300 мкг/добу навіть при значному (до 2 років) прийомі не є токсичною і не зумовлює побічних ефектів.
Нині багато експертів вважають, що для профілактики адекватною дозою є ≥100 мкг селену на добу, а безпечною лікувальною дозою для дорослих, у тому числі для жінок у період вагітності і лактації, є 300 мкг/добу (Європа) і навіть 400 мкг/добу (США).
Цефасель – єдиний таблетований препарат селену на фармацевтичному ринку України, доступний в дозуваннях 100 і 300 мкг.
Результати досліджень показують, що додатковий прийом селену при захворюваннях ЩЗ, особливо при імунних тиреопатіях, з погляду патофізіології може розцінюватися як перевірений і доцільний терапевтичний захід. Чинниками, що забезпечують більше насичення організму селеном, є адекватне добове дозування препарату і тривалість курсу лікування. Наприклад, 10-тижневий термін недостатній для забезпечення стійкого підвищення рівня селену в крові. У порівнянні зі щоденною дозою 100 і 200 мкг/добу дозування 300 мкг/добу забезпечує (за умов тривалого прийому) більше стійке насичення організму мікроелементом, що особливо актуально при лікуванні хронічної патології.
Післяпологовий тиреоїдит (ППТ)
ППТ є особливою формою АІТ (прихованою), що виникає після пологів. Основною причиною ППТ є надмірна реактивація імунної системи після природної гестаційної імуносупресії (феномен рикошету), яка в схильних осіб (носії АТ ТПО) призводить до появи деструктивного АІТ. Захворювання маніфестує через 8-12 тиж після пологів транзиторним тиреотоксикозом, який згодом переходить у гіпотиреоїдну фазу. Приблизно через 6-8 міс після початку гіпотиреоїдної фази у хворих знову відновлюється еутиреоїдний стан, але у 25-30% жінок спостерігається перехід у стійкий гіпотиреоз. При повторній вагітності ризик розвитку ППТ досягає 70%. Функціональні порушення ЩЗ у пацієнток з ППТ не завжди є клінічно вираженими.
Критерії діагностики ППТ включають зв’язок захворювання з пологами (поширеність ППТ – 5-9% всіх вагітностей); помірно збільшену щільну неболючу ЩЗ; транзиторний тиреотоксикоз, який носить деструктивний характер, з низькою швидкістю поглинання ізотопів I131 та технецію на фоні підвищення рівня вільного Т4 і/або Т3 в крові.
Для жінок, які годують груддю, препаратом вибору є технецій. Після введення звичайної дози технецію годування безпечне вже через 12 год.
Функція ЩЗ зазвичай міняється за схемою: тиреотоксикоз – гіпотиреоз – еутиреоз. У крові хворих на ППТ відсутній високий титр тиреостимулюючих АТ, що в комплексі з вищеназваними критеріями відрізняє транзиторний тиреотоксикоз на фоні ППТ від дифузного токсичного зоба, натомість наявний високий титр антимікросомальних антитіл (АТ ТПО, АТ до тиреоглобуліну). Під час УЗД ЩЗ виявляються дифузні або мультифокальні гіпоехогенні зміни, при гістологічному і цитологічному дослідженні – лімфоїдна інфільтрація. У період тиреотоксикозу внаслідок деструкції тканини залози виявляють збільшення екскреції йоду із сечею. Раннє підвищення в крові рівня тиреоглобуліну (індикатора тиреоїдної дисфункції) дає можливість виявити жінок з підвищеним ризиком розвитку ППТ.
Згідно з рекомендаціями Американської тиреоїдної асоціації (2016), якщо тиреотоксикоз уперше виявляється в жінки в післяпологовому періоді, необхідно обстеження з метою диференційної діагностики ППТ і післяпологової маніфестації хвороби Грейвса. Інші рекомендації з ведення пацієнток з ППТ представлені в таблиці 2.
Медикаментозний (цитокініндукований) тиреоїдит
Медикаментозний тиреоїдит (МТ) є ще одним варіантом АІТ. Цей варіант зустрічається в пацієнтів, які тривали час отримують терапію інтерфероном α, інтерлейкіном‑2 з приводу хронічного гепатиту С, злоякісних захворювань, лейкемії. Хвороба має двофазний перебіг: коротка фаза транзиторного тиреотоксикозу змінюється фазою гіпотиреозу. МТ у 4,4 разу частіше розвивається в жінок. Попереднє носійство АТ ТПО також підвищує ризик МТ (у 3,9 разу). Час розвитку захворювання не залежить від початку і тривалості терапії інтерфероном α (від 4 тиж до 24 міс). При лабораторній діагностиці в крові виявляється високий титр АТ ТПО, однак слід пам’ятати, що 20% жінок є носіями антитиреоїдних АТ, тому виявлення АТ до ЩЗ в пацієнток, які отримують інтерферон α, ще не означає патогенетичного зв’язку цього феномена з призначеним лікуванням. За характером перебігу цітокініндукований тиреоїдит схожий з ППТ, тому лікування також є аналогічним. Еутиреоз відновлюється після відміни терапії цитокінами.
Пацієнтам, які приймають ліки, що спричиняють тиреотоксикоз, включно з інтерфероном α, інтерлейкіном‑2, інгібіторами тирозинкінази та літію, слід раз на півроку клінічно та біохімічно контролювати функцію ЩЗ. Пацієнти, в яких розвивається тиреотоксикоз, мають підлягати подальшій оцінці для визначення етіології та призначення відповідного лікування.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 19 (440), жовтень 2018 р.




