13 червня, 2019
Ошибки и осложнения в ортопедии и травматологии
Боль является ощущением, хорошо знакомым каждому человеку. C точки зрения врача боль – понятие клинически и патогенетически сложное и неоднородное, вместе с тем это один из основополагающих моментов, который определяет качество жизни пациента. Различные подходы к лечению болевых синдромов, с которыми сталкиваются в своей практике врачи-травматологи, были представлены на научно-практической конференции «Вторая зимняя школа травматологов», которая состоялась 13-15 декабря 2018 года в г. Яремче.
 В ходе конференции с обширным и содержательным докладом на тему «Нейродистрофический синдром у пациентов с переломом дистального эпиметафиза лучевой кости» выступил член-корреспондент НАМН Украины, руководитель отделения микрохирургии и реконструктивно-восстановительной хирургии верхней конечности ГУ «Институт травматологии и ортопедии НАМН Украины», доктор медицинских наук, профессор С.С. Страфун.
В ходе конференции с обширным и содержательным докладом на тему «Нейродистрофический синдром у пациентов с переломом дистального эпиметафиза лучевой кости» выступил член-корреспондент НАМН Украины, руководитель отделения микрохирургии и реконструктивно-восстановительной хирургии верхней конечности ГУ «Институт травматологии и ортопедии НАМН Украины», доктор медицинских наук, профессор С.С. Страфун.
Свой доклад он начал с данных статистики. Так, было отмечено, что среди 1200 прооперированных пациентов за 3 года у 66 (5,5%) развился нейродистрофический синдром (НДС). При этом ежедневно 3-6 пациентов с нейродистрофией обращаются на амбулаторный прием (15-25%), что составляет до 400 человек ежегодно. Половина этих пациентов приходят на повторные консультации (от одной до трех).
Группа риска по развитию НДС – это женщины среднего и пожилого возраста, которые после операции жалуются на постоянные боли в прооперированном суставе; часто это пациенты после длительного и болезненного ношения шины (например, контрактура Дюпюитрена).
Профессор С.С. Страфун отметил, что НДС – достаточно нередкий синдром, сопровождающийся терминологической путаницей. Так, по определению Эванса (1935 г.) – это пекущая боль из-за выраженной симптоматической стимуляции, которая сопровождается покраснением, отеком и даже кистозной атрофией костной ткани. При этом существует несколько названий длительного болевого синдрома: НДС, синдром Зудека, нейродистрофия, трофо-невротический остеопороз, рефлекторная альгодистрофия и т.д. Однако наиболее приемлемое за рубежом название – это комплексный регионарный болевой синдром (КРБС) І и ІІ типов.
 К КРБС I типа относят случаи, когда болевой синдром возникает после травмы конечностей, сопровождается длительными вазомоторными и трофическими нарушениями, остеопорозом и не связан с поражением периферического нерва. Однако этот болевой синдром может не всегда быть связан с травмой и сама боль бывает разной. Выделяют такие виды боли:
К КРБС I типа относят случаи, когда болевой синдром возникает после травмы конечностей, сопровождается длительными вазомоторными и трофическими нарушениями, остеопорозом и не связан с поражением периферического нерва. Однако этот болевой синдром может не всегда быть связан с травмой и сама боль бывает разной. Выделяют такие виды боли:
- стимулонезависимая боль – болевой синдром или дизестезические ощущения, возникающие в спокойствии, без наличия раздражителя;
- стимулозависимая боль – аллодиния, может иметь место как при центральном, так и при периферическом механизме сенситизации.
КРБС I типа можно условно разделить на две формы:
- «теплая форма» – нейродистрофические нарушения, сопровождающиеся вазодилатацией и локальной гипертермией кисти;
- «холодная форма» – нейродистрофические нарушения, сопровождающиеся вазоспазмом и локальной гипотермией кисти.
КРБС ІІ типа предполагает болевой синдром, связанный с непосредственной травмой периферического нерва, и сопровождается вазомоторными и трофическими нарушениями (например, «туннельный синдром»).
Международная ассоциация изучения боли (International Association for the Study of Pain, IASP) разработала диагностические критерии для двух типов КРБС (табл. 1).
К факторам, влияющим на развитие КРБС, относятся: многоразовые попытки закрытой репозиции первично невправимых переломов, слишком ранняя и слишком активная разработка движений в суставах.
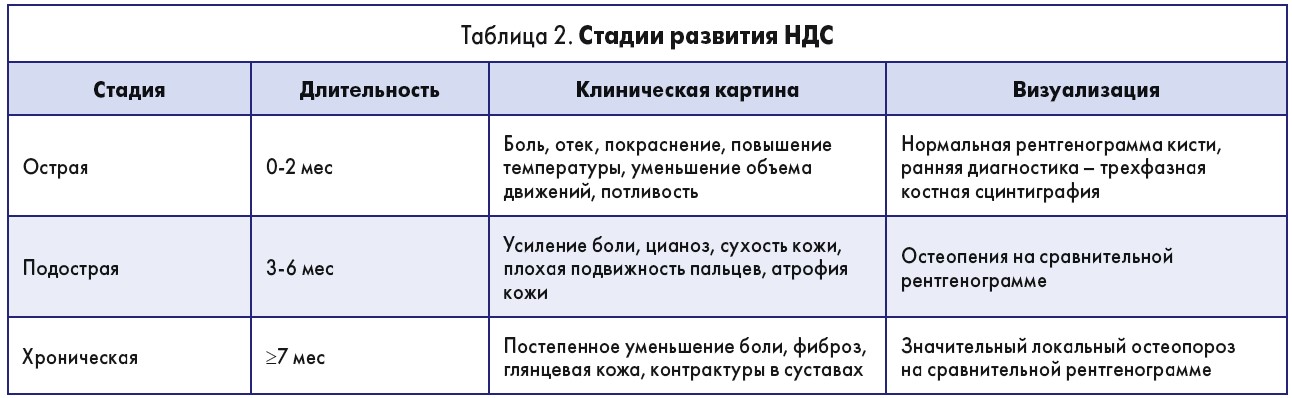
Стадии развития НДС представлены в табл. 2.
Докладчик отметил, что патогенез данного состояния до конца не изучен и на сегодняшний день учеными предложено несколько теорий развития НДС.
Фоизье в 1947 г. внедрил термин «посттравматический артериальный вазоспазм» и получил хорошее обезболивание после симпатэктомии, отметив, что спазм касается преимущественно артериол, а представление о лечении декларировал достаточно упрощенно: главная терапевтическая задача – раскрыть периферическое артериальное русло.
Мелзак и Уолл в 1965 г. предложили «теорию заслонок», которая основана на взаимодействии болевых и тактильных сенсоров с разными анатомо-функциональными единицами вегетативной нервной системы, включая волокна и промежуточные нейроны спинного мозга (в том числе желатинозной субстанции) и узлов симпатического столба.
Ланкфорд в 1980 г. предложил свою теорию патогенеза НДС:
- боль травматического генеза или вследствие заболевания различной интенсивности и продолжительности;
- специфичный диатез (склонность/готовность организма, проявляющаяся гипергидрозом, снижением температуры ладоней и стоп. Более подвержены женщины в возрасте 30-60 лет);
- аномальный симпатический рефлекс.
 В норме при боли и травме для приостановки кровопотери возникает вазоспазм. Через некоторое время постепенно возникает вазодилатация, обеспечивающая трофику и регенерацию тканей. У пациентов, склонных к рефлекторной симпатической дистрофии (РСД), в связи с аномальным симпатическим рефлексом, вазодилатация отсутствует или существенно отстает во времени, вызывая стойкие трофические нарушения.
В норме при боли и травме для приостановки кровопотери возникает вазоспазм. Через некоторое время постепенно возникает вазодилатация, обеспечивающая трофику и регенерацию тканей. У пациентов, склонных к рефлекторной симпатической дистрофии (РСД), в связи с аномальным симпатическим рефлексом, вазодилатация отсутствует или существенно отстает во времени, вызывая стойкие трофические нарушения.
У пациентов с КРБС І типа порог возбудимости афферентных нервов очень низкий. При КРБС ІІ типа имеет место каузалгический характер боли, поскольку связан с раздражением периферического нерва (из-за сдавливания или частичного повреждения). Например, частичное повреждение локтевого нерва на уровне кубитального канала сопровождается очень интенсивным болевым синдромом. Развитие НДС при контрактуре Дюпюитрена возникает тогда, когда врачу после иммобилизации не удалось до конца «разогнуть» пациенту пальцы и он применяет силовые методы для восстановления их позиции.
Дифференциальная диагностика КРБС проводится с:
- повреждением нерва (регенераторная гиперпатия);
- системным артритом (ревматоидный артрит, псориаз, кристаллоидная артропатия);
- неинфекционными хроническими синовиитами;
- инфекционным артритом кистевого сустава (отсутствие суставного хряща – главное рентгенологическое отличие инфекционного артрита от НДС);
- рожистым воспалением;
- тромбозом венозных сосудов;
- лимфедемой (после мастэктомии);
- микседемой (гипофункция щитовидной железы).
Схема проведения симпатических блокад со спиртом и фенолом базируется на рекомендациях Общества реабилитологов и Общества анестезиологов Нидерландов (Netherlands Society of Rehabilitation Specialists and Netherlands Society of Anesthesiologists), 2006 г.
Регламентируемое количество симпатических блокад у пациентов с КРБС и симпатически опосредованной болью при отсутствии выраженного положительного эффекта – не более трех:
І фаза (6 нед) – не более 5 блокад;
ІІ фаза (6 нед) – не более 3 блокад;
ІІІ фаза (6 нед) – не более 3 блокад.
Всего за курс лечения (18 нед) пациенту не может быть проведено более 11 блокад!
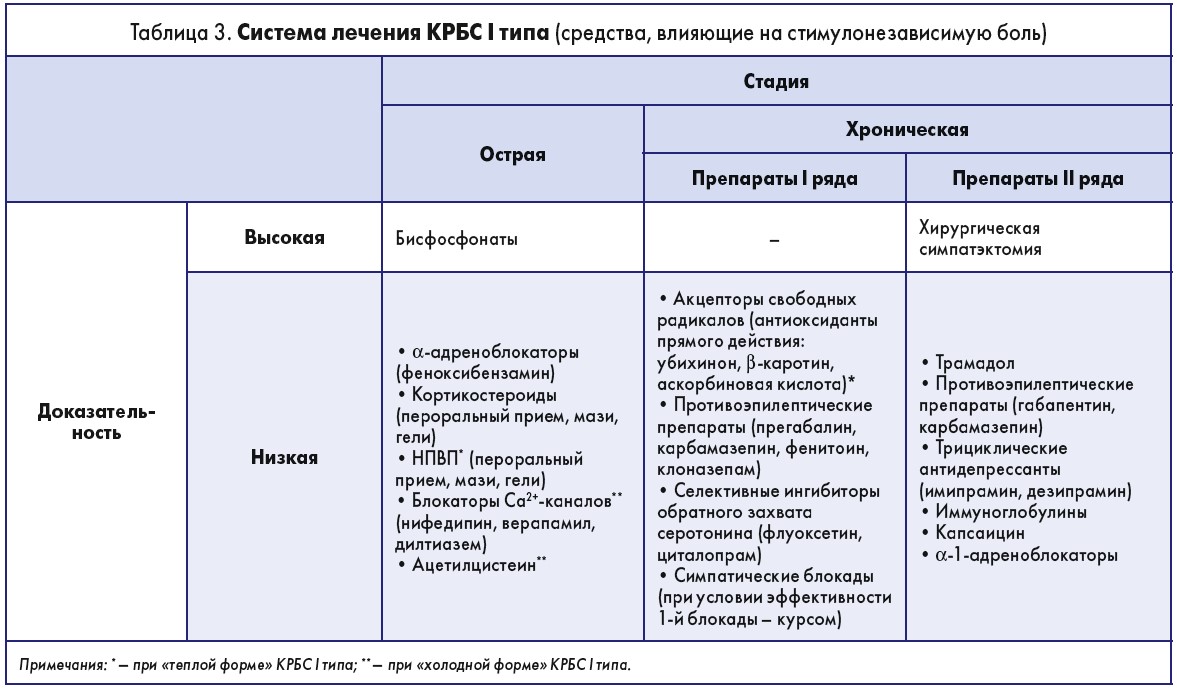
Система лечения КРБС І типа
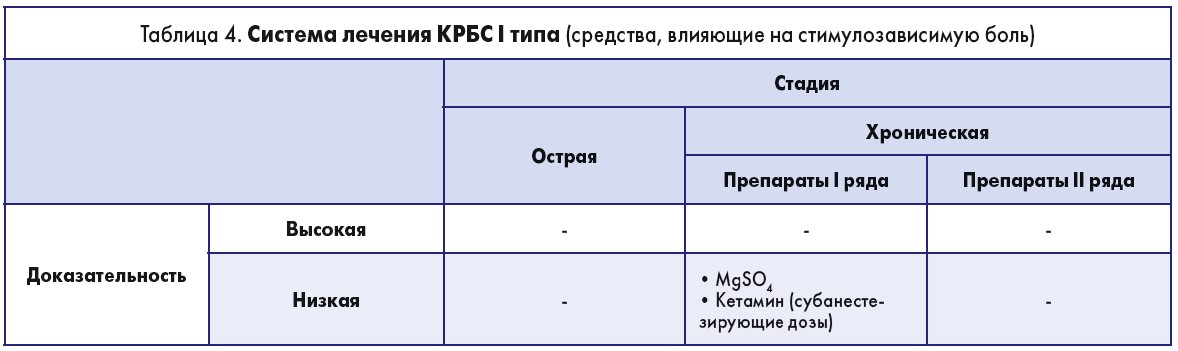
Медикаментозные средства, влияющие на стимулонезависимую и стимулозависимую боль, представлены в табл. 3, 4.
Методы немедикаментозного лечения КРБС І типа, независимо от механизма развития, представлены в табл. 5.
Оперативное лечение рекомендуется отложить до исчезновения симптомов КРБС І типа (достижение ремиссии). Это не касается оперативных вмешательств с целью устранения первичной причины развития НДС. При этом длительность операции и кровопотерю следует максимально уменьшить.
Зеркальная терапия помогает установить зрительную связь с мышцами и усилить сенсомоторную связь между мышцами и мозгом. При ее применении используют визуальную стимуляцию и демонстрируют нормальное функционирование конечности. Таким образом, в процессе реабилитации значительную роль играет не только физическая, но и когнитивная сфера.
Для профилактики развития КРБС І типа применяют (согласно рекомендациям Perez R.S., Zollinger P.E., Dijkstra P.U., Thomassen-Hilgersom I.L., Zuurmond W.W., Rosenbrand K.C.J., Geertzen J.H., 2010):
- витамин С – при переломах дистального эпиметафиза лучевой кости достоверно снижает риск развития КРБС;
- регионарная анестезия и уменьшение времени турникета достоверно снижает риск развития КРБС.
Уровни доказательности применения лекарственных средств при КРБС І типа (Perez R.S., Zollinger P.E., Dijkstra P.U., Thomassen-Hilgersom I.L., Zuurmond W.W., Rosenbrand K.C.J., Geertzen J.H., 2011).
Слабый или недоказанный эффект:
- Нестероидные противовоспалительные препараты (НПВП)
- Опиаты, блокада местным анестетиком, капсаицин
- Симпатическая блокада
Пероральные миорелаксанты
- Ботулотоксин, диметилсульфоксид
- Кортикостероиды, α-адреноблокаторы
- Блокаторы кальциевых каналов (нифедипин)
- Психотерапия
- ЧЭНС
Мощный или достоверно доказанный эффект:
- Антидепрессанты
- Антиконвульсанты (габапентины) 600-1800 мг в течение 2 мес
- Бисфосфанаты – выраженный положительный достоверный эффект (І уровень доказательности по Forouzanfar и соавт.)
- Хирургическая симпатэктомия – достоверный эффект снижения боли, но не увеличение функции
- Электростимуляция спинного мозга – улучшение качества жизни, но не функции конечности
- Физиотерапия – выраженный достоверный эффект
- Трудотерапия – выраженный достоверный эффект
- Ампутация – не дает положительного эффекта
Психологическая поддержка для таких пациентов очень важна. Она должна включать в себя следующее:
- всестороннее информирование о природе возникшего заболевания, процессы, протекающие в конечности, их характеристики по интенсивности и длительности.
- выдача на руки методических рекомендаций с разъяснениями по комплексу необходимых упражнений и правилами их дозирования;
- устное заверение пациента в окончательном выздоровлении в течение 7-10 мес с момента начала заболевания;
- оповещение об отсутствии высокоэффективных и быстродействующих методик лечения;
- беседа с родственниками, социализация и настраивание на позитив и выздоровление, ежедневный самоконтроль, еженедельный контроль у методиста, ежемесячный – у врача для поддержания настроя и контроля характерологических расстройств.
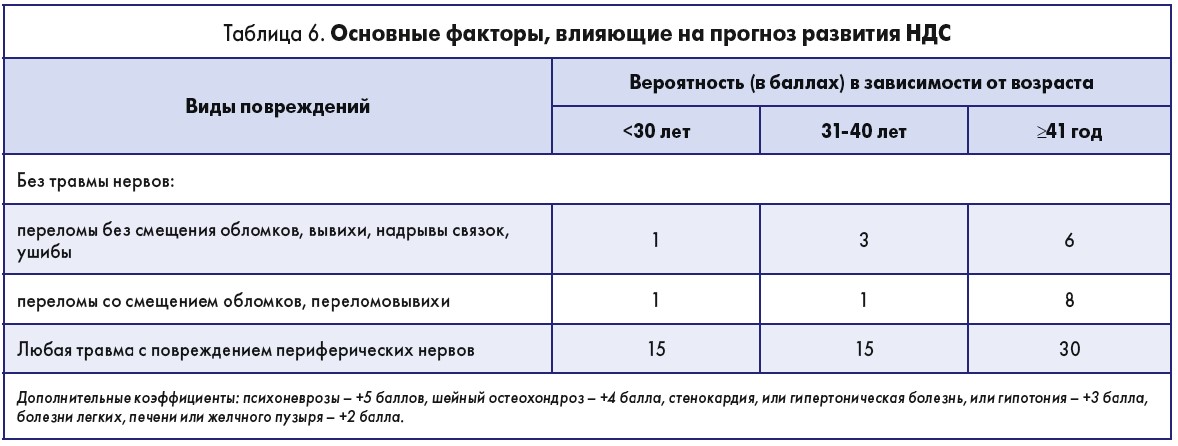
Возраст пациента, вид повреждений, наличие сопутствующих заболеваний были отмечены докладчиком как основные факторы, которые влияют на прогноз развития НДС (табл. 6).
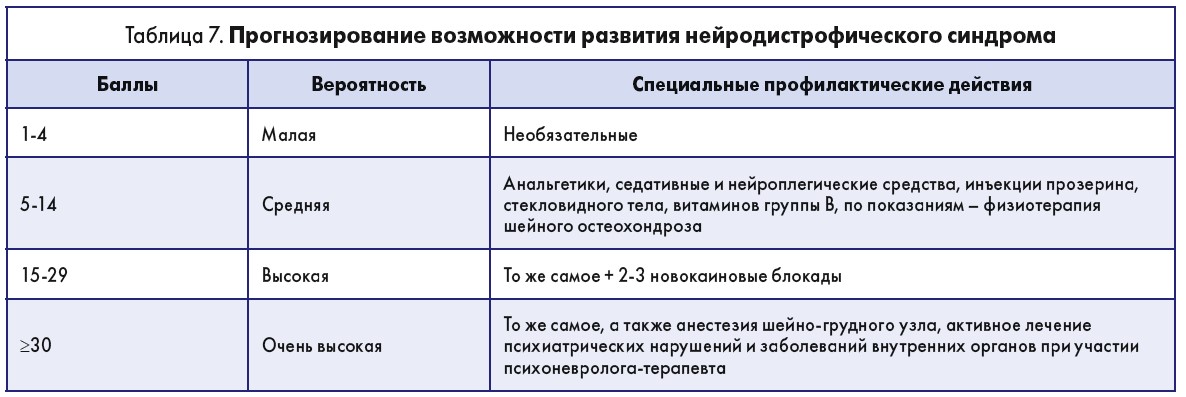
Возможность развития НДС можно определить по табл. 7.
Заканчивая доклад, профессор С.С. Страфун подчеркнул, что для хорошего результата необходима мотивация пациента, врача и ребилитолога, отсутствие которой приводит к конфликту и углублению триггерных механизмов нейродистрофии. Патримониальное отношение к пациенту, периодические осмотры, подбадривание, непротокольная атмосфера лечения, обуславливающая позитивный настрой пациента, позволяет ему пройти весь период заболевания, вплоть до разрешения НДС, без значительных эмоциональных, социальных и экономических потерь.
 «Комплексный регионарный болевой синдром. Современное состояние проблемы» – такие вопросы затронул в своем выступлении врач ортопед-травматолог высшей категории ГУ «Институт травматологии и ортопедии НАМН Украины», кандидат медицинских наук В.В. Котюк.
«Комплексный регионарный болевой синдром. Современное состояние проблемы» – такие вопросы затронул в своем выступлении врач ортопед-травматолог высшей категории ГУ «Институт травматологии и ортопедии НАМН Украины», кандидат медицинских наук В.В. Котюк.
КРБС I типа – заболевание, знакомое на практике многим врачам. Суть его состоит в развитии регионарного болевого синдрома, диспропорционального во времени и степени по отношению к обычному течению посттравматического периода, которое не соответствует зонам иннервации определенных нервов и проявляется в дистальных отделах конечностей сенсорными, двигательными, судомоторными, вазомоторными и/или трофическими нарушениями.
Случаи КРБС учащаются в период военных действий и катастроф (40% случаев развивается после переломов, 12% – после инсультов, 1-5% – после инфарктов).
Критерии диагностики Veldman:
- Диффузная боль во время движений и нагрузки
- Градиент температуры между больной и контрлатеральной конечностью
- Разница в цвете между больной и контрлатеральной конечностью
- Разница в объеме между больной и контрлатеральной конечностью
- Ограничение амплитуды активных движений больной конечности
Диагноз КРБС ставится на основании наличия четырех из пяти диагностических симптомов.
Критерии R.M. Atkins (2003 г.) для ортопедов:
- Нейропатическая боль
- Сосудистые нарушения и нарушения потоотделения
- Отек
- Тугоподвижность суставов
- Контрактура в суставе
Эти симптомы должны подкрепляться рентгенологическими признаками остеопороза через 3 мес или повышенным накоплением радиофармпрепарата при остеосцинтиграфии на ранней стадии заболевания.
Механизм развития КРБС I типа:
- Центральная сенситизация
- Периферическая сенситизация
- Нарушение функций симпатической нервной системы
- Перестройка сенсорных и подвижных зон коры головного мозга
Существуют центральная и периферическая составляющие патогенеза КРБС I типа, и это важно определить у пациента для правильной стратегии лечения.
Дифференциальная диагностика:
- Тромбоз глубоких вен
- Артериальная недостаточность
- Болезнь Рейно
- Лимфатический отек
- Инфекционные процессы
- Диабетическая нейропатия, нейропатия мелких волокон, полинейропатия, радикулопатия
- Туннельные нейропатии
- Компартмент-синдром
- Эритромелалгия
- Плексопатии и заболевания позвоночника
- Новообразования: опухоль Панкоста
- Психосоматическая посттравматическая дистония
- Ревматические заболевания
- Посттравматический артроз
- Несращение переломов
Докладчик заметил, что КРБС І типа – это диагноз исключения других заболеваний. На сегодняшний день ни один из инструментальных методов не может ни подтвердить, ни исключить диагноз КРБС. Однако они могут выявить субклинические симптомы, объективизировать их количественно, оценить динамику в процессе лечения и исключить другие заболевания или травмы. Радиоизотопное сканирование на сегодняшний день – претендент на золотой стандарт диагностики.
Основная проблема при лечении КРБС І типа состоит не в отсутствии средств, а в большом выборе различных препаратов, которые могут быть эффективными для данного пациента. Выбор препаратов необходимо базировать на особенностях патогенеза, которые превалируют у конкретного пациента.
В терапии КРБС применяются следующие медикаментозные средства:
- Кортикостероиды – для влияния на аутоиммунную составляющую.
- Антиконвульсанты: габапентин – для блокировки антагонистов NMDA; прегабалин; реже – карбамазепин, фенитоин, клоназепам.
- Антидепрессанты для борьбы со страхом движений и прямого действия на нейропатическую боль.
- Противовоспалительные средства – димексид (диметилсульфоксид), эффективность которого описана в многочисленных исследованиях.
Базовым методом немедикаментозной терапии является физиотерапия, которую надо начинать как можно раньше. Также неотъемлемая часть реабилитации – это психотерапия.
.jpg) Актуальный доклад «Боль и тревога» представил заведующий кафедрой неврологии, нейрохирургии и психиатрии медицинского факультета Ужгородского национального университета, доктор медицинских наук, доцент М.М. Орос.
Актуальный доклад «Боль и тревога» представил заведующий кафедрой неврологии, нейрохирургии и психиатрии медицинского факультета Ужгородского национального университета, доктор медицинских наук, доцент М.М. Орос.
Свой доклад он начал сразу с разбора клинического случая, чем привлек внимание не только практикующих врачей, но и студентов. Его пациент (1992 г. р.) жаловался на боль в межлопаточной зоне позвоночника, ощущение роста горба, боли в области сердца, плохой сон, также присутствовала боязнь стать инвалидом. После травмы четырехлетней давности боли усилились за последние полгода. В анамнезе туберкулез, инфекционный гепатит.
Объективно: менингеальные симптомы отсутствуют, субкортикальные рефлексы в норме, артериальное давление (АД) – 165/110 мм рт. ст., частота сердечных сокращений (ЧСС) – 90 уд./мин (реакция на белые халаты), общее состояние не нарушено, лабораторные показатели без значительных отклонений.
Результаты магнитно-резонансной томографии: множественные протрузии, гиперкифоз.
Диагноз: остеохондроз грудного отдела позвоночника, хроническая люмбалгия. Болезнь Шермана – Мау. Клиновидная деформация грудных позвонков.
Лечение: диклофенак (Диклак®), флупиртин, физиотерапия: фонофорез, амплипульс, лазер, массаж, профилактор Евминова, мануальная терапия.
Пациент почувствовал временное улучшение, но боли в позвоночнике не исчезли. Тогда к лечению был добавлен прегабалин (Линбаг) в таблетках.
Был ли у пациента ноцицептивный момент? Однозначно, был.
 Докладчик отметил интересный момент восприятия боли – она зависит от биопсихосоциальных аспектов человека, и нет прямой корреляции между самим повреждением и болью, доказательством чего служат примеры травматизации своего тела туземцами, связанные с культурально-религиозными особенностями племен.
Докладчик отметил интересный момент восприятия боли – она зависит от биопсихосоциальных аспектов человека, и нет прямой корреляции между самим повреждением и болью, доказательством чего служат примеры травматизации своего тела туземцами, связанные с культурально-религиозными особенностями племен.
Хроническая боль – это мозговое расстройство. Выступающий описал патофизиологию эмоциональной составляющей (тревоги, волнения) и реорганизацию синаптических связей с нейрохимическими изменениями в кортексе. Он подчеркнул влияние генетических и внешних факторов (психотравма детства, социальный опыт) на дальнейшее развитие подобных расстройств в более старшем возрасте и возникновение так называемого круга самозапугивания. Однако переживания нужны нам для позитивных убеждений. Они помогают предотвратить негативные события, иногда – найти решения, мотивируют, готовят к встрече с проблемами, а переживания о ком-то означают заботу.
Для диагностики генерализованных тревожных расстройств (ГТР) существуют критерии DSM‑5 (Diagnostic and Statistical Manual of mental disorders):
- чрезмерная тревога и переживания в течение не менее чем 6 мес;
- невозможность контроля переживаний;
- тревога, приводящая к нарушениям в социальной, профессиональной и других сферах.
Почему же это не такая же болезнь, как, например, энтеровирус? Хотя все эти длительные нарушения приводят к «соматизации» тревоги, особенно у людей, не способных распознать и выразить свои чувства (алекситимия).
М.М. Орос подчеркнул, что на сегодняшний день существуют различные препараты для лечения ГТР, но особое место занимает прегабалин (Линбаг) как препарат первой линии. Преимуществами применения препарата Линбаг являются:
- быстрое анксиолитическое действие (на 1-й неделе терапии);
- устранение психических и соматических проявлений тревоги;
- нормализация сна;
- уменьшение проявлений субсиндромальной депрессии.
В данном клиническом случае врач назначал пациенту Линбаг (начальная доза – 75 мг/день с увеличением до 600 мг/день на протяжении 8 нед). Для нормализации сна препарат рекомендован в дозе 150-300 мг/сут. Отменять его рекомендуется постепенно.
Таким образом, являясь хроническим заболеванием, ГРТ нуждается в длительной терапии, поэтому препараты должны быть эффективными, иметь хорошую переносимость, минимальное лекарственное взаимодействие, быстрое начало действия и не вызывать «синдром отмены».
М.М. Орос представил вниманию коллег еще один доклад – «Нейропатический болевой синдром». Переходя к этой теме, он привел статистические данные, свидетельствующие о том, что 30-80% пациентов по всему миру не получают полноценной обезболивающей терапии.
Докладчик охарактеризовал боль как рефлекторный ответ, который может иметь различную продолжительность и бывает трех видов:
- ноцицептивная (вызвана воспалительным и невоспалительным компонентом в ответ на внешний фактор);
- нейропатическая (возникает при первичном повреждении или дисфункции нервной системы);
- боль с ноцицептивным и нейропатическим компонентами (возникает вследствие повреждений или болезней, которые затрагивают соматосенсорную систему).
Примерами ноцицептивной боли могут быть постоперационные или воспалительные суставные боли, когда пациент избегает движений в поврежденном суставе (страх движения). Боли в спине могут иметь смешанный характер (ноцицептивный и нейропатический).
Чем обычно блокируют боль? Периферическую боль (посттравматического или послеоперационного характера) купируют с помощью НПВП. Например, среди известных НПВП диклофенак натрия (Диклак®) – один из лучших представителей этого класса. Сочетание выраженного обезболивающего эффекта и хорошей переносимости делают его одним из наиболее часто назначаемых и длительно принимаемых препаратов.
Местно возможно применение Диклак® геля; для приема во внутрь – Диклак® таблеток 75 мг, с модифицированным высвобождением; для внутримышечного применения – Диклак® раствора 75 мг/3 мл.
Однако существуют факторы, приводящие к переходу полицептивной боли в хроническую:
- характеристика ноцицептивного сигнала (интенсивность, длительность);
- психосоциальные факторы;
- состояние антиноцицептивных систем.
Хроническая боль ведет к потере сигнальной функции, изменяется клиническая картина, что в дальнейшем плохо поддается лечению.
Хроническая нейропатическая боль часто имеет неясную природу и резистентна к опиатам, механизм ее появления – эктопическая импульсация (в связи со сменой работы ионных каналов), а отсутствие нисходящего сигнала вызывает усиление восприятия боли через дисбаланс между восходящими и нисходящими сигналами. После повреждения нерва и усиления импульсации может возникнуть центральная сенситизация. Это тот случай, когда «предотвратить легче, чем лечить».
Докладчик привел примеры позитивных сенсорных симптомов (спонтанная боль, аллодиния, гипералгезия, диз- и парестезия) и негативных (гипестезия, гипо- и аналгезия).
Существуют различные диагностические опросники для помощи в определении вида боли (ноцицептивная или нейропатическая) и соответственно в определении тактики дальнейшего лечения. Согласно рекомендациям Международной ассоциации по изучению боли (International Association for the Study of Pain – IASP), а также Канадского общества по изучению боли, препаратами первого ряда в терапии нейропатической боли позиционируют лиганды кальциевых альфа‑2-дельта каналов: прегабалин, габапентин. Эти рекомендации подтверждены данными, полученными в 105 клинических исследованиях.
Прегабалин (Линбаг) эффективен в лечении периферической нейропатической боли. Линбаг капсулы доступны нескольких дозировках: 75, 150 и 300 мг. При этом очень важно подобрать адекватную дозу, кратность приема и курс лечения. Отменять Линбаг нужно постепенно.
Под вопросом остается применение витаминов группы В при лечении болевой периферической нейропатии. К сожалению, на этот счет количество рандомизированных клинических исследований ограничено.
Доклад был завершен фразой канадского врача Уильяма Ослера: «Кто понимает боль, тот знает медицину». Как здесь не согласиться?
 Проблематика «Сепсис: обновленные рекомендации. Болевой синдром в хирургической практике» была раскрыта в докладе заведующего кафедрой анестезиологии и интенсивной терапии Ивано-Франковского национального медицинского университета, доктора медицинских наук, профессора И.И. Титова.
Проблематика «Сепсис: обновленные рекомендации. Болевой синдром в хирургической практике» была раскрыта в докладе заведующего кафедрой анестезиологии и интенсивной терапии Ивано-Франковского национального медицинского университета, доктора медицинских наук, профессора И.И. Титова.
После актуализации темы спикер отметил, что статистические данные в Украине по смертности от сепсиса, к сожалению, не ведутся, хотя в США эти цифры достаточно высоки – 200 тыс. смертей в год (что составляет 20-40% от всех случаев летальности).
Осложнением сепсиса является септический шок (СШ) – состояние, которое проявляется крайней степенью циркуляторных, клеточных и метаболических нарушений с большим риском смертности, в сравнении с самим сепсисом (60-80% летальности, по статистическим данным США).
Говоря о диагностике сепсиса и СШ, докладчик отметил следующие моменты:
- подозрение на сепсис оценивается по шкале qSOFA (quick Sequential Organ Failure Assesment): изменение состояния сознания, падение АД ≤100 мм рт. ст., тахипноэ – >22 уд./мин;
- оценка 2 балла и выше при наличии очага инфекции свидетельствует о начальной стадии развития сепсиса; оценка по шкале SOFA для определения органной дисфункции (от 0 до 4 баллов: уровень билирубина, креатинина, коагулограмма, респираторная функция и т. д.);
- уровень лактата >2 ммоль/л и прогрессирующая гипотензия при адекватной инфузионной терапии и вазопрессорной поддержке свидетельствуют о развитии СШ.
Антибактериальную терапию, применяемую для лечения сепсиса (на протяжение 10 сут), докладчик разделил на два этапа: старт – ескалационная стратегия, после идентификации возбудителя – деескалационная стратегия.
Было отмечено, что продление антибактериальной терапии необходимо при замедленном клиническом ответе, наличии очага инфекции, бактериемии MRSA (метициллин-резистентный золотистый стафилококк), у пациентов с иммуносупрессией.
Применение вазопрессоров:
- норадреналин – препарат выбора при СШ;
- возможное параллельное применение вазопрессина (до 0,03 ЕД/мин) или адреналина;
- дофамин – как альтернативный вазопрессорный препарат (при низком риске развития тахиаритмий и/или абсолютной брадикардии);
- добутамин – при явных признаках стойкой гипоперфузии, при условиях адекватной инфузионной и вазопрессорной терапии.
Препараты крови:
- трансфузия эритроцитарной массы при Hb <70 г/л;
- тромбоцитарная масса применяется при активном кровотечении (поддержка ≥50×109). Использование глюкокортикостероидов (ГКС), как и натрия гидрокарбоната и иммуноглобулинов, при СШ рутинно не рекомендуется. Данных по положительному использованию антикоагулянтов не выявлено.
Рекомендована профилактика тромбоэмболии преимущественно нефракционированным гепарином в сравнении с низкомолекулярным.
При нутритивной поддержке не рекомендовано применение омега‑3 жирных кислот, аргинина и глутамина.
Профессор И.И. Титов подчеркнул, что сепсис и СШ являются в 80% случаев ульцерогенными, что дает основание применять ингибиторы протонной помпы (ИПП) с лечебно-профилактической целью. Среди представителей ИПП (эзомепразол, омепразол, лансопразол) пантопразол (Пангастро®) является эффективным (угнетение секреции соляной кислоты желудка на 86% после 60 мин внутривенного введения), отличается быстротой действия (через 15 мин после начала приема) и одобрен FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США). Пангастро® характеризуется минимальным лекарственным взаимодействием, что является важным для пациентов с сепсисом, которые уже принимают определенное количество препаратов.
Докладчик также остановился на актуальной в травматологии и ортопедии проблеме постоперационного обезболивания. По алгоритмам обезболивания ВОЗ, кетопрофен (Кетонал®) входит в первую и вторую линии обезболивающей терапии, при этом имея минимальный риск поражения почек (в сравнении с кеторолаком и мелоксикамом). Вещество проявляет обезболивающее действие на уровне с морфином, но имеет хороший профиль безопасности со стороны сердечно-сосудистой системы.
Кетонал® разрешен для применения в странах Европейского Союза, в отличие от кеторолака, который запрещен во многих ведущих европейских странах.
Было подчеркнуто, что мощный эффект плюс минимальный риск осложнений позволяет использовать Кетонал® длительно (в сравнении с нимесулидом, напроксеном, кеторолаком), а широкий выбор форм выпуска позволяет применять его в разных клинических ситуациях. Благодаря двойному виду пелет в капсуле Кетонал® Дуо (40% – медленного высвобождения и 60% – быстрого), его можно использовать 1 раз в сутки.
В заключение было подчеркнуто, что при лечении сепсиса важно не применять потенциально опасные терапевтические средства. При болевом синдроме следует использовать эффективные и удобные для примененияи анальгетики и контролировать желудочную кислотность с помощью качественных ИПП, резюмировал профессор И.И. Титов.
Таким образом, в рамках научно-практической конференции «Вторая зимняя школа травматологов» были раскрыты аспекты этиологии, патогенеза, диагностики и лечения болевых синдромов, которые не так часто встречаются в каждодневной практике врача-травматолога, однако заслуживают пристального внимания, когда речь идет о конкретном пациенте. Большое внимание было уделено проблемам КРБС. Акцент был сделан на трудоемкости и длительности лечения этого синдрома, на необходимости большей освещенности вопросов прогнозирования, что, безусловно, должно способствовать адресной профилактике и превентивному лечению пациентов.
Подготовила Марина Астахова
Информация для специалистов сферы здравоохранения
3-15-АНП-РЕЦ-0319