28 червня, 2019
Роль дисліпідемій у дитячому віці в розвитку атеросклерозу дорослих
 Сьогодні доведено той факт, що причинами розвитку багатьох захворювань системи кровообігу в дорослому віці, які зазвичай повільно розвиваються, є різні патологічні стани, що беруть свій початок у дитячому віці. Тому діагностика й оцінювання прогнозу стану серцево-судинної системи у дітей лежать в основі запобігання захворюваності та смертності в осіб старшого віку.
Сьогодні доведено той факт, що причинами розвитку багатьох захворювань системи кровообігу в дорослому віці, які зазвичай повільно розвиваються, є різні патологічні стани, що беруть свій початок у дитячому віці. Тому діагностика й оцінювання прогнозу стану серцево-судинної системи у дітей лежать в основі запобігання захворюваності та смертності в осіб старшого віку.
Останнім часом значно збільшилася кількість і частота серцево-судинних захворювань, випадків раптової смерті у підлітків та осіб молодого віку при фізичному навантаженні, випадків інфаркту, ішемічного інсульту у дітей, предикторами яких були атеросклеротичні ураження судин, що розвиваються без виражених клінічних проявів (C. Stefanadis et al., 2017; J. Won et al., 2018). У дитячому віці при впливі несприятливих, провокувальних чинників морфологічно спостерігається накопичення ліпідів в інтимі артерій: уже навіть на 3‑4‑му році життя виявляють окремі жирові прожилки в артеріях, а атеросклеротичні бляшки можуть почати формуватися з 13-15 років (Э.А. Юрьева и соавт., 2014). Особливість атеросклеротичних змін у стінках судин у дитячому віці полягає в тому, що клінічний перебіг усіх цих уражень безсимптомний (латентний період), тому виявлення, профілактика прогресування, розвитку патологічного процесу із залученням органів є нагальною потребою з метою запобігання розвитку тяжких органічних уражень серцево-судинної системи як у дитячому, так і в дорослому віці.
Атеросклероз (код за Міжнародною класифікацією хвороб 10-го перегляду I70) – варіабельна комбінація змін внутрішньої оболонки (інтими) артерій, що включає скупчення ліпідів, складних вуглеводів, клітин гематологічного походження, фіброзної тканини, кальцифікацію та супутні зміни середньої оболонки артеріальної стінки (медії).
Епідеміологія
Аналізуючи дані різних досліджень (S. Mendis, Р. Puska et al., 2016), можна відзначити наявність ознак раннього атеросклерозу більш ніж у 50% американських дітей віком 10-14 років. Серед молодих японців (1 місяць – 39 років) за даними загальнонаціонального дослідження під час аутопсії у 29% випадків було виявлено наявність жирових прожилок в аорті у дітей віком менше 1 року та в 3,1% коронарних артерій у дітей віком від 1 до 9 років. Частота виявлення жирових прожилок у коронарних артеріях збільшувалася з віком: від 50% у віці 2-15 років до 85% у віці 21-39 років. Вона корелювала із збільшенням індексу маси тіла (ІМТ), підвищенням артеріального тиску, рівня сироваткового загального холестерину (ЗХС) і холестерину ліпопротеїнів низької щільності. За даними внутрішньосудинного ультразвукового дослідження, у 17% здорових молодих осіб до 20 років, у 37% – 20-29 років, у 60% – 30-39 років, у 71% – 40‑49 років та у 85% осіб старших 50 років наявні ознаки атеросклерозу коронарних артерій. Однак у молодому віці ці порушення можуть мати зворотний розвиток, якщо своєчасно провести лікувально-профілактичні заходи.
Етіологія
Виникнення атеросклерозу в будь-якому віці, в тому числі дитячому, залежить від багатьох різних факторів, тобто його розвиток є поліетіологічним. Морфологічною основою атеросклерозу є утворення холестеринових бляшок в інтимі артерій зі звуженням їх просвіту, утрудненням внутрішньосудинного кровотоку аж до його повного зникнення. Окрім того, у разі приєднання запального процесу в стінці судини може виникнути виразка бляшки, що стає причиною утворення тромбу та розвитку тромбоемболії судин, призводить до смертельно небезпечних патологічних станів.
До факторів ризику розвитку атеросклерозу в дитячому віці належать:
- обтяжена спадковість щодо серцево-судинної патології у батьків;
- внутрішньоутробна затримка росту або розвитку плода;
- дисліпопротеїнемія у дитячому віці;
- артеріальна гіпертензія;
- велика маса тіла при народженні й ожиріння під час росту дитини;
- нераціональне харчування;
- недостатня рухова активність і зменшення фізичних навантажень;
- куріння (як активне, так і пасивне);
- психоемоційні перевантаження та стреси;
- порушення толерантності до глюкози;
- перенесена хвороба Кавасакі.
Одним з факторів, що ініціює розвиток цього патологічного процесу в молодому віці, є вплив ксенобіотиків (наприклад, поліциклічних ароматичних вуглеводнів, бензпірену, важких металів тощо), які потрапляють в організм з будь-яких виробничих, невиробничих джерел і накопичуються роками.
Патогенез
Холестерин нерозчинний у водному середовищі, у крові зв’язується з певними білками, формуючи білково-жирові комплекси, які називають ліпопротеїнами. Тріацилгліцериди, вільний холестерин, складні ліпіди є основними ліпідами, які беруть участь в енергетичних і різних анаболічних процесах в організмі людини. Тріацилгліцериди – складні сполуки, які під дією панкреатичних і жовчних кислот розпадаються на дрібніші складові та всмоктуються ентероцитами, вільний холестерин всмоктується у вільному стані. В ентероцитах розщеплені жири перетворюються у свої транспортні форми (хіломікрони), вкриті шаром активних білків і фосфоліпідів, які через мембрану ентероцитів потрапляють у лімфатичну систему, а далі – у периферичний кровообіг та органи. Ліпопротеїни допомагають хіломікронам не розчинитися в крові дочасно, перш ніж вони досягнуть потрібних органів. Ліпопротеїни відрізняються за щільністю та поділяються на такі підкласи:
- ліпопротеїни дуже низької щільності (ЛПДНЩ);
- ліпопротеїни низької щільності (ЛПНЩ);
- ліпопротеїни високої щільності (ЛПВЩ).
ЛПНЩ є основним «транспортом» для холестерину та перетворених жирів у необхідні органи. ЛПНЩ можуть стати причиною гіперхолестеринемії, але відбувається це тільки тоді, коли ЛПНЩ втрачають можливість розносити хіломікрони у тканини. Саме тоді розвивається такий загальний стан, як гіперліпопротеїнемія, а гіперхолестеринемія є її підвидом.
ЛПВЩ евакуюють зайвий холестерин із клітин і тканин, транспортують невикористаний холестерин від тканин у печінку, де з нього синтезуються жовчні кислоти з подальшим виведенням з організму через шлунково-кишковий тракт. Це найголовніший захисник організму, що виконує антиатерогенну функцію.
Зважаючи на вагому роль ліпідів і пов’язаних з ними порушень в атеросклеротичному процесі, слід розглянути поняття дисліпідемій. Під останніми розуміють порушення функції та/або складу ліпідів і ліпопротеїнів крові, що можуть виникати унаслідок багатьох причин та здатні самостійно або у взаємодії з іншими факторами ризику спричиняти маніфестацію атеросклеротичного процесу. Велике значення має так звана атерогенна ліпідна тріада, що включає зростання рівня ЛПДНЩ і пов’язане з цим підвищення рівня тригліцеридів (ТГ), ЛПНЩ та зниження рівня ЛПВЩ.
Крім терміна «дисліпідемія», який є найбільш широким, для характеристики порушень ліпідного спектра крові використовують і терміни «гіперліпопротеїнемія» та «гіперліпідемія».
Термін «гіперліпопротеїнемія» означає будь-яке підвищення рівня ліпідів і ліпопротеїнів у плазмі крові вище за оптимальні значення.
Термін «гіперліпідемія» є найбільш простим, тому що для його використання досить лише визначити підвищення рівня ліпідів крові (холестерину та ТГ) вище за оптимальний.
Дисліпідемії можуть бути наслідком як генетичних зрушень (первинні дисліпідемії) та/або супутніх захворювань (вторинні дисліпідемії).
Порушення ліпідного обміну є фундаментом атеросклеротичного процесу: надлишкове накопичення ліпідних фракцій сприяє формуванню атеросклеротичних нашарувань. Порушення ліпідного обміну можуть мати різні прояви: збільшення рівня атерогенних фракцій холестерину – ЛПНЩ, ЛПДНЩ, зниження рівня антиатерогенної фракції холестерину – ЛПВЩ. Поєднання ендотеліальної дисфункції та дисліпідемії призводить до початку формування бляшок, що складаються з кришки, яка включає клітини гладеньких м’язів і фіброзної тканини під шаром ендотелію, і ядра, що містить жири. Оскільки бляшка випинається в просвіт судини, зменшуючи його діаметр, вона створює передумови для погіршення забезпечення кров’ю тих органів і тканин, які розташовані в басейні кровопостачання ураженої судини. Особливо це стає помітним і клінічно значущим в умовах підвищеного функціонального навантаження органа, наприклад, серця, нижніх кінцівок. Виникнення диспропорції між потребою органа під час фізичної активності в кисні, який доставляється необхідним об’ємом крові, та його реальним надходженням лежить в основі розвитку гіпоксії органа. Саме тканинна гіпоксія (гостра або хронічна) зумовлює появу клінічних симптомів при атеросклерозі.
Одним із факторів ризику розвитку атеросклерозу є гіперкоагулянтна активність крові. Підвищення рівня фібриногену в крові збільшує ймовірність розвитку атеросклерозу в 3-4 рази. До факторів ризику належить також збільшення активності фактора згортання VII, підвищення вмісту в крові інгібітора активатора плазміногену, D-димера – продукту деградації фібрину, підвищення агрегації тромбоцитів (при цьому часто виявляється посилення експресії гена рецепторів тромбоцитів GP Ilb/IIIa).
Розвиток атеросклерозу судин проходить три основні фази.
- Стадія ендотеліального пошкодження, що включає альтерацію ендотелію та адгезію лейкоцитів і тромбоцитів.
- Стадія пошкодження інтими, що включає міграцію моноцитів в інтиму і перетворення їх у макрофаги, фагоцитоз ліпідів макрофагами, формування фіброзної капсули.
- Стадія пошкодження інтими-медії, що включає відкладення кальцію, порушення кровообігу, розрив капсули, кровотечу, вивільнення прокоагулянтів, тромбоз, емболію, аневризму судин.
Окрім того виділяють декілька клінічних стадій розвитку атеросклерозу.
- Доліпідна (ліпіди ще не фіксуються на судинній стінці, тільки пошкоджують її).
- Ліпідоз (ліпіди інфільтрують судинну стінку, утворюючи на поверхні інтими жовтуваті плями, що не заважають руху крові, стадія не має клінічних проявів, може відбуватися зворотний розвиток).
- Атероматоз (формуються бляшки, які виступають у просвіт судини, мають сполучнотканинну капсулу та ліпідний детрит усередині).
- Розрив капсули (нестабільні жовті бляшки з тонкою сполучнотканинною капсулою, які характеризуються високою ймовірністю розриву капсули і потрапляння детриту в кровообіг, що може стати причиною тромбоемболії, інфаркту, інсульту).
- Ущільнення та кальциноз (стабільні білі бляшки мають щільну кришку, вони не схильні до розривів, можуть значно звужувати просвіт судин аж до повної облітерації, особливо якщо в бляшці відкладаються солі кальцію).
У літературі обговорюються теорії запалення й імунної відповіді на пошкодження, які якнайкраще розкривають основні механізми розвитку саме безліпідного (доліпідного) ураження інтими артерій, що є характерним для осіб молодого віку. Медіатори запалення, насамперед фактор некрозу пухлини та інтерлейкін‑6, активують синтез і вивільнення у кров ЛПДНЩ паралельно із пригніченням ліпопротеїнової ліпази. У результаті цього у крові розвиваються гіперхолестеринемія та гіпертригліцеридемія, знижується вміст ЛПВЩ. Разом з тим медіатори запалення знижують активність NO-синтетази та стимулюють локальну продукцію С-реактивного білка, який посилює секрецію вазоконстрикторів (ендотеліну та тромбоксану), знижує виділення вазодилататорів (оксиду азоту (NO) та простацикліну) і, як наслідок, виникає дисфункція ендотелію, що призводить до пошкодження стінок судин. Після пригнічення запальної реакції показники метаболізму ліпопротеїнів частково нормалізуються, однак порушення присутні ще протягом тривалого періоду.
Класифікація
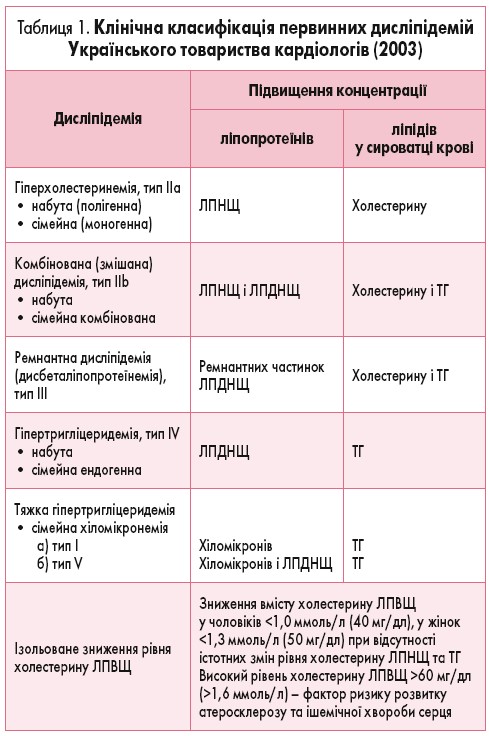 За клінічною класифікацією дисліпідемій (М.І. Лутай, 2003, табл. 1) у дорослих рівні ліпідів крові вважають патологічними, якщо вміст ЗХС становить >6,2 ммоль/л (240 мг/дл), ЛПНЩ >4,1 ммоль/л (160 мг/дл) і ТГ >2,3 ммоль/л (200 мг/дл).
За клінічною класифікацією дисліпідемій (М.І. Лутай, 2003, табл. 1) у дорослих рівні ліпідів крові вважають патологічними, якщо вміст ЗХС становить >6,2 ммоль/л (240 мг/дл), ЛПНЩ >4,1 ммоль/л (160 мг/дл) і ТГ >2,3 ммоль/л (200 мг/дл).
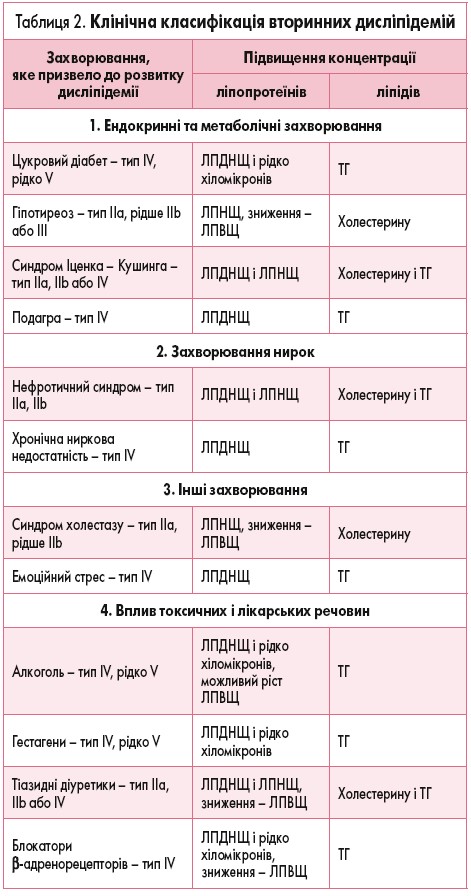
Як видно з класифікації, дисліпідемія може бути вторинною щодо інших станів, це необхідно намагатися усунути перед початком дієти й особливо медикаментозної терапії (табл. 2). Виключення потребує клінічного оцінювання та виконання деяких клінічних тестів: визначення рівня тиреотропного гормону, аланінамінотрансферази, альбуміну, глюкози, глікозильованого гемоглобіну та креатиніну в плазмі крові, середнього вмісту еритроцитів; виявлення глюкози та білка в сечі. Пацієнти, що можуть мати спадкові хвороби типу сімейної гіперхолестеринемії, мають отримати консультацію фахівців, зокрема зі встановленням молекулярного генетичного діагнозу.
Всесвітня організація охорони здоров’я класифікує атеросклероз за походженням і локалізацією.
За походженням виділяють:
- гемодинамічний атеросклероз, який розвивається у разі артеріальної гіпертензії та інших судинних порушень як наслідок високої швидкості руху крові та механічного впливу на еластичність судини;
- метаболічний атеросклероз, який виникає на тлі спадково-конституціональних порушень ліпідного обміну, аліментарних розладів, ендокринних захворювань (гіпотиреоз, цукровий діабет, хвороби печінки та нирок);
- змішаний атеросклероз.
 За локалізацією в судинах органів і систем розрізняють атеросклероз:
За локалізацією в судинах органів і систем розрізняють атеросклероз:
- судин головного мозку;
- сонних артерій;
- коронарних артерій;
- аорти;
- ниркових артерій;
- мезентеріальних судин;
- артерій нижніх кінцівок;
- артерій очного дна.
У Міжнародній класифікації хвороб 10-го перегляду виділено такі коди:
I70. Атеросклероз.
I70.1. Атеросклероз ниркових артерій / нирка Голдблатт.
I70.2. Атеросклероз артерій кінцівок / атеросклеротична гангрена, склероз Менкеберга.
I70.9. Генералізований і неуточнений атеросклероз.
I67.2. Церебральний атеросклероз.
I25.1. Атеросклероз коронарних артерій.
I27.0. Атеросклероз легеневих артерій.
K55.1. Атеросклероз мезентеріальних судин у розділі «Хронічні судинні хвороби».
Клінічна картина
Клінічні прояви атеросклерозу у дітей чітко не виражені. Найчастіше у пацієнтів молодого віку спостерігається доклінічна стадія атеросклерозу. Холестерин може відкладатися у судинах різних частин тіла, може виявлятися у вигляді жовтуватих плям навколо повік (ксантелазма), на зовнішній межі райдужної оболонки ока (рогівкова дуга) і у вигляді горбків у ділянках сухожиль верхніх кінцівок, а також ліктів, колін і стоп (ксантома сухожилля).
Найбільш показовими та найдетальніше вивченими клінічними проявами атеросклерозу у дітей є симптоми сімейної гіперхолестеринемії. Сімейна гіперхолестеринемія (СГ) – гетерогенна аутосомно-домінантна хвороба, при якій спостерігається надзвичайно висока гіперхолестеринемія з раннього дитячого віку, зокрема, дуже високий рівень ЛПНЩ, а також раннє (у молодому віці) ураження органів і систем. Патогенетично це проявляється тим, що унаслідок генетичних порушень ліпопротеїни не можуть зв’язуватися з холестерином і переносити його у тканини. Ще одним фактором, що сприяє розвитку цього захворювання, є підвищений синтез холестерину в організмі. У частини пацієнтів відбуваються мутації в гені рецептора ЛПНЩ, який кодує білок ЛПНЩ-рецептора, що відповідає за поглинання ЛПНЩ з кровообігу, або аполіпопротеїну В (апо-В), який є частиною ЛПНЩ, що зв’язується з рецептором (процес, необхідний для зв’язування ЛПНЩ з рецептором).
Гомозиготна форма СГ розвивається тоді, коли обоє батьків мають порушення у структурі гена рецепторів до ЛПНЩ. Гомозиготна форма СГ супроводжується тяжкими патологічними серцево-судинними змінами у дітей, зустрічається з частотою 1 на 1 млн новонароджених.
Гетерозиготна СГ є більш поширеним генетичним захворюванням, у загальній популяції у більшості країн вона фіксується з частотою 1 на 500 осіб. Гетерозиготна СГ виникає за наявності в одного з батьків дефектного гена до ЛПНЩ-рецепторів. У пацієнтів із гетерозиготною формою СГ серцево-судинні захворювання можуть виникати у віці від 30 до 40 років. Гетерозиготна форма СГ часто залишається невиявленою до розвитку серцево-судинної недостатності.
У дітей із сімейною формою атеросклерозу зовнішній вигляд має специфічні особливості: спостерігається сухість шкіри, знижений тургор тканин (в’ялість шкіри), ліпідна смуга на рогівці очей внаслідок відкладення ліпідів, ксантоми, які найчастіше локалізуються навколо очей і в ділянці ліктьових суглобів (по згинальній поверхні). Патолого-анатомічно виявляють масивний атероматоз клапана і висхідної частини дуги аорти, у великих артеріях спостерігаються подібні, але менш виражені зміни із відкладанням холестеринових бляшок в артеріях органів.
Атеросклероз аорти характеризується відсутністю специфічних скарг. Із загальних скарг можна виділити швидку втомлюваність, погану переносимість фізичних навантажень. Специфічні ознаки – аорталгії (пекучий біль за грудниною, що іррадіює в руку, шию, верхню частину живота і спину), – які не мають характеру чітких нападів, виникають епізодично, з’являються під час фізичного навантаження, при цьому пацієнт може страждати годинами.
Симптоми атеросклерозу коронарних судин – біль за грудниною і відчуття нестачі повітря. Вираженість болю може бути різною, від відчуття тяжкості до пекучого і колючого болю, він може іррадіювати в ліве плече, лопатку, нижню щелепу, епігастрій. Спочатку симптоми з’являються при фізичних навантаженнях, потім і в стані спокою.
Атеросклероз судин шиї проявляється постійним головним болем, запамороченням, яке посилюється при розумових і фізичних навантаженнях.
Атеросклероз судин головного мозку проявляється періодичним головним болем, запамороченням, відсутністю концентрації уваги, можливе зниження слуху, відчуття шуму в голові.
Атеросклероз черевного відділу аорти супроводжується порушенням кровопостачання органів черевної порожнини, тому з’являються скарги на біль у животі, нудоту, порушення дефекації. Якщо в патологічний процес залучаються судини нирок – розвиваються набряки, підвищується артеріальний тиск, виявляють зміни в аналізі сечі.
При розвитку оклюзії судин нижніх кінцівок з’являються скарги на похолодання стоп, пальців, слабкість, парестезії, під час руху виникають біль, судоми в м’язах, порушується трофіка шкіри.
Діагностика
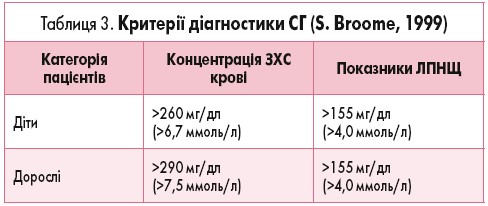 Діагноз СГ ґрунтується на даних анамнезу (гіперхолестеринемія у батьків, випадки ранньої смерті у сім’ї через захворювання серцево-судинної системи), наявності ксантом, ксантелазм у ділянці верхніх і нижніх повік, відкладень холестерину на внутрішній оболонці райдужки очей (arcus lipoidea), підвищенні рівня ЗХС за рахунок ЛПНЩ до 75-13 ммоль/л у пацієнтів з гетерозиготною формою і до 16-20 ммоль/л – із гомозиготною (табл. 3). Найточніше діагноз СГ можна встановити на підставі аналізу ДНК на присутність мутації в гені рецептора до ЛПНЩ.
Діагноз СГ ґрунтується на даних анамнезу (гіперхолестеринемія у батьків, випадки ранньої смерті у сім’ї через захворювання серцево-судинної системи), наявності ксантом, ксантелазм у ділянці верхніх і нижніх повік, відкладень холестерину на внутрішній оболонці райдужки очей (arcus lipoidea), підвищенні рівня ЗХС за рахунок ЛПНЩ до 75-13 ммоль/л у пацієнтів з гетерозиготною формою і до 16-20 ммоль/л – із гомозиготною (табл. 3). Найточніше діагноз СГ можна встановити на підставі аналізу ДНК на присутність мутації в гені рецептора до ЛПНЩ.
Визначена сімейна гіперхолестеринемія. Окрім зазначених симптомів спостерігається наявність ксантом сухожиль чи їх наявність у родичів 1-ї або 2-ї лінії спорідненості. Під час генетичного дослідження виявляють мутацію гена рецептора до ЛПНЩ, сімейний дефект апо-В‑100 чи мутацію PCSK9.
Можлива гіперхолестеринемія. Інфаркт міокарда в сімейному анамнезі:
- у родича 2-ї лінії молодшого 50 років;
- у родича 1-ї лінії молодшого 60 років або підвищення рівня ЗХС в сімейному анамнезі:
– >290 мг/дл (>7,5 ммоль/л) – у дорослих родичів 1-ї та 2-ї лінії;
– >260 мг/дл (>6,7 ммоль/л) – у дітей молодших 16 років.
Діагноз атеросклероз у дітей ґрунтується на наявності скарг, даних анамнезу, лабораторних та інструментальних досліджень.
Діагностичні заходи у разі припущення наявності атеросклерозу включають:
- загальний огляд із пальпацією всіх доступних артерій та аускультацією серця;
- офісне вимірювання, добовий моніторинг артеріального тиску;
- оцінювання ІМТ.
Лабораторні й інструментальні дослідження:
- аналіз крові на згортання, ліпідний профіль;
- ехокардіографія;
- електрокардіографія та добовий моніторинг електрокардіограми й артеріального тиску;
- проби з фізичним навантаженням (велоергометрія, тредміл-тест);
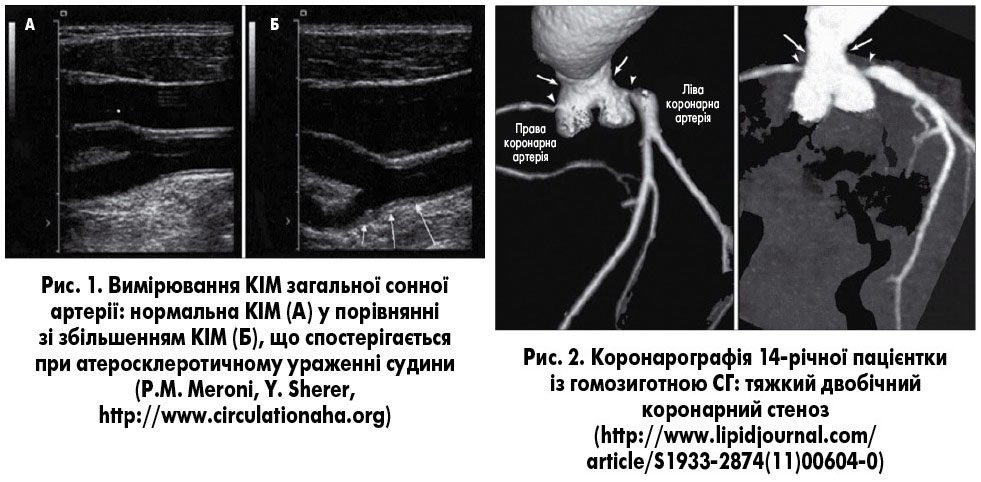
- доплерографічне дослідження екстрамедулярних артерій (внутрішня та загальна сонна) із вимірюванням комплексу інтима-медія (КІМ), внутрішньомозкових судин (рис. 1);
- ангіографія з контрастуванням;
- магнітно-резонансна томографія, в тому числі із контрастуванням;
- коронарографія – рентгенологічна візуалізація судин (рис. 2).
Ведення пацієнтів
Клінічні ознаки атеросклерозу найчастіше проявляються уже в дорослому віці. У дітей і підлітків насамперед слід проводити профілактику розвитку атеросклерозу, спрямовану на «оздоровлення» способу життя як дитини, так і всіх членів сім’ї. Діти та їхні батьки мають отримувати в доступній для них формі інформацію про здоровий спосіб життя, наявність у родині факторів ризику атеросклеротичних уражень судин і появу клінічної симптоматики. Необхідно проаналізувати систему харчування сім’ї, провести відповідну корекцію, зменшити споживання солі до менш ніж 6 г на добу, обмежити споживання цукру та солодощів.
 У таблиці 4 представлено рекомендації щодо харчування при атеросклерозі.
У таблиці 4 представлено рекомендації щодо харчування при атеросклерозі.
Основними принципами гіполіпідемічної дієти є зменшення маси тіла при її надлишку. Через 3 місяці, в разі неефективності стандартної дієти, споживання жирів слід обмежити до 25-30% добової калорійності, в тому числі менше 7% за рахунок насичених жирних кислот. Дуже важливо підібрати дітям відповідне фізичне навантаження (лікувальна фізкультура, ходьба, біг, фізичні вправи). Виявлено, що в осіб молодого віку з надлишковою масою тіла й ожирінням комбінація дієтотерапії з фізичними навантаженнями була більш ефективною щодо зниження маси тіла та КІМ порівняно з ізольованою дієтотерапією.
Алгоритм виявлення атеросклеротичних змін у судинах у дитини має включати:
- оцінювання наявності основних факторів ризику та ранній розвиток серцево-судинних захворювань у батьків, бабусь і дідусів дитини;
- визначення маси тіла й ІМТ (ІМТ >85 процентилю свідчить про ризик розвитку надлишкової маси тіла, >95 процентилю – про надлишкову масу тіла);
- вимірювання артеріального тиску починаючи з 3 років під час кожного огляду, оцінювання проводять відповідно до вікових нормативів, статі та зросту. Систолічний і/або діастолічний артеріальний тиск >90 процентилю відповідає високому нормальному артеріальному тиску, >95 процентилю – артеріальній гіпертензії;
- з’ясування відомостей про куріння батьків, що проживають з дитиною, та самої дитини;
- визначення рівня ліпідів крові натще з 2 років при наявності сімейних факторів ризику.
Характеристика рівня ЗХС у дітей і підлітків:
- бажаний (прийнятний) <170 мг/дл (4,4 ммоль/л);
- граничний – 170-199 мг/дл (4,4-5,15 ммоль/л);
- високий – 200 мг/дл (5,2 ммоль/л) і більше.
 Якщо у дитини при двох і більше аналізах ліпідного профілю натще, виконаних з інтервалом 2 тижні (але не більше 3 місяців), виявлено патологічні зміни, виникає необхідність призначення медикаментозної терапії.
Якщо у дитини при двох і більше аналізах ліпідного профілю натще, виконаних з інтервалом 2 тижні (але не більше 3 місяців), виявлено патологічні зміни, виникає необхідність призначення медикаментозної терапії.
Терапію статинами слід починати з найнижчої дози одноразово на день. Під час лікування статинами необхідний моніторинг клінічних симптомів з боку кістково-м’язової системи (міалгії, м’язової слабкості) та контроль рівня печінкових трансаміназ і креатинкінази через кожні 4 тижні. Терапію можна продовжити, якщо у пацієнтів досягнуто цільового рівня холестерину ЛПНЩ без патологічних відхилень контрольних показників лабораторних досліджень. Повторне оцінювання проводять через 8 тижнів, 3 місяці. Пацієнтам з порушеннями лабораторних показників або побічними реакціями потрібно припинити прийом препаратів до нормалізації цих параметрів.
У разі недосягнення цільового рівня холестерину ЛПНЩ принаймні через 3 місяці лікування дозу препарату можна збільшити на 10 мг. Якщо рівень холестерину ЛПНЩ не досягає цільових значень через 3 місяці, можливе підвищення дози на 10 мг. Ризик та ефективність ескалації доз вивчали в кількох клінічних дослідженнях щодо застосування статинів у пацієнтів дитячого віку, в яких продемонстровано безпеку такої терапії. Разом із статинами доцільно призначати препарати, які посилюють секрецію жовчних кислот, або інгібітори абсорбції холестерину.
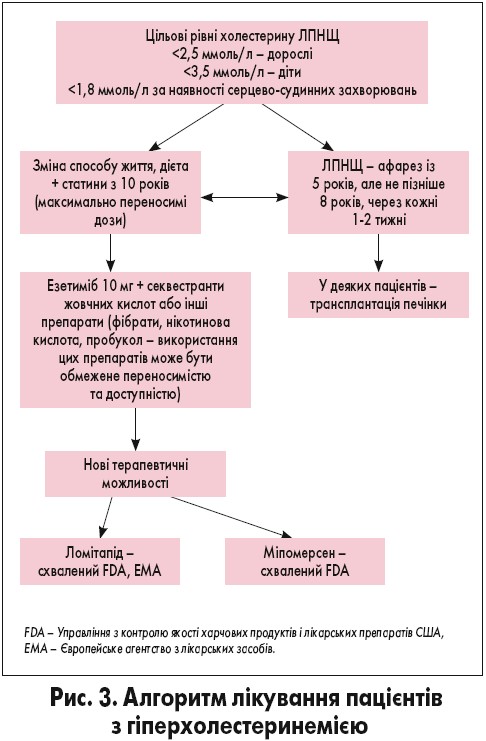
Алгоритм лікування пацієнтів із СГ представлено на рисунку 3.
Таким чином, своєчасне виявлення пацієнтів з гіперхолестеринемією, особливо дитячого віку, їх адекватне ведення згідно з міжнародними рекомендаціями здатне знизити швидкість розвитку атеросклеротичних процесів та ризик виникнення фатальних серцево-судинних подій у майбутньому.
Список літератури знаходиться в редакції.
Тематичний номер «Педіатрія» №2 (49), травень 2019 р.