10 жовтня, 2019
Практичне ведення супутніх серцево-судинних захворювань при ревматоїдному артриті
Ревматоїдний артрит (РА) – поширене хронічне запальне захворювання суглобів, яке уражає до 1% населення планети та призводить до інвалідності, спричиненої ураженням суглобів або позасуглобовими проявами (Smolen J. et al., 2016). Незважаючи на те що за останні 20 років досягнуто значних успіхів у розумінні патогенезу та лікуванні РА, тривалість життя при цій хворобі менша, ніж у загальній популяції (Dadoun S. et al., 2013).
Супутні серцево-судинні захворювання (ССЗ) – часті позасуглобові прояви РА (табл. 1), ризик виникнення яких удвічі вищий, аніж у людей без РА (Sen D. et al., 2014; Nurmohamed M. et al., 2015; Houri Levi E. et al., 2016). Найбільше клінічне значення має прискорений атеросклероз, особливо у формі ішемічної хвороби серця (ІХС), оскільки це основна причина передчасної смерті при більшості аутоімунних ревматичних станів (Hollan I. et al., 2013). Відтак ризик смерті та захворюваності на ССЗ збільшується на 60 і 48% відповідно (Meune C. et al., 2009; Avina-Zubieta J. et al., 2012).
Підвищений ризик розвитку ССЗ у пацієнтів із РА зумовлений не лише традиційними факторами ризику (ФР), хоча їх вплив при цій хворобі високий (Baghdadi L. et al., 2015). З’являється дедалі більше доказів, що РА, як і цукровий діабет, можна вважати незалежним ФР ССЗ (Lindhardsen J. et al., 2011). Тому для оцінки ризику розвитку ССЗ у пацієнта з РА необхідно враховувати чимало нюансів.
Клінічні прояви у хворих на РА часто атипові, що зумовлює гіподіагностику та відсутність адекватного лікування ССЗ (Maradit-Kremers H. et al., 2005; Davis J. et al., 2008). Традиційні методи візуалізації часто пропускають субклінічні прояви ССЗ, натомість нові діагностичні методи дають змогу виявити субклінічну дисфункцію міокарда та мікросудинні хвороби (Greulich S. et al., 2016). Крім фармакологічних і нефармакологічних впливів на традиційні ФР, для зниження ризику ССЗ дуже важливо контролювати запалення й активність РА, оскільки є дані, що це зменшує смертність від ССЗ (Roubille C. et al., 2015; Myasoedova E. et al., 2017). Тривають дискусії про оптимізацію зниження ризику ССЗ і ведення коморбідності при РА. Нещодавно на підставі нових доказів робоча група Європейської протиревматичної ліги (EULAR) оновила рекомендації 2009 року щодо стратегій зниження ризику ССЗ у хворих на запальні захворювання суглобів, зокрема РА (Agca R. et al., 2017).
Патогенез
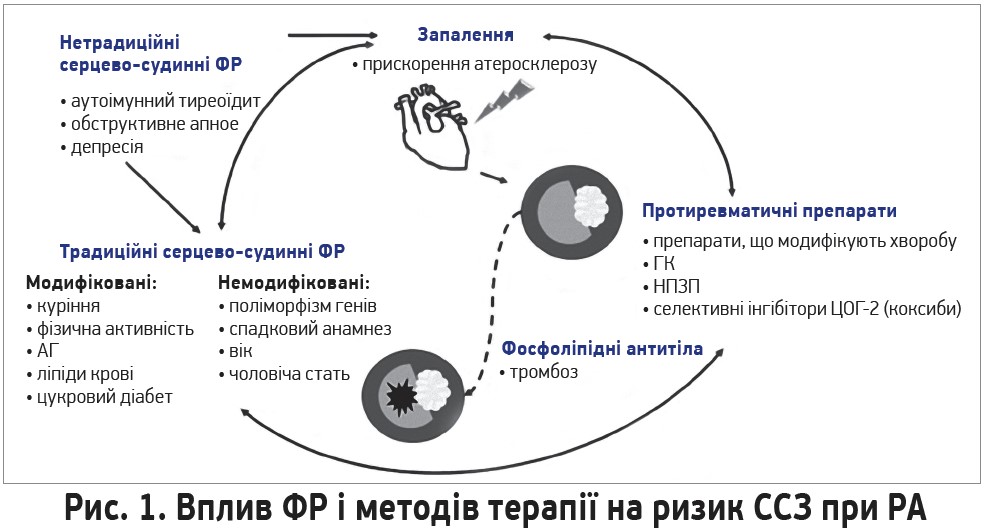
Патогенетичні механізми, котрі прискорюють виникнення ССЗ при РА, доволі складні й до кінця не з’ясовані (рис. 1). Кілька варіантів поліморфізму генів у локусах головного регіону комплексу гістосумісності пов’язані як з атеросклерозом, так і з РА. Виявлено зв’язки спільних епітопів алелів HLA-DRB1*04 з дисфункцією ендотелію та ризиком ССЗ. Описано варіанти поліморфізму, пов’язані з дисліпідемією, артеріальною гіпертензією (АГ) та ризиком серцево-судинних ускладнень у пацієнтів із РА, незалежні від наявності традиційних ФР (Nurmohamed M. et al., 2015). Традиційні та нещодавно визначені ФР підсумовано в таблиці 2 (Gualtierotti R. et al., 2017).
Імунні механізми та запалення можуть прискорювати атеросклероз навіть у ранніх фазах багатьох аутоімунних захворювань, адже між запаленням і коагуляційним шляхом існує широка перехресна взаємодія (Hollan I. et al., 2013; Durante A., Bronzato S., 2015; van den Oever I. et al., 2014). Активація прозапальних цитокінів спричиняє дисфункцію ендотелію, інсулінорезистентність, дисліпідемію та протромботичний стан із порушеннями в системах згортання та фібринолізу (Cugno M. et al., 2010). Запалення відіграє важливу роль як при РА, так і при атеросклерозі (Libby P. et al., 2011). Нещодавно з’ясовано, що РА й ІХС пов’язують процеси цитрулінування та карбамілювання (Cambridge G. et al., 2013).
Оцінка ризику ССЗ
За сучасними уявленнями, РА вважають незалежним ФР ССЗ, що враховано в рекомендаціях Європейського товариства кардіологів (ESC) із профілактики ССЗ (Piepoli M. et al., 2016). Серед ФР, пов’язаних із РА, заслуговують на увагу висока активність, тривалість хвороби >10 років, наявність позасуглобових проявів, РФ та/або АЦПА (Ingegnoli F. et al., 2013; Agca R. et al., 2017).
Слід обов’язково враховувати стани та ФР, не пов’язані з РА: цукровий діабет, хронічна хвороба нирок, АГ, терапія з приводу раку, періодонтит, синдром обструктивного апное уві сні, еректильна дисфункція, сімейний анамнез, етнічна приналежність, психосоціальні фактори (соціально-економічний статус, порушення настрою). Для характеристики ваги переважно застосовують індекс маси тіла, але при РА, особливо за умови терапії ГК, депонування жиру в тілі часто змінене (синдром Кушинга). За таких обставин краще використовувати окружність талії (Giles J. et al., 2010). З іншого боку, в пацієнтів із тривалим перебігом і високою активністю РА часто є кахексія, котра також належить до ФР ССЗ (Okano T. et al., 2017).
Досі не визначено значення запальних (високочутливий С-реактивний протеїн, фібриноген), ліпідних (аполіпопротеїни) та тромботичних (гомоцистеїн, асоційована з ліпопротеїном фосфоліпаза А2) біомаркерів в оцінці ризику ССЗ (Yang X. et al., 2015; Montecucco F. et al., 2015; Sodergren A. et al., 2015; Kim J. et al., 2016). Генетичний аналіз на мутацію метилен-тетрагідрофолат-редуктази (МТФР) рекомендовано лише особам із гіпергомоцистеїнемією (Haemostasis, Thrombosis Task Force BCfSiH, 2001). Для оцінки субклінічного ураження судин при РА запропоновано багато методів візуалізації, як-от ехокардіографія, багатошарова комп’ютерна томографія для визначення кальцифікації коронарних артерій, ультрасонографія сонних артерій (УСА) для вимірювання товщини комплексу інтима-медіа, визначення жорсткості артерій за швидкістю поширення пульсової хвилі чи індексом аугментації, визначення гомілково-плечового індексу тощо (Ambrosino P. et al., 2015; Ikdahl E. et al., 2016; Ozturk K., 2016; Al-Mohaissen M., Chan K., 2016; Liu J. et al., 2017; Scanlon E. et al., 2017). Серед них для клінічної практики EULAR пропонує лише УСА, оскільки є докази, що каротидні бляшки асоціюються з тривалістю й активністю РА та виникненням ІХС із поганим виживанням (Im C. et al., 2015; Pope J. et al., 2016). Отож рутинне визначення біомаркерів і проведення методів візуалізації не рекомендовано для щоденної клінічної практики (Piepoli M. et al., 2016).
Найпоширенішим інструментом оцінки 10-річного ризику фатальних ССЗ у загальній популяції є шкала SCORE (The Systematic Coronary Risk Evaluation), що включає такі ФР, як стать, вік, статус куріння, систолічний артеріальний тиск (АТ) і ліпідний профіль (Conroy R. et al., 2003). Проте моделі прогнозування ризику для загальної популяції недооцінюють ризик ССЗ у пацієнтів із РА (Hollan I. et al., 2015). Тому для оцінки ризику в цій когорті створено низку калькуляторів ризику та запропоновано корекційні фактори (Wiersma T. et al., 2012; Solomon D. et al., 2015; Arts E. et al., 2016). Зокрема, експерти EULAR рекомендують ризик, визначений за шкалою SCORE, множити на коефіцієнт 1,5.
Використовуючи шкалу SCORE, треба пам’ятати про низку обмежень. Оскільки на РА переважно хворіють жінки, ризик виникнення ССЗ може бути недооцінений навіть після корекції за приписом EULAR. Так, у молодої жінки можливий загальний показник ризику «0» із нульовим ефектом корекції. Такі випадки потребують проведення УСА. Рівні ліпідів крові слід вимірювати в неактивній фазі, щоб уникнути потенційного впливу системного запалення чи специфічної терапії (Filippatos T. et al., 2013; Liao K. et al., 2014; de Groot L. et al., 2015). Відношення холестерин (ХС) / ХС ліпопротеїнів високої щільності (ЛПВЩ) є надійнішим показником в активній фазі РА, ніж окремі показники ліпідограми (Choy E., Sattar N., 2009). Крім того, в активній фазі можливі особливі форми АГ, тому замість офісного вимірювання АТ краще проводити 24-годинний амбулаторний моніторинг (Hamamoto K. et al., 2016).
За рекомендаціями EULAR, повторну оцінку ризику у хворих на РА з низьким-помірним ризиком треба проводити кожні 5 років (Ray K. et al., 2014; Agca R. et al., 2017); в осіб із помірним-високим ризиком – частіше, принаймні щороку (рис. 2).
Профілактика ССЗ при РА
На сьогодні немає клінічних досліджень, які вивчали б оптимальне ведення ССЗ у пацієнтів із РА. Тому більшість рекомендацій екстраполюються з досліджень і міжнародних настанов для загальної популяції чи ґрунтуються на думці експертів.
Зниженню ризику ССЗ сприяє належний контроль активності РА, оскільки є багато повідомлень про зв’язок між запальним навантаженням і ризиком ССЗ (Arts E. et al., 2015; Myasoedova E. et al., 2016). Кількість і тривалість загострень підвищують ризик ССЗ, хоча власне тривалість РА, найімовірніше, не має незалежного впливу на ризик (Arts E. et al., 2015; Zhang J. et al., 2014). Таким чином, хронічне запалення треба розглядати як модифікований ФР, а його зменшення за допомогою ПРПМХ відіграє ключову роль у зниженні ризику ССЗ. Отже, рання діагностика й агресивне лікування РА забезпечують не тільки контроль активності, а й зменшують ризик розвитку ССЗ. Як і в загальній популяції, пацієнтам із високим / дуже високим ризиком (SCORE >5% і >10% відповідно) показане негайне лікування ФР (Agca R. et al., 2017). Незалежно від рівня ризику, всі пацієнти мають отримувати рекомендації щодо модифікації способу життя, що передбачає пояснення важливості регулярних фізичних вправ, здорового харчування та відмови від куріння (рис. 2). Покращити прихильність до лікування можуть когнітивно-поведінкові методи (John H. et al., 2013).
Гіподинамія підвищує ризик розвитку ССЗ у пацієнтів із РА (Hernandez-Hernandez V. et al., 2014). Натомість регулярні фізичні вправи зменшують запалення, ймовірно, за рахунок зменшення вмісту жиру в організмі; немає також протипоказань до вправ високої інтенсивності (Metsios G. et al., 2014; Lemmey A. et al., 2009). Відповідно до рекомендацій ESC, пацієнтам показана фізична активність середньої інтенсивності принаймні 150 хв/тиж або активні аеробні фізичні навантаження 75 хв/тиж (Piepoli M. et al., 2016). Ізотонічні фізичні вправи стимулюють формування кісток і зменшують втрату кісткової маси. Щоб уникнути ризику падіння в пацієнтів літнього віку, доцільно проводити оздоровчі заняття, що покращують рівновагу та моторику.
Особливі раціони харчування, як-от середземноморська дієта, не лише знижують ризик ССЗ, а й контролюють активність РА (Estruch R. et al., 2013). Тому цей вид дієти рекомендовано EULAR. Важливо обмежувати споживання натрію (оптимально до 3 г/добу), але збагачувати раціон продуктами, що містять вітамін D та омега-3 жирні кислоти. Гіпергомоцистеїнемія підвищує ризик інсульту та ССЗ (Wald D. et al., 2002). Цей розлад може спричинити метотрексат – антагоніст фолієвої кислоти, котрий порушує метаболізм гомоцистеїну, знижуючи активність МТФР (Grosflam J., Weinblatt M., 1991). Хоча нещодавній Кокранівський огляд не представив доказів того, що втручання, спрямовані на зниження гомоцистеїну, здатні зменшити ризик ССЗ, під час терапії метотрексатом рекомендовано призначати фолієву кислоту (Marti-Carvajal A. et al., 2015; Gualtierotti R. et al., 2017).
Важливу роль у патогенезі РА відіграє активне й пасивне куріння. Тому всім пацієнтам рекомендовано припинити курити. Для досягнення мети можна застосовувати замісну нікотинову терапію й електронні сигарети (Anderson R. et al., 2016; Law M. et al., 1997; Bullen C. et al., 2013).
Немає доказів того, що лікування АГ і гіперліпідемії та цільові рівні тиску чи ліпідів крові у хворих на РА мають відрізнятися від інших пацієнтів (Agca R. et al., 2017). Проте є докази недостатньої діагностики та терапії АГ у хворих на РА (Protogerou A. et al., 2013). Вибір антигіпертензивного препарату має проводитися індивідуально з огляду на клінічні ознаки ССЗ, безсимптомне ураження органів і протипоказання до антигіпертензивних препаратів. Статини достатньо вивчені в пацієнтів із РА, а їх ефективність у зниженні ХС, захворюваності та смертності від ССЗ і прояви побічної дії такі самі, як у пацієнтів без РА (Semb A. et al., 2012). Зокрема, частота міалгії та рабдоміолізу в пацієнтів із РА така сама, як у загальній популяції (Buettner C. et al., 2012). Статини мають протизапальні властивості, котрі, очевидно, підсилюють дію ПРПМХ, хоча це потребує підтвердження (Lv S. et al., 2015). Ліпідознижувальні препарати інших класів також можуть бути корисними (Danninger K. et al., 2014). Слід також зважати на вплив протиревматичних препаратів на АГ та ліпідний профіль, особливо в разі призначення ГК, НПЗП, циклоспорину, лефлуноміду, тоцилізумабу й тофацитинібу (Agca R. et al., 2017). Через відсутність доказів і підвищений ризик кровотеч антитромбоцитарна терапія вже не застосовується для первинної профілактики, але показана для вторинної профілактики після ІМ, інсульту чи при ураженні периферичних артерій відповідно до загальних рекомендацій (Piepoli M. et al., 2016).
Лікування ІХС та СН у хворих на РА
Навіть за умови аналогічного лікування результати в пацієнтів із РА гірші, ніж у загальній популяції, що, вочевидь, зумовлено недооцінкою ризику чи недостатнім впливом на ФР (Davis J. et al., 2008; Francis M. et al., 2010; Protogerou A. et al., 2013). Насамперед це стосується жінок у зв’язку з поширеною думкою про більшу захищеність і виникнення ССЗ на 10 років пізніше, ніж у чоловіків (Garcia M. et al., 2016). Ця хибна думка особливо небезпечна при РА, оскільки хвороба переважно уражає жінок на третій-п’ятій декаді життя та суттєво підвищує коморбідність і смертність від ССЗ. Окрім того, частими проявами ССЗ у жінок є ІМ на тлі неоклюзивних коронарних артерій або їх спонтанного розшарування, ураження периферичних артерій і СН зі збереженою фракцією викиду (Crea F. et al., 2014; Kobayshi H. et al., 2016). На це слід зважати при виборі втручань, які ґрунтуються на доказах для загальної популяції, де на ССЗ частіше страждають чоловіки, в яких переважають атеросклеротичні прояви ІХС.
У пацієнтів із застійною СН III-IV класів за NYHA комбінація синтетичних (c-) та біологічних (б-) ПРПМХ безпечніша за монотерапію інгібіторами ФНП (Singh J. et al., 2016).
Вплив протиревматичних препаратів на ризик ССЗ
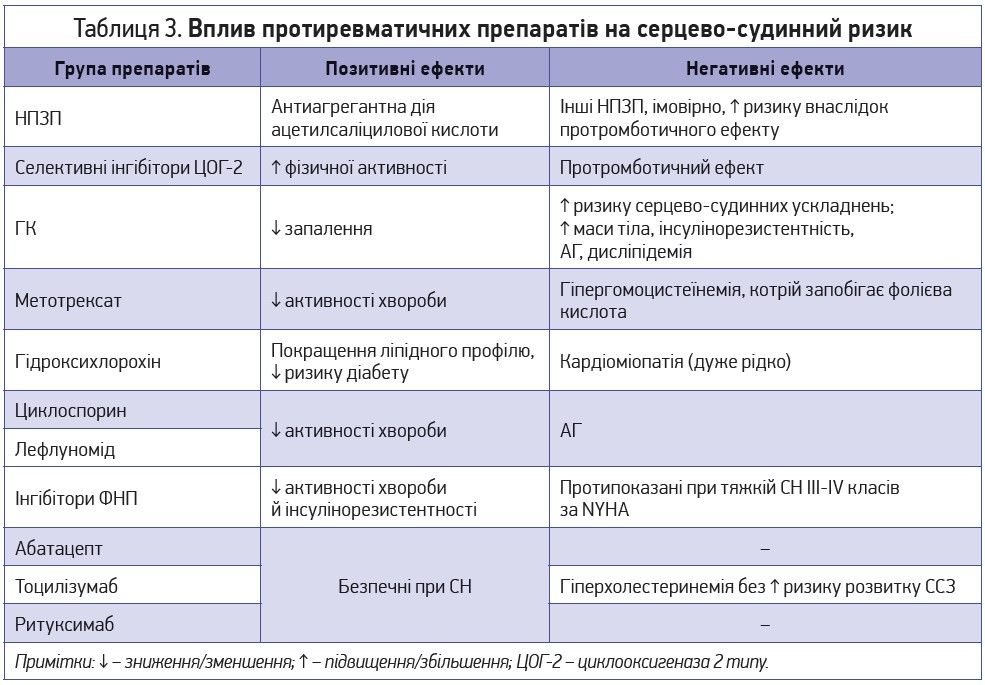
Оскільки контроль системного запалення може знизити ризик ССЗ і смерті, дуже бажаним є досягнення ремісії чи низької активності РА за умови уникнення лікарських засобів, які підвищують ризик ССЗ. Відповідно до найновіших міжнародних рекомендацій, ГК та c-ПРПМХ вважаються терапією першої лінії для індукції ремісії, тоді як б-ПРПМХ є основою лікування середньотяжких і тяжких форм РА (Smolen J. et al., 2017). Що стосується НПЗП, то їх слід призначати короткими курсами для підтримувальної терапії (табл. 3).
Тривале використання НПЗП та ГК підвищує ризик ССЗ (Roubille C. et al., 2015; del Rincon I. et al., 2014). Як неселективні, так і селективні НПЗП несприятливо впливають на наслідки ССЗ у пацієнтів із РА. Диклофенак протипоказаний хворим із застійною СН, ІХС, хворобами периферичних і мозкових артерій, а нові дані підтверджують такі обмеження щодо використання ібупрофену. Целекоксиб або низькі дози ГК краще призначати пацієнтам, які приймають клопідогрель, варфарин або інші антагоністи вітаміну K. У нещодавньому рандомізованому контрольованому дослідженні целекоксиб не поступався в профілі серцево-судинної безпеки двом широко вживаним неселективним НПЗП – напроксену й ібупрофену (Nissen S. et al., 2016). Навіть ацетамінофен, що широко застосовують як безпечний аналгетик, може погіршувати результати антигіпертензивної терапії (Gualtierotti R. et al., 2013). На сьогодні не визначено добових і кумулятивних доз і тривалості застосування ГК, які потенційно підвищують ризик ССЗ, але рекомендовано максимально мінімізувати добові дози та тривалість терапії (van Sijl A. et al., 2014).
Застосування c-ПРПМХ, особливо тривале, асоціюється зі зниженням ризику ССЗ (Roubille C. et al., 2015). Метотрексат може знижувати ризик ССЗ, оскільки сприятливо впливає на його сурогатний маркер – жорсткість артерій (Micha R. et al., 2011; Smolen J. et al., 2017; Ajeganova S. et al., 2012). Сульфасалазин знижує ризик ССЗ меншою мірою, ніж метотрексат, проте дані досить обмежені через нечасте його використання при РА (van Halm V. et al., 2006; Kerr G. et al., 2014). Гідроксихлорохін здатний покращувати ліпідний профіль і зменшувати ризик виникнення діабету (Wasko M. et al., 2007). Циклоспорин і лефлуномід підвищують АТ, тому їх не слід призначати при супутній АГ (Kellner H. et al., 2010; Robert N. et al., 2010).
Застосування інгібіторів ФНП значно знижує ризик ССЗ у пацієнтів із РА, особливо в тих, хто реагує на цей вид терапії (Bili A. et al., 2014; Ljung L. et al., 2016). Ці спостереження надалі підтверджують думку про те, що зниження ризику ССЗ пояснюється жорстким контролем запалення. Позитивний вплив на сурогатні маркери ССЗ (товщина комплексу інтима-медіа, жорсткість артерій) описано в пацієнтів, які лікувалися інгібіторами ФНП, тоцилізумабом і ритуксимабом (Rao V. et al., 2015; Vassilopoulos D. et al., 2015; Gualtierotti R. et al., 2016; Bacchiega B. et al., 2017). Здатність б-ПРПМХ підвищувати рівні ліпідів крові потребує контролю показників ліпідограми впродовж терапії, особливо при застосуванні тоцилізумабу (Souto A. et al., 2015). Проте вплив таких змін на наслідки ССЗ не доведений, хоча загалом ці препарати мають хороший профіль безпеки (Gualtierotti R., 2017). При застосуванні інгібіторів ФНП та/або c-ПРПМХ спостерігалося збільшення основних ліпідів крові, проте це врівноважувалося покращенням відношення між загальним ХС і ХС ЛПВЩ (Liao K. et al., 2014). Ритуксимаб, тоцилізумаб і, ймовірно, тофацитиніб можуть збільшувати окремі ліпідні компоненти, не змінюючи ХС / ХС ЛПВЩ, але й не підвищуючи ризику ССЗ (Gualtierotti R., 2017). Для корекції таких порушень можна застосовувати статини (Souto A. et al., 2015).
Отже, у хворих на РА ризик ССЗ вищий, аніж у загальній популяції, що пояснюється спільними патогенетичними механізмами, тому контроль хронічного запалення може зменшити ризик ССЗ. Усі пацієнти з РА потребують повторної оцінки ризику, що гарантуватиме адекватне персоналізоване лікування та застосовування ранніх стратегій профілактики. Оцінюючи ризик ССЗ і результати терапії, треба враховувати обмеження шкали SCORE, нетрадиційні ФР і вплив протиревматичної терапії. Щоб з’ясувати, чи лікування супутніх ССЗ у хворих на РА має відрізнятися від принципів терапії в загальній популяції, потрібні подальші дослідження.
Підготувала Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 18 (463), вересень 2019 р.