4 грудня, 2019
Доказова медицина: нюанси застосування в умовах сучасної клінічної практики
 Сьогодні заснована на доказах медицина надає фахівцям дорожню карту для застосування достовірних наукових даних у конкретних клінічних випадках. Незважаючи на певні недоліки, принципи доказової медицини (ДМ) впевнено реалізовуються в медичній практиці, а вміння ними користуватися є важливим завданням лікаря. На сторінках «Рубрики експерта» голова експертної групи МОЗ України за напрямами «Отоларингологія. Дитяча отоларингологія. Сурдологія», завідувач кафедри оториноларингології та офтальмології з курсом хірургії голови і шиї Івано-Франківського національного медичного університету, доктор медичних наук, професор Василь Іванович Попович представив огляд основних проблем імплементації принципів ДМ в сучасну клінічну практику.
Сьогодні заснована на доказах медицина надає фахівцям дорожню карту для застосування достовірних наукових даних у конкретних клінічних випадках. Незважаючи на певні недоліки, принципи доказової медицини (ДМ) впевнено реалізовуються в медичній практиці, а вміння ними користуватися є важливим завданням лікаря. На сторінках «Рубрики експерта» голова експертної групи МОЗ України за напрямами «Отоларингологія. Дитяча отоларингологія. Сурдологія», завідувач кафедри оториноларингології та офтальмології з курсом хірургії голови і шиї Івано-Франківського національного медичного університету, доктор медичних наук, професор Василь Іванович Попович представив огляд основних проблем імплементації принципів ДМ в сучасну клінічну практику.
Передмова
Необхідність у медицині, заснованій на доказах, виникла через низку причин, серед яких виділяють: постійне збільшення обсягу наукової інформації, потреба в її аналізі, систематизації та узагальненні; щорічне впровадження в медичну практику нових методів та засобів лікування, які активно вивчаються в численних клінічних дослідженнях. При цьому результати досліджень подекуди виявляються контраверсійними або ж і прямо протилежними. Разом із тим, на тлі впровадження нових технологій і засобів лікування в клінічну практику спостерігаються постійний ріст видатків на систему охорони здоров’я та нестача ресурсів. Тому виникла потреба в стандартизації лікувальних підходів та вибір методів і засобів, які мають найбільшу ефективність, безпеку та добре сприймаються пацієнтами.
З упровадженням принципів ДМ зростає і значення лікаря, адже для успішної медичної практики він має володіти знанням сучасних методів діагностики й лікування, а також постійно оновлювати свої навички. Водночас лікарю необхідно зберігати критичний підхід до оцінки наукових даних, особливо в умовах постійного зростання обсягу медичної інформації.
Важливе значення принципи ДМ також мають для викладання в медичних вишах. Студенти й інтерни без практичного досвіду більше схильні до суб’єктивного підходу в лікуванні захворювань, тому набуття здатності до критичного аналізу наукової інформації під час навчання є необхідною умовою для успішної клінічної практики в майбутньому.
Сьогодні є різні погляди на ДМ щодо її екстраполяції на конкретного пацієнта в умовах клінічної практики. Так, ДМ порівнюють із книгою рецептів, а деякі адепти рандомізованих клінічних досліджень (РКД) доводять їх значення до абсолюту. Проте слід пам’ятати, що, хоча сучасна медицина стає високотехнологічною і максимально наближеною до точної науки, особистість лікаря та його клінічний досвід завжди матимуть надзвичайно важливе значення в лікувальному процесі. Таким чином, практичне застосування приципів ДМ передбачає поєднання наукових даних з індивідуальним клінічним досвідом лікаря.
Визначення поняття «доказова медицина» та принципи практичного використання наукових доказів
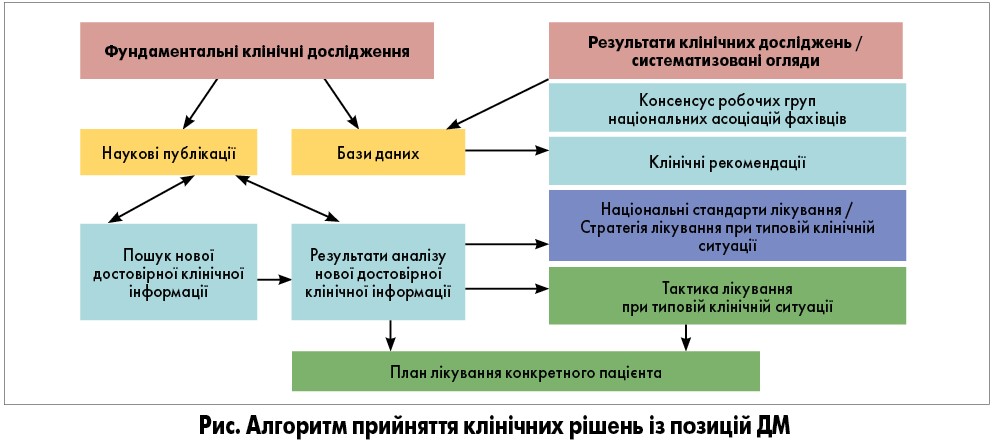
ДМ – це використання наукових методів у процесі застосування вже наявних даних. У цілому такий підхід сприяє прийняттю оптимальних рішень для покращення організації системи охорони здоров’я. Водночас у парадигмі ДМ сучасні наукові досягнення в поєднанні з реальним клінічним досвідом дають можливість вибрати найкраще медичне рішення для конкретного пацієнта. Головними об’єктами ДМ є стандарти лікування, відображені в клінічних рекомендаціях. Разом із тим суб’єктний статус лікаря дозволяє певним чином порушувати стандарти щодо конкретної клінічної ситуації, ураховуючи постійне оновлення наукових даних. Основні етапи прийняття клінічних рішень відображені на рисунку. При цьому треба зауважити, що результати клінічних досліджень не враховують індивідуальні особливості пацієнтів, тому не завжди здатні допомогти лікарю в конкретній ситуації.
У свій час D.L. Sackett та співавт. (1998) виділили 5 етапів імплементації принципів ДМ у клінічну практику:
- Визначення клінічно значущого питання.
- Пошук найкращих доказів.
- Оцінка якості отриманих доказів.
- Застосування отриманих доказів.
- Оцінка ефективності ДМ в умовах клінічної практики.
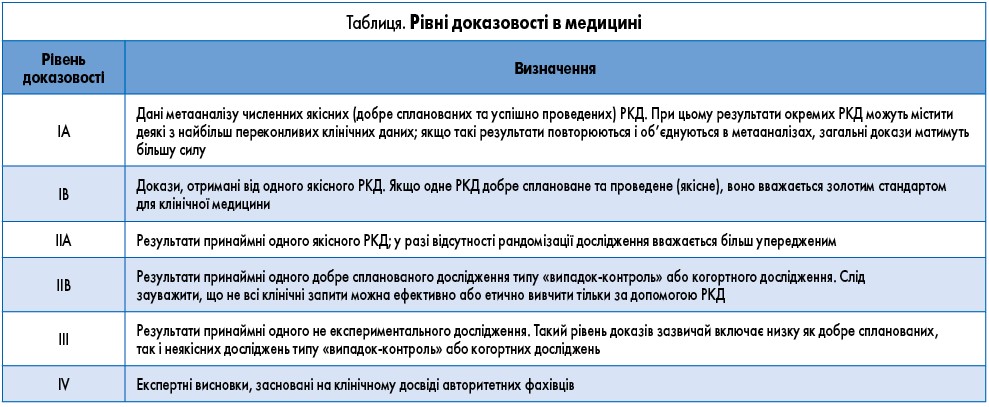
ДМ стартує від клінічного запиту, а саме – від реальної проблеми, яку лікарю необхідно вирішити разом із пацієнтом. У процесі пошуку клінічного рішення логічно виникає потреба в наукових доказах, що максимально відповідають наявному клінічному запиту. Власне наукові дані включають результати досліджень і думки науковців. При цьому не всі дані мають однакову силу; рекомендації експертів менш надійні, ніж результати якісно проведеного дослідження, яке, у свою чергу, менш надійне за результати низки якісно проведених досліджень. Таким чином, рівень отриманих доказів має бути оцінений відповідно до їх сили, а в процесі прийняття клінічних рішень лікарю необхідно фокусуватися на більш переконливих результатах досліджень. Загалом докази, отримані в ході досліджень, поділяють на 6 рівнів (табл.).
Отже, усі результати клінічних досліджень можуть бути класифіковані відповідно до вищенаведених рівнів доказовості. Наступним кроком у реалізації принципів ДМ є екстраполяція наукових даних на конкретний клінічний випадок. При цьому необхідно пам’ятати, що більшість досліджень містять специфічні критерії включення та виключення учасників, а також ураховують певні групи населення, які є добре вивченими на момент проведення клінічного випробування. На практиці це означатиме, що конкретний пацієнт найвірогідніше буде мати одну або кілька суттєвих відмінностей від популяції, в якій було отримано результати дослідження. Тому в кожному випадку застосування результатів клінічних випробувань має розглядатися виключно з точки зору впливу тих чи інших відмінностей пацієнта від встановлених популяційних характеристик. Але, застосовуючи наукові докази, слід також ураховувати інтереси та переконання конкретного пацієнта. Якщо результати досліджень, які планується застосувати на практиці, несумісні зі світоглядом пацієнта, вони не можуть бути йому рекомендовані.
Практична оцінка результатів досліджень
R. Steves і співавт. (2004) вважають, що ДМ покликана об’єднувати такі різні речі, як актуальні наукові дані, клінічний досвід та переконання конкретного пацієнта, задля імплементації найкращих медичних практик у систему охорони здоров’я.
Після того як був сформований клінічний запит, знайдені та стратифіковані відповідні наукові дані, а досвід лікаря – застосований для екстраполяції останніх на конкретного пацієнта, фінальним етапом є практична оцінка:
- Чи допомогло це медичне втручання?
- Чи є очікуваними результати даного медичного втручання?
- Яку нову інформацію отримано від застосування даного медичного втручання в умовах реальної клінічної практики?
- Яким чином отриману інформацію можна застосувати в майбутніх клінічних ситуаціях та в інших пацієнтів?
Очевидно, що ДМ починається з клінічного запиту і до нього ж повертається з тим, щоби продемонструвати, як усе це працює. Отже, ДМ є своєрідним perpetuummobile ефективності практичного застосування, а не разовим лінійним процесом.
Проблемні питання застосування наукових доказів
Ураховуючи реалії клінічної практики в будь-якій галузі медицини, екстраполяція наукових даних на конкретного пацієнта не завжди дає прогнозовані результати. Разом із тим є ціла низка об’єктивних і суб’єктивних факторів, які також впливають на ефективність імплементації наукових доказів. Розглянемо деякі з них.
Упередженість наукових публікацій
ДМ базується на даних наукових публікацій, ураховуючи передусім докази І та ІІ класів. Аналіз багатьох досліджень показує, що позитивні результати публікуються частіше, аніж негативні. У підсумку це призводить до переміщення фокусу уваги в бік позитивних результатів, здатних спотворити отримані докази. Окрім того, результати клінічних випробувань, які проводяться на замовлення фармацевтичних компаній, найвірогідніше будуть опубліковані для подальшого застосування досліджуваного лікарського засобу або пристрою в рутинній медичній практиці. Відповідно, і цей фактор також може спотворити отримані докази.
Обмеження щодо проведення РКД
У ДМ приорітет належить результатам РКД. Водночас РКД, попри їхню безперечну переконливість, можуть проводитися не за всіма клінічними запитами. Наприклад, якщо захворювання має незначну поширеність, є орфанним, можуть виникнути проблеми з набором достатньої кількості учасників для проведення РКД, результати якого в цьому разі не будуть релевантними для прийняття клінічних рішень. Важливим також є етичний фактор; наукова цінність результатів досліджень не може бути протиставлена дотриманню загальноприйнятих етичних норм. І зрештою, на сьогодні створюється набагато більше клінічних запитів, аніж можливостей проведення РКД, отже, постає питання щодо наявності ресурсів та пріоритетності напрямів досліджень.
Відставання практичного втілення результатів досліджень
Планування і проведення якісного РКД потребує певного часу, у тому числі для аналізу отриманих результатів, складення звітів та підготовки наукової публікації. Медичний ландшафт за цей час також може дуже змінитися; це може спричинити втрату актуальності та необхідність оновлення наукових даних, що також потребуватиме певного часу.
Урахування індивідуальних потреб пацієнтів
Сьогодні в клінічній практиці не надто ретельно враховуються всі потреби та уподобання пацієнтів. Такий підхід частково пояснюється тим, що практикуючі лікарі більше концентруються на суто медичній проблемі та способах її вирішення, ніж на ретельному аналізі індивідуальних факторів, здатних впливати на ефективність лікування. Крім того, широке використання достовірних наукових доказів, ефективність яких доведена в якісних РКД, логічно призводить до стандартизації лікувальних підходів, в яких не завжди враховуються індивідуальні потреби та цінності пацієнтів. Проте необхідно пам’ятати, що сучасні клінічні рекомендації постійно оновлюються з урахуванням принципів персоніфікованої медицини, а лікар завжди має право застосувати свій практичний досвід у конкретній ситуації.
Вибір засобу фармакотерапії в щоденній клінічній практиці згідно з принципами ДМ
В умовах сьогодення, коли на світовому та вітчизняному фармацевтичних ринках постійно з’являються нові найменування лікарських засобів, потреба критичної оцінки наукової інформації зростає за експонентою. Адже лікар, що практикує, вимушений щодня вирішувати дилему: якщо в конкретному клінічному випадку обраний препарат виявився ефективним, то діагноз і лікування є адекватними. В іншому разі або діагноз є помилковим, або препарат виявився неефективним; відповідно, клінічна ситуація виходить на новий рівень потреб – як з боку збільшення видатків, так і з боку втрати дорогоцінного для пацієнта й лікаря часу.
Зазвичай лікарі отримують наукову інформацію про засоби фармакотерапії з різних джерел – від наукових публікацій (у тому числі із сумнівними результатами некоректно проведених досліджень) до відвертої реклами нових препаратів. У таких реаліях принципи ДМ та критична оцінка наукової інформації допомагають точно та усвідомлено використовувати результати клінічних випробувань у виборі засобу фармакотерапії для конкретного пацієнта. Такий підхід дає можливість не лише зменшити кількість лікарських помилок, але й полегшити процес прийняття клінічних рішень для лікаря, адміністрації медичних закладів або юристів. Крім того, це дозволяє зменшити видатки на додаткову діагностику та лікування і зберегти час як пацієнта, так і медичного персоналу.
Необхідно також згадати постійну нестачу ресурсів на тлі росту видатків на придбання нових лікарських засобів та методів лікування. Тому потреба у виборі препарату з доведеною високою ефективністю та широким профілем безпеки набуває все більшого значення. Гостроти цій проблемі також надає зростаюча кількість генериків на фармацевтичному ринку, хоча заради справедливості треба зазначити, що висока вартість лікарського засобу також не гарантує його ефективність. Отже, для того щоби прийняти адекватне клінічне рішення, лікарю потрібна своєрідна «точка опори», якою може бути вибір препарату з доведеною ефективністю та безпекою відповідно до принципів ДМ. І тут постає питання: що вибрати в конкретній клінічній ситуації – оригінальний препарат чи генерик?
Оригінальні препарати
Загалом процес упровадження оригінальних (референтних) лікарських засобів у клінічну практику виглядає так. На передреєстраційному етапі відбувається вивчення фізико-хімічних властивостей та активності препарату щодо етіопатогенетичних механізмів захворювання, дослідження in vitro та на тваринних моделях. Клінічні дослідження у здорових добровольців і пацієнтів є фінальним етапом, який дає можливість найбільш достовірно оцінити прогнозовану ефективність лікарського засобу та безпеку його застосування. Програма клінічних досліджень нових оригінальних (референтних) лікарських засобів складається з таких кроків:
- Вивчення фармакологічних властивостей препарату у людини (І фаза): оцінка сприйняття різних доз; оцінка метаболізму; визначення фармакокінетики та фармакодинаміки; оцінка активності та взаємодії з іншими лікарськими засобами.
- Пошукові терапевтичні дослідження (ІІ фаза): пошук застосування по терапевтичній мішені; підбір дози для подальших досліджень; отримання вихідних даних для розробки дизайну, кінцевих точок і методології підтверджувальних досліджень.
- Підтверджувальні терапевтичні дослідження (ІІІ фаза): підтвердження доказів ефективності; визначення профілю безпеки; отримання необхідних даних для оцінки співвідношення «користь-ризик» з метою обґрунтування реєстрації; встановлення залежності «доза-ефект».
Результатом успішного виконання програми клінічних досліджень є отримання реєстраційного посвідчення лікарського засобу. При цьому проведення кожної фази клінічних досліджень відповідно до наукових та регуляторних вимог, а також процес отримання реєстраційного посвідчення потребують значних людських і фінансових ресурсів, а також часу. Окрім того, сам референтний лікарський засіб є продуктом високих технологій. Відповідно, у підсумку вищенаведені фактори впливають на кінцеву вартість оригінального препарату. У подальшому його патентний захист триває 20 років, після чого на ринку з’являються його копії-генерики. Для пролонгації патентного захисту деякі фармацевтичні компанії сьогодні практикують модифікацію своїх оригінальних препаратів.
Генеричні препарати
У свою чергу, генеричний препарат (генерик) повинен мати такий самий якісний та кількісний склад діючої речовини й лікарську форму, що й референтний засіб, та доведену з ним взаємозамінність. Проте практика показує, що в багатьох випадках взаємозамінні препарати від різних виробників проявляють неоднакову ефективність. А з економічної точки зору, часто постає проблема заміни оргінального лікарського засобу генериком. Тому взаємозамінним може бути тільки генеричний препарат із доведеною еквівалентністю референтному лікарському засобу. Для різних лікарських форм є різні методи оцінки еквівалентності. Основними критеріями фармацевтичної еквівалентності вважають:
- ідентичність дози та хімічних властивостей діючої речовини;
- ідентичність лікарської форми;
- ідентичність або подібність складу допоміжних речовин;
- подібність фармацевтичної розробки;
- відповідність вимогам GMP;
- аналогічний шлях введення препарату.
У визначенні взаємозамінності препаратів (генерика на референтний) найбільш релевантною є біоеквівалентність, яка базується на порівняльних фармакокінетичних дослідженнях. Доведена біоеквівалентність є маркером ефективності та безпеки генеричного лікарського засобу, який, відтак, може замінити референтний препарат без корекції дози та додаткового терапевтичного моніторингу. Разом із тим відмінності між генериком і оригінальним препаратом можуть стосуватися допоміжних речовин і технології виробництва.
У сучасних економічних реаліях проблема взаємозамінності препаратів є актуальною для багатьох національних систем охорони здоров’я, які намагаються використовувати генерики з доведеною ефективністю та безпекою. Однак дискусії щодо переваг референтних препаратів теж тривають на тлі поширення генериків сумнівної якості та недостатньої кількості досліджень їхньої біоеквівалентності.
Вибір засобу антибактеріальної терапії в парадигмі ДМ
Доведені ефективність та безпека лікарського засобу набувають особливого значення в лікуванні інфекційно-запальних захворювань, зокрема за допомогою антибактеріальної терапії (АБТ). Антибіотики є класом препаратів, які найчастіше застосовують у клінічній практиці. За визначенням ВООЗ, недостатня концентрація препарату в крові призводить до:
- зниження ефективності АБТ;
- збільшення кількості та поширення резистентності бактеріальних та вірусних патогенів;
- зростання числа ускладень;
- збільшення економічних витрат;
- зниження якості лікування та тривалості життя пацієнтів.
Щодо безпеки вибору засобу АБТ потрібно виділити певні групи ризику: діти й особи похилого віку. Наприклад, у дітей найбільш частими причинами розвитку небажаних ефектів застосування препаратів АБТ є їх необґрунтоване призначення, зокрема при гострих респіраторних інфекціях або для запобігання бактеріальним ускладненням при інтеркурентних захворюваннях. Щодо пацієнтів похилого віку, то неадекватне застосування антибактеріальних препаратів провокує розвиток загрозливих для життя ускладень через наявність мультиморбідної патології в переважної більшості хворих. Зрозуміло, що ризик розвитку небажаних реакцій на тлі відсутності терапевтичного ефекту суттєво збільшується при використанні засобів АБТ сумнівної якості.
З позицій ДМ раціональний вибір антибактеріального препарату здійснюється відповідно до:
- вірогідної етіології збудників;
- вірогідної резистентності збудників у даному регіоні;
- клінічних доказів ефективності саме цього препарату (або комбінації препаратів) для АБТ у даному регіоні.
Раціональне призначення антибактеріальних препаратів належної якості є необхідною умовою, спрямованою на обмеження розвитку антибіотикорезистентності (АБР). Перед проведенням АБТ також необхідно врахувати таке:
- антибіотики можуть використовуватися тільки в пацієнтів з ознаками інфекційної патології, зумовленої мікробною флорою. Застосування антибіотиків у пацієнтів із вірусними, грибковими патогенами або без ознак бактеріальної інфекції веде до зниження колонізаційної та загальної резистентності організму і може спричинити розвиток суперінфекції;
- при емпірічному виборі антибіотика слід урахувати епідеміологічні дані, результати досліджень чутливості аналогічних штамів збудників, клінічних даних та економічної доцільності;
- у разі необхідності зниження токсичності в конкретного пацієнта можлива корекція адекватної цілеспрямованої АБТ;
- вибір засобу АБТ має здійснюватися на основі національних клінічних настанов та рекомендацій, а також регіональних даних щодо чутливості мікроорганізмів.
Необхідно врахувати і той факт, що в Україні антибактеріальні препарати здебільшого відпускають без рецепта, і ця ситуація сприяє розвитку АБР. Практикуючий лікар може впливати на зниження вірогідності розвитку АБР призначенням антибіотиків із доведеною ефективністю, а пацієнт – чітким дотриманням рекомендацій під час курсу АБТ. Слід також додати, що в педіатрії та геронтології призначення засобу АБТ із доведеними ефективністю, безпекою та асоційованого з найменшим рівнем розвитку АБР є вкрай важливим.
Отже, застосування принципів ДМ у сучасній медичній практиці передбачає критичну оцінку наукової інформації та опору на власний клінічний досвід. Такий підхід допоможе лікарю відповідально приймати терапевтичні рішення і бути при цьому впевненим в ефективнсті та безпеці методу лікування для конкретного пацієнта.
Підготувала Наталія Позднякова
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 3 (59), 2019 р.