28 грудня, 2019
Оновлені рекомендації ESC/EAS щодо менеджменту осіб із дисліпідемією
У серпні 2019 р. Європейське товариство кардіологів (ESC) та Європейське товариство з атеросклерозу (EAS) опублікували в European Heart Journal сучасні клінічні рекомендації щодо менеджменту пацієнтів із дисліпідемією з метою зниження серцево-судинного ризику. Попередні настанови ЕСС/ЕАС були розроблені 2016 р. Поява нових даних за останні кілька років зумовила оновлення керівних принципів.
У чому полягає профілактика серцево-судинних захворювань?
Серцево-судинні захворювання (ССЗ), серед яких атеросклеротичні (АССЗ), є причиною понад 4 млн летальних випадків у Європі щороку, причому більшу частку складають жінки – 2,2 млн, тоді як чоловіки – 1,8 млн, хоча смерть внаслідок ССЗ до 65 років частіше трапляється серед чоловіків (490 тис. та 193 тис. відповідно). Важливість профілактики АССЗ залишається безперечною. Слід проводити пропаганду на рівні загальної популяції шляхом залучення до здорового способу життя та зменшення причинних факторів ризику ССЗ, як-то холестерин (ХС) ліпопротеїдів низької щільності (ЛПНЩ) та рівень артеріального тиску (АТ).
Обґрунтування оцінки загального ризику ССЗ та її впровадження
У сучасних рекомендаціях щодо профілактики АССЗ вказано на необхідність оцінки загальної вірогідності розвитку ССЗ, оскільки цей показник впливає на об’єм профілактичних методів. Скринінг факторів ризику, зокрема рівня ліпідного профілю, слід враховувати у чоловіків >40 років та в жінок >50 років або після менопаузи. Шкалу, розроблену для оцінки ризику фатального ССЗ протягом 10 років (SCORE), може бути повторно калібровано для використання у різних популяціях; відкориговані версії для багатьох країн Європи можна знайти на сайті www. heartscore.org.
В осіб із помірним ризиком ССЗ наявні деякі фактори, що можуть вплинути на його зростання, а саме підвищений рівень аполіпоротеїну B (апо-В), ліпопротеїну (a), тригліцеридів (ТГ) або C-реактивного білка, розвиток альбумінурії, атеросклерозу / бляшок у сонних чи стегнових артеріях. Також враховують оцінку кальцифікації коронарних артерій за допомогою контрастної комп’ютерної томографії (КТ), індексу Агатстона або коронарного кальцієвого показника (ККП) (>100 одиниць), швидкості каротидно-феморальної пульсової хвилі (>10 м/с), гомілково-плечового індексу (<0,9).
Особи із документально підтвердженим АССЗ, цукровим діабетом (ЦД) 1-го або 2-го типу, високою ймовірністю індивідуальних факторів ризику або хронічною хворобою нирок (ХХН) здебільшого мають високий або дуже високий загальний ризик ССЗ. У таких пацієнтів важливо активно контролювати всі фактори ризику, а не використовувати додаткові методи оцінки. Для загальної популяції рекомендовано застосовувати систему SCORE. Результат, отриманий за цією шкалою, вказує на те, що загальна вірогідність виникнення ССЗ приблизно втричі вища, ніж така фатального ССЗ у чоловіків; тому значення SCORE, що дорівнює 5%, відповідає 15% ризику розвитку ССЗ (фатальне + нефатальне); мультиплікатор вищий у жінок і нижчий в осіб похилого віку.
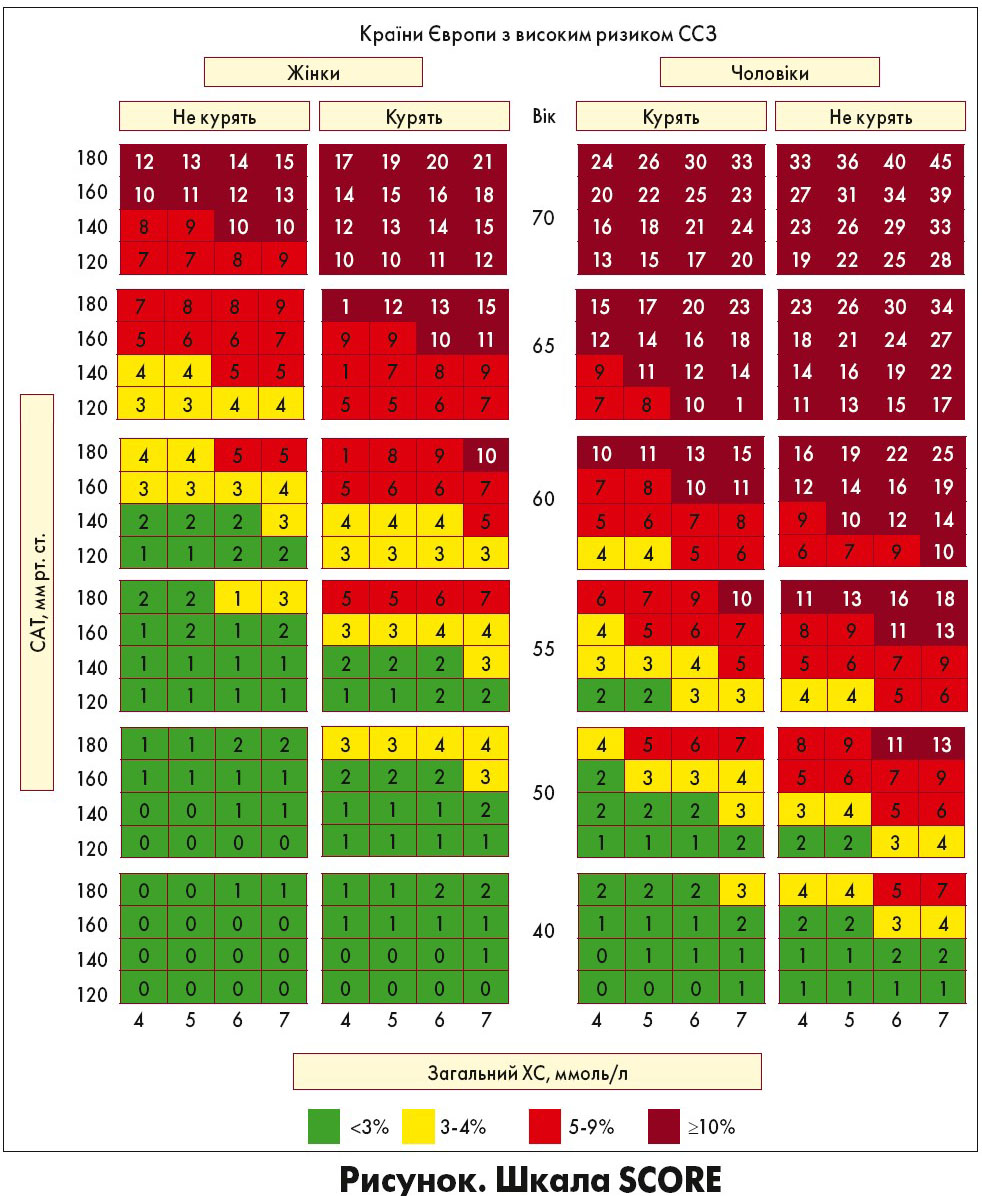
Інший підхід – метод, що вираховує вік ризику ССЗ за принципом, коли вік людини однаковий за рівнем ризику, але з ідеальним рівнем факторів ризику (відмова від куріння, загальний ХС ≤4 ммоль/л, або ≤155 м/дл та систолічний артеріальний тиск [САТ] ≤120 мм рт. ст.). Цей параметр можна оцінити візуально відповідно до шкали SCORE (рисунок), за якою для особи з факторами ризику ССЗ вік ризику визначається як той, в якому за ідеального рівня факторів ризику людина досягала б одного рівня ризику. Даний показник також автоматично розраховується в межах останньої редакції інструментарію HeartScore (доступний за посиланням www.heartscore.org). Довічний ризик також може бути використаний для оцінки впливу факторів ризику ССЗ у молодих осіб. Так, чим більший їхній тягар, тим вищий ризик впродовж усього життя.
Ще одна проблема стосується літніх осіб, особливо чоловіків, у яких вірогідність смертності від ССЗ перевищує 5‑10%, з огляду лише на вік, навіть якщо інші рівні факторів ризику відносно низькі. Тому перед початком лікування цієї когорти пацієнтів клініцисти мають проводити ретельну оцінку, щоб уникнути розвитку побічних ефектів.
Додатково слід враховувати наявність факторів, що можуть впливати на модифікацію SCORE, як-то:
- соціальна депривація;
- ожиріння та вісцеральне ожиріння, що вимірюють за допомогою індексу маси тіла та окружності талії відповідно;
- гіподинамія;
- психосоціальний стрес;
- сімейний анамнез передчасного ССЗ (чоловіки <55 років та жінки <60 років);
- хронічне імунно-опосередковане запальне захворювання;
- основні психіатричні розлади;
- антиретровірусна терапія;
- миготлива аритмія;
- гіпертрофія лівого шлуночка;
- ХХН;
- синдром обструктивного апное уві сні;
- неалкогольна жирова хвороба печінки.
Втім, деякі фактори, як-то високий рівень ліпопротеїдів високої щільності (ЛПВЩ) <2,3 ммоль/л (90 мг/дл) або сімейний анамнез довголіття, можуть бути пов’язані з нижчим ризиком ССЗ.
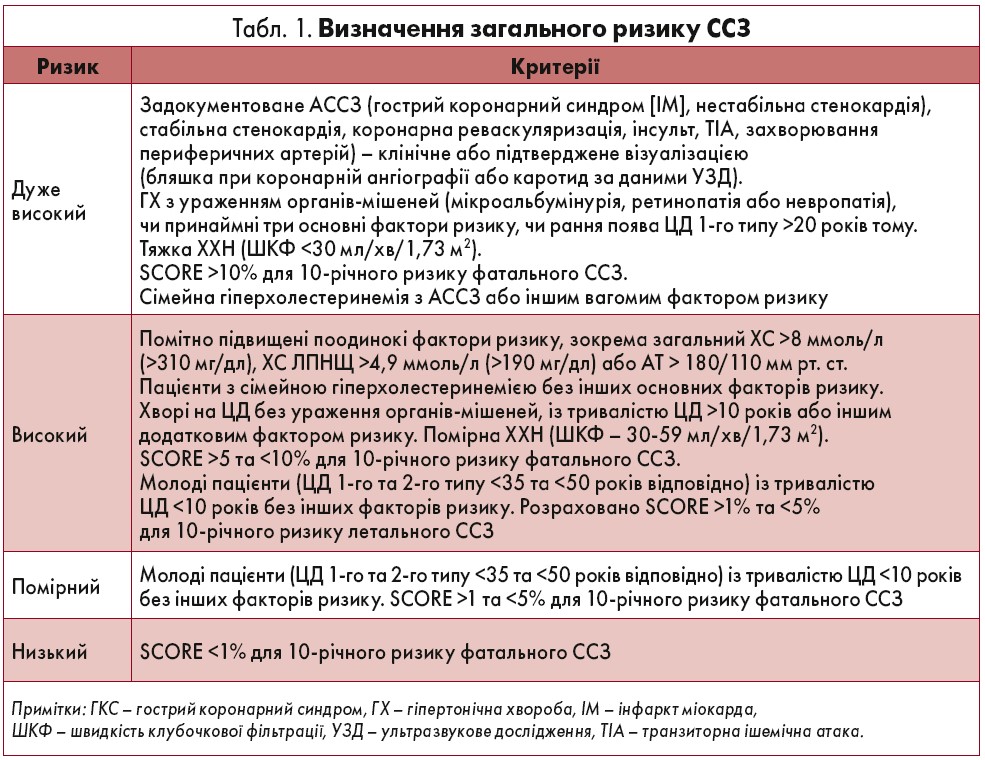
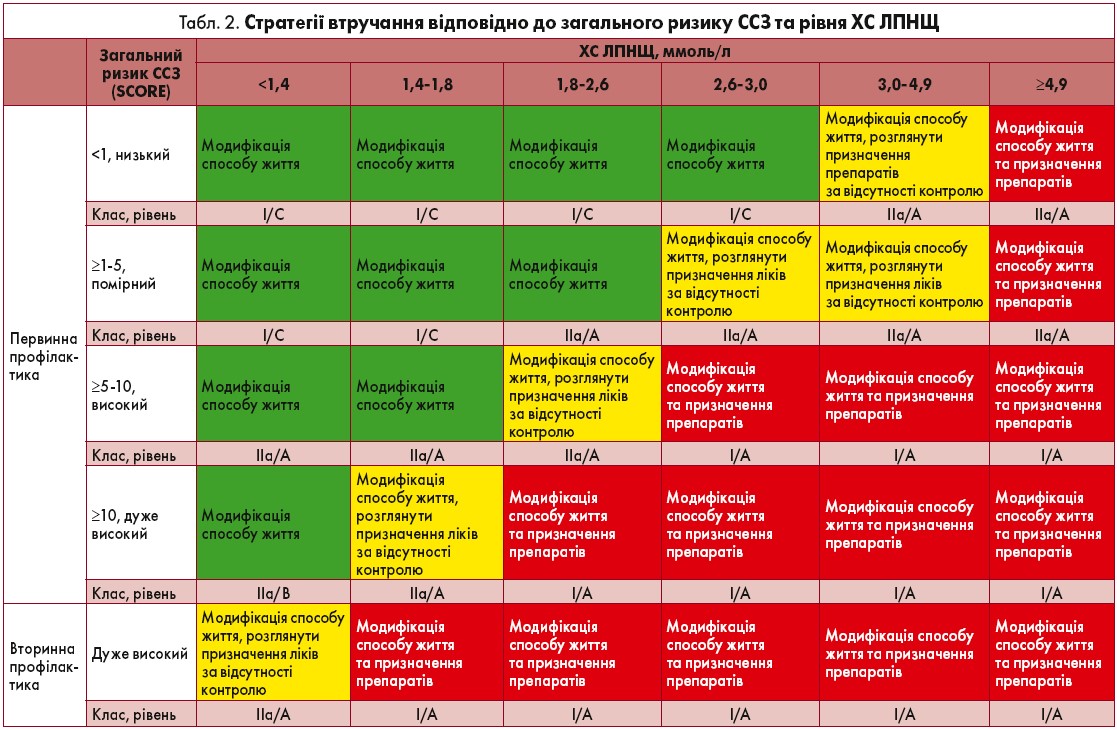
Визначення загального ризику ССЗ залежно від клінічних характеристик та даних лабораторних, інструментальних досліджень представлено в таблиці 1. Після встановлення ймовірності розвитку ССЗ слід обрати наступну терапевтичну стратегію з огляду на показники ліпідограми (табл. 2).
Оцінка наявності >50% стенозу просвіту коронарних судин та складу бляшок за допомогою коронарної КТ-ангіографії також має додаткове прогностичне значення порівняно із традиційними моделями стратифікації ризику:
- в осіб із низьким або помірним ризиком слід розглянути проведення ультрасонографії для детекції бляшки у просвіті сонних або стегнових артерій для модифікації ризику (IIa/B);
- в асимптоматичних осіб із низьким або помірним ризиком потрібно розглянути визначення ККП із застосуванням КТ-ангіографії для модифікації ризику (IIa/B).
Загалом оцінку ККП за допомогою КТ доцільно розглядати у пацієнтів, в яких нормального рівня ЛПНЩ не вдається досягти лише за рахунок модифікації способу життя, а фармакологічна терапія є варіантом вибору.
Узагальнені рекомендації щодо оцінки ризику ССЗ
- Загальна оцінка ризику із використанням SCORE рекомендована для асимптомних дорослих >40 років без ознак ССЗ, ЦД, ХХН, сімейної гіперхолестеринемії або ХС ЛПНЩ >4,9 ммоль/л (І/С).
- Високий та дуже високий ризик ССЗ визначають на підставі задокументованих ССЗ, ЦД, помірної або тяжкої ХХН, дуже високого рівня індивідуальних факторів ризику, сімейної гіперхолестеринемії чи значної вірогідності розвитку відповідно до SCORE. Такі пацієнти є пріоритетом ретельного контролю факторів ризику (І/С).
- Оцінку ризику необхідно проводити у загальній популяції та не рекомендовано у пацієнтів із ЦД та сімейною гіперхолестеринемією (ІІІ/С).
Рекомендації щодо вимірювання ліпідів та ліпопротеїнів для оцінки ризику АССЗ
1. Рівень загального ХС слід використовувати для виявлення загального ризику ССЗ за допомогою SCORE (І/С).
1. Аналіз ХС ЛПВЩ рекомендований для оцінки майбутнього ризику шляхом застосування онлайн-системи SCORE (І/С).
1. Аналіз ХС ЛПНЩ доцільно застосовувати як первинну оцінку ліпідів для скринінгу, діагностики та менеджменту пацієнтів (І/С).
1. Визначення ТГ рекомендоване як частина рутинного аналізу ліпідів (І/С).
1. Рівень ХС ліпопротеїдів невисокої щільності (ЛПНВЩ) слід вимірювати для оцінки ризику в осіб із високим вмістом ТГ, ЦД, ожирінням або дуже низькою концентрацією ХС ЛПНЩ (І/С).
1. Аналіз апо-В рекомендований для визначення ризику переважно у пацієнтів із високим рівнем ТГ, ЦД, ожирінням, метаболічним синдромом або дуже низьким вмістом ХС ЛПНЩ. Ймовірне використання цього показника як альтернативи ХС ЛПНЩ у межах первинної оцінки для скринінгу, діагностики та менеджменту хворих; також він може мати перевагу над ХС ЛПНВЩ в осіб із високим рівнем ТГ, ЦД, ожирінням або дуже низьким вмістом ХС ЛПНЩ (І/С).
1. Ліпопротеїн (а) варто визначати щонайменше раз у житті для ідентифікації дуже високого рівня даного показника >180 мг/дл, що може свідчити про довічний ризик АССЗ та гетерозиготну сімейну гіперхолестеринемію (ІІа/С).
1. Ліпопротеїн (а) має бути розглянутий для виявлення у пацієнтів із сімейним анамнезом передчасних ССЗ, а також розв’язання спірного питання щодо встановлення помірного або високого ризику (ІІа/С).
Загальні терапевтичні мішені та задачі щодо профілактики ССЗ
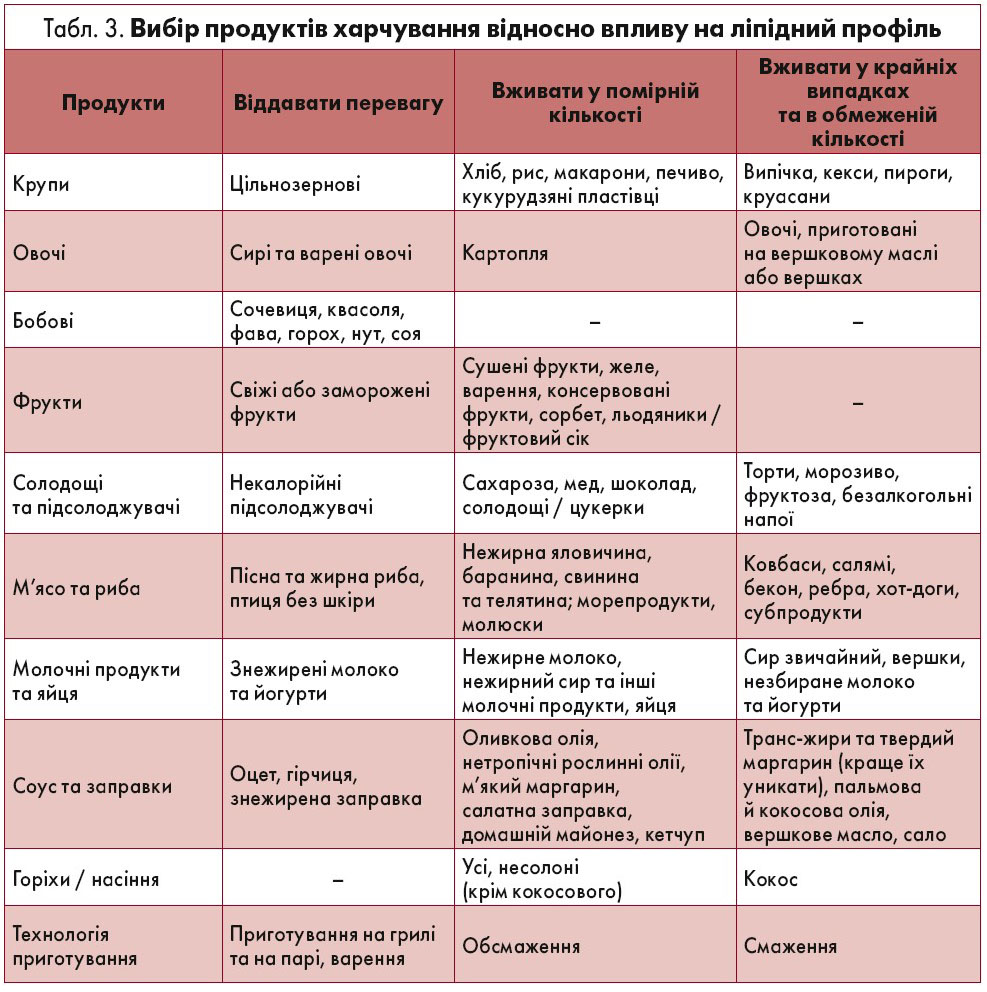
Такі лікувальні аспекти передбачають уникнення вживання нікотину в будь-якій формі, впровадження здорового харчування з низьким вмістом насичених жирів з акцентом на цільнозернові продукти, овочі, фрукти та рибу (табл. 3). Фізичні навантаження помірної інтенсивності необхідно виконувати протягом 3,5‑7 год на тиждень або 30‑60 хв більшість днів. Контроль маси тіла потрібно здійснювати з огляду на індекс маси тіла (20‑25 кг/м2) та окружність талії (<94 см у чоловіків та <80 см у жінок). Також слід утримувати АТ на рівні <140/90 мм рт. ст.
Корекція ХС ЛПНЩ при первинній або вторинній профілактиці за дуже високого ризику ССЗ передбачає застосування терапевтичної схеми, що забезпечує зниження на ≥50% ХС ЛПНЩ від початкового значення та досягнення цільового рівня ХС ЛПНЩ <1,4 ммоль/л (<55 мг/дл). За відсутності поточного використання статинів, ймовірно, знадобиться призначення високоінтенсивної терапії. За наявності лікування необхідне підвищення його інтенсивності. У разі розвитку АССЗ, повторної судинної катастрофи впродовж двох років та приймання максимально толерантної дози статину має бути розглянутий цільовий рівень ХС ЛПНЩ <1,0 ммоль/л, або <40 мг/дл (ІІb/В).
За наявності високого ризику ССЗ терапевтична тактика має забезпечувати зниження на ≥50% ХС ЛПНЩ від початкового показника та досягнення цільового рівня ХС ЛПНЩ <1,8 ммоль/л, або <70 мг/дл (І/А). У разі помірного ризику ССЗ доцільно прагнути цільового рівня ХС ЛПНЩ <2,6 ммоль/л, або <100 мг/дл (ІІа/А) та низького – <3,0 ммоль/л, або <116 мг/дл (ІІb/А).
Вторинний цільовий показник ХС ЛПНВЩ має складати <2,2; 2,6 та 3,4 ммоль/л (<85, 100 і 130 мг/дл) для осіб із дуже високим, високим та помірним ризиком ССЗ відповідно. Вторинний цільовий рівень апо-В повинен бути <65, 80 та 100 мг/дл для пацієнтів із дуже високим, високим та помірним ризиком ССЗ відповідно. Щодо вмісту ТГ чіткі цільові значення не визначені, але параметр <1,7 ммоль/л (<150 мг/дл) пов’язаний із меншою вірогідністю розвитку ССЗ, а вищий показник свідчить про необхідність пошуку інших факторів ризику. У пацієнтів із ЦД рівень глікованого гемоглобіну (HbA1С) має бути в межах <7% (<53 ммоль/л).
Рекомендації щодо способу життя для покращення ліпідного профілю плазми
Регулярні фізичні вправи приводять до зниження ваги, що покращує чутливість до інсуліну, підвищує вміст ХС ЛПВЩ (збільшення 0,01 ммоль/л на кожне зменшення кілограма маси тіла) та знижує рівень ТГ. До речі, вживання алкоголю має значний вплив на цей показник, особливо в осіб, які страждають на гіпергліцеридемію. Споживання значної кількості дієтичної фруктози (>10% від загальної спожитої з їжею енергії) сприяє підвищенню TГ, особливо за наявності гіпергліцеридемії або ожиріння.
Уникання споживання будь-яких жирів (насичених, ненасичених) є ключовим заходом профілактики ССЗ. Дієтичні волокна (особливо розчинного типу), що містяться в бобових, фруктах, овочах і крупах (наприклад, овес та ячмінь), чинять гіпохолестеринемічну дію. Норма вуглеводів має становити 45‑55% від загальної кількості енергії. Щоденне споживання 2 г фітостеролів (ситостерол, кампестерол та стигмастерол), що наявні у рослинних оліях та в меншій кількості – в овочах, свіжих фруктах, горіхах, зернах та бобових, може ефективно знижувати рівень ТГ та ХС ЛПНЩ на 7‑10%. Фітостероли конкурують із ХС за всмоктування в кишечнику.
Монаколін та червоний дріжджовий рис проявляють гіпохолестеринемічні ефекти, пов’язані з пригніченням гідроксиметилглутарил-коензим A (ГМГ-КoA) редуктази. Наявні препарати мають різну концентрацію монаколінів і зменшують концентрацію TГ та ХС ЛПНЩ по-різному. Бета-глюкан – в’язка клітковина вівса та ячменю
Препарати для лікування дисліпідемії
Статини
Статини знижують синтез ХС у печінці за рахунок конкурентного інгібування ферменту ГМГ-КoA-редуктази, що обмежує швидкість біосинтезу ХС. Режим високої інтенсивності визначається як доза статину, що в середньому зменшує вміст ХС ЛПНЩ на ≥50%, терапія середньої інтенсивності – на 30‑50%. Статини зазвичай знижують рівень TГ на 10‑20% від базових значень. Потужніші статини (аторвастатин, розувастатин та пітавастатин) демонструють стійке зменшення ТГ, особливо за високих доз. Серед інших потенційно важливих ефектів статинів протизапальний та антиоксидантний.
Рабдоміоліз – найсуттєвіша форма ушкодження м’язів, спричинена прийманням статинів, яка характеризується сильним м’язовим болем, некрозом та міоглобінурією, що потенційно може призвести до ниркової недостатності та смерті. При рабдоміолізі рівень креатинкінази (КК) підвищений у ≥10 разів, а часто ≥40 разів. За оцінками, частота рабдоміолізу становить 1‑3 випадки на 100 тис. пацієнто-років.
Легке підвищення рівня аланінамінотрансферази (АЛТ) спостерігається у 0,5‑2,0% хворих, які отримують лікування статинами, частіше у разі приймання високоактивних препаратів або високої дози. Прогресування печінкової недостатності надзвичайно рідкісне, тому рутинний моніторинг АЛТ під час терапії статинами більше не рекомендований. При вивченні пацієнтів із легким підвищенням рівня АЛТ внаслідок стеатозу при лікуванні статинами не отримано жодних ознак того, що вони викликають погіршення симптомів при захворюванні печінки.
Показано, що у хворих, які перебувають на терапії статином, підвищений ризик розвитку дисглікемії
Інгібітори всмоктування ХС
Езетиміб пригнічує кишкове всмоктування ХС на рівні щіточкової облямівки кишечника та не впливає на таке жиророзчинних поживних речовин. Даний лікарський засіб інгібує абсорбцію ХС, тим самим зменшує кількість ХС, що надходить до печінки. У клінічних дослідженнях езетиміб при монотерапії в дозі 10 мг/добу знижує ХС ЛПНЩ у хворих на гіперхолестеринемію на 15‑22%. Езетиміб, що додають до постійного лікування статинами, зменшує вміст ХС ЛПНЩ додатково на 21‑27% порівняно із плацебо.
Секвестранти жовчних кислот
Жовчні кислоти синтезуються в печінці з ХС та вивільняються у просвіт кишечника, проте більша їхня частка повертається в печінку із клубової кишки шляхом активного всмоктування. Доступними є секвестранти жовчних кислот: холестирамін, колестипол, колесевелам. Препарати, що зв’язують жовчні кислоти, перешкоджають реабсорбції як препарату, так і ХС у кров. Приймання 24 г холестираміну, 20 г колестиполу або 4,5 г колесевеламу в добовій дозі забезпечує зниження рівня ХС ЛПНЩ на 18‑25%. Найчастіші несприятливі наслідки для шлунково-кишкового тракту (ШКТ) – метеоризм, закреп, диспепсія та нудота, нерідко виникають навіть при прийманні в малих дозах, що обмежує практичне застосування секвестрантів.
Інгібітори PCSK9
Інгібітори пропротеїнконвертази 9-го субтилізин-кексинового типу (PCSK9) націлені на білок, який бере участь у контролі ХС ЛПНЩ. На даний час єдиними схваленими інгібіторами PCSK9 є два препарати моноклональних людських антитіл: алірокумаб та еволокумаб. Терапія статинами підвищує рівень циркулюючого PCSK9 у сироватці крові; таким чином, найкращий ефект (у середньому зниження ХС ЛПНЩ на 60%) цих лікарських засобів був продемонстрований у поєднанні зі статинами. Інгібітори PCSK9 вводять підшкірно кожний другий тиждень або раз на місяць у різних дозах. Серед найчастіших побічних ефектів повідомлялося про свербіж у місці ін’єкції та грипоподібні симптоми.
Ломітапід
Інгібітор мікросомального білка-переносника ТГ ломітапід перешкоджає утворенню ЛПНЩ у печінці та хіломікронів у кишечнику. В дослідженнях препарат знижував ХС ЛПНЩ на 50% на 26-му та на 44% на 56-му тижні. Ломітапід пов’язаний із підвищенням рівня амінотрансферази, що потребує контролю функції печінки під час терапії.
Міпомерсен
Міпомерсен – антисмисловий олігонуклеотид, здатний зв’язувати інформаційну рибонуклеїнову кислоту (іРНК) апо-B‑100, що запускає селективну деградацію молекул іРНК. Після підшкірної ін’єкції міпомерсен переважно транспортується до печінки, де зв’язується зі специфічною іРНК. Таким чином він запобігає трансляції білка апо-B‑100 та, отже, зменшує вироблення атерогенних ліпідів і ліпопротеїдів, зокрема ЛПНЩ та ліпопротеїну (a). Однак основні занепокоєння щодо безпеки міпомерсену пов’язані з токсичністю для печінки. Препарат може призвести до розвитку стеатозу.
Фібрати
Фібрати є агоністами рецепторів, які активуються проліфератором пероксисом-α (PPAR-α), що діють через фактори транскрипції, регулюючи різні етапи метаболізму ліпідів та ліпопротеїнів. Приймання фібратів дозволяє знизити рівень TГ на 50%, ХС ЛПНЩ на ≤20% (але може спостерігатися парадоксальне незначне зростання ХС ЛПНЩ при високому вмісті TГ) та підвищити ХС ЛПВЩ на ≤20%. Фібрати здебільшого добре переносяться, про порушення ШКТ повідомлялося у <5% пацієнтів, а шкірні висипання – у 2%. Міопатія, підвищення рівня ферментів печінки та жовчнокам’яна хвороба являють собою найпоширеніші побічні ефекти, пов’язані з фібратами. Відомо, що фібрати збільшують концентрацію креатиніну та гомоцистеїну в сироватці крові, а також ризик панкреатиту.
Поліненасичені жирні кислоти омега-3
ПЖК ω3 (ейкозапентаєнову та докозагексаєнову кислоти) можна використовувати у фармакологічних дозах
Нікотинова кислота
Варто зауважити, що у печінці нікотинова кислота інгібує 1,2-діацилгліцерин-ацилтрансферазу, що приводить до зниження секреції ліпопротеїнів дуже низької щільності (ЛПДНЩ) та ЛПНЩ. Нікотинова кислота здебільшого підвищує ХС ЛПВЩ та апо-A1. Наразі у Європі не затверджено жодних ліків, що містять нікотинову кислоту.
Інгібітори перенесення холестерилових ефірів
Дальцетрапіб, евацетрапіб та анацетрапіб на сьогодні проходять клінічні випробування. Втім результати, отримані у дослідженні дальцетрапібу, не свідчать на користь його ефективності. Своєю чергою анацетрапіб показав зниження ризику коронарних подій на 9%, але наразі вживаються заходи щодо ухвалення даного препарату.
Рекомендації щодо оптимальної терапевтичної стратегії
Фармакологічне зниження ХС ЛПНЩ
Рекомендовано призначити високоактивні статини до найвищої толерантної дози для досягнення зниження ризику ССЗ (І/А). Якщо мети не досягнуто, до високоактивного статину в найвищій толерантній дозі слід додати езетиміб (І/В). Для вторинної профілактики пацієнтам із дуже високим ризиком, які не досягли терапевтичної мети на тлі приймання статину в найвищій толерантній дозі та езетимібу, доцільно додати інгібітори PCSK9 (І/А).
Для хворих із дуже високим ризиком та сімейною гіперхолестеринемією (з АССЗ або іншим вагомим фактором ризику), що не досягли цільових рівнів ХС ЛПНЩ на тлі приймання статину в найвищій толерантній дозі та езетимібу, потрібно додати інгібітори PCSK9 (І/С).
Медикаментозна терапія пацієнтів із гіпертригліцеридемією
Статинотерапія рекомендована як стратегія першого вибору для зменшення ризику ССЗ в осіб із високим ризиком та гіпертригліцеридемією (ТГ >2,3 ммоль/л) (І/В).
Менеджмент пацієнтів із сімейною гіперхолестеринемією
Діагностику сімейної гіперхолестеринемії розглядають у пацієнтів з ішемічною хворобою серця (ІХС): <55 років у чоловіків та <60 років у жінок, а також в осіб із ранніми фатальними та нефатальними ССЗ, сухожильними ксантомами у сімейному анамнезі, хворих із високим рівнем ХС ЛПНЩ (у дорослих >5 ммоль/л, або >190 мг/дл; у дітей >5 ммоль/л, або >150 мг/дл), а також у батьків осіб, що відповідають переліченим критеріям (І/С). Сімейну гіперхолестеринемію діагностують з огляду на клінічні критерії та, за можливості, після проведення генетичних аналізів (мутація в генах ЛПНЩ, апо-B чи PCSK9) (І/С). Якщо захворювання підтверджене, рекомендований скринінг родичів хворого (І/С).
Пацієнтів із сімейною гіперхолестеринемією та АССЗ або тих, хто має інші вагомі фактори ризику, потрібно лікувати як осіб із дуже високим ризиком, а таких без АССЗ та інших факторів ризику – як осіб із високим ризиком (І/С). Для хворих із сімейною гіперхолестеринемією та АССЗ, що відносяться до групи дуже високого ризику, рекомендоване зниження рівня ХС на ≥50% від вихідного та ХС ЛПНЩ <1,4 ммоль/л (<55 мг/дл). Якщо мети не досягнуто, доцільно призначити комбіновану терапію (І/С).
Лікування із застосуванням інгібіторів PCSK9 рекомендоване для пацієнтів із сімейною гіперхолестеринемією та дуже високим ризиком, якщо терапевтичної мети не досягнуто, за умови приймання максимально толерантної дози статину та езетимібу (І/С).
У дітей дослідження на сімейну гіперхолестеринемію рекомендовано проводити з 5-річного віку або раніше за припущення діагнозу (І/С).
Терапія дисліпідемії в осіб похилого віку
Статинотерапію рекомендовано призначати пацієнтам похилого віку з АССЗ за тією самою тактикою, що й молодшим особам (І/А). Лікування статинами доцільно застосовувати як первинну профілактику згідно зі ступенем ризику в літніх осіб ≤75 років (І/А). Якщо виявлено порушення функції нирок та/або потенційну лікарську взаємодію, ініціюють використання статинів із низьких доз за наступного титрування до досягнення цільового рівня ХС ЛПНЩ (І/С).
Терапія дисліпідемії при ЦД
У пацієнтів із ЦД 2-го типу та дуже високим ризиком рекомендовано знижувати рівень ХС ЛПНЩ на ≥50% від початкового, цільовий показник ХС ЛПНЩ складає <1,4 ммоль/л, або <55 мг/дл (І/А). У хворих на ЦД 2-го типу з високим ризиком доцільно зменшувати ХС ЛПНЩ на ≥50% від вихідного, цільовий рівень ХС ЛПНЩ становить <1,8 ммоль/л, чи <70 мг/дл (І/А). Статини рекомендовані пацієнтам із ЦД 1-го типу та високим або дуже високим ризиком (І/А). Препарати не рекомендовані пацієнткам дітородного віку з/без ЦД та тим, які планують вагітність або не застосовують надійної контрацепції (ІІІ/С).
Менеджмент пацієнтів із гострим коронарним синдромом
Усім пацієнтам із гострим коронарним синдромом (ГКС) без протипоказань або непереносимості статинів у анамнезі рекомендовано розпочати або продовжити застосування препаратів у високих дозах незалежно від початкового рівня ХС ЛПНЩ (І/А). Якщо цільового значення ХС ЛПНЩ не вдалося досягти після 4‑6 тижнів лікування максимально толерантною дозою статинів, слід додати езетиміб (І/В). Якщо цільового рівня ХС ЛПНЩ не було досягнуто через 4‑6 тижнів терапії комбінацією статинів у максимально толерантній дозі та езетимібу, рекомендовано додати інгібітор PCSK9 (І/В).
Гіпохолестеринемічна терапія для попередження АССЗ в осіб з ішемічним інсультом
Пацієнти з перенесеним ішемічним інсультом або транзиторною ішемічною атакою відносяться до групи дуже високого ризику АССЗ, навіть за умови повного відновлення після інсульту. Тому для таких хворих рекомендовано забезпечити інтенсивну гіпохолестеринемічну терапію (І/А).
Терапія дисліпідемії при хронічній серцевій недостатності та клапанній патології серця
Гіпохолестеринемічну терапію не слід призначати пацієнтам із серцевою недостатністю за умови відсутності показань для лікування (ІІІ/А). Ініціацію гіпохолестеринемічної терапії не рекомендовано особам зі стенозом аортального клапана без ІХС для зменшення прогресування аортального стенозу за відсутності підґрунтя для лікування (ІІІ/А).
Контроль ліпідного профілю в осіб зі зниженою ШКФ відповідно до помірної та термінальної ХХН
Пацієнтів із ХХН 3‑5-ї стадії за Ініціативою щодо поліпшення якості результатів лікування захворювань нирок слід відносити до групи високого та дуже високого ризику АССЗ (І/А). Призначення статинів або комбінації статини + езетиміб рекомендоване особам із ХХН 3‑5-ї стадії, що не потребують діалізу (І/А). Хворим на ХХН 3‑5-ї стадії, які потребують діалізу та не страждають на АССЗ, не варто починати статинотерапію (ІІІ/А).
Гіпохолестеринемічна терапія у пацієнтів із різними клінічними станами
Атеросклероз периферичних судин (включно з ІХС). Таким пацієнтам рекомендоване призначення гіполіпідемічної терапії, зокрема статинів у максимально толерантних дозах + езетиміб або комбінації з інгібітором PCSK9 для зниження ризику АССЗ (І/А).
Хронічні імунно-опосередковані запальні захворювання. Використання гіполіпідемічних препаратів на підставі наявності хронічної імунно-опосередкованої запальної хвороби не рекомендоване (ІІІ/С). Серйозні психічні розлади. Важливо враховувати такі стани для модифікації та оцінки загального ризику ССЗ (І/С). Рекомендовано використовувати універсальні протоколи лікування для контролю загального ризику ССЗ в осіб із серйозними психічними розладами на рівні з пацієнтами, що не мають подібних захворювань (І/С). Доцільно ретельно стежити за хворими із серйозними психічними порушннями з метою модифікації способу життя та підвищення комплаєнсу щодо медикаментозної терапії (І/С).
Поширені запитання та відповіді
? Як часто слід перевіряти ліпідний профіль?
Перш ніж розпочинати гіполіпідемічну терапію, слід провести щонайменше два вимірювання рівня ліпідів крові з інтервалом в 1‑12 тижнів, за винятком, коли потрібне оперативне втручання при ГКС та у пацієнтів із високим ризиком.
? Як часто треба перевіряти ліпідний профіль пацієнта після початку терапії або її корекції?
Ліпідний профіль хворого після ініціації лікування або його корекції варто перевіряти через кожні вісім (±4) тижнів.
? Як часто слід перевіряти ліпідний профіль після досягнення цільового або оптимального рівня ліпідів?
Потрібно перевіряти ліпідний профіль щорічно (якщо не виникають проблеми із прихильністю чи інші конкретні причини для частішого дослідження).
? Як часто необхідно вимірювати АЛТ у пацієнтів, що приймають гіполіпідемічні препарати?
Перед призначенням терапії, одноразово через 8‑12 тижнів після початку лікування або збільшення дози. Потім регулярний контроль АЛТ під час приймання статинів не потрібний, якщо не розвиваються симптоми, що свідчать про захворювання печінки. Під час лікування фібратами рекомендований моніторинг АЛТ.
? Якою має бути тактика при виявленні цитолізу в пацієнта на гіполіпідемічній терапії?
Якщо АЛТ підвищено менше ніж втричі від норми, слід продовжити терапію та провести повторний аналіз через 4‑6 тижнів. Якщо АЛТ підвищено втричі від норми або більше, треба зменшити дозу та виконати повторну оцінку через 4‑6 тижнів. Поступове підвищення дози можна розглянути після того, як АЛТ повернеться до норми. Якщо показник АЛТ залишається підвищеним, варто перевірити наявність інших причин.
? Як часто потрібно вимірювати КФК у пацієнтів, які приймають гіполіпідемічні препарати?
Перед початком терапії. Якщо базовий рівень креатинфосфокінази (КФК) підвищений у чотири рази від норми, перш ніж починати медикаментозне лікування слід перевірити даний показник повторно. Моніторинг КФК не потрібний. Варто перевірити КФК, якщо у пацієнта розвинулася міалгія.
? Якою має бути лікувальна тактика при підвищенні КФК?
Якщо підвищення менше ніж у чотири рази від норми та симптоми ураження м’язів відсутні, рекомендовано продовжувати терапію за контролю КФК. Якщо симптоми наявні та зберігаються протягом певного часу, треба припинити використання статинів та знову проаналізувати симптоми через шість тижнів; слід повторно оцінити показання до призначення статинів. За підвищення менше ніж у 10 разів від норми необхідно продовжувати зниження дозування терапії під контролем КФК 2‑6 тижнів. Якщо підвищення більше ніж у 10 разів від норми, рекомендовано припинити терапію, перевірити функцію нирок та контролювати КФК кожні два тижні.
Необхідно розглянути можливість підвищення рівня КФК з інших причин, як-то фізичне навантаження. Варто припустити розвиток міопатії, якщо вміст КФК залишається значним. Рекомендовано розглянути доцільність призначення комбінованої терапії або альтернативного препарату.
? У яких пацієнтів слід перевіряти HbA1С або глюкозу в крові?
Необхідно регулярно перевіряти HbA1С або глюкозу в пацієнтів із високим ризиком розвитку ЦД, а також при використанні статинів у високих дозах.
Підготувала Маргарита Марчук
Із повною версією документа можна ознайомитися на сайті www.escardio.org
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (66) листопад 2019 р.