7 лютого, 2020
Вибір гепатопротектора для лікування уражень печінки
 Особливістю сучасного популяційного здоров’я можна вважати погіршення функціонального стану печінки, що зумовлено сукупністю екзогенних та ендогенних факторів. Ураження печінки відносяться до найпоширеніших порушень, вони практично завжди виступають коморбідним фоном і впливають на ефективність терапії інших хвороб, тому проблема медикаментозного лікування гепатопатології є вкрай актуальною та потребує уваги клініцистів [1, 2].
Особливістю сучасного популяційного здоров’я можна вважати погіршення функціонального стану печінки, що зумовлено сукупністю екзогенних та ендогенних факторів. Ураження печінки відносяться до найпоширеніших порушень, вони практично завжди виступають коморбідним фоном і впливають на ефективність терапії інших хвороб, тому проблема медикаментозного лікування гепатопатології є вкрай актуальною та потребує уваги клініцистів [1, 2].
Насамперед це стосується засад застосування гепатопротекторів (А05В – препарати, що використовуються при захворюваннях печінки), місце яких у стратегії і тактиці лікування уражень печінки дотепер остаточно не визначене, їх призначення відбувається переважно емпірично чи взагалі випадково, всі препарати вважаються нешкідливими та показаними в усіх випадках. Слід зазначити, що деякі гепатопротектори посідають чільні місця в топ‑10 продажів медикаментів у нашій країні і при цьому взагалі не належать до життєво важливих лікарських засобів. У запропонованій нами системі профілактики уражень печінки [2] гепатопротектори є базисними медикаментами ІІІ етапу. Наявні в сучасній науковій літературі публікації щодо гепатопротекторів переважно стосуються використання лише якогось одного засобу та носять рекламний характер.
З метою підсумувати принципи раціонального використання гепатопротекторів для лікування уражень печінки на основі аналізу сучасної наукової літератури проведено аналіз джерел у базі PubMed і вітчизняних періодичних виданнях за ключовими словами «гепатопротектори», «розторопша», «есенціальні фосфоліпіди», «урсодезоксихолева кислота», «лікування гепатиту», «лікування стеатозу», «лікування цирозу печінки».
Результати та обговорення
Гепатопротектори – неоднорідні група лікарських засобів (від 500 до 700, за різними джерелами), які через різноманітні механізми захищають клітини печінки від пошкодження і тим самим активують її функції. Класифікація гепатопротекторів остаточно не узгоджена, із цього приводу тривають наукові дискусії. На наш погляд, доцільно розподіляти ці засоби на 4 групи: 1) препарати розторопші плямистої й інших рослин; 2) препарати есенціальних фосфоліпідів (ЕФЛ), амінокислот і лецитини; 3) похідні урсодезоксихолевої кислоти та жовчевмісні препарати; 4) інші тваринні, синтетичні та комбіновані препарати. До спільних механізмів дії гепатопротекторів відносяться [5, 8-10]: пригнічення перекисного окиснення ліпідів та зв’язування надлишку продуктів окиснення; підвищення активності ферментів, що беруть участь в окисненні, репарація (відновлення) мембран клітин гепатоцитів; збільшення запасів глутатіону, таурину та сульфатів, що підвищує антитоксичну активність гепатоцитів; зменшення синтезу прозапальних цитокінів і стабілізація мембрани гепатоциту (протизапальний ефект); зменшення некрозу гепатоцитів, стимуляція активності колагеназ і блокада ферментів синтезу сполучної тканини (антифібротична дія). Більшість гепатопротекторів є комплексними препаратами (містять не одну речовину) та похідними рослин, що значно збільшує кількість механізмів дії, однак часто всі клітинні механізми – реалізатори ефекту засобу невідомі, а ефективність препарату перевірена чи доведена лише емпірично в клініці.
На думку провідних клініцистів, при більшості нозологій і клінічних ситуацій гепатопротектори мають лише допоміжне значення, оскільки не покращують перебігу печінкової патології, хоча дещо знижують смертність [6, 8, 9]. Безумовно, гепатопротектори найчастіше застосовуються для лікування різноманітних хвороб печінки, проте доцільність їх використання слід розглядати після вирішення питання етіотропної терапії (медикаментозної та/або немедикаментозної) і завжди пам’ятати про поліпрагмазію та принцип протидії організму лікам, особливо коли йдеться про комплексні та полікомпонентні рослинні засоби, роль яких у розвитку та прогресуванні токсичних уражень печінки останнім часом переглядається.
Ми вважаємо, що вибір гепатопротектора для лікування ураження печінки можливий за нозологічним (гепатит, цироз печінки тощо) чи синдромальним (цитоліз, холестаз, фіброзування тощо) принципами.
Нозологічний підхід до вибору гепатопротектора
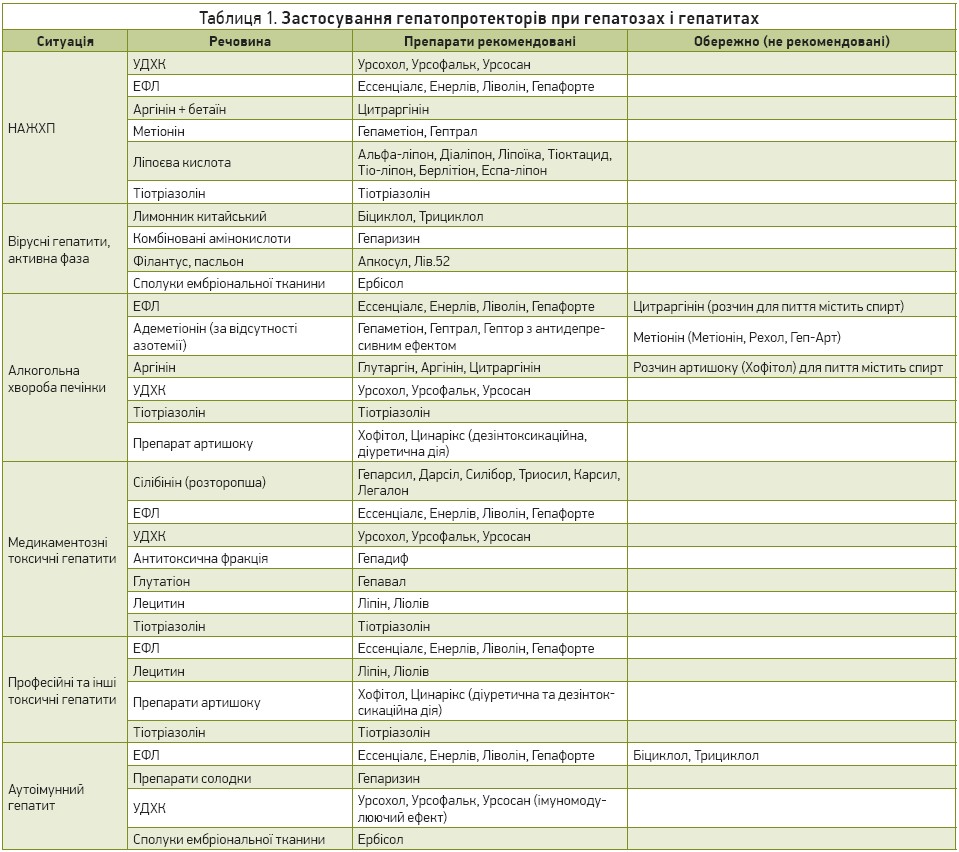
Неалкогольна жирова хвороба печінки (НАЖХП, жировий гепатоз, стеатогепатоз), яка виникає за умов інфільтрації 66% гепатоцитів ліпідами, є найчастішим патологічним станом сьогодення, що зумовлено поширенням порушень вуглеводного та ліпідного метаболізму в населення. НАЖХП потребує передусім корекції провідної причини, модифікації стилю життя, патогенетичної терапії (препарати, які зменшують інсулінорезистентність і підвищують чутливість до інсуліну, ліпідознижувальна терапія, засоби пригнічення активності ренін-ангіотензин-альдостеронової системи) [2, 11]. Гепатопротектори захищають мембрани гепатоцитів від пошкоджень, покращуючи та відновлюючи їхні фізико-хімічні властивості і транспортні системи; збільшують антиоксидантний потенціал та, що особливо важливо, мають гіполіпідемічний і ліпотропний ефекти. З‑поміж гепатопротекторів найбільше значення мають урсодезоксихолева кислота (УДХК), ЕФЛ, похідні ліпоєвої та амінокислот (аргініну, метіоніну, холіну), тіотріазолін (табл. 1). Менш переконливий позитивний вплив мають комбіновані рослинні препарати [10] (Апкосул, Лів.52, Вімлів) і гомеопатичні засоби. Оскільки стратегічним напрямом лікування стеатозу є нормалізація ліпідного та вуглеводного метаболізму, гепатопротектора терапія має проводитися тривалими курсами обов’язково на фоні оптимізації харчування та фізичної активності. Перевага надається пероральним гепатопротекторним засобам із застосуванням декількома повторними курсами тривалістю до 2 міс кожен.
Гепатити лікують залежно від походження, активності, вираженості основних клініко-лабораторних синдромів, використовуючи, крім обов’язкових модифікації стилю життя й етіотропної терапії, гепатопротектори. Вірусні гепатити потребують передусім противірусного лікування, що призначається з урахуванням не тільки виду вірусу, стадії (реплікація), генотипу, кількості вірусних копій тощо, а й доступності та вартості медикаментів. Гепатопротектори мають застосовуватися переважно у випадках відмови від противірусної терапії або після неї. На практиці противірусні препарати призначають одночасно з гепатопротекторами, однак дані наукових досліджень неоднозначні. Це стосується, зокрема, одночасного застосування інтерферонів, які мають вплинути на вірус внітрішньоклітинно, та гепатопротекторів, які зміцнюють мембрану клітини і тим самим перешкоджають проникненню лікарського засобу до клітини. З урахуванням цього при відмові від противірусної терапії чи після неї перевагу слід надавати рослинним засобам з певною противірусною активністю та сполукам ембріональної тканини. Противірусна активність описана в низки рослин, як-от: лимонник китайський, який сповільнює апоптоз і має противірусний ефект через зниження вмісту HBV-ДНК та HCV-РНК; філантус гіркий, що інактивує віруси гепатиту В через пригнічення активності їхньої ДНК‑полімерази; пасльон; солодка, гліциризин якої регулює активацію Т‑клітин, індукує інтерферон-γ, активує NK‑клітини, сприяє диференціації Т‑лімфоцитів тимуса. Органічні сполуки ембріональної тканини активують цитотоксичні Т‑лімфоцити та Т‑кілери, відповідальні за знищення клітин-вірусоносіїв, а також індукують синтез інтерферонів α, β і γ, підвищуючи їх рівень у крові в 4-6 разів, що сприяє прискоренню елімінації вірусу. Певна противірусна активність описана також у комплексних рослинних засобів, утім, її недостатньо для подолання вірусу в печінці. Противірусна та протизапальна активність були підставами для застосування похідних розторопші [6, 9] для лікування вірусних гепатитів, хоча результати не є однозначними [10]. Виражені синдроми мезенхімального запалення, цитолізу, холестазу можуть коригуватися гепатопротекторами.
Алкогольний токсичний гепатит є формою алкогольної хвороби печінки, який за поширеністю посідає друге місце серед усіх уражень печінки і рідко діагностується на практиці [2]. Алкогольним ураженням печінки приділяється мало уваги як лікарями, так і науковцями. Зважаючи на часте вживання алкоголю в нашій країні, у тому числі слабоалкогольних напоїв, частота алкогольного ураження печінки має бути досить високою. Основою лікування алкогольного гепатиту є категорична відмова пацієнта від алкоголю будь-якого виду в будь-якій кількості. Важливою складовою лікування власне алкоголізму та алкогольної нейропатії зокрема є гепатопротектори. Рекомендовано призначати гепатопротектори з різними провідними механізмами дії, які зміцнюють і відновлюють пошкоджені мембрани гепатоцитів, зменшують процеси пероксидації, активують ферментні системи клітин печінки і її детоксикаційну здатність. Це передусім ЕФЛ, препарати амінокислот адеметіоніну й аргініну, УДХК, похідні артишоку та синтетичний тіотріазолін. Є дані про застосування похідних розторопші [5, 9], хоча незаангажовані науковці відзначають певні розбіжності в доказах ефективності [10]. Не слід використовувати оральні форми препаратів, які містять спирт, навіть і в невеликій кількості. Похідних метіоніну також краще уникати, натомість застосовувати адеметіонін, оскільки перетворення метіоніну в пошкодженій алкоголем печінці може бути недостатнім і це спровокує пришвидшення азотемії. Виражені синдроми мезенхімального запалення, цитолізу, холестазу можуть коригуватися гепатопротекторами; при цьому слід пам’ятати, що алкогольне ураження печінки часто супроводжується розвитком синдрому холестазу, який обмежує використання деяких гепатопротекторів (табл. 2).
Медикаментозний токсичний гепатит є недостатньо дослідженою формою ураження печінки, він може бути спричинений величезною кількістю препаратів, серед яких на першому місці протипухлинні та протитуберкульозні засоби з тривалим періодом застосування, а також антибіотики, психотропні та протисудомні ліки, статини тощо. З‑поміж гепатопротекторів для лікування медикаментозних уражень печінки найбільше значення мають похідні розторопші; ЕФЛ, які захищають мітохондрії та мікросомальні ензими від пошкодження; УДХК, що прискорює виведення токсинів із жовчю; похідні амінокислот (лецитину, глутатіону) й антитоксична фракція екстракту печінки, тіотріазолін.
Інші токсичні гепатити, передовсім професійні, що найчастіше зумовлені впливом свинцю (вихлопні гази), кадмію (викиди підприємств, теплових електростанцій), інших важких металів, потребують перш за все повного припинення контакту з етіологічним чинником, чого не завжди можливо досягти, а отже, ефективність лікування буде невисокою. Крім вищеназваних антитоксичних гепатопротекторів (ЕФЛ, похідні лецитину), використовуються препарати артишоку з діуретичними та дезінтоксикаційними властивостями.
Наявні літературні дані щодо лікування аутоімунного гепатиту гепатопротекторами є найменш конкретними. Комбінований рослинний засіб, складовою якого є гліциризин із солодки, регулює активацію Т‑клітин, індукує інтерферон-γ, активує NK‑клітини, сприяє диференціації Т‑лімфоцитів тимуса; ЕФЛ активують продукцію антитіл до різних антигенів; похідні УДХК мають імуномодулюючий ефект; Ербісол, що містить сполуки ембріональної тканини, активує цитотоксичні Т‑лімфоцити та Т‑кілери, індукує синтез природних антитіл. Виражені синдроми мезенхімального запалення, цитолізу, холестазу можуть коригуватися гепатопротекторами, як і фіброзування.
Цироз печінки практично завжди є наслідком гепатиту, який може залишатися непоміченим. Режим і лікувальні заходи у хворих на цироз печінки визначаються етіологічними факторами, ступенем активності та компенсації, наявністю системних ускладнень і супутньої патології. Необхідно повністю виключити алкогольні напої, гепатотоксичні речовини, транквілізатори та снодійні засоби. Призначати гепатопротектори слід не емпірично, а за чіткими показаннями – за синдромами: цитолітичним, мезенхімально-запальним, холестатичним, інтоксикаційним унаслідок шунтування, гепаторенальним, енцефалопатичним, оскільки правилом ведення пацієнта із цирозом печінки є максимальне обмеження медикаментозного навантаження.
Синдромальний підхід до вибору гепатопротектора
У багатьох складних клінічних ситуаціях стратегія лікування будується не стільки на етіологічному варіанті ураження печінки, скільки на синдромному, тобто на синдромах цитолізу, мезенхімального запалення, холестазу, фіброзування, детоксикації, гепаторенального, енцефалопатичного тощо, що дозволяє швидше усунути клінічні та/або лабораторні прояви ушкодження печінки.
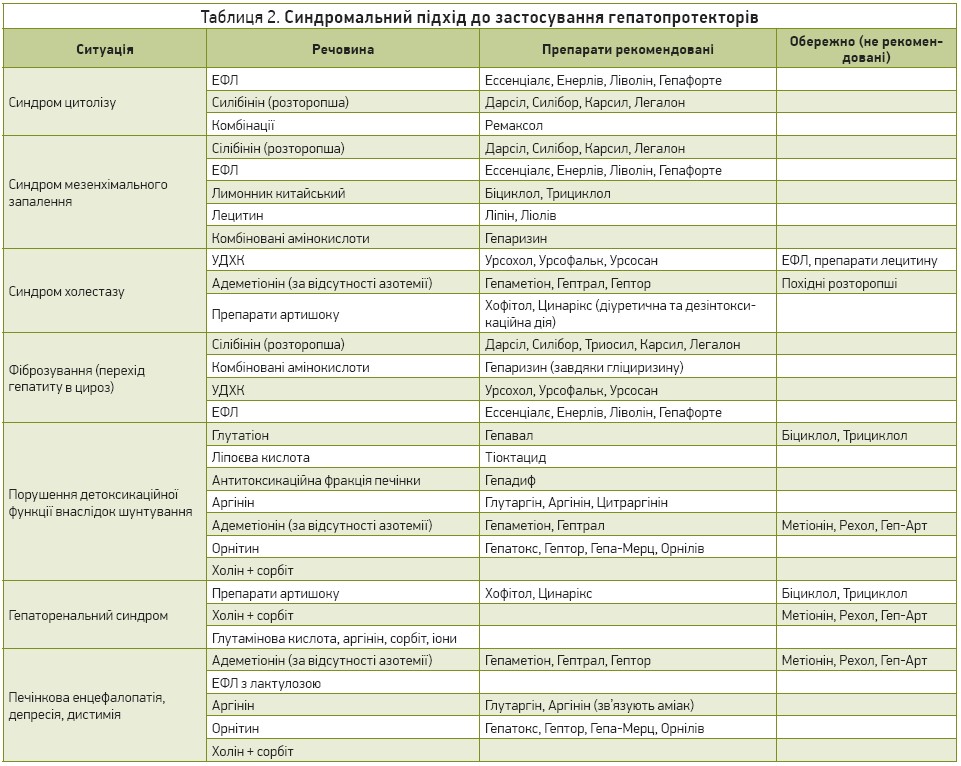
Синдром цитолізу, що лабораторно проявляється зростанням рівня трансаміназ, суттєво зменшується під впливом ЕФЛ, які відновлюють мембрани гепатоцитів за рахунок вбудови ЕФЛ у місця пошкодження мембран й активують функції транспортних систем; похідних розторопші, які мають мембраностабілізувальну дію внаслідок стимуляції полімерази А ядра, збільшення синтезу білків на рибосомах і підвищення утворення фосфоліпідів [6]. За умов значної вираженості синдрому цитолізу рекомендується крапельне введення комбінованих розчинів, які підвищують стійкість мембран гепатоцитів до перекисного окиснення та відновлюють активність ферментів, у стаціонарних умовах.
Синдром мезенхімального запалення, якому притаманні зростання осадових проб, рівня гострофазових білків, ШОЕ, коригується препаратами розторопші [6], протизапальна дія якої зумовлена зменшенням активності ліпоксигенази та простагландинсинтази, пригніченням утворення лейкотрієнів (В4), простагландинів і ядерного фактора κВ; ЕФЛ, які пригнічують синтез прозапальних цитокінів і нормалізують продукцію простагландинів; УДХК, яка зменшує продукцію трансформуючого фактора росту α та фактора некрозу пухлин α; похідними лимоннику китайського, лецитином і комбінованими амінокислотними засобами. Слід сказати, що практично всі гепатопротектори мають певну протизапальну дію, що забезпечується різними механізмами: стабілізацією мембран гепатоцитів, зменшенням активності низки ферментів (ліпоксигенази, простагландинсинтази) та пригніченням продукції активних речовин запалення (цитокіни/інтерлейкіни, простагландини, фактор некрозу пухлин α, трансформуючий фактор росту α).
Синдром холестазу, що лабораторно маніфестує зростанням умісту лужної фосфатази та γ-глутамілтранспептидази, досить добре піддається корекції під впливом УДХК, що підтверджено власним багаторічним клінічним досвідом [3], адеметіоніну, препаратів артишоку. Антихолестатичний ефект УДХК пояснюється пригніченням синтезу токсичних жовчних кислот (ЖК) у жовч за рахунок конкурентного захоплення УДХК рецепторами тонкої кишки та стимуляцією екзоцитозу в гепатоцитах унаслідок активації Са2+-залежної
Фіброзоутворення та перехід гепатиту в цироз завжди є наслідком тривалого активного запалення. Останнє призводить до розвитку цирозу печінки, при якому морфологічні зміни стають незворотними. Цей процес відбувається постійно, але переважно він прихований як від лікарів, так і від пацієнтів, оскільки дотепер ми не маємо впроваджених недискутабельних лабораторних критеріїв фіброзування, хоча запропоновані різні шкали та системи обрахунку балів. Гепатопротектори мають допоміжне значення для зниження фіброзоутворення, однак зменшення проявів та активності запалення і цитолізу під впливом цих засобів автоматично зменшить у подальшому формування сполучної тканини. Серед гепатопротекторів, які зменшують саме фіброзування, можна назвати похідні розторопші [6, 9], які діють через пригнічення активності ядерного фактора κВ, протеїнкіназ, зменшення кількості вільних радикалів, зниження активності зірчастих клітин печінки, зменшення їх проліферації та трансформації в міофібробласти, безпосереднє пригнічення синтезу колагену; ЕФЛ, які сповільнюють синтез колагену та підвищують активність колагенази; УДХК; комбіновані амінокислотні засоби.
Порушення детоксикаційної функції внаслідок шунтування (портальний цироз, портальна гіпертензія, портокавальне шунтування) може дещо зменшуватися за умов застосування гепатопротекторів через зв’язування аміаку та/або прискорення утворення сечовини з нього. З такою метою запропоновано використовувати похідні глутатіону, ліпоєвої кислоти, амінокислот аргініну, орнітину; а також комбінацію холіну із сорбітом, антитоксичну фракцію печінки. Адеметіонін застосовується в разі відсутності азотемії. Похідних метіоніну краще уникати через сповільнення перетворення його на активну форму у випадку цирозу.
Лікування гепаторенального синдрому (прогресуючого зниження ниркового кровотоку та швидкості клубочкової фільтрації, що є формою ниркової недостатності на фоні цирозу печінки) є значною проблемою, оскільки в такого пацієнта вже наявна недостатність щонайменше двох життєво важливих органів – печінки та нирок. Пацієнтам відміняють усі гепато- та нефротоксичні препарати, призначають альбумін із вазопресином, гемодіаліз. Застосування гепатопротекторів можливе тільки на ранніх стадіях гепаторенального синдрому, коли швидкість клубочкової фільтрації та функціональні показники печінки змінені незначно. Запропоновані препарати артишоку, які мають діуретичну та дезінтоксикаційну дію, а також комбінації холіну із сорбітом і глутамінової кислоти з аргініном, сорбітом й іонами (інфузія в стаціонарних умовах). Уникати слід препаратів лимоннику китайського та метіоніну.
Печінкова енцефалопатія, супутні депресія, дистимія, що є частими проявами декомпенсації цирозу печінки, характеризуються порушеннями свідомості, поведінки, зміною особистісних рис, неврологічними симптомами, змінами на електроенцефалограмі внаслідок токсичного впливу на центральну нервову систему аміаку й інших шкідливих речовин, що адсорбуються з кишок. Прояви печінкової енцефалопатії зменшуються за умов адекватного лікування порушень детоксикаційної функції печінки та/або гепаторенального синдрому. Гепатопротектори мають допоміжне значення в терапії печінкової енцефалопатії і можуть використовуватися лише на І-ІІ стадіях цього патологічного процесу, також можливе їх застосування з метою профілактики. Рекомендовані похідні амінокислот аргініну, адеметіоніну (але не метіоніну) з антидепресивним ефектом і комбіновані засоби.
Висновки
Проблема застосування гепатопротекторів для лікування уражень печінки є актуальною та потребує уваги клініцистів. Гепатопротектори (препарати розторопші й інших рослин, похідні амінокислот, ЕФЛ, лецитини, УДХК, жовчевмісні засоби та ін.) мають протизапальний, антиоксидантний, детоксикаційний, мембраностабілізувальний ефекти. Підбір гепатопротектора для лікування уражень печінки може здійснюватися за нозологічним (стеатоз, гепатит) чи синдромальним (цитоліз, запалення, холестаз, фіброзування, енцефалопатія, інтоксикація) принципом.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 1 (470), січень 2020 р.