2 березня, 2020
Оптимізація ведення пацієнтів із госпітальною пневмонією
Акцент на подолання діагностично-лікувальних перешкод
У вересні, у палаці мистецтв «Український дім», відбувся знаковий для вітчизняної медичної спільноти захід – Конгрес анестезіологів України. Програма заходу охопила широкий спектр питань щодо анестезіологічного забезпечення та ведення пацієнтів, які перебувають в критичному стані. Велику зацікавленість присутніх викликала доповідь президента Асоціації анестезіологів України, професора кафедри анестезіології та інтенсивної терапії Національного медичного університету ім. О.О. Богомольця (м. Київ), доктора медичних наук Сергія Олександровича Дуброва. Темою його виступу стала госпітальна пневмонія.
– Пневмонія – гостре інфекційне захворювання переважно бактеріальної етіології (80-90%), яке характеризується вогнищевим пошкодженням респіраторних відділів легень і наявністю внутрішньоальвеолярної ексудації.
Діагностичні критерії захворювання [1]:
- температура тіла ≥38,5 °C або <36,0 °C;
- гнійне мокротиння;
- лейкоцитоз >11 000 в 1 мм3;
- лейкопенія <4000 в 1 мм3;
- поява нових інфільтратів на рентгенограмі органів грудної клітки (ОГК);
- виявлення збудників у мокротинні, крові або плевральному випоті.
На жаль, зазначені критерії не завжди допомагають діагностувати пневмонію, особливо в умовах відділення інтенсивної терапії (ВІТ). Які ж основні перешкоди ускладнюють верифікацію діагнозу?
1. Неспецифічність гіпертермії та змін у лейкограмі.
Лихоманка та лейкоцитоз можуть бути зумовлені не лише пневмонією, а й проявами основного захворювання (комбінована травма), синдромом системної запальної відповіді та неінфекційними причинами. За даними Meduri та співавт., у 42% пацієнтів із підозрою на негоспітальну пневмонію (НП) лихоманка була спричинена позалегеневими вогнищами інфекції [2].
2. Недостатня чутливість та специфічність рентгенологічного дослідження ОГК при НП, особливо вентилятор-асоційованій (ВАП).
Чутливість цього методу складає 50-78%, а специфічність – 40-60%. Нові інфільтрати на рентгенограмі ОГК можуть бути зумовлені низкою інших патологічних станів, наприклад ателектазом, застійною серцевою недостатністю, тромбоемболією легеневої артерії, туберкульозом та ін. Водночас при проведенні комп’ютерної томографії ОГК у 26% пацієнтів були виявлені свіжі інфільтрати, які не візуалізувалися рентгенологічно. Результати аутопсії свідчать: клінічний діагноз пневмонії в 10-29% випадків не підтверджувався морфологічно, а в 20-40% випадків під час розтину виявляли пневмонію, яка не була діагностована прижиттєво [3].
3. Неналежна мікробіологічна діагностика.
Дана проблема зумовлена як незадовільною якістю роботи бактеріологічних лабораторій (що є наслідком недостатнього фінансування і, своєю чергою, слабкої мотивації працівників і недбалого відношення до клінічного матеріалу), так і відсутністю взаємодії клінічних лікарів із мікробіологами.
Адекватна мікробіологічна діагностика має:
- Відповідати часовим проміжкам: попередній результат – через 24 год; кінцевий результат із видовою ідентифікацією та антибіотикограмою – через 48-72 години.
- Включати консультацію лікаря-мікробіолога.
Найбільша небезпека неналежної мікробіологічної діагностики та антимікробної терапії полягає в розвитку нечутливості до антибіотиків (АБ) та збільшенні поширеності резистентних штамів у лікувальних закладах [4].
Це напряму впливає на летальність. Згідно з даними Leone M. Garcin та співавт., летальність пацієнтів із ВАП, в яких емпірична антибактеріальна терапія була неадекватною, становить 47%, тоді як при правильному виборі антимікробної тактики даний показник дорівнює 20% (р=0,04) [5].
У міжнародному дослідженні з вивчення частоти виникнення інфекційних ускладнень та їхніх наслідків у ВІТ (n=13 769) було виявлено, що в 51% пацієнтів розвинулись інфекційні ускладнення, із них 63,5% припадало на інфекції дихальних шляхів. Показник летальності у ВІТ у пацієнтів із нозокоміальними інфекційними ускладненнями був майже в 2,5 разу вищий у порівнянні з неінфікованими пацієнтами (25 проти 11% відповідно), а госпітальна летальність – у 2,2 разу більшою (33 проти 15% відповідно) [6].
Основні принципи емпіричного вибору адекватних АБ:
- Знання госпіталітету відділення, тобто найпоширеніших у відділенні патогенів та їхньої чутливості до АБ.
- Широке впровадження в клінічну практику бактеріоскопії, яка є швидким і простим методом виявлення основних характеристик збудника (фарбування за Грамом, морфологія). Потрібно пам’ятати про оцінку якості зразка мокротиння: у ньому має виявлятися >25 лейкоцитів та <10 епітеліальних клітин.
- Ураховувати бактеріальну чутливість та фармакодинамічні характеристики АБ.
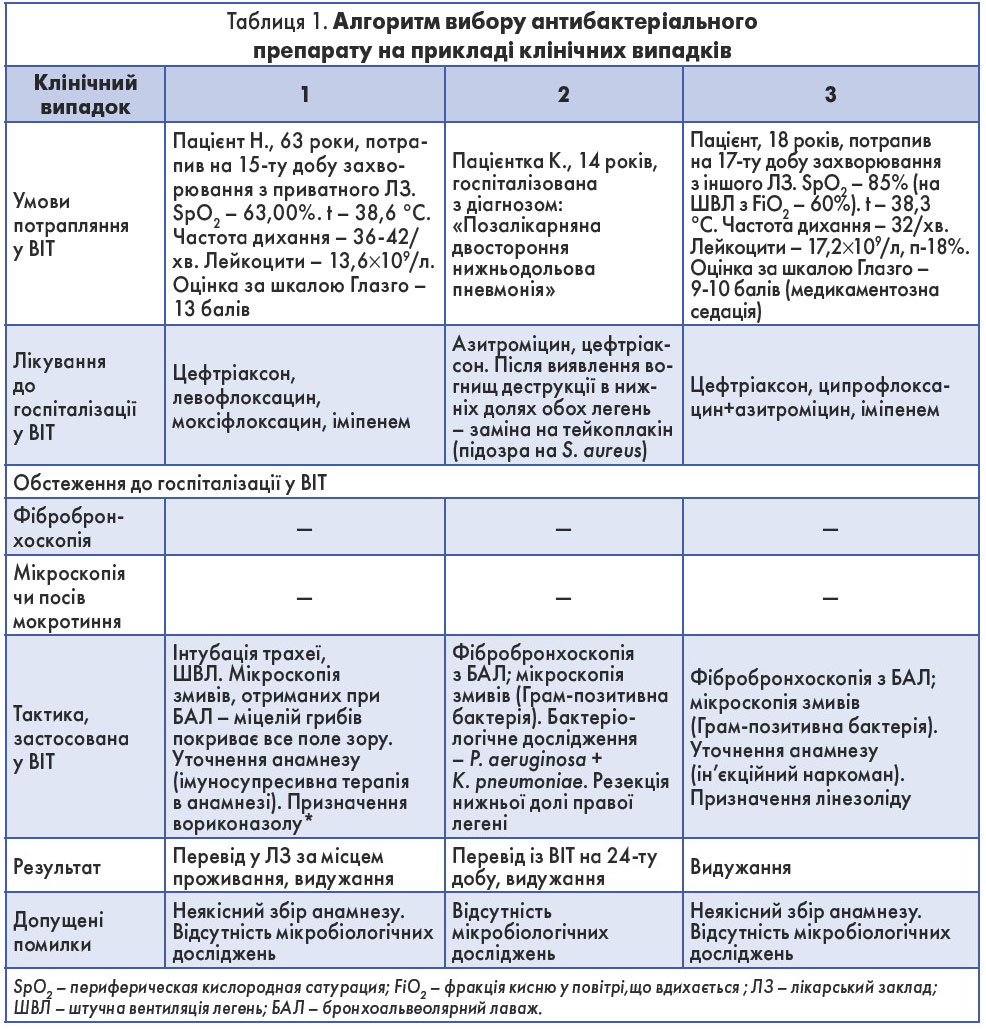
Для кращого розуміння алгоритму вибору антибактеріального препарату доцільно розглянути кілька клінічних випадків (табл. 1).
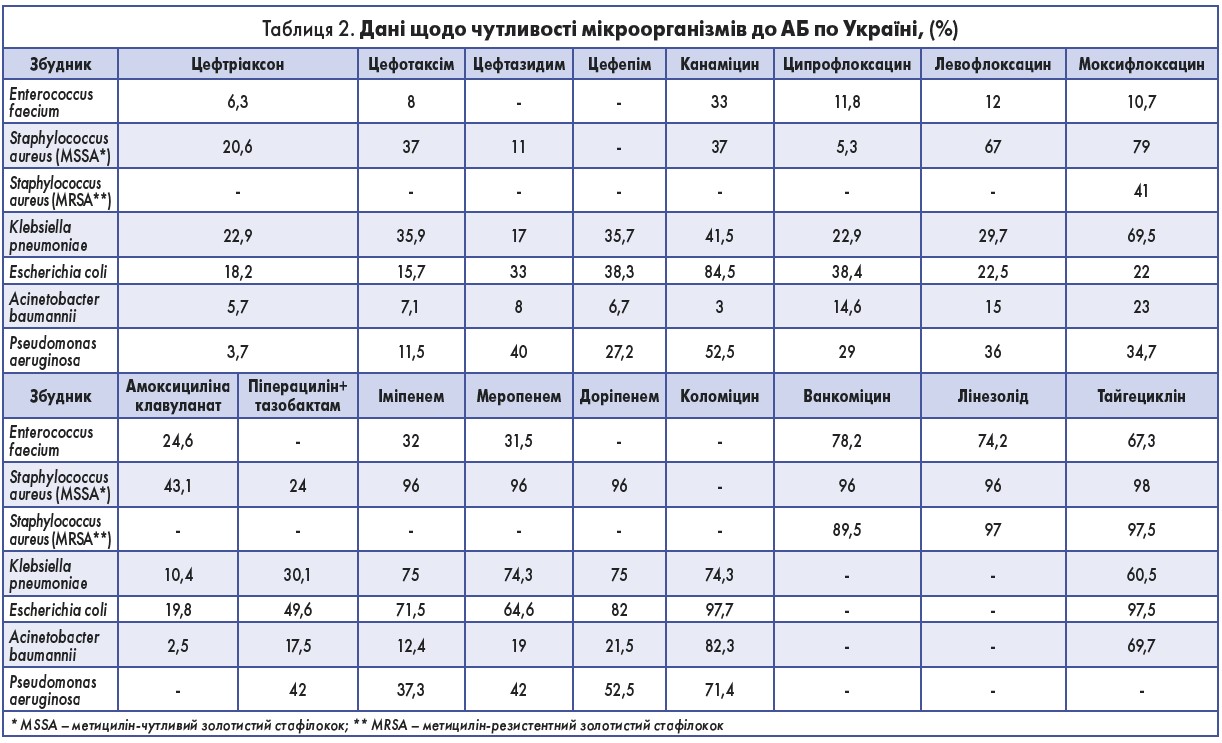
У кожному з наведених випадків відсутність мікробіологічних досліджень призвела до неправильного вибору АБ і розвитку ускладнень. Верифікація збудника не тільки дає можливість вилікувати кожного окремого пацієнта, але й допомагає створити картину госпіталітету відділення. Так, на основі спектра виділених культур від пацієнтів Київської клінічної міської лікарні № 17 були визначені збудники, які найчастіше викликали інфекційні ускладнення, та їхня резистентність до того чи іншого АБ. Дані щодо чутливості мікроорганізмів до АБ у цілому по Україні представлені в таблиці 2 [7].
Таким чином, в Україні, як і всюди у світі, чутливість мікроорганізмів до АБ стрімко падає. Рішення цієї проблеми полягає в раціональній антибіотикотерапії та створенні нових антибактеріальних препаратів.
У світі спостерігається тенденція до щорічного зменшення кількості синтезованих АБ: за останні 7 років FDA було схвалено лише 5 препаратів для системного застосування. Одним із цих лікарських засобів є цефтазидим/авібактам.
Цефтазидим/авібактам показаний при [8]: ускладнених інфекціях сечовивідних шляхів, ускладнених внутрішньочеревних інфекціях.
Цефтазидим/авібактам активний по відношенню до карбапенем-резистентних ентеробактерій (CRE) та продуцентів β-лактамаз розширеного спектру (ESBL).
Фактори ризику CRE±ESBL [8]:
- Колонізація.
- Отримання АБ широкого спектру дії (особливо при застосуванні карбапенемів).
- Історія тривалої госпіталізації.
- Інвазивні пристрої.
- Імуносупресія.
- Інфекція, що виникла у ВІТ.
Ефективність цього препарату вивчалася як у клінічних дослідженнях, так і в реальній практиці. Згідно з даними Shields та співавт., у пацієнтів із бактеріємією CRE K. pneumoniae показники клінічного успіху на 30-й день лікування були значно вищими в пацієнтів, які отримували цефтазидим/авібактам, порівняно з тими, хто приймав карбапенем плюс аміноглікозид (р=0,04) або колістин (р=0,009) та інші схеми (р=0,004) [9].
Ефективність цефтазидиму/авібактаму в умовах реальної клінічної практики була підтверджена на 77 довільно відібраних пацієнтах, які лікувалися від CRE інфекцій. Чутливість виділених патогенів (K. pneumoniae, E. coli, Enterobacter spp.) до препарату на вихідному рівні становила 100%; медіана мінімальної інгібуючої концентрації = 1 мкг/мл, а до K. pneumoniae з мутацією гена blaKPC – 93% [10].
У іще одному дослідженні ефективність цефтазидиму/авібактаму в лікуванні інфекцій, спричинених карбапенем-резистентними Enterobactericeae, порівнювали з колістином. Рівень госпітальної смертності протягом 30 днів становив 9% для групи цефтазидиму/авібактаму проти 32% у пацієнтів, що отримували колістин. Крім того, цефтазидим/авібактам мав на 64% більшу ймовірність кращого результату порівняно з колістином [11].
Отже, цефтазидим/авібактам має підтверджену ефективність та безпеку і низку очевидних переваг у пацієнтів з інфекційними ускладненнями, викликаними карбапенем-резистентними ентеробактеріями та продуцентами
Cписок літератури знаходиться в редакції.
Підготувала Ганна Кирпач
За підтримки компанії «Пфайзер Експорт Бі. Ві.» в Україні
*ВІФЕНД (вориконазол) порошок для розчину для інфузій, по 200 мг у флаконі № 1; таблетки, вкриті плівковою оболонкою, по 50 мг № 10, 200 мг № 14 у картонній коробці
Коротка інструкція для медичного застосування препарату
Показання до застосування: Профілактика інвазивних грибкових інфекцій при алогенній трансплантації кісткового мозку у пацієнтів з високим ризиком такого ускладнення. Віфенд застосовують дорослим і дітям для лікування інвазивного аспергільозу; кандидемії, що не супроводжується нейтропенією; тяжких інвазивних інфекцій, спричинених Candida (включаючи С. krusei), резистентних до флуконазолу; тяжких грибкових інфекцій, спричинених видами Scedosporium і Fusarium. Пацієнтам із прогресуючими інфекціями та інфекціями, що потенційно загрожують життю, Віфенд слід застосовувати у якості стартової терапії. Спосіб застосування та дози: Віфенд (таблетки) слід застосовувати щонайменше за 1 годину до або після прийому їжі. Перед початком застосування препарату Віфенд та протягом його застосування необхідно проводити моніторинг щодо порушень електролітного балансу, таких як гіпокаліємія, гіпомагніємія та гіпокальціємія, та за необхідності провести їх корекцію. Перед застосуванням у вигляді внутрішньовенної інфузії препарат слід відновити та розвести. Віфенд не призначений для болюсного введення. Рекомендовано вводити Віфенд із максимальною швидкістю
Перед використанням препарату необхідно ознайомитись з повною інструкцією для застосування.
Інформація для лікарів та фармацевтів. Призначено для розповсюдження на семінарах, конференціях, симпозіумах з медичної тематики.
Реєстраційні посвідчення № UA/2666/02/01 від 30.08.2019 р., № UA/2666/01/02 і UA/2666/01/01 від 16.08.2019 р.
За додатковою інформацією звертайтеся у Представництво «Пфайзер Експорт Бі. Ві.» в Україні 03680, м. Київ, вул. Н. Амосова, 12;
тел. (044) 391-60-50
МЕРОНЕМ (меропенем) порошок для розчину для ін’єкцій; по 500 мг або 1000 мг у скляних флаконах, по 10 флаконів в картонній коробці.
Показання до застосування. Дорослі та діти віком від 3 місяців: пневмонія, у тому числі негоспітальна та госпітальна пневмонії; бронхолегеневі інфекції при муковісцидозі; ускладнені інфекції сечовивідних шляхів; ускладнені інтраабдомінальні інфекції; інфекції під час пологів і післяпологові інфекції; ускладнені інфекції шкіри і м’яких тканин; гострий бактеріальний менінгіт. Меронем можна застосовувати для лікування пацієнтів з нейтропенією і лихоманкою при підозрі на те, що вона спричинена бактеріальною інфекцією. Лікування пацієнтів з бактеріємією, яка пов’язана або може бути пов’язана з будь-якою з зазначених вище інфекцій. Слід враховувати офіційні рекомендації щодо відповідного застосування антибактеріальних препаратів. Спосіб застосування та дози. Доза меропенему і тривалість лікування залежить від виду збудника хвороби, тяжкості захворювання та індивідуальної чутливості пацієнта: для дорослих та дітей з масою тіла більше 50 кг доза становить від 500 мг до 2 г кожні 8 год, для дітей віком від 3 місяців до 11 років і з масою тіла до 50 кг – від 10 до 40 мг/кг кожні 8 год. Меронем зазвичай слід застосовувати у вигляді внутрішньовенної інфузії тривалістю від 15 до 30 хвилин. Крім того, дози препарату до 1 г (у дітей – до 20 мг/кг) можна вводити у вигляді внутрішньовенної болюсної ін’єкції протягом приблизно 5 хвилин. Приготовлений розчин потрібно використати негайно. Протипоказання. Підвищена чутливість до діючої речовини або до будь-якої з допоміжних речовин препарату. Підвищена чутливість до будь-якого іншого антибактеріального засобу групи карбапенемів. Тяжка підвищена чутливість (наприклад анафілактичні реакції, тяжкі реакції з боку шкіри) до будь-якого іншого типу бета-лактамного антибактеріального засобу (наприклад, пеніцилінів або цефалоспоринів). Побічні реакції. Тромбоцитемія, головний біль, діарея, блювання, нудота, біль у животі, підвищення рівнів трансаміназ, підвищення рівнів лужної фосфатази у крові, підвищення рівнів лактатдегідрогенази у крові, висип, свербіж, запалення, біль у місці ін’єкції. Більш детально – див. інст. Особливості застосування. У зв’язку з ризиком розвитку печінкової токсичності (порушення функції печінки з холестазом і цитолізом) під час лікування меропенемом слід ретельно контролювати печінкові функції. Під час лікування меропенемом у пацієнтів з уже існуючими захворюванням печінки слід ретельно контролювати печінкові функції, при цьому корекція дози не потрібна. Для пацієнтів з порушенням функції нирок коригування дози препарату потрібне, якщо кліренс креатиніну у пацієнтів становить менше 51 мл/хв. Лікування меропенемом може спричинити розвиток позитивного прямого або непрямого тесту Кумбса. Одночасне застосування меропенему і вальпроєвої кислоти/вальпроату натрію не рекомендується. Меронем містить близько 4,0 мЕкв натрію на 1 г дози препарату, що необхідно враховувати при призначенні препарату пацієнтам, які перебувають на дієті з контрольованим вмістом натрію. Препарат застосовувати дітям віком від 3 місяців. Взаємодія з іншими лікарськими засобами та інші види взаємодій. Дослідження щодо взаємодії препарату з окремо взятими лікарськими засобами, крім пробенециду, не проводилися. Пробенецид конкурує з меропенемом щодо активного канальцієвого виведення і, таким чином, пригнічує ниркову секрецію меропенему, що призводить до збільшення періоду напіввиведення та підвищення концентрації меропенему у плазмі крові. Слід проявляти обережність у випадку одночасного застосування пробенециду з меропенемом. Через швидкий початок дії та ступінь зниження одночасне застосування вальпроєвої кислоти і карбапенемів вважається таким, що не піддається коригуванню, тому слід уникати такої взаємодії. Одночасне застосування з варфарином може збільшити його антикоагулянтний ефект. Рекомендується проводити частий контроль рівнів МНВ під час і незабаром після одночасного застосування антибіотиків з пероральним антикоагулянтом. Фармакологічні властивості. Меропенем чинить бактерицидну дію шляхом інгібування синтезу стінок бактеріальних клітин у грампозитивних і грамнегативних бактерій шляхом зв’язування з білками, що зв’язують пеніцилін (РВР). Категорія відпуску. За рецептом. Перед використанням препарату необхідно ознайомитись з повною інструкцією для застосування.
Інформація для лікарів та фармацевтів. Призначено для розповсюдження на семінарах, конференціях, симпозіумах з медичної тематики.
Реєстраційне посвідчення МОЗ України № иА/0186/01/01; № иА/0186/01/02, затверджено Наказом МОЗУ № 1979 від 31.10.2018 р.; зі змінами, затвердженими Наказом МОЗУ № 1212 від 30.05.2019.
За додатковою інформацією звертайтеся у:
Представництво “Пфайзер Експорт Бі. Ві.” в Україні:
03038, м. Київ, вул. Амосова, 12. Тел. (044) 391-60-50.
ЗИВОКС (лінезолід), розчин для інфузій, по 2 мг у 1 мл розчину, по 300 мл в системі для внутрішньовенного введення, по 1 системі в упаковці з ламінованої фольги; таблетки, вкриті плівковою оболонкою, по 600 мг, по 10 таблеток у блістері, по 1 блістеру в картонній коробці.
Показання до застосування: Лікування інфекцій, спричинених чутливими штамами анаеробних або аеробних грампозитивних мікроорганізмів, включаючи інфекції, що супроводжуються бактеріємією, такі як: нозокоміальна пневмонія; негоспітальна пневмонія; ускладнені інфекції шкіри та її структур, зокрема інфекції на фоні діабетичної стопи без супутнього остеомієліту, спричинені Staphylococcus aureus (метицилінчутливими та метицилінрезистентними ізолятами), Streptococcus pyogenes або Streptococcus agalactiae; неускладнені інфекції шкіри та її структур, спричинені Staphylococcus aureus (тільки метицилінчутливими ізолятами) або Streptococcus pyogenes; інфекції, спричинені ентерококами, включаючи резистентні до ванкоміцину штами Enterococcus faecium та faecalis. Якщо збудники інфекції включають грамнегативні мікроорганізми, клінічно показане призначення комбінованої терапії. Спосіб застосування та дози: Зивокс дорослим та дітям від 12 років призначають по 600 мг кожні 12 годин внутрішньовенно або перорально, при неускладнених інфекціях шкіри та її структур – дорослі: 400 мг перорально кожні 12 годин, діти віком від 12 років: 600 мг перорально кожні 12 годин. Тривалість в/в інфузії 30-120 хвилин. Максимальна доза для дорослих і дітей не має перевищувати 600 мг 2 рази на добу. Дітям в/в застосовують з перших днів життя. Таблетки застосовують дітям старше 12 років. Дозування дітям вказані в інструкції до застосування. У разі переводу пацієнта з парентеральної форми на пероральну підбір дози не потрібен, оскільки біодоступність лінезоліду при прийомі внутрішньо становить майже 100%. Детальніше див. повну інстр. Протипоказання: гіперчутливість до лінезоліду або будь-якого іншого компоненту препарату. Зивокс не слід застосовувати пацієнтам, які приймають будь-які медичні препарати, що пригнічують моноаміноксидазу А та В (наприклад, фенелзин, ізокарбоксазид, селегілін, моклобемід), або протягом двох тижнів після прийому таких препаратів. За винятком випадків, коли є можливість ретельного спостереження та моніторингу артеріального тиску, Зивокс не слід призначати пацієнтам з такими супутніми клінічними станами або супутнім прийомом нижчезазначених препаратів: неконтрольована артеріальна гіпертензія, феохромоцитома, карциноїд, тиреотоксикоз, біполярна депресія, шизоафективний розлад, гострі епізоди запаморочення; інгібітори зворотного захоплення серотоніну, трициклічні антидепресанти, агоністи 5-НТ 1 рецепторів серотоніну (триптани), прямі та непрямі симпатоміметики (включаючи адренергічні бронходилататори, псевдоефедрин, фенілпропаноламін), вазопресори (епінефрин, норепінефрин), допамінергічні сполуки (допамін, добутамін), петидин або буспірон. Побічна дія: найчастіше повідомлялося про головний біль, діарею, нудоту та кандидоз. Часто спостерігали: кандидоз або грибкові інфекції, головний біль, перверсії смаку, діарею, нудоту, блювання, аномальні функціональні печінкові проби, збільшення рівнів аланінамінотрансферази, аспартатамінотрансферази або лужної фосфатази, підвищення азоту сечовини крові, зміни в біохімічному, клінічному аналізі крові. Детальніше див. повну інстр. Особливості застосування: Повідомлялося про виникнення оборотної мієлосупресії, вираженність якої може бути залежної від дози препарату та тривалості лікування. Про випадки псевдомембранозного коліту повідомлялося при застосуванні майже всіх антибактеріальних препаратів, включаючи лінезолід; ступінь його тяжкості може варіювати від незначного до такого, що становить загрозу для життя. При застосуванні лінезоліду повідомляли про розвиток лактоацидозу. Пацієнти, у яких під час застосування лінезоліду виникають симптоми та прояви метаболічного ацидозу, включаючи рецидивуючу нудоту або блювання, біль у животі, низький рівень бікарбонатів або гіпервентиляцію, повинні негайно звернутися за медичною допомогою. Повідомлялося про розвиток периферичної нейропатії, а також нейропатії зорового нерва, яка іноді прогресувала до втрати зору у пацієнтів, які отримували лікування препаратом Зивокс. Повідомлялося про випадки судом у пацієнтів, які отримували терапію препаратом Зивокс. Застосування антибіотиків іноді може призводити до надмірного росту нечутливих організмів. У разі виникнення суперінфекцій під час лікування слід вживати відповідних заходів. В період вагітності Зивокс слід призначати лише у випадку, коли очікувана перевага від лікування для матері вища за потенційний ризик для плода. Слід припинити годування груддю протягом лікування препаратом. Детальніше див. повну інструкцію з медичного застосування. Взаємодія з іншими лікарськими засобами: Зивокс розчин сумісний з: 5% розчином декстрози, 0,9% розчином хлориду натрію, розчином Рінгер-лактату для ін’екцій. Лінезолід є неселективним інгібітором моноамінооксидази (МАО) зворотної дії. Тому застосування лінезоліду не рекомендоване, якщо неможливо проводити пильне спостереження та моніторинг стану пацієнта. У здорових добровольців з нормальним артеріальним тиском лінезолід посилює підйом артеріального тиску, спричинений псевдоефедрином та фенілпропаноламіду гідрохлоридом. Детальніше див. повну інструкцію з медичного застосування. Фармакологічні властивості: Зивокс – це антибактеріальний препарат. Умови відпуску: За рецептом.
Перед використанням препарату необхідно ознайомитись з інструкцією для медичного застосування та проконсультуватись з лікарем.
Інформація для лікарів і фармацевтів. Призначено для розповсюдження на семінарах, симпозіумах, конференціях з медичної тематики.
Реєстраційні посвідчення № UA/1969/01/01, затверджено Наказом МОЗУ № 798 від 31.10.2014 р., зі змінами, затвердженими Наказом МОЗУ № 1385 від 08.11.2017 р., та UA/1969/02/01, затверджено Наказом МОЗУ № 1212 від 30.05.2019 р.
За додатковою інформацією звертайтесь до:
Представництва «Пфайзер Експорт Бі. Ві.» в Україні: 03038, м. Київ, вул. Амосова, 12. Бізнес-центр «Горизонт парк», тел.: (044) 391-60-50.
ТИГАЦИЛ (тайгециклін) по 50 мг у скляних флаконах, по 10 флаконів в картонній коробці.
Показання до застосування. Ускладнені інфекції шкіри та м’яких тканин, за винятком iнфiковaно діабетичної стопи; ускладнені інтраабдомінальні інфекції. Тигацил слід застосовувати тільки у випадках, коли інші антибіотики не прийнятні до застосування. Спосіб застосування та дози. Тривалість лікування слід обирати залежно від тяжкості захворювання, локалізації інфекції та клінічної відповіді пацієнта. Початкова рекомендована доза для дорослих становить 100 мг, надалі слід застосовувати по 50 мг кожні 12 годин впродовж 5-14 днів. Тайгециклін слід застосовувати для лікування дітей віком від 8 років тільки після консультації з лікарем, який має достатній досвід лікування інфекцій. Діти віком від 8 до 12 років: 1,2 мг/кг тайгецикліну кожні 12 годин внутрішньовенно, максимальна доза - 50мг кожні 12 годин протягом 5-14 днів. Підлітки віком від 12 до 18 років: 50 мг кожні 12 годин протягом 5-14 днів. Тайгециклін застосовують лише шляхом внутрішньовенної інфузії тривалістю від 30 до 60 хвилин. Дітям бажано вводити тайгециклін у виглядівнутрішньовенної інфузії тривалістю понад 60 хвилин. Приготовлений розчин потрібно використати негайно. Протипоказання. Гіперчутливість до діючої речовини чи до будь-якої з допоміжних речовин, вказаних у розділі «Склад». Пацієнти з гілерчутливістю до антибіотиків тетрациклінового ряду можуть мати гілерчутливість до тайгецикліну. Побічні реакції. Найчастішими побічними реакціями були нудота (21%) та блювання (13%), сепсис/септичний шок, пневмонія, абсцес, інфекції подовження активованого часткового тромбопластинового часу, подовження протромбінового часу, гіпоглікемія, гіпопротеїнемія, запаморочення, флебіт, діарея, біль у черевній порожнині, диспепсія, анорексія, підвищення рівня аспартатамінотрансферази (АсАТ) в сироватці крові, підвищення рівня аланінаміно-трансферази (АлАТ) в сироватці крові, гілербілірубінемія, свербіж, висипання, погіршення загоєння, peaкції у місці ін’єкції; головний біль, підвищення рівня амілази в сироватці крові, підвищення рівня азоту сечовини в крові. Особливості застосування. Пацієнтам з порушенням функції нирок та пацієнтам, які знаходяться на гемодіалізі, пацієнтам літнього віку, пацієнтам із легким чи помірним ураженням печінки корекція дози не потрібна. Перед початком та під час застосування тайгецикліну необхідно регулярно проводити функціональні печінкові проби, перевіряти параметри коагуляції, показники крові, рівні амілази та ліпази. Безпеку та ефективність застосування препарату Тигацил дітям віком до 8 років не було встановлено. Тигацил не слід застосовувати дітям до 8 років через зміну забарвлення зубів. Тайгециклін не слід застосовувати вагітним, окрім клінічних випадків, коли жінка потребує застосування тайгецикліну. Не можна виключити ризику для новонароджених/немовлят у людини. Необхідно прийняти рішення припинити годування груддю або припинити/перервати терапію тайгецикліном з огляду на користь грудного вигодовування для дитини та користь терапії для жінки. При застосуванні тайгецикліну може виникнути запаморочення, що може впливати на зщатність керувати автотранспортом та іншими механізмами. Взаємодія з іншими лікарськими засобами та інші види взаємодій. При одночасному застосуванні тайгециміну з антикоагулянтами слід ретельно контролювати результати досліджень коагуляції. Варфарин не впливав на фармакокінетичний профіль тайгецикліну. Тайгециклін in vitro не проявляє властивостей конкурентного інгібітopy або інгiбітopy необоротної дії щодо ензимів СУР 450. При одночасному застосуванні тайгецикліну з дигоксином потреби в коригуванні дози немає. При дослідженнях in vitro між тайгецикліном та антибіотиками інших масів, які часто застосовують у тepaпії антагонізму виявлено не було. Супутне застосування антибіотиків з пероральними протизаплідними засобами може знизити ефективність протизаплідних засобів. згідно з результатами дослідження in vitro, тайгециклін є субстратом Р-глікопротеїну. Комбіноване застосування з інгібіторами
Перед використанням препарату необхідно ознайомитись з повною інструкцією для застосування.
Інформація для лікарів та фармацевтів. Призначено для розповсюдження на семінарах, конференціях, симпозіумах з медичної тематики.
Реєстраційне посвідчення М03 України № UA/1234 7/01/01 від 04.07.2017 р., Наказ М03 України № 760 від 04.07.2017 р.
 За додатковою інформацією звертайтесь до:
За додатковою інформацією звертайтесь до:
Представництва «Пфайзер Експорт Бі. Ві.» в Україні: 03038, м. Київ, вул. Амосова, 12. Бізнес-центр «Горизонт парк», тел.: (044) 391-60-50.
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (49), 2019 р.