28 жовтня, 2020
Антитромботична терапія у пацієнтів із гострим коронарним синдромом, ускладненим кардіогенним шоком або позалікарняною зупинкою серця
Своєчасна ефективна антитромботична терапія має вирішальне значення для поліпшення клінічних наслідків в осіб із гострим коронарним синдромом (ГКС). Мінімізація вірогідності тромбозу та кровотеч у хворих на ГКС із дуже високим ризиком, особливо внаслідок кардіогенного шоку (КШ) або успішно реанімованих після зупинки серця у позалікарняних умовах (ЗСПУ), є вкрай важливою. Такі пацієнти мають 30‑50% ризик смерті або повторної ішемічної події протягом наступних 30 днів. Робоча група Європейського товариства кардіологів (ESC) з питань тромбозу спільно з Асоціацією спеціалістів із гострої серцево-судинної допомоги (ACCA) та Європейською асоціацією черезшкірних кардіоваскулярних втручань (EAPCI) 2020 року представили рекомендації з ведення пацієнтів із КШ або після ЗСПУ ймовірної ішемічної етіології. Також було висвітлено проблеми, пов’язані з ризиком розвитку тромбозу та кровотеч. Пропонуємо до вашої уваги огляд даної настанови.
Автори провели пошук публікацій у базах даних PubMed/MEDLINE, Ovid/Embase та Кокранівській бібліотеці до 1 вересня 2019 р. Систематичний огляд виявлених матеріалів, сучасні рекомендації, вплив перебігу хвороби й дисфункції органів, дані фармакокінетики та фармакодинаміки були використані для оцінки доказової бази антитромботичної терапії та формування консенсусу при прийнятті клінічних рішень.
Вплив індивідуальних характеристик пацієнта на фармакотерапію
Фармакокінетичні зміни щодо абсорбції, розподілу, метаболізму та екскреції препаратів, які трапляються в пацієнтів у тяжкому стані, можуть чинити суттєвий вплив на фармакотерапію. При КШ ефективність пероральних антитромботичних засобів знижується через відстрочення приймання, зменшення шлункового кровотоку й порушення моторики, затримання спорожнення шлунка та/або зниження абсорбції (Chapman et al., 2007). Також КШ може зменшити печінковий кровоток, збільшити застійні явища та, як наслідок, погіршити функцію печінки, знизивши швидкість біотрансформації ліків (Deitchman, Derendorf, 2014).
Таким чином, регулярний моніторинг антикоагулянтів за допомогою відповідних аналізів має особливе клінічне значення у пацієнтів із КШ, зокрема знизить ризик суб- чи супратерапевтичних доз.
Медикаментозне лікування
Ацетилсаліцилова кислота
Ацетилсаліцилова кислота (АСК) є препаратом першого вибору в пацієнтів із ГКС, включно із ЗСПУ або КШ (рис. 1) (Ibanez et al., 2018). АСК слід застосовувати якомога скоріше у навантажувальній дозі 150‑300 мг перорально чи внутрішньовенно (в/в). Дані обсерваційних досліджень показали, що пацієнти із КШ, які рідше отримували АСК, ніж такі без КШ, мали гірший прогноз (Krumholz et al., 1995; Dziewierz et al., 2010; Frilling et al., 2001). Серед хворих із КШ та ЗСПУ, яким провели первинне черезшкірне коронарне втручання (ЧКВ), частота раннього тромбозу стента в осіб із залишковою реактивністю тромбоцитів при стандартному дозуванні АСК становила 21,4% порівняно із 1,8% у тих, хто не мав підвищеної реактивності тромбоцитів (Tilemann et al., 2018).
Дані нещодавно проведеного рандомізованого дослідження показали, що разова доза АСК 250 або 500 мг в/в порівняно із 300 мг перорально забезпечує швидше й повніше пригнічення утворення тромбоксану та агрегації тромбоцитів без збільшення кровотечі (Zeymer et al., 2017). У настанові ESC рекомендоване в/в введення АСК у дозі 75‑250 мг, якщо пероральне приймання неможливе (Ibanez et al., 2018). Хоча докази обмежені та ґрунтуються лише на дослідженнях фармакокінетики чи фармакодинаміки, в/в АСК, імовірно, є кращим за пероральне використання, принаймні одразу після реанімації (Noc et al., 2014).
Тож робоча група дійшла висновку, що у пацієнтів із КШ або ЗСПУ в/в введення АСК у дозі 75‑250 мг є ефективним та може мати переваги перед пероральним застосуванням.
Інгібітори P2Y12-рецепторів
Відмінності у фармакології між пероральними інгібіторами P2Y12-рецепторів та єдиним доступним парентеральним інгібітором P2Y12 (кангрелором) можуть мати значення для пацієнтів у тяжкому стані. Зниження абсорбції є основним обмеженням призначення пероральних інгібіторів P2Y12-рецепторів при ГКС, особливо в осіб із ШК або ЗСПУ, в яких важливо забезпечити седативний ефект чи цільове регулювання температури (ЦРТ), при блюванні, гастропарезі або неможливості ковтання (Tantry et al., 2018). Клопідогрель асоційований із високою варіабельністю відповіді, включно з неадекватним інгібуванням активації тромбоцитів, індукованої АДФ, та відносно повільним початком дії, особливо у пацієнтів із КШ або ЦРТ (до 24 год) (Schoergenhofer et al., 2018).
До того ж середній рівень гальмування тромбоцитів значно нижчий у хворих при застосуванні клопідогрелю порівняно із прасугрелом або тікагрелором (Bednar et al., 2016). Введення суспензії подрібненого тікагрелору або прасугрелу через назогастральний зонд або застосування ородиспергованого тікагрелору може бути оптимальною стратегією подвійної антитромбоцитарної терапії (Qamar et al., 2018; Rollini et al., 2016; Parodi et al., 2015).
Тому за відсутності високого ризику кровотечі хворим із КШ чи ЦРТ доцільно призначати прасугрел або тікагрелор. Клопідогрель слід застосовувати лише при ГКС у пацієнтів із КШ та високим ризиком кровотечі (наприклад, із попередньою внутрішньочерепною, нещодавньою шлунково-кишковою кровотечею або тих, хто потребує лікування оральними антикоагулянтами).
Використання опіатів, таких як морфін та фентаніл, спричиняє затримання всмоктування клопідогрелю, прасугрелу та тікагрелору в кишечнику. Це відстрочує початок дії пероральних інгібіторів P2Y12-рецепторів та підвищує ризик розвитку ішемічних подій (Montalescot et al., 2014; Meine et al., 2005; Farag et al., 2018).
Варто розглянути можливість призначення парентеральних антикоагулянтів до початку застосування пероральних інгібіторів P2Y12-рецепторів. Кангрелор має переваги через нижчий ризик кровотечі, якщо під час ЧКВ немає порушення мікроциркуляції обструктивного ґенезу або потреби у невідкладному відкритому введенні засобу, коли може виникнути необхідність використання інгібітора рецепторів глікопротеїну IIb/IIIa (GPI).
Інгібітори рецепторів глікопротеїну IIb/IIIa
GPI, зокрема абциксимаб, ептифібатид та тирофібан, здатні зменшити тяжкі кардіальні побічні ефекти, як-то смерть, ГІМ та невідкладна реваскуляризація, особливо у хворих на ГКС із високим ризиком, які перенесли ЧКВ (Safley et al., 2015; Rubboli et al., 2018). У пацієнтів із ГКС, КШ або ЗСПУ, яким провели ЧКВ, GPI може покращити клінічні результати. GPI зазвичай застосовують в/в болюсно з подальшою інфузією, однак було зареєстровано 56 випадків аналогічної ефективності ліків при внутрішньокоронарному чи внутрішньосередковому болюсному введенні (Sun et al., 2017; Elbadawi et al., 2017).
GPI можна використовувати як міст для досягнення достатнього інгібування тромбоцитів за умови очікування початку лікування пероральним інгібітором P2Y12-рецепторів. Ці препарати є особливо прийнятними для пацієнтів у тяжкому стані, для яких важлива коротка тривалість лікування. Оскільки ефект різних GPI зіставний, їх можна використовувати взаємозамінно з урахуванням шляху елімінації та періоду напіввиведення. Однак слід зауважити, що застосування GPI пов’язане з підвищенням ризику кровотечі (Safley et al., 2015; Rubboli et al., 2018).
Гепарини та прямі інгібітори тромбіну
Застосування низькомолекулярного гепарину (НМГ) може бути менш ефективним в умовах КШ, особливо після ЧКВ, через високу частоту гострого ураження нирок та печінки у даній популяції хворих (van Diepen et al., 2017; Thiele et al., 2017).
Крім того, перехресне лікування НФГ та НМГ перешкоджає проведенню ЧКВ.
Нефракціонований гепарин (НФГ) є препаратом вибору для пацієнтів із КШ перед або під час ЧКВ, а також для продовження антикоагуляції після процедури. НФГ у дозі 70‑100 ОД/кг в/в болюсно показав користь як стандартний антикоагулянт при ЧКВ у пацієнтів із ГКС без підйому сегмента ST та в осіб з інфарктом міокарда (ІМ) з елевацією сегмента ST. Зменшення дози НФГ (50‑70 ОД/кг) слід розглядати у разі запланованого супутнього застосування GPI (Neumann et al., 2019). Дозування НФГ знижують за необхідності ЦРТ, і може знадобитися тривале переривання інфузії, щоб забезпечити адекватний кліренс препарату під контролем активованого часу згортання крові.
Використання еноксапарину можливе як альтернатива НФГ при ЧКВ, особливо у пацієнтів, які попередньо отримували еноксапарин підшкірно (Silvain et al., 2012).
Прямі інгібітори тромбіну в/в мають більш передбачуваний антикоагулянтний ефект порівняно з НФГ через відсутність зв’язування з білками плазми крові та можливої гепарин-індукованої тромбоцитопенії (Alban, 2008; Xiao, The’roux, 1998). Бівалірудин можна розглядати як альтернативу НФГ, особливо у пацієнтів із високим ризиком кровотечі, включно з КШ.
Антитромботичні стратегії відносно радіального та стегнового доступу ЧКВ
Згідно з метааналізом даних пацієнтів, які перенесли первинну ЧКВ, включно з тими, хто мав КШ, при трансрадіальному доступі (ТРД) зменшувалася кількість великих кровотеч на >50% та 30-денна смертність на 35‑50% порівняно із трансфеморальним доступом (Gandhi et al., 2015; Luca et al., 2013). В іншому метааналізі, який включав 27 491 хворого на ГКС, при ТРД частота кровотеч знижувалася переважно із застосуванням НФГ, тоді як при лікуванні бівалірудином – лише через стегновий доступ (Mina et al., 2016).
Тож робоча група підсумувала, що ТРД є тактикою вибору в осіб із ГКС, які перенесли ЧКВ із КШ або ЗСПУ, зокрема інтубованих та вентильованих пацієнтів. ТРД ефективно мінімізує кровотечі у даній когорті хворих.
Рання антитромботична терапія після ЧКВ у ВІТ
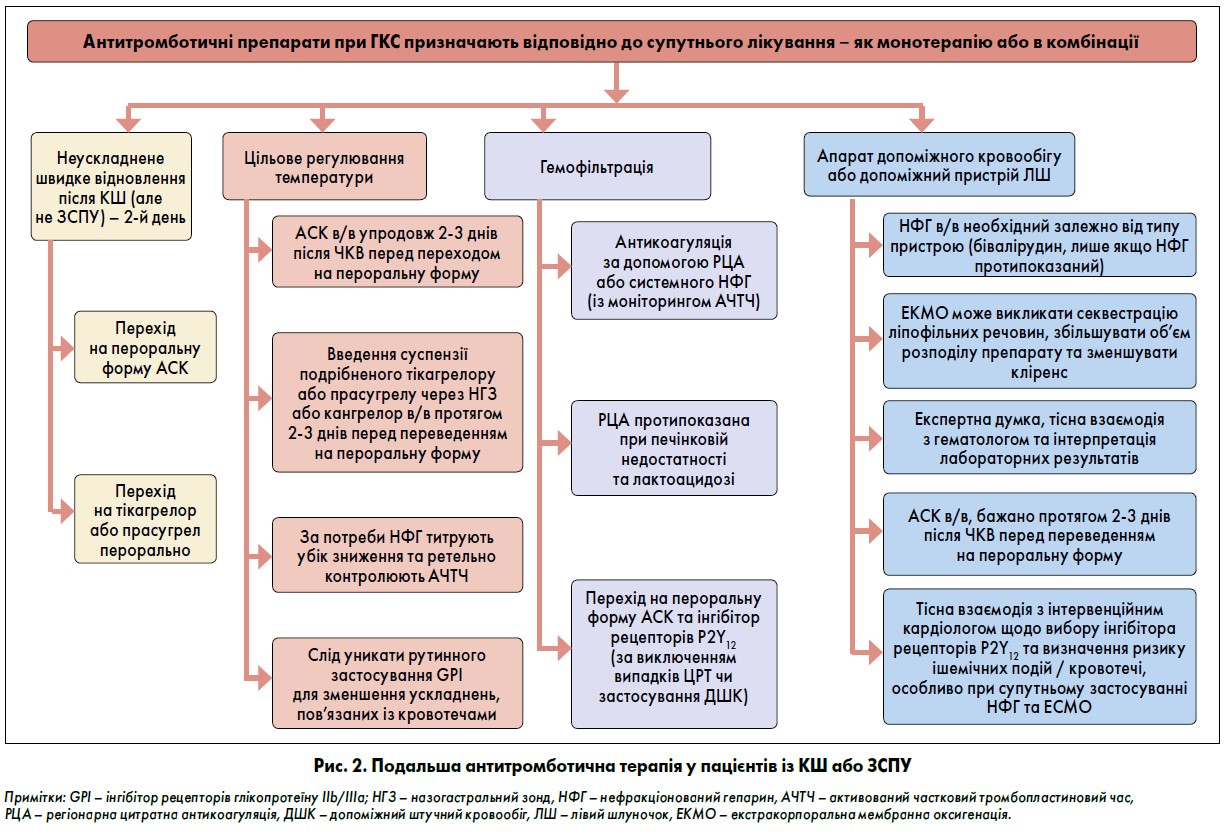
Цільове регулювання температури
У пацієнтів відділення інтенсивної терапії (ВІТ), які перенесли ЧКВ, ЦРТ може викликати легку дисфункцію тромбоцитів, хоча це не пов’язано з підвищеним ризиком кровотечі за відсутності ацидозу (Wolberg et al., 2004). У таких хворих АСК в/в може бути варіантом вибору протягом перших 2‑3 днів після ЧКВ до переходу на пероральну терапію.
У метааналізі п’ятьох рандомізованих та нерандомізованих досліджень із залученням 290 пацієнтів, яким виконували ЦРТ, приймання тікагрелору та прасугрелу не асоціювалося з нижчою частотою тромбозу стента або внутрішньолікарняної смертності порівняно із клопідогрелем (Elbadawi et al., 2018). Застосування подрібненого/ородиспергованого тікагрелору або подрібненого прасугрелу, що вводять у вигляді суспензії через назогастральний зонд, або кангрелору в/в можна розглянути у перші 2‑3 дні після ЧКВ, перш ніж перейти на пероральну антитромбоцитарну терапію.
При ЦРТ потреба у використанні НФГ різко зменшується. За необхідності застосування НФГ слід титрувати у бік зменшення під ретельним контролем, щоб підтримувати активований частковий тромбопластиновий час (АЧТЧ) у межах терапевтичного діапазону (рис. 2) (Wahby et al., 2014; Fevold et al., 2015). Також слід уникати рутинного використання GPI при ЦРТ, щоб зменшити ускладнення, пов’язані з кровотечами (Jimenez-Britez et al., 2016).
Гемофільтрація
Безперервна вено-венозна гемофільтрація зазвичай використовується як замісна ниркова терапія в пацієнтів у критичному стані (рис. 2). Вплив останньої на ефективність антитромботичних препаратів значно варіює та здебільшого непередбачуваний, оскільки фармакокінетичні дані часто відсутні, та може залежати від режиму й тривалості лікування, дозування, площі поверхні, швидкості потоку крові тощо (Roberts et al., 2018; Awdishu, Bouchard, 2011). Регіонарна цитратна антикоагуляція (у разі доступності) та системне застосування НФГ (із моніторингом АЧТЧ) є оптимальною стратегією у пацієнтів, які перенесли безперервну вено-венозну гемофільтрацію (Wu et al., 2012). Хворим на гостру печінкову недостатність та лактоацидоз регіонарна цитратна антикоагуляція протипоказана.
Антитромботична терапія у тяжких хворих на допоміжних апаратах кровообігу або ЛШ
Пацієнтам із КШ та/або ЗСПУ може знадобитися механічна підтримка кровообігу. Залежно від типу допоміжного апарату часто необхідне проведення антикоагуляції. Це допоможе уникнути кровотеч та ішемічних ускладнень, що нерідко виникають одночасно. За тяжких клінічних умов антикоагуляція зазвичай досягається в/в введенням НФГ (Rossi et al., 2012). Бівалірудин слід розглядати лише тоді, коли НФГ протипоказаний. Ефективність антикоагуляції можна контролювати за допомогою різних тестувань, які включають оцінку АЧТЧ, активованого часу згортання крові, рівня антифактора згортання та тромбоеластографію (Lequier et al., 2014; Winkler, 2017; Koster et al., 2019).
Вплив екстракорпоральної мембранної оксигенації на ефективність та безпеку антитромботичних препаратів до кінця не ясний. Пацієнти із ГКС і терміновим ЧКВ повинні отримувати подвійну антитромбоцитарну терапію, що включає АСК та інгібітор рецептора P2Y12 (зазвичай клопідогрель). Застосування кангрелору може бути розглянуте в даних клінічних умовах через швидку нейтралізацію ефекту попереднього лікування у разі виникнення кровотечі. Загалом екстракорпоральна мембранна оксигенація може зумовити секвестрацію ліпофільних речовин, збільшити об’єм розподілу препарату в організмі та зменшити кліренс.
Тож у даної категорії хворих важливим є комплексний підхід, а саме експертна думка, тісна взаємодія з гематологом та інтервенційним кардіологом, а також інтерпретація лабораторних результатів відповідно до клінічної ситуації.
Пацієнти із фібриляцією передсердь
Фібриляція передсердь (ФП) спостерігається приблизно у 20% пацієнтів із ГКС, ускладненим КШ, порівняно з лише 9% хворих на неускладнений ГКС. В осіб із КШ та ГКС, які на момент госпіталізації мали ФП, летальність вища порівняно з тими, у кого ФП було встановлено вперше (Feistritzer et al., 2019; Kalarus et al., 2019). Пацієнтам із раніше виявленою або вперше діагностованою ФП рекомендована потрійна антитромботична терапія, що включає АСК, клопідогрель та антикоагулянт, як початкова стратегія впродовж першого місяця в осіб із ФП та без значного ризику кровотечі (Ibanez et al., 2018; Boriani et al., 2019).
Пацієнтам із ГКС та КШ, які перенесли первинне ЧКВ та отримують антитромбоцитарну терапію, слід призначити додаткові парентеральні антикоагулянти у низьких дозах незалежно від часу приймання останньої дози пероральної форми препаратів. У хворих ВІТ, що є гемодинамічно нестабільними після первинного ЧКВ, найбільш доцільне застосування НФГ. Пацієнти із ГКС, КШ та наявною ФП, які лікуються пероральними антикоагулянтами, мають отримувати стандартну навантажувальну дозу АСК (як і особи без ФП), а клопідогрель (навантажувальна доза – 600 мг) є препаратом вибору з-поміж інгібіторів рецепторів P2Y12 (Ibanez et al., 2018; Roffi et al., 2016; Lip et al., 2019).
Висновки
Пацієнти із ГКС, що перенесли КШ або ЗСПУ імовірного ішемічного ґенезу, становлять групу дуже високого ризику, в яких мінімізація вірогідності тромбозу є критично важливою для поліпшення клінічних наслідків. На ефективність та безпеку антитромботичних препаратів можуть здійснювати значний вплив різні чинники, як-то порушення всмоктування, метаболізму, зміна розподілу та/або виведення, пов’язана з ними поліорганна недостатність, супутнє лікування тощо. Ретельний підбір антитромботичних засобів, мінімізація взаємодії ліків, а також моніторинг факторів, що впливають на їхню ефективність і безпеку, можуть знизити ризик суб- чи супратерапевтичних доз та асоційованих із цим несприятливих явищ.
Потрібні додаткові дослідження з оцінки ефективності антитромботичних препаратів у хворих із КШ або ЗСПУ, їхньої фармакокінетики й фармакодинаміки для досягнення ефективного інгібування тромбоцитів та антикоагуляції з мінімальним ризиком, що є особливо важливим у популяції пацієнтів із ГКС групи високого ризику.
Довідка «ЗУ»
На українському ринку представлено вітчизняний препарат ацетилсаліцилової кислоти Магнікор виробництва АТ «Київський вітамінний завод». Цей лікарський засіб відповідає світовим стандартам ефективності та безпеки. Крім того, Магнікор доступний у зручному дозуванні (75, 150 мг) для навантажувальної та підтримувальної терапії.
Ще один препарат АТ «КВЗ», що пройшов перевірку часом і заслужив довіру українських пацієнтів і лікарів, – Атерокард (клопідогрель, 75 мг).
Обидва препарати мають приємне для пацієнта співвідношення ціна/якість, що суттєво підвищує прихильність до лікування.
Підготувала Олена Коробка
Оригінальний текст документа читайте на сайті www.academic.oup.com
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (71) 2020 р.