23 лютого, 2021
Первинна та вторинна профілактика ішемічного інсульту і внутрішньомозкових крововиливів
Інсульт суттєво впливає на якість життя пацієнтів, є значним тягарем для них та основною причиною втрати працездатності. Тому первинна профілактика (першого інсульту) та вторинна профілактика (повторної події) є вкрай важливими. Є дві ключові стратегії зменшення глобального тягаря інсульту: ефективне лікування пацієнтів із гострим інсультом для мінімізації інвалідності та смертності, а також запобігання розвитку першого й повторного епізодів. В огляді H.‑C. Diener і G.J. Hankey розглянуті основні кроки первинної та вторинної профілактики ішемічного інсульту і внутрішньомозкових крововиливів (ВМК). У пацієнтів із високою ймовірністю першого та повторного інсульту також спостерігається ризик розвитку серцево-судинних (СС) подій і кардіальної смерті. Тому рекомендації також включають терапевтичні заходи для запобігання інфаркту міокарда (ІМ) і лікування захворювань периферичних артерій (ЗПА). Пропонуємо до вашої уваги ключові положення даного матеріалу, опублікованого у виданні Journal of the American College of Cardiology (2020; 75 (15): 1804‑1818).
Первинна профілактика ішемічного інсульту включає модифікацію способу життя та режиму харчування, контроль факторів ризику, зокрема артеріальної гіпертензії (АГ), цукрового діабету (ЦД) і порушення ліпідного обміну, антитромбоцитарну терапію для пацієнтів із високим СС-ризиком та антикоагулянтну – при фібриляції передсердь (ФП). Вторинна профілактика ішемічного інсульту передбачає проведення додаткової операції на сонній артерії або стентування в окремих симптомних пацієнтів, закриття відкритого овального вікна (ВОВ) після криптогенного інсульту, лікування інсулінорезистентності та внутрішньочерепного стенозу. Найважливіші стратегії первинної та вторинної профілактики внутрішньомозкових крововиливів (ВМК) включають терапію АГ, зменшення споживання алкоголю й оклюзію вушка лівого передсердя у пацієнтів із ФП та протипоказаннями для застосування оральних антикоагулянтів (ОАК).
Основні підходи для запобігання розвитку інсульту:
1. Підхід «високого ризику», спрямований на зменшення поширеності та факторів ризику серед осіб із високою ймовірністю виникнення інсульту.
2. «Популяційний» підхід, спрямований на зменшення поширеності факторів ризику у загальній популяції.
Першу стратегію зазвичай реалізують клініцисти та медсестри, другу – уряди чи організації охорони здоров’я.
Первинна профілактика ішемічного інсульту
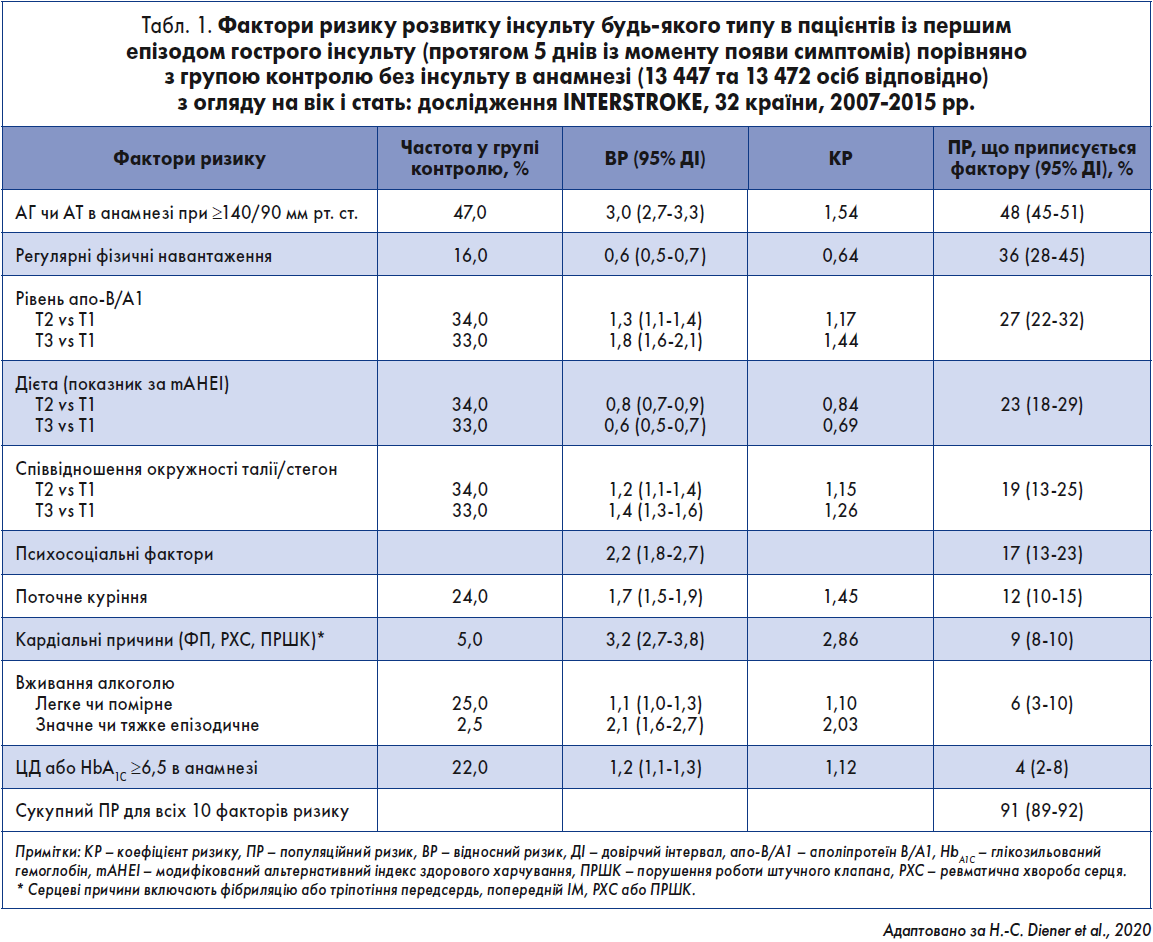
Дослідження типу «випадок/контроль» показали, що серед 10 факторів СС-ризику та супутніх захворювань ризик інсульту становить 90% (табл. 1) (O’Donnell et al., 2016).
Модифікація способу життя
У межах первинної профілактики інсульту рекомендовано корекцію способу життя, зокрема запровадження нормального режиму харчування, зниження ваги, припинення куріння та регулярну фізичну активність (Dehghan et al., 2012; Duncan et al., 2019; Willey et al., 2009). Був проведений систематичний огляд даних рандомізованих контрольованих досліджень (РКД) із застосуванням різних варіантів модифікації дієти та їхнього впливу на ризик інсульту. За отриманими даними, використання харчових добавок із фолієвою кислотою пов’язане з меншою ймовірністю розвитку інсульту порівняно з контролем (7 РКД, n=24 525, 694 події). Комплекс вітамінів групи В та середземноморська дієта асоціювалися з тенденцією до зниження ризику інсульту порівняно з контролем (12 РКД, n=43 339, 2064 події та 3 РКД, n=9052, 167 подій відповідно), а комбінація кальцію і вітаміну D – із підвищенням імовірності інсульту (7 РКД, n=19 227, 484 події). Крім того, зменшення споживання солі корелювало зі зниженням ризику смертності через серцево-судинні захворювання (ССЗ) в осіб з АГ (3 РКД, n=2656, 106 летальних випадків), а також від усіх причин у пацієнтів із нормальним артеріальним тиском (АТ) (3 РКД, n=3518, 79 летальних випадків) (Khan et al., 2019).
Лікування АГ
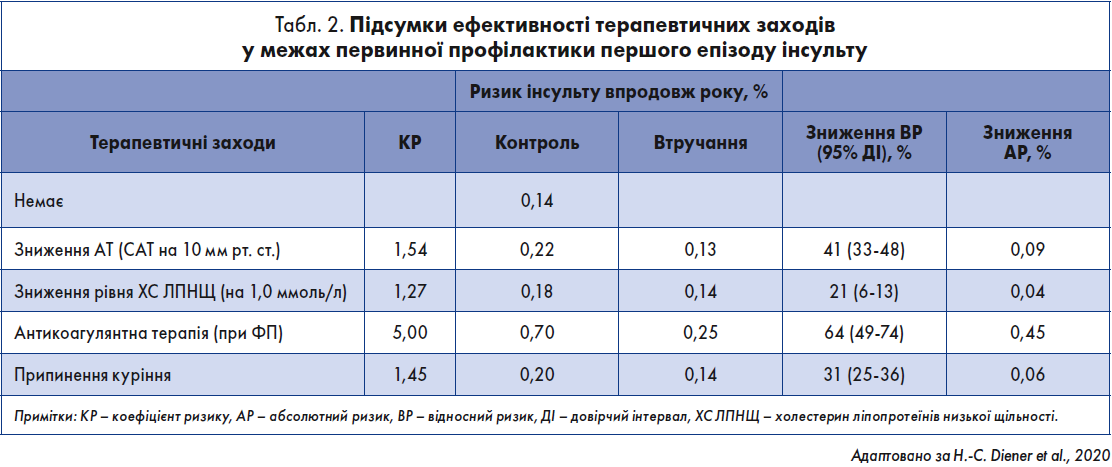
Зниження АТ в осіб з АГ є пріоритетним завданням для запобігання розвитку ішемічного інсульту. Кожне зниження систолічного АТ (САТ) на 10 мм рт. ст. та діастолічного АТ (ДАТ) на 5 мм рт. ст. зменшує імовірність інсульту на 41% (табл. 2) (Law et al., 2009). САТ потрібно обережно знижувати до <140/90 мм рт. ст. у пацієнтів без ЦД та <130/80 мм рт. ст. у діабетиків (Mendis et al., 2005; Williams et al., 2018). Більшість класів антигіпертензивних препаратів показали користь у зниженні ризику інсульту, за винятком α-адреноблокаторів (ALLHAT Collaborative Research Group, 2000).
Контроль гіперглікемії
Інтенсивне лікування гіперглікемії у хворих на ЦД знижує ризик мікросудинних ускладнень, але не інсульту (Skyler et al., 2009; Reaven et al., 2019). У 13 РКД, в яких взяли участь 58 160 пацієнтів із ЦД 2-го типу, інтенсивна терапія з метою зниження рівня глюкози не чинила значного впливу на частоту розвитку інсульту порівняно зі стандартним лікуванням (Fang et al., 2016). Інгібітори натрійзалежного котранспортера глюкози 2-го типу знижували ризик серйозних СС-подій, включно з інсультом, порівняно із плацебо, проте основний ефект стосувався частоти та прогресування серцевої недостатності (Acharya, Deedwania, 2019).
Порушення ліпідного обміну
Статини ефективніші для первинної профілактики гострого коронарного синдрому та ІМ, аніж ішемічного інсульту. За даними систематичного огляду та мережевого метааналізу РКД із включенням статинів для первинної профілактики ССЗ (n=94 283), застосування статинів як класу корелювало зі статистично значущим зниженням ризику нефатального ІМ, смертності від ССЗ та нефатального інсульту. Абсолютна користь статинотерапії залежить від індивідуального ризику оклюзій та потенційного досягнення зниження рівня холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ). При кожному зменшенні концентрації ХС ЛПНЩ на 1 ммоль/л у разі застосування статинів імовірність первинного інсульту знижується приблизно на 21%. У межах 39 випробувань, присвячених первинній та вторинній профілактиці ВМК (n=287 651), зниження рівня ліпідів не асоціювалося зі статистично значущим підвищенням ризику ВМК (Judge et al., 2019).
Серед статинів аторвастатин та розувастатин є найефективнішими препаратами для зниження частоти СС-подій (Yebyo et al., 2019). Лікування статинами сприяє значному зменшенню основних СС-ускладнень незалежно від віку, проте доступно менше доказів їхньої користі в осіб віком >75 років, які не мають очевидних ознак ССЗ (Cholesterol Treatment Trialists Collaboration, 2019). За результатами нещодавнього метааналізу 20 РКД, в яких вивчали додавання інгібіторів пропротеїн конвертази субтилін/кексин типу 9 (PCSK9) до статинів порівняно із плацебо (32 329 та 28 549 хворих відповідно), повідомлялося про зниження імовірності інсульту на 23% при застосуванні інгібіторів PCSK9 (Casula et al., 2019).
Нестатинова терапія, що включає дієту, використання секвестрантів жовчних кислот, обхідного шунтування та езетимібу, діє переважно шляхом підвищення експресії рецепторів ЛПНЩ для зниження рівня ХС ЛПНЩ. Вона пов’язана з подібними до статинотерапії основними СС-подіями при зміні вмісту ХС ЛПНЩ (Mach et al., 2020).
Антитромботична терапія
За даними 10 РКД, застосування ацетилсаліцилової кислоти (АСК) в осіб, які не страждають на ССЗ, асоційоване з нижчим ризиком ішемічного інсульту порівняно з контролем (1,27 та 1,48% відповідно). У 12 РКД спостерігався зіставний підвищений ризик внутрішньочерепних кровотеч при лікуванні АСК порівняно з контролем (0,43 та 0,32% відповідно). Крім того, використання АСК у хворих без ССЗ корелює з меншою ймовірністю комбінованої кінцевої точки, як-от інсульт, ІМ та смертність від ССЗ (60,2% порівняно з 65,2% у групі контролю на 10 тис. пацієнто-років), але з подібним підвищеним ризиком великих кровотеч (23,1% порівняно з 16,4% у групі контролю на 10 тис. пацієнто-років) (Zheng, Roddick, 2019).
ФП є основним фактором ризику розвитку ішемічного інсульту. Застосування ОАК зменшує імовірність інсульту на 60‑80% порівняно з відсутністю лікування. У метааналізі даних 4 РКД, в яких 42 411 осіб із ФП отримували прямий оральний антикоагулянт (ПОАК), а 29272 – варфарин, ПОАК значно знизили ризик інсульту або системної емболії на 19% порівняно з варфарином (3,1 та 3,8% відповідно) та геморагічного інсульту – на 50% (0,44 та 0,90% відповідно) (Ruff et al., 2014).
Додаткові переваги ПОАК полягають у тому, що за їхнього приймання не потрібен регулярний контроль антикоагуляційної активності, до того ж вони не взаємодіють з їжею. Серед обмежень використання цих препаратів слід відзначити те, що вони не схвалені для лікування осіб із прогресивною нирковою недостатністю (кліренс креатиніну <15 мл/хв) або пацієнтів на діалізі. АСК та комбінація АСК/клопідогрелю мають обмежену користь у профілактиці інсульту при ФП, тому їх слід призначати лише хворим, які відмовляються від антикоагулянтної терапії. Варто зауважити, що комбінація АСК + клопідогрель ефективніша за монотерапію АСК, однак користь нівелюється підвищеним ризиком кровотечі (Connolly et al., 2009; Steffel et al., 2018).
Безсимптомний каротидний стеноз
Пацієнти з безсимптомним стенозом сонної артерії мають дуже низький ризик розвитку інсульту (<0,5% на рік) при поточному лікуванні (Marquardt et al., 2010). Рандомізовані дослідження, в яких порівнювали каротидну ендартеректомію (КЕА) та фармакотерапію, проводили тоді, коли оптимальне лікування, зокрема статинами, було недоступне (Raman et al., 2013). Ефективне медикаментозне лікування, найімовірніше, має такі самі переваги, як КЕА або стентування (Reiff et al., 2019; Gaba et al., 2018). У дослідженні Mackey et al. (1997) вивчали пацієнтів із безсимптомним стенозом сонної артерії, рандомізованих на групи АСК у дозі 325 мг щодня (n=188) та плацебо (n=184). Після спостереження, яке в середньому тривало 2,3 року, суттєвих відмінностей у річній частоті ішемічних ускладнень, як-от транзиторна ішемічна атака (ТІА), ішемічний інсульт, нестабільна стенокардія, ІМ та смерть із будь-якої причини, між двома групами лікування не виявлено (11,0 та 12,3% відповідно). Тому лишається незрозумілим, чи може АСК запобігати розвитку СС-подій в осіб із безсимптомним каротидним стенозом (Murphy et al., 2019).
У дослідженні COMPASS порівнювали застосування ривароксабану в низьких дозах (2×2,5 мг/добу) плюс АСК (100 мг/добу), монотерапію ривароксабаном (1×5 мг/добу) або АСК (1×100 мг/добу) у пацієнтів зі стабільною ішемічною хворобою серця (ІХС) та ЗПА (Eikelboom et al., 2017). У хворих із безсимптомним стенозом сонної артерії мала місце тенденція до ліпшої користі комбінованого лікування порівняно з монотерапією (Anand et al., 2017). У країнах із низьким рівнем доходів, де доступність лікування може бути обмеженою, використання поліпілу, що містить АСК, аторвастатин, гідрохлоротіазид та еналаприл/валсартан, може запобігти розвитку інсульту в осіб із високим ризиком.
Первинна профілактика ВМК
Основними факторами ризику ВМК є вік, АГ, приймання антитромботичних препаратів і тяжке ураження дрібних судин, включно з амілоїдною ангіопатією. Серед чинників ризику модифікованими є лише високий АТ та застосування антитромботичних засобів. У дослідженні PROGRESS (2003) лікування периндодоприлом та індапамідом зменшувало імовірність першого та повторного ВМК. Між зниженням АТ та ризику ВМК спостерігалася майже лінійна залежність. Як показало випробування SPS3, зниження САТ <130 мм рт. ст. у пацієнтів із захворюванням дрібних судин зменшувало ймовірність ВМК (Benavente et al., 2013). Збільшення споживання алкоголю та куріння є факторами ризику розвитку ВМК, тож їх слід уникати.
Як було зазначено вище, АСК має обмежену ефективність у первинній профілактиці інсульту та корелює з підвищеним ризиком ВМК і великих кровотеч. ПОАК мають переваги перед антагоністами вітаміну К (АВК) для запобігання розвитку інсульту в пацієнтів із ФП завдяки тому, що знижують ризик ВМК порівняно з останніми на 50‑80% (Ruff et al., 2014; Kirchhof et al., 2016). Під час дослідження AVERROES у хворих на ФП, в яких не було показань для використання варфарину, апіксабан асоціювався із ризиком ВМК, зіставним із таким для АСК, але був ефективнішим у межах профілактики ішемічного інсульту (Connolly et al., 2011).
Таким чином, лікування АГ є основною терапевтичною стратегією для зниження ризику ВМК. АСК не слід застосовувати для первинної профілактики СС-подій. Для пацієнтів із ФП, які потребують профілактики тромбоутворень, ПОАК є кращими препаратами вибору порівняно з АВК. Гіполіпідемічні засоби не пов’язані з підвищеним ризиком розвитку ВМК у межах первинної профілактики.
Вторинна профілактика після ТІА та ішемічного інсульту
Після перенесеного ішемічного інсульту або ТІА ймовірність повторної події без лікування становить близько 10% через тиждень, 15% через місяць та 18% через три місяці (Coull et al., 2004). Довгостроковий ризик повторного інсульту становить орієнтовно 10, 25 і 40% через 1, 5 та 10 років відповідно (Mohan et al., 2011). Негайне обстеження пацієнтів з інсультом або ТІА є дуже важливим, а своєчасно розпочате лікування у межах вторинної профілактики залежно від основної причини зменшує ймовірність повторного інсульту до 80% (Rothwell et al., 2007; Amarenco et al., 2018).
Підсумки ефективності лікувальних заходів під час вторинної профілактики повторного епізоду інсульту наведені в таблиці 3.
Антигіпертензивна терапія
Антигіпертензивне лікування знижує ризик повторного інсульту приблизно на чверть (Xie et al., 2016). Зниження АТ зумовлює зменшення імовірності виникнення повторного інсульту. Стійке зниження САТ та ДАТ на 5,1 і 2,5 мм рт. ст. відповідно зменшує імовірність повторного інсульту приблизно на 1/7, 10 і 5 мм рт. ст. – на 1/3 відповідно (Law et al., 2009). Нещодавній метааналіз даних чотирьох досліджень, включно із RESPECT (n=4895), показав переваги інтенсивного зниження АТ (<130/80 мм рт. ст.) у межах вторинної профілактики інсульту, при цьому абсолютний ризик зменшився на 1,5% (Kitagawa et al., 2019). Ефект зниження АТ для вторинної профілактики інсульту є стійким незалежно від попередньої АГ та більшості підтипів інсульту. Оптимальний цільовий рівень АТ після лакунарного інсульту ще не визначений, але може становити для САТ 120‑128 мм рт. ст., а для ДАТ 65‑70 мм рт. ст. (Odden et al., 2016).
Антигіпертензивні препарати, найімовірніше, ефективні у межах вторинної профілактики інсульту (Rashid et al., 2003; Katsanos et al., 2017). Для β-блокатора атенололу продемонстровано найнижчу користь через підвищену варіабельність АТ між візитами до лікаря. Важливим є досягнення цільового рівня АТ: <140/90 мм рт. ст. у пацієнтів без ЦД та <130/80 мм рт. ст. у діабетиків. Із цією метою значна частка хворих потребує призначення комбінованої терапії. Також слід враховувати можливі супутні захворювання, такі як ниркова недостатність та застійна серцева недостатність. На додаток до медикаментозного лікування рекомендовано модифікацію способу життя для зниження АТ.
Порушення ліпідного обміну
Кореляція між рівнем ХС та ризиком повторного ішемічного інсульту є не такою потужною, як із ризиком ІМ. У дослідженні Heart Protection Study серед 20 536 пацієнтів із високим ризиком 3280 мали ТІА або інсульт в анамнезі. Лікування симвастатином у дозі 40 мг протягом п’яти років асоціювалося зі зниженням частоти СС-подій на 20% та абсолютного ризику на 5,1% порівняно із плацебо (Heart Protection Study Collaborative Group, 2002).
У випробуванні SPARCL (2006) 4731 хворого із попередньою ТІА (31%) або інсультом (ішемічний – 67%, геморагічний – 2%) та рівнем ХС ЛПНЩ 2,59-4,9 ммоль/л рандомізували для приймання 80 мг аторвастатину чи плацебо. Середній період спостереження становив 4,9 року. Аторвастатин зменшував імовірність повторного інсульту на 16% порівняно із плацебо, зокрема ішемічного, але підвищував ризик геморагічного інсульту.
За метааналізом результатів досліджень, застосування ліпідознижувальних стратегій терапії не асоціювалося зі статистично значущим підвищенням ризику ВМК у межах первинної та вторинної профілактики (Ziff et al., 2019).
Тож зменшення концентрації ХС ЛПНЩ приблизно на 1 ммоль/л при застосуванні статинів знижує ризик повторного інсульту щонайменше на 12% (Amarenco, Labreuche, 2009). Інтенсивніше зменшення вмісту ХС ЛПНЩ пов’язане з подальшим зниженням ризику інсульту (Collins et al., 2016). У випробуванні Treat Stroke to Target було показано, що серед 2860 пацієнтів із нещодавно перенесеним ішемічним інсультом або ТІА та середнім вихідним ХС ЛПНЩ 3,5 ммоль/л, у котрих випадковий розподіл за цільовим рівнем ХС ЛПНЩ становив 1,8 ммоль/л, мав місце нижчий ризик СС-подій, ніж при показнику 2,3‑2,8 ммоль/л через 3,5 роки спостереження (Amarenco et al., 2020).
Отримані результати узгоджуються з настановою Європейського товариства кардіологів та Європейського товариства атеросклерозу (ESC/EAS, 2019), в якій рекомендований цільовий показник ХС ЛПНЩ становить 1,4 ммоль/л для пацієнтів групи високого СС-ризику. Зокрема, у документі зазначено, що в межах вторинної профілактики у хворих із дуже високим ризиком слід досягти зниження концентрації ХС ЛПНЩ на ≥50% від вихідного рівня та ХС ЛПНЩ <1,4 ммоль/л. Для осіб з атеросклеротичними ССЗ, в яких друга СС-подія розвинулася протягом двох років під час максимально переносимої терапії статинами, цільовий рівень ХС ЛПНЩ є <1,0 ммоль/л (Mach et al., 2020).
За доступними даними випробувань, інгібітори PCSK9 використовують для лікування гіперхолестеринемії у пацієнтів із поганою відповіддю на статинотерапію або її непереносимістю. Кількість осіб з інсультом, включених до цих досліджень, і частка повторних інсультів були невеликими. Отже, можливу користь інгібіторів PCSK9 для запобігання розвитку вторинного інсульту остаточно не підтверджено (Climent et al., 2020).
Таким чином, пацієнти з ТІА або ішемічним інсультом та ІХС потребують призначення статинотерапії. Ця рекомендація не залежить від вихідного рівня ХС ЛПНЩ. В осіб з ішемічним інсультом або ТІА внаслідок атеросклерозу без ІХС та вмістом ХС ЛПНЩ 2,59-4,91 ммоль/л слід застосовувати аторвастатин у дозі 80 мг.
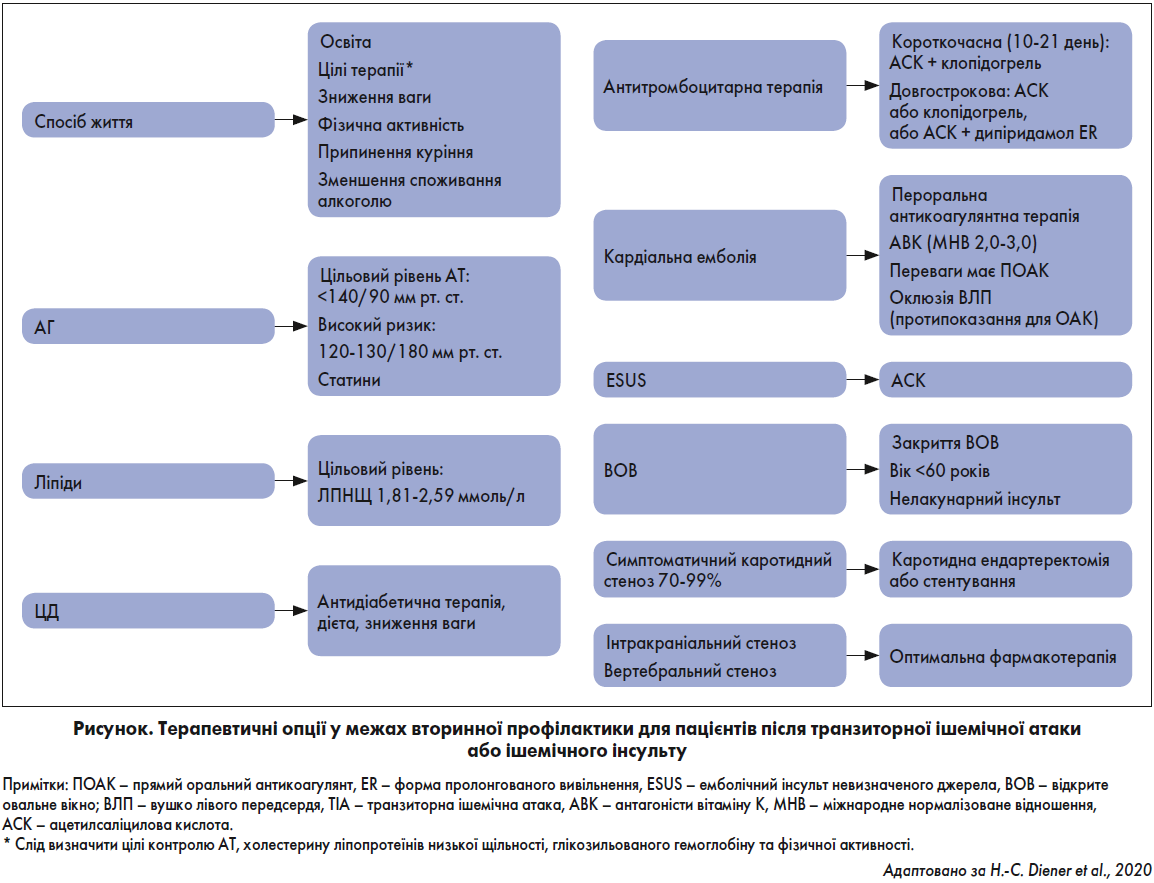
Терапевтичні опції у межах вторинної профілактики для пацієнтів після ТІА та ішемічного інсульту представлені на рисунку.
Пацієнти із ЦД
Інтенсивне зниження рівня глюкози крові у хворих на ЦД не зменшує імовірності виникнення інсульту та збільшує смертність (Ray et al., 2009). Метааналіз даних трьох РКД (загалом 4980 пацієнтів з інсультом, інсулінорезистентністю, предіабетом та ЦД) показав, що терапія піоглітазоном асоціювалася з нижчим ризиком повторного інсульту й серйозних СС-подій (Lee et al., 2017). Інгібітори натрійзалежного котранспортера глюкози 2-го типу зменшували ризик смерті через серцеву недостатність, але не повторного інсульту (Zinman et al., 2017).
Також був проведений метааналіз даних чотирьох випробувань із залученням 33 457 осіб із ЦД та високим ризиком СС-подій, які отримували агоніст рецепторів глюкагоноподібного пептиду‑1 (арГПП‑1), наприклад ліраглутид. Згідно з результатами, лікування арГПП‑1 порівняно із плацебо показало тенденцію до зниження ризику інсульту (Bethel et al., 2018). Основною метою терапії ЦД на сьогодні лишається контроль ваги за допомогою належного режиму харчування та регулярної фізичної активності (за потреби, операцій на шлунку).
Антитромбоцитарна терапія
У пацієнтів із ТІА та ішемічним інсультом ризик повторної події найвищий у гострій фазі (Coull et al., 2004; Mohan et al., 2011). Предикторами раннього рецидиву інсульту є атеросклероз великих артерій, коротший час від початку інсульту, показник 6‑7 балів за шкалою ABCD2 (A – вік [Age], B – АТ [Blood pressure], C – клінічні ознаки [Clinical features], D – тривалість симптомів [Duration of symptoms], D – ЦД в анамнезі [History of Diabetes]), яка слугує для визначення раннього ризику інсульту протягом перших 2, 7 та 90 днів після ТІА, а також множинні вогнища інфаркту при візуалізації головного мозку.
За даними об’єднаного аналізу результатів 12 випробувань із залученням 15 778 учасників, у яких вивчали АСК порівняно з контролем у межах вторинної профілактики інсульту, терапія АСК знижувала ризик раннього повторного ішемічного інсульту через шість тижнів приблизно на 60% та інвалідизувального або летального – на 70% (Antithrombotic Trialists’ Collaboration, 2002). S.C. Johnston et al. (2016) не підтвердили, що тікагрелор перевершував АСК за ефективністю зниження частоти несприятливих наслідків первинного інсульту, ІМ або смерті через 90 днів у 13 199 пацієнтів із нетяжким ішемічним інсультом або ТІА високого ризику, незважаючи на зменшення частоти основної вторинної кінцевої точки – повторного ішемічного інсульту.
Метааналіз трьох РКД включав 10 447 пацієнтів із гострою некардіоемболічною ТІА або малим ішемічним інсультом, визначеними як ≤3 бали за шкалою інсульту Національного інституту охорони здоров’я (NIHSS). Було виявлено, що при додаванні клопідогрелю до АСК (подвійна антитромбоцитарна терапія) протягом 24 год від появи симптомів ризик нефатального повторного інсульту через 90 днів знижувався на 30% порівняно з терапією лише АСК (Kennedy et al., 2007; Wang et al., 2013; Johnston et al., 2018). При монотерапії АСК мало місце ймовірне збільшення середньої або великої екстракраніальної кровотечі. Більшість випадків інсульту і майже всі переваги подвійної антитромбоцитарної терапії спостерігалися протягом 10‑21 дня після рандомізації; після цього незначний кумулятивний ризик кровотечі нівелював користь такого лікування (Prasad et al., 2018).
У довгостроковій перспективі антитромбоцитарна терапія переважно АСК знижує ризик інсульту приблизно на 19% упродовж трьох років, а комбінованої кінцевої точки (інсульт, ІМ та СС-смерть) – орієнтовно на 13% (Antithrombotic Trialists’ Collaboration, 2002). Ефективність АСК при вторинній профілактиці інсульту не залежить від дози в діапазоні 30‑1600 мг/добу (Algra, van Gijn, 1999; Patrono et al., 2005). Тому рекомендована підтримувальна доза препарату (після навантажувальної 300 мг) становить 75-100 мг/добу.
Окрім того, дослідники порівнювали монотерапію клопідогрелем (75 мг/добу) та АСК (325 мг/добу) у 19 185 пацієнтів з інсультом, ІМ або ЗПА. При застосуванні клопідогрелю спостерігалося ефективніше зниження відносного ризику комбінованої первинної кінцевої точки – інсульту, ІМ та СС-смерті – на 8,7%. У підгрупі осіб із попередньою ТІА або ішемічним інсультом зниження цього показника при лікуванні клопідогрелем порівняно з АСК становило 7,3%. Комбінація 75 мг клопідогрелю та 75 мг АСК не була дієвішою за монотерапію клопідогрелем у профілактиці інсульту чи інших основних СС-подій серед хворих на ТІА або ішемічний інсульт із високим ризиком, до того ж асоціювалася зі збільшенням кровотечі (Diener et al., 2004).
Поєднання клопідогрелю та АСК також не було ефективнішим за монотерапію АСК у профілактиці інсульту та інших основних СС-подій серед 15 603 пацієнтів із високим СС-ризиком або 3020 осіб із нещодавно перенесеним лакунарним інсультом. При цьому частота кровотеч при комбінованому лікуванні порівняно з монотерапією АСК зростала (Bhatt et al., 2007; Benavente et al., 2012).
У метааналізі даних шести РКД (загалом 7795 пацієнтів із ішемічним інсультом або ТІА) порівнювали поєднання низьких доз АСК та дипіридамолу з монотерапією АСК. Було показано, що комбінована терапія зменшувала ймовірність основних СС-подій приблизно на 18% (Greving et al., 2019).
У прямому порівняльному дослідженні монотерапії клопідогрелем та комбінації АСК + дипіридамол пролонгованого вивільнення (ER) у 20 332 пацієнтів з ішемічним інсультом (середній період спостереження – 2,4 року) не було виявлено різниці в ефективності щодо всіх кінцевих точок та в жодній підгрупі хворих. Комбінована терапія була пов’язана з більшою кількістю внутрішньочерепних кровотеч та вибулих учасників через головний біль порівняно з клопідогрелем (Greving et al., 2019).
Інгібітор фосфодіестерази III типу цилостазол у дозі 100 мг двічі на день знижував частоту повторного інсульту на третину порівняно з АСК через три роки при зниженні абсолютного ризику 0,9% на рік. Поєднання цилостазолу з АСК або клопідогрелем корелювало зі зменшенням частоти повторних ішемічних інсультів (2,2 vs 4,5% на рік відповідно), а також зіставним ризиком великих або небезпечних для життя кровотеч (0,6 vs 0,9% на рік відповідно) порівняно з лікуванням тільки АСК або клопідогрелем у 1879 пацієнтів з некардіоемболічним ішемічним інсультом високого ризику при середньому періоді спостереження 1,4 року (Toyoda et al., 2019).
Таким чином, для лікування пацієнтів з ТІА або ішемічним інсультом слід призначати АСК, клопідогрель або АСК + дипіридамол ER. Короткочасне застосування подвійної антитромбоцитарної терапії до 21 дня можна розглядати в осіб із гострим малим інсультом або ТІА та високим ризиком рецидиву. Комбінація клопідогрелю та АСК не є ефективнішою, ніж монотерапія АСК або клопідогрелем та пов’язана з вищим ризиком кровотечі. Тікагрелор не є дієвішим за АСК у пацієнтів із ТІА або малим інсультом для профілактики комбінованої кінцевої точки (інсульт, ІМ або СС-смерть), але може бути кращим для запобігання ішемічного інсульту.
У разі повторної ішемічної події слід оцінити її патофізіологію. За наявності показань для проведення антитромбоцитарної терапії слід оцінити ризик рецидиву та відповідним чином адаптувати її. У пацієнтів із лакунарним інсультом не продемонстровано значущих переваг подвійного антитромбоцитарного лікування клопідогрелем та АСК порівняно з АСК окремо. Комбінована терапія асоційована з більшою ймовірністю розвитку геморагічних несприятливих подій.
Антикоагулянтна терапія при ТІА або ішемічному інсульті та кардіоемболії
Застосування ОАК у пацієнтів із малим ішемічним інсультом або ТІА знижує ризик повторної події приблизно на 66% порівняно із плацебо (4 vs 12% на рік відповідно) (EAFT Trial Investigators, 1993). Частота великих кровотеч під час антикоагулянтної терапії становила 2,8% на рік. ОАК варфарин є ефективнішим за АСК для профілактики СС-ускладнень та повторних інсультів, а також за комбінацію АСК і клопідогрелю у хворих із ФП (Saxena, Koudstaal, 2004; Connolly et al., 2006). Оптимальне міжнародне нормалізоване відношення (МНВ) для пероральної антикоагулянтної терапії АВК становить 2,0‑3,0 (Kirchhof et al., 2016). Показник >3,0 свідчить про підвищений ризик великих кровотеч, особливо у літніх осіб (Hylek et al., 2007).
За даними чотирьох РКД, присвячених порівнянню ПОАК з варфарином (n=71684), 24% пацієнтів із ФП мали попередній інсульт або ТІА в анамнезі (Ruff et al., 2014). Пропорційне зменшення імовірності інсульту або системної емболії при ПОАК порівняно з варфарином було послідовним серед осіб із попереднім інсультом чи ТІА (4,9 vs 5,7% відповідно) та хворих без попереднього інсульту або ТІА (2,3 vs 3% відповідно). Крім того, тенденція до зниження ризику серйозних кровотеч під час ПОАК порівняно з варфарином була послідовною у пацієнтів з попереднім інсультом або ТІА (5,7 vs 6,4% відповідно) та осіб без цих подій (5,2 vs 6,2% відповідно) (Ntaios et al., 2017).
Дані щодо ефективності, безпеки й доступності ідаруцизумабу для зміни активності дабігатрану та андексанету альфа (інгібіторів фактора Ха) у разі кровотечі підтверджують переваги ПОАК порівняно з варфарином у межах вторинної профілактики інсульту серед хворих на ФП (Pollack et al., 2015; Connolly et al., 2019).
Оптимальний час для початку пероральної антикоагулянтної терапії після гострого ТІА або ішемічного інсульту залишається невизначеним, оскільки цих пацієнтів було виключено із досліджень ПОАК (Paciaroni et al., 2017; Arihiro et al., 2016). Розмір інфаркту мозку (а отже, і клінічна тяжкість інсульту) є основним фактором, що визначає геморагічну трансформацію інфаркту, тому емпірична рекомендація полягає в тому, що слід розпочинати антикоагуляцію з першого дня у пацієнтів з ТІА (без інфаркту мозку), на 3-й день – із легким або малим інсультом, на 6-й день – із помірним інсультом та через два тижні – за тяжкої події без виявленої виразної гемодинамічної трансформації за даними комп’ютерної томографії (Kirchhof et al., 2016).
Таким чином, пацієнтам із кардіоемболією, зокрема ФП, слід призначати пероральну антикоагулянтну терапію. Можливі варіанти включають варфарин (МНВ 2,0‑3,0) або ПОАК апіксабан, дабігатран, едоксабан та ривароксабан. Хворим, які мають протипоказання або не бажають застосовувати ОАК, слід використовувати 81‑325 мг/добу АСК або комбінацію АСК та клопідогрелю. Особи з механічними клапанами серця мають отримувати антикоагулянтне лікування при МНВ 2,0‑3,5 залежно від клапана. ПОАК протипоказані пацієнтам із мітральним стенозом від помірного до тяжкого ступеня, ревматичною хворобою серця або порушення роботи механічного клапана серця. В осіб із ТІА або малим інсультом пероральну антикоагулянтну терапію можна розпочинати відразу ж після виключення ВМК. Комбінація АСК та клопідогрелю поступається за ефективністю пероральній антикоагулянтній терапії варфарином та пов’язана із зіставним ризиком кровотечі.
Вторинна профілактика у пацієнтів з емболічним інсультом невизначеного джерела
Раніше інсульти класифікували на захворювання великих судин, захворювання дрібних судин із лакунами; спричинені кардіальними джерелами емболії, як-от ФП; інсульт через рідкісні причини, як-от васкуліт або зловживання психоактивними речовинами, а також криптогенні інсульти, коли причину виникнення неможливо уточнити (Adams et al., 1993). Нещодавно термін «криптогенний інсульт» був замінений на «емболічний інсульт невизначеного джерела» (ESUS). З огляду на припущення, що при ESUS із часом можуть бути виявлені раніше невідомі джерела емболії або ФП, було проведено два масштабні рандомізовані дослідження: RESPECT ESUS та NAVI-GATE ESUS, в яких порівнювали ефективність АСК та ПОАК (дабігатрану й ривароксабану відповідно) (Diener et al., 2019; Hart et al., 2018). За отриманими результатами, ПОАК не перевершували за ефективністю АСК у межах вторинної профілактики повторного інсульту. Ризик великих кровотеч під час антикоагулянтної терапії дабігатраном та АСК був порівнянним.
Криптогенний інсульт та ВОВ
Автопсія та візуалізаційні дослідження показали, що ВОВ зустрічається приблизно у 25% популяції та 44% молодих пацієнтів з інсультом. У більш ранніх рандомізованих випробуваннях CLOSURE, RESPECT та PC вивчали процедуру закриття ВОВ порівняно з лише фармакологічним лікуванням в осіб із криптогенним інсультом. За отриманими даними, не було показано переваг закриття ВОВ перед антитромботичною терапією для запобігання повторному інсульту (Furlan et al., 2012; Carroll et al., 2013; Meier et al., 2013). У трьох нещодавніх дослідженнях з більшою тривалістю спостереження спостерігалася значна користь закриття ВОВ у хворих віком <60 років із криптогенним інсультом (Mas et al., 2017; Sondergaard et al., 2017; Saver et al., 2017).
Був виконаний метааналіз даних восьми рандомізованих досліджень, в яких порівнювали оклюзію ВОВ із медикаментозним лікуванням у 3313 пацієнтів (Mir et al., 2018). Результати показали, що на 1 тис. хворих, які отримували антитромбоцитарну терапію, трапляється 100 ішемічних інсультів, а на 1 тис. пацієнтів після оклюзії ВОВ + антитромбоцитарні засоби – 13 ішемічних інсультів протягом п’яти років. Великі кровотечі були виявлені у 14 на 1 тис. пацієнтів, що приймали антитромбоцитарні препарати, та 7 на 1 тис. осіб при оклюзії ВОВ. На додачу, дослідники порівнювали клінічні наслідки оклюзії ВОВ + антитромбоцитарні препарати та антикоагулянтну терапію. При застосуванні антикоагулянтів та оклюзії ВОВ спостерігалося 29 та 13 на 1 тис. ішемічних інсультів відповідно.
Отримані результати досліджень та метааналізів сприяли оновленню наявних настанов (Klijn et al., 2019). Так, закриття ВОВ рекомендоване пацієнтам віком до 60 років із криптогенним інсультом та великим ВОВ або великим шунтом справа наліво. Однак досі незрозуміло, чи матимуть переваги від процедури хворі >60 років та особи з супутнім артеріосклерозом.
КЕА або стентування в осіб із симптоматичним виразним стенозом внутрішньої сонної артерії
Періопераційний ризик інсульту або смерті, пов’язаних з КЕА, у разі симптоматичного стенозу сонної артерії становить близько 7%. У довгостроковій перспективі додавання КЕА до оптимального медикаментозного лікування зменшувало ймовірність інсульту або летальних випадків через п’ять років наполовину в пацієнтів із нещодавнім симптоматичним каротидним стенозом від 70 до 99% і на чверть – у таких пацієнтів зі стенозом від 50 до 69% (Orrapin, Rerkasem, 2017). Хворі зі стенозом внутрішньої сонної артерії <50% не отримували користі від КЕА. АСК слід призначати до, під час та після операції на сонній артерії (Chaturvedi et al., 2005).
Згідно з даними 10 РКД за участю 5797 симптомних пацієнтів, стентування сонної артерії (ССА) пов’язане з нижчим ризиком періопераційного ІМ, ураження черепних нервів та гематоми у місці доступу порівняно із КEA, але вищим ризиком інсульту або смерті через 30 днів, особливо у пацієнтів віком від 70 років. У довгостроковій перспективі частота інсульту або летальних випадків вища при ССА, ніж при КEA, через різницю між ризиками під час процедури. За винятком хірургічних ризиків, довгострокові показники є зіставними після КEA та ССА для іпсилатерального (4% через дев’ять років), інвалідизувального та летального інсульту, кумулятивних серйозних СС-подій тощо (Bonati et al., 2015; Brott et al., 2016). Рестенози частіше зустрічаються після ССА (10%), але не пов’язані з підвищенням частоти пізнього іпсилатерального інсульту.
У низці випробувань хворі зі значним стенозом внутрішньої сонної артерії були рандомізовані для проведення КЕА або балонної ангіопластики зі стентуванням. У дослідженні SPACE 1200 симптомних пацієнтів протягом шести місяців після ТІА або малого інсульту розподілили для виконання КЕА або стентування (Ringleb et al., 2006). Іпсилатеральний інсульт або летальні випадки впродовж 30 днів мали місце у 6,84% осіб, які перенесли стентування, та 6,34% – після КЕА (Stingele et al., 2008). Отримані дані двох випробувань показали нижчу частоту ускладнень при КЕА. Середньострокові результати були зіставними, а частота рестенозів – вищою після стентування (Mas et al., 2006).
У рандомізованому дослідженні CREST порівнювали ефективність стентування та КЕА у 2502 симптомних та безсимптомних пацієнтів після ССА (Brott et al., 2010). Первинна кінцева точка включала інсульт, ІМ або смерть від будь-яких причин під час періопераційного періоду або іпсилатеральний інсульт протягом чотирьох років після рандомізації. Частота первинної кінцевої точки суттєво не відрізнялася між двома групами (7,2 і 6,8% для стентування та КЕА). Частота перипроцедурного інсульту була вищою у групі стентування (4,1 vs з 2,3% при КЕА), тоді як ризик ІМ – у групі КЕА (1,1 і 2,3% для стентування та КЕА). Частота ішемічного інсульту після периопераційного періоду була однаковою між групами (2,0 та 2,4% відповідно).
Таким чином, у симптомних пацієнтів зі значним стенозом внутрішньої сонної артерії необхідне проведення КEA. ССА є розумною альтернативою КЕА у хворих, які мають протипоказання або високий ризик, пов’язаний із КЕА (Bonati et al., 2012). Профілактичний ефект ССА найвищий у перші 2‑4 тижні після ТІА або незначного інсульту. Користь від КЕА нижча у пацієнтів зі стенозом 50‑70%, у жінок зі стенозом високого ступеня, а також при проведенні операції через 12 тижнів після першої події. Хворі не отримують переваг від хірургічного втручання, коли кількість ускладнень під час процедури перевищує 6%. Антитромбоцитарну терапію АСК рекомендовано застосовувати до, під час та після КЕА. ССА асоційований із дещо вищою частотою короткочасних ускладнень порівняно з КЕА. Подвійну антитромбоцитарну терапію клопідогрелем (75 мг) та АСК (75‑100 мг) слід призначати хворим після ССА протягом 1‑3 місяців на основі екстраполяції результатів досліджень стентування коронарних артерій.
Вторинна профілактика ВМК
Спеціальних рандомізованих досліджень щодо лікування АГ після ВМК не проводилося. У РКД TRIDENT, що триває, вивчають ефект інтенсивнішого контролю АТ за допомогою фіксованої комбінації трьох препаратів у низьких дозах в одній таблетці на додаток до стандартної терапії в осіб із гострим інсультом в анамнезі внаслідок ВМК до розвитку повторного інсульту. У пацієнтів із високим ризиком ішемічного інсульту або СС-подій та недавно перенесеним ВМК за відсутності підвищеної імовірності рецидиву ВМК можна відновити антитромбоцитарну терапію (Al-Shahi Salman et al., 2019; RESTART Collaboration, 2019).
У дослідження RESTART було залучено 537 учасників після ВМК. У 12 із 268 хворих, що отримували антитромбоцитарну терапію, мав місце рецидив ВМК порівняно з 9% тих, хто не застосовував такого лікування. У 7% пацієнтів, яким призначили антиагреганти, спостерігалися серйозні геморагічні події порівняно з 9% тих, хто не отримував лікування. В осіб із ФП та ВМК можливе відновлення пероральної антикоагулянтної терапії має базуватися на оцінці ризику ішемічного інсульту та контролі умов, що призводять до ВМК. Часовий інтервал до відновлення антикоагуляції залежить від тяжкості інсульту та розміру ішемічного ураження (Kirchhof et al., 2016). ПОАК мають переваги перед АВК через нижчий ризик розвитку ВМК (Ruff et al., 2014).
Підготувала Олена Коробка