24 лютого, 2021
Порушення калій-магнієвого гомеостазу при COVID‑19 і сучасні способи корекції
Коронавірусна хвороба (COVID‑19) спричиняє множинні патологічні реакції, як-от гіпертермія, гіпервентиляція, анорексія та гастроентерит, які, своєю чергою, призводять до порушення електролітного балансу в організмі. Гіпокаліємія та гіпомагніємія можуть обтяжувати перебіг коронавірусної інфекції, зумовлювати респіраторні, кардіоваскулярні, неврологічні й інші ускладнення.
Магній і калій (із натрієм і кальцієм) є базовими елементами людського організму, що підтримують гомеостаз і функціонування клітин [1]. У нормі концентрація магнію в сироватці крові становить 1,7-2,2 мг/дл (1,5-1,9 мЕкв/л, або 0,75-0,95 ммоль/л) незалежно від віку [2, 3]. Магній – основний внутрішньоклітинний катіон, кофактор >600 ферментів, який бере участь у біохімічних реакціях енергетичного обміну, синтезу білків і нуклеїнових кислот, а також має важливу роль у регуляції роботи імунної системи. Дефіцит магнію через недостатнє споживання з їжею в практично здорових людей є відносно рідкісним явищем, оскільки нирки дуже чутливо регулюють екскрецію магнію. Натомість у разі гострих і хронічних захворювань гіпомагніємія – надзвичайно поширений стан, який (за різними оцінками) спостерігається в 11-61% госпіталізованих пацієнтів, хоча часто залишається нерозпізнаним, адже рівень магнію рідко визначається в рутинній практиці [3].
Гіпокаліємія також часто трапляється в медичній практиці, особливо у хворих із загостреннями хронічних захворювань, які потребують інфузійної та діуретичної терапії. Калій утворює внутрішньоклітинну буферну систему, призначення котрої полягає в підтриманні кислотно-лужного балансу всередині клітин. У разі тяжких захворювань, отруєнь, травм, шоку буферна система до певної межі перешкоджає руйнуванню клітин. Окрім того, калій дуже важливий для нормальної роботи нервової системи та мускулатури, утворення глікогену й обміну білка. Зниження рівня калію до <3,5 мЕкв/л є потенційно небезпечним розладом, який може підвищувати ризик порушень серцевого ритму. Можливі причини розвитку гіпокаліємії в пацієнтів із COVID‑19 включають патологічну активацію ренін-ангіотензин-альдостеронової системи (РААС), шлунково-кишкові втрати, вторинну анорексію, ураження тубулярного апарату нирок, зокрема через прямий цитотоксичний ефект вірусу SARS-CoV‑2 [4, 5].
Ретроспективний аналіз 290 госпіталізованих пацієнтів із підтвердженою COVID‑19 помірної тяжкості, котрі лікувалися в третинній клініці м. Модена (Італія), виявив гіпокаліємію в 119 осіб, що становило 41% вибірки [6]. Зниження концентрації калію було здебільшого помірним (3-3,4 мЕкв/л) і поєднувалося з гіпокальціємією та гіпомагніємією. Основними причинами електролітних розладів були діуретична терапія (53,4%) та кортикостероїди (23,3%). Автори дійшли висновку, що гіпокаліємія є поширеним порушенням серед пацієнтів із COVID‑19 і найчастіше спричинена втратами калію із сечею. Хоча дефіцит калію був здебільшого помірним і не асоціювався з тяжким перебігом інфекції, італійські клініцисти вважають за потрібне призначати госпіталізованим пацієнтам препарати калію для профілактики потенційно небезпечних аритмій [6].
У пацієнтів із тяжким перебігом інфекції, котрі лікуються у відділенні інтенсивної терапії, електролітні порушення з’являються ще частіше. За повідомленнями з Китаю, гіпокаліємію виявили в 93% критично хворих на COVID‑19 [5]. Близько половини пацієнтів із гіпокаліємією також мали знижений рівень магнію. Механізми регуляції обміну цих елементів взаємопов’язані. Низький рівень магнію перешкоджає компенсації гіпокаліємії через порушення функції натрій-калієвої АТФ-ази (що зумовлює виснаження внутрішньоклітинних запасів калію) та спричиняє втрату калію через дистальні канальці нирок [7, 8]. У китайському дослідженні деякі пацієнти потребували інфузійного введення до 3 г калію на добу [5]. Припинення надмірної втрати калію через підвищену ниркову екскрецію є важливим позитивним прогностичним фактором, який вказує на початок компенсації дисбалансу РААС і одужання критично хворих на COVID‑19 [5].
Роль магнію в боротьбі з COVID‑19
У медицині описані протизапальні, антиспастичні, вазодилатувальні та нейропротекторні властивості препаратів магнію [1]. Нові публікації розглядають ефекти магнію з погляду профілактики та лікування COVID‑19.
Цитокіновий шторм та ураження легень. У контексті коронавірусної пневмонії гіпомагніємія асоціюється з т. зв. цитокіновим штормом – масовим вивільненням прозапальних медіаторів, яке спричиняє системну запальну реакцію та може зумовлювати критичне ураження легень й інших органів [3]. Численні маркери ендотеліальної дисфункції, окисного стресу та системного запалення (IL‑6, TNF, розчинна молекула клітинної адгезії-1, С-реактивний білок) реагують підвищенням на низький рівень магнію [2]. Натомість у разі введення магнію ефект блокування кальцієвих каналів перешкоджає притоку кальцію в імунокомпетентні клітини, внаслідок чого обмежується активація ядерного фактора NF-κB і продукція прозапальних цитокінів, зокрема IL-6, який вважається ініціатором цитокінового шторму [1-3]. Нещодавні систематичні огляди рандомізованих контрольованих досліджень продемонстрували зворотний зв’язок між прийомом магнію, рівнями С-реактивного білка та вираженішим ефектом у пацієнтів із системним запаленням [9, 10]. На моделі гострого ураження легень уведення магнію зменшувало навколобронхіальну інфільтрацію клітинами запалення, альвеолярну септальну інфільтрацію й альвеолярний набряк [11].
Окрім того, магній широко відомий як антагоніст кальцію, що сприяє релаксації посмугованих м’язів бронхів, тому препарати магнію широко використовуються при респіраторних захворюваннях [1]. Отже, застосування магнію за рахунок протизапального, антиоксидантного ефектів і бронходилатації може сприяти кращому контролю респіраторних симптомів, а також запобігати розвитку цитокінового шторму при COVID‑19 (рис.).
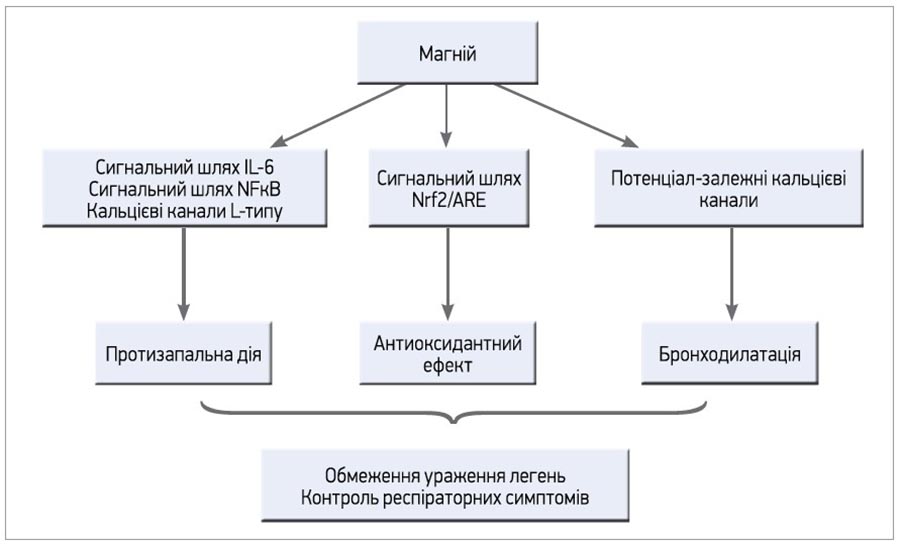 Рис. Можливі механізми впливу магнію на патогенез ураження легень при COVID‑19 і клінічні ефекти [1]
Рис. Можливі механізми впливу магнію на патогенез ураження легень при COVID‑19 і клінічні ефекти [1]
Контроль кардіоваскулярних симптомів. Магній інгібує вивільнення кальцію з ендоплазматичного ретикулуму, пригнічує скоротливість посмугованих м’язів судин, а тому діє як вазодилататор, знижує систолічний, діастолічний і середній артеріальний тиск [12]. Окрім того, механізми впливу магнію на функцію серцево-судинної системи можуть бути опосередковані ефектом активації калієвих каналів, що полегшує відтік іонів кальцію з клітини, підвищенням продукції оксиду азоту ендотелієм, а також блокуванням кальцієвих каналів N-типу, що зумовлює пригнічення вивільнення норадреналіну [13].
Доведено, що прийом препаратів магнію допомагає контролювати артеріальну гіпертензію, знижує ризик фібриляції передсердь, пом’якшує перебіг субклінічного атеросклерозу та запобігає іншим серцево-судинним захворюванням [12-14]. Ці результати обґрунтовують додатковий прийом магнію для значної частки пацієнтів із COVID‑19 і коморбідними серцево-судинними захворюваннями.
COVID‑19, захисний ефект вітаміну D та роль магнію. Вітамін D знижує ризик інфекцій через множинні механізми, зокрема індукцію кателіцидинів і дефензинів, які пригнічують реплікацію вірусів, а також деякі прозапальні цитокіни, що ініціюють запалення й ураження легень [15]. Активна форма вітаміну D (кальцитріол або 1,25-дигідроксихолекальциферол) за структурою є стероїдним гормоном і діє як модулятор імунної системи, пригнічуючи експресію медіаторів запалення та стимулюючи функцію макрофагів. Зростає кількість опублікованих ретроспективних досліджень, за допомогою яких було виявлено дефіцит вітаміну D серед пацієнтів із COVID‑19 [3]. Окрім того, дослідження у 20 європейських країнах підтвердило зв’язок дефіциту вітаміну D зі смертністю від коронавірусної інфекції [16]. Призначення вітаміну D уже застосовується в практиці профілактики та лікування COVID‑19, хоча й без надійного підкріплення контрольованими дослідженнями.
Магній відіграє важливу роль у процесах активації та реалізації фізіологічних функцій вітаміну D; за його дефіциту можуть порушуватися синтез і секреція паратиреоїдного гормона, а також зменшуватися кількість активних рецепторів до вітаміну D у цільових клітинах. Сироватковий рівень 1,25(OH)D часто залишається низьким у пацієнтів із недостатністю магнію, незважаючи на прийом препаратів вітаміну D [3].
Нещодавно в ретроспективному обсерваційному дослідженні продемонстровано статистично значуще зменшення потреби в кисневій терапії серед госпіталізованих пацієнтів із COVID‑19, які щодня впродовж 2 тиж приймали 1000 МО вітаміну D3, 150 мг магнію і 500 мкг вітаміну В12, прийом яких був значущим протекторним чинником проти погіршення перебігу інфекції після врахування віку, статі та впливу супутніх захворювань [17].
Роль калію в забезпеченні імунної відповіді
Калій діє синергічно з магнієм для забезпечення багатьох фізіологічних процесів, включно з реалізацією імунних реакцій [18-21]. Зокрема, в експериментальних роботах було встановлено, що при зниженні внутрішньоклітинної концентрації іонів калію лейкоцити втрачають здатність повноцінно виконувати свої функції [22]. Результати інших досліджень показали, що гіпокаліємія асоціюється з тяжчим перебігом інфекційних процесів та їх більш несприятливими наслідками [23-25]. Згодом з’ясувалося, що й інфекція, зумовлена вірусом SARS-CoV-2, не є винятком із цього правила. Ще на початку пандемії COVID-19 китайські вчені встановили, що в 93% пацієнтів із тяжким або дуже тяжким перебігом цього захворювання має місце гіпокаліємія [26].
Практичні рекомендації з корекції електролітних порушень при COVID‑19
Внутрішньовенні інфузії магнію дають змогу швидко відновити рівень мікроелемента в невідкладних ситуаціях (наприклад, у разі цитокінового шторму). Поповнення запасів магнію за допомогою пероральних препаратів є доступним і потенційно корисним втручанням на ранніх стадіях захворювання, а також для профілактики.
Відповідно до актуальної редакції Дієтичних рекомендацій для американців (2015-2020), рекомендована щоденна норма споживання магнію становить 310-320 мг для дорослих жінок і 400-420 мг для чоловіків, що можна рекомендувати також для осіб із м’якими симптомами COVID‑19 або з метою профілактики [1]. Особливо корисним додавання магнію є для пацієнтів із лабораторно підтвердженим помірним дефіцитом (сироваткова концентрація в межах 0,5-0,75 ммоль/л).
В умовах відділень інтенсивної терапії доцільно проводити інфузійне введення магнію пацієнтам із COVID‑19, у яких розвиваються помірна/тяжка гіпокаліємія, цитокіновий шторм, а також у разі підозри на гіпомагніємію. Рекомендована доза для корекції гіпомагніємії становить 1 г (8 мЕкв) внутрішньовенно кожні 6 год до 4 інфузій за легкої гіпомагніємії чи 250 мг/кг упродовж 4 год у разі тяжкої гіпомагніємії. У критично хворих осіб із легкою та помірною гіпомагнезіємією введення 1 г (8 мЕкв) магнію підвищує сироваткову концентрацію на 0,15 мЕкв/л упродовж 18-30 год. За тяжчого дефіциту магнію може знадобитися терапія вищими дозами [3].
Як уже зазначалося, дефіцит магнію в критично хворих осіб часто поєднується з гіпокаліємію та гіпокальціємією. Крім того, дефіцит магнію робить гіпокаліємію рефрактерною до лікування інфузіями калію. Якщо в пацієнта підтверджується гіпомагніємія чи погранична концентрація магнію на нижній межі норми, слід проводити одночасно корекцію й гіпомагніємії, й гіпокаліємії, щоби запобігти подальшому падінню рівня калію після припинення інфузії препаратів калію [3].
Висновки
- Дефіцит калію та магнію часто розвивається за COVID‑19 і може погіршувати прогноз через підвищену сприйнятливість пацієнтів до системного запалення та несприятливих серцево-судинних ефектів.
- Пероральний прийом препаратів магнію в межах рекомендованого добового споживання можна рекомендувати пацієнтам із легкими симптомами COVID‑19, а також із метою профілактики.
- У пацієнтів із тяжким перебігом COVID‑19 інфузійну корекцію дефіциту магнію доцільно проводити одночасно з уведенням калію, оскільки механізми регуляції гомеостазу цих катіонів взаємопов’язані.
Довідка «ЗУ»
Добре відомим на українському ринку препаратом, який поєднує у своєму складі калієву та магнієву солі аспарагінової кислоти, є Панангін Форте. Цей препарат має широкий спектр кардіо-, ангіо- та церебропротекторних ефектів, завдяки чому може розглядатись як стандартний компонент медикаментозних схем базисної терапії в пацієнтів із кардіальною патологією, цукровим діабетом і різноманітними проявами ендотеліальної дисфункції.
Панангін Форте:
- швидко відновлює рівні K та Mg в організмі;
- не має кумулятивного ефекту;
- покращує метаболічні процеси, зокрема в міокарді;
- чинить антиаритмічну дію;
- знижує ризик розвитку тромботичних ускладнень;може застосовуватись як із профілактичною метою, так і у відновлювальному періоді.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 2 (495), 2021 р.



