16 червня, 2024
Уромуне®-МВ140 у профілактиці рецидивуючих інфекцій сечовивідних шляхів: інноваційний підхід із доведеною ефективністю
Рецидивуючі інфeкції сечовивідних шляхів (рІСШ) залишаються нагальною соціальною проблемою та фінансовим тягарем для системи охорони здоров’я. Зростаюча поширеність рІСШ і глобальний виклик, спричинений зростанням антибіотикорезистентності у світі, спонукає науковців, експертів і практикуючих лікарів впроваджувати ефективні неантибіотичні засоби та інноваційні підходи з метою запобігання епізодам ІСШ.
Ключові слова: рецидивуючі інфекції сечових шляхів, антибіотикорезистентність, імуноактивна профілактика, сублінгвальна вакцина, Уромуне®-МВ140.
Соціально-економічний вплив рІСШ: чи достатньо одного лікування для покращення якості життя пацієнта?
ІСШ займають перше місце у списку медичних проблем, які значно впливають на здоров’я та повсякденну діяльність людини. Анатомічні особливості, нетиповий збудник, наявність супутніх захворювань і/або встановлення сечового катетера чи сечовивідного стента ускладнюють перебіг ІСШ, що зумовлює труднощі з вибором терапевтичної стратегії. І хоча неускладнені ІСШ, як правило, краще піддаються лікуванню, певні обставини, такі як підвищення стійкості бактерій до антибіотиків, неадекватне лікування первинного гострого циститу, анатомічні дефекти, що призводять до стазу, обструкції або міхурово-сечовідного рефлюксу, атрофічний вагініт і дивертикули сечового міхура, можуть спровокувати рецидиви [1]. Рецидивуючі ІСШ характеризуються появою ≥2 симптоматичних епізодів протягом 6 міс або ≥3 епізодів – упродовж 12 міс [2].
За статистикою, принаймні один епізод симптоматичної ІСШ виникає у 50% жінок, при цьому приблизно у 26% із них спостерігається рецидив протягом 6 міс після лікування початкового епізоду [3]. У дослідженні, проведеному в закладі первинної медичної допомоги, 53% жінок старше 55 років і 36% молодих жінок повідомили про рецидив ІСШ протягом одного року [4].
Незважаючи на те що переважну кількість пацієнтів, які страждають від рІСШ, становлять жінки, 20% таких діагнозів припадає на чоловіче населення. Експерти зазначають, що статеві гормони можуть відігравати певну роль у трансформації первинної ІСШ у повторну проблему. Так, у дослідженні на тваринній моделі самці демонстрували слабшу імунну відповідь на ІСШ, можливо, через вплив андрогенів [5].
Тягар рІСШ включає як особистісний, так і суспільний аспект. Останній полягає у збільшенні навантаження на систему охорони здоров’я, витрат на медичну допомогу, включаючи витрати, пов’язані з візитами амбулаторних пацієнтів, випискою рецептів на протимікробні препарати, госпіталізацією, а також виплат, пов’язаних із втратою непрацездатності через хворобу та лікуванням супутніх захворювань. Так, у США на консультації щодо ІСШ припадає від 1 до 6% усіх звернень до медичних закладів (близько 7 млн візитів, що у фінансовому еквіваленті складає близько 1,6 млрд доларів США на рік).
Раптовий, швидкий і болісний початок захворювання, що зумовлює неспроможність займатися звичною діяльністю, часто викликає занепокоєння пацієнтів, призводячи до появи симптомів тривоги та депресії. Соціальний вплив рІСШ особливо помітний у працюючих жінок у пременопаузі. У людей похилого віку потенційний вплив симптомів рІСШ на загальний стан здоров’я, включаючи такі проблеми, як нетримання сечі, також асоціюється зі значним психологічним тягарем і погіршенням якості життя [6]. Висока поширеність рІСШ є модифікованою детермінантою як соціального, так і персонального тягаря, утім одного лише лікування інфекцій часто недостатньо для покращення якості життя та загального самопочуття [1].
У багатонаціональному веб-дослідженні GESPRIT оцінювався вплив рІСШ на систему охорони здоров’я у країнах Європи, а також на конкретного пацієнта [9]. Дорослі жінки (≥18 років) із рІСШ в анамнезі, які на момент опитування мали симптоми гострої інфекції (n=1275) або перенесли ІСШ протягом попередніх 4 тижнів (n=666), заповнили онлайн-анкету. Учасниці повідомили про значний вплив захворювання на якість життя (згідно з оцінкою за опитувальником «Ваше здоров’я та самопочуття» [SF‑12 v2]), зумовлений занепокоєнням через вимушений простій на роботі та утриманням від звичної діяльності. Слід зазначити, що більшість опитаних (близько 80%) отримували лікування антибіотиками. Профілактика повторних епізодів ІСШ часто відкладалася після того, як був встановлений рецидив захворювання (≥3 епізодів ІСШ за 12 міс), а превентивні поведінкові заходи часто виявлялися неефективними [7].
Проблема антибіотикорезистентності: чому терапія рІСШ не завжди ефективна?
ІСШ на сьогодні є однією з найпоширеніших причин використання антибіотиків у всьому світі. Аналіз рекомендацій щодо лікування рІСШ за 2022 рік показав, що безперервний прийом антибіотиків або застосування протимікробних препаратів після статевого акту продовжує широко практикуватися [8], однак це лише сприяє поширенню антибіотикорезистентності. Тривалий прийом антибіотиків чинить шкідливий вплив на кишкову мікробіоту, а також часто пов’язаний із виникненням побічних ефектів. Глобальний виклик щодо боротьби з прогресуючою антибіотикорезистентністю привів експертів міжнародних організацій до висновку, що призначення протимікробних препаратів як засобів супресивної терапії або тривалої профілактики більше не є доцільним [9, 10].
Арсенал ефективних антибіотиків швидко скорочується, і масштаби цієї проблеми важко переоцінити [11]. Високий рівень резистентності до багатьох часто призначуваних антибактеріальних препаратів реєструється у всьому світі, водночас у країнах Африки спостерігається 100% стійкість ізолятів Escherichia coli до амоксициліну [12]. Доведено, що резистентні штами E. coli, такі як ST131 (O25: H4), здатні провокувати спалахи ІСШ. Разом із тим поява та поширення резистентних до карбапенему Enterobacteriaceae є глобальною загрозою для громадського здоров’я [11, 13]. Трансмісивна резистентність Enterobacteriaceae наразі зростає також до колістину (через ген mcr‑1) із потенціалом швидкого поширення [14]. Наведені дані означають, що більшість існуючих інструментів боротьби проти мультирезистентних грамнегативних бактерій втрачають ефективність.
Збільшення використання антибіотиків у людей і тварин спричинило удосконалення механізмів бактеріальної резистентності [15]. Остання виникає внаслідок послідовних чи нових хромосомних мутацій, мобільних генетичних елементів або комбінації цих факторів. Такі мобільні генетичні елементи, як плазміди та транспозони, забезпечують швидке поширення резистентності між бактеріями. Усі відомі механізми резистентності патогенів можуть інактивувати антибіотик, впливати на його концентрацію, доступну в точці дії, або змінювати мішень протимікробного засобу [16].
Інновації у профілактиці рІСШ: як скоротити використання антибіотиків?
Враховуючи ситуацію з антибіотикорезистентністю у світі, існує нагальна потреба у впровадженні неантибіотичних стратегій для запобігання неускладненим ІСШ. Потенційні неантибіотичні заходи, які можуть зменшити ризик рецидивів ІСШ, включають поведінкові зміни (запобігання стресам, дієта та здоровий спосіб життя, достатній рівень гідратації, гігієна, регулярне повне спорожнення сечового міхура тощо), вживання харчових добавок (таких, як китайські лікарські трави та продукти із журавлини), прийом нестероїдних протизапальних препаратів, пробіотиків, D-манози, метенаміну гіпурату, естрогенів. Інноваційні медичні заходи, як-от застосування сублінгвальних бактеріальних вакцин, зарекомендували себе як дієвий підхід у профілактиці бактеріальних рІСШ у дорослих, що дозволяє зменшити використання антибіотиків і запобігти можливим побічним ефектам, скоротити кількість епізодів інфекцій, покращити загальне самопочуття та якість життя пацієнтів [17].
У 2023 році рекомендації щодо діагностичної оцінки та лікувальних підходів до рІСШ зазнали чималих змін. Це, зокрема, стосувалося імуноактивної профілактики, ефективність якої, за даними рандомізованих клінічних досліджень, перевищила плацебо у пацієнтів із рІСШ. Імуноактивні агенти, такі як пероральні бактеріальні вакцини, рекомендовані Європейською асоціацією урологів (EAU), Асоціацією наукових медичних товариств Німеччини (AWMF), Товариством акушерів і гінекологів Швейцарії (SSGO), Іспанським товариством інфекційних хвороб і клінічної мікробіології (SEIMC) та Мексиканським коледжем спеціалістів із гінекології та акушерства (COMEGO) як довготривала профілактична стратегія менеджменту неускладнених рІСШ [8]. Відповідно до висновків систематичного огляду клінічних випробувань 2020 року, бактеріальні вакцини здатні зменшувати частоту рецидивів ІСШ і потребу в антибіотиках [18]. Оскільки ІСШ розвиваються на поверхнях слизових оболонок, важливо, щоб вакцина індукувала відповідну цільову імунну відповідь.
Сублінгвальна вакцина Уромуне®-МВ140 (Uromune®-MV140, Inmunotek S.L., Іспанія) є однією з найбільш вивчених вакцин у світі, ефективність якої у профілактиці рІСШ була доведена в ході клінічних досліджень [19]. Під час нещодавніх клінічних випробувань ІІ-ІІІ фази у 26 країнах Уромуне®-МВ140 продемонструвала високий профіль ефективності та безпеки в запобіганні ризику рецидивів ІСШ [20]. З 2010 року Уромуне®-МВ140 доступна у клінічній практиці в різних країнах світу, включаючи Іспанію, Португалію, Сполучене Королівство Великої Британії та Північної Ірландії, Литву, Нідерланди, Швецію, Норвегію, Австралію, Нову Зеландію та Чилі. Нещодавно дана сублінгвальна вакцина була схвалена в Мексиці та Домініканській Республіці, пройшла реєстрацію в Міністерстві охорони здоров’я Канади.
До складу сублінгвальної вакцини Уромуне®-MB140 входять чотири цільноклітинні селективні інактивовані бактеріальні штами (E. coli, Klebsiella pneumoniae, Enterococcus faecalis, Proteus vulgaris) у більш природній для імунної системи формі, максимізуючи її імуногенний потенціал. Доведено, що імунна відповідь, викликана сумішшю бактерій, є вищою, ніж відповідь на окремі штами бактерій. Бактеріальні штами, які містяться у сублінгвальній вакцині Уромуне®-MВ140, охоплюють 80-90% збудників ІСШ. За допомогою сублінгвальної імунізації вдається уникнути розпаду бактерій у шлунково-кишковому тракті та індукувати інтенсивну й довготривалу відповідь у слизовій оболонці сечостатевого тракту.
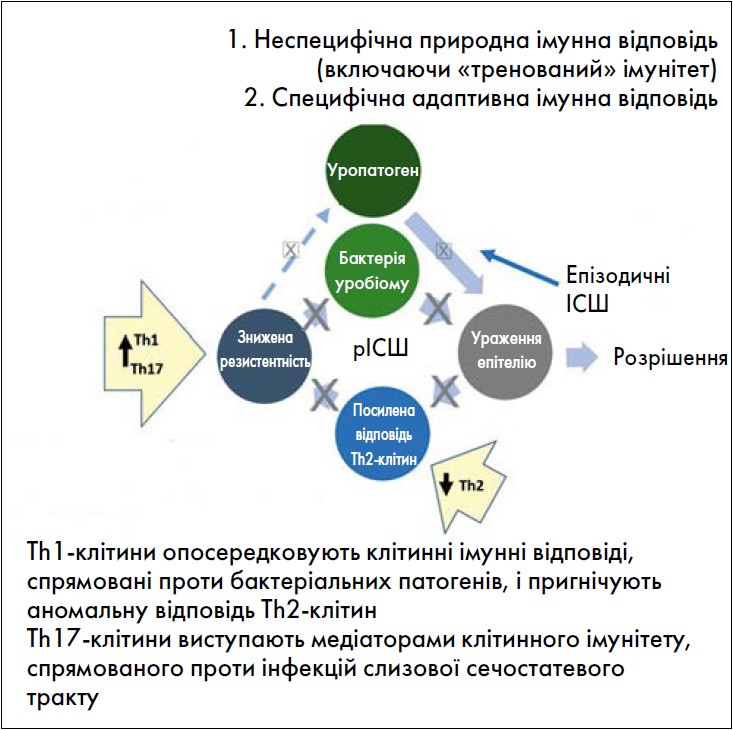
Уромуне®-МВ140 стимулює специфічну імунну відповідь (Th17/Th1), що є головним механізмом резистентності організму до бактеріальних ІСШ. Вакцина індукує регуляторну відповідь Т-клітин шляхом підготовки дендритних клітин до утворення Th1-, Th17- і Т-клітин, що секретують інтерлейкін 10, а також пригнічує шкідливі відповіді Th2‑клітин, пов’язані з рецидивом ІСШ [21] (рисунок).
Рис. Механізм дії сублінгвальної вакцини
(Nickel J.C., Doiron R.C., 2023)
Перевірена ефективність Уромуне®-МВ140 у різних популяціях: аналіз міжнародних досліджень
У систематичному огляді J.C. Nickel (2020) було проаналізовано 19 досліджень, присвячених оцінці результатів застосування Уромуне®-МВ140 для профілактики рІСШ [22]. Доведено, що у пацієнтів, які отримували вакцину впродовж 3 міс, епізоди ІСШ виникали значно рідше порівняно з тими, кому було призначено 6‑місячну антибіотикопрофілактику.
Сублінгвальна вакцина Уромуне®-MB140 продемонструвала ефективність у когортному дослідженні Lorenzo-Gomez et al. (2015) із зареєстрованим абсолютним зниженням ризику ІСШ на 90% (абсолютне зниження ризику [ARR] 90,28%; довірчий інтервал [ДІ] 87,18-93,38; кількість пацієнтів, яку потрібно пролікувати [NNT] 1,1; ДІ 1,1-1,1) [23]. Пацієнти були розподілені на дві групи: учасники першої групи отримували сублінгвальну вакцину Уромуне®-МВ140 (два розпилення по 100 мкл кожне щодня протягом 3 міс), а другої — по 200 мг сульфаметоксазолу та 40 мг триметоприму впродовж 6 міс. Через 12 міс тільки у 9,7% осіб із групи Уромуне®-МВ140 розвинулася ІСШ порівняно зі 100% жінок, які отримували антибіотики (р<0,0001).
Двома роками раніше Lorenzo-Gomez M.F. et al. (2013) встановили, що застосування сублінгвальної вакцини значно зменшувало кількість повторних епізодів ІСШ порівняно з антибіотикопрофілактикою. Так, ефективність Уромуне®-МВ140 склала 75% у перші 3 міс та 86 і 77% відповідно через 9 і 15 міс спостереження. Кількість пацієнтів, у яких не було зареєстровано жодного випадку ІСШ через 3, 9 і 15 міс, склала 101, 90 і 55 відповідно у групі Уромуне®-МВ140 проти 9, 4 і 0 у групі пацієнтів, які отримували антибіотики (р<0,0001) [24]. Ці багатообіцяючі результати були підтверджені британським когортним дослідженням B.Yang et al. (2018) за участю жінок (середній вік – 56 років) із рІСШ, які отримували 3‑місячний курс сублінгвальної вакцини. За даними авторів, 78% жінок, які отримували Уромуне®-МВ140, не мали повторних епізодів інфекції впродовж усього періоду спостереження. До лікування всі жінки перенесли ≥3 епізодів ІСШ протягом попередніх 12 місяців. Переважна більшість рецидивів виникала у жінок у постменопаузі [25].
У дослідженні Ramнrez Sevilla C. (2019) із великою вибіркою із 784 пацієнтів зменшення кількості епізодів ІСШ до 0 або 1 спостерігалося у 71,7% хворих (73,9% жінок і 61% чоловіків) у групі Уромуне®-МВ140 через 3 міс після прийому і 64,7% (65,9% жінок і 58,8% чоловіків) після 6 міс спостереження [26]. Світова медична спільнота з інтересом очікує на результати подвійного сліпого плацебо-контрольованого дослідження (NCT02543827), яке наразі триває [27].
Уже доступні результати випробувань щодо аналізу ефективності та безпеки Уромуне®-МВ140 у найбільш уразливих категорій пацієнтів. Так, автори досліджень за участю чоловіків і/або жінок з ускладненими ІСШ, у тому числі чоловіків із простатитом [28], нейрогенним сечовим міхуром [29], аутоімунними захворюваннями та пацієнтів з імуносупресією, опосередкованою лікуванням [30], хронічною хворобою нирок і трансплантованою ниркою [31-34], лімфопроліферативними розладами [35], ослаблених людей похилого віку [36, 37], дітей [38] і хворих у післяопераційному періоді [39], повідомляли про суттєве зниження частоти ІСШ (у межах 30-50%) і/або видиме покращення якості життя після лікування вакциною Уромуне®-MВ140. У проспективному аналізі Lorenzo-Gуmez et al. (2021) вивчали дієвість сублінгвальної вакцини у групі немічних людей похилого віку, які постійно перебувають у будинках престарілих (160 жінок, середній вік – 82,67 року; 40 чоловіків, середній вік – 80,23 року). Досліджувані мали в середньому 4 епізоди ІСШ (або безсимптомної бактеріурії) на місяць, які лікували антибіотиками. Після курсу Уромуне®-МВ140 частота ІСШ у жінок знизилася в середньому до 0,1 епізоду на місяць. У 18% жінок не було зареєстровано жодного епізоду ІСШ протягом 12 міс від початку застосування вакцини, водночас ще 81,7% мали <3 епізодів ІСШ на рік [36].
Доведений профіль безпеки Уромуне®-МВ140
Дослідження, які оцінювали сублінгвальну вакцину Уромуне®-МВ140 у популяціях жінок із рІСШ, продемонстрували її високий профіль безпеки. У двох великих порівняльних дослідженнях (Уромуне®-МВ140 проти антибіотиків у профілактиці рІСШ) не було зареєстровано жодної побічної реакції при застосуванні вакцини [23]. У дослідженні B. Yang et al. (2018) незначні побічні ефекти спостерігалися у статистично незначущої кількості пацієнтів [25]. Вісім із 784 учасників дослідження Ramнrez Sevilla C. et al. (2019) відмічали сухість у роті протягом курсу застосування Уромуне®-МВ140, ще чотири пацієнти скаржилися на біль в епігастральній ділянці [26]. Carriуn-Lуpez et al. (2020) доповіли про два випадки легкого глоситу серед 166 пацієнтів, які отримували Уромуне®-МВ140 [40]. Лише дві із 1407 жінок у п’яти дослідженнях, що увійшли до систематичного огляду J.C. Nickel et al. (2023), вирішили припинити лікування Уромуне®-МВ140 [20].
Високий профіль безпеки сублінгвальної вакцини Уромуне®-МВ140 підтверджується висновками першого в Північній Америці дослідження клінічного досвіду [41], а також звітами понад 22 тис. пацієнтів, які отримували вакцину (дані зібрані до грудня 2021 року) у програмах розширеного доступу (compassionate use program, ClinicalTrial.Gov: NCT 04173013).
Економічна ефективність Уромуне®-МВ140: як зменшити навантаження на систему охорони здоров’я?
Результати обсерваційного проспективного дослідження за участю жінок із рІСШ продемонстрували, що застосування вакцини Уромуне®-МВ140 сприяло достовірному зниженню частоти ІСШ, що зумовило зменшення потреб у ресурсах охорони здоров’я та значне глобальне скорочення витрат, пов’язаних із використанням антибіотиків, консультаціями терапевта, спеціалізованою допомогою та додатковими діагностичними тестами. Річне використання антибіотиків, визначене як число використаних антибактеріальних засобів і кількість їх упаковок, скоротилося на 42,5 і 60,7% відповідно [40]. Кількість випадків госпіталізацій до відділення невідкладної допомоги зменшилася на 71,8% (95% ДІ 58,8-84,8) порівняно з періодом до призначення Уромуне®-МВ140. Що стосується візитів до уролога, до застосування імунотерапії загалом 91% пацієнтів потребували додаткових консультацій, що призвело до середнього відсоткового збільшення числа консультацій на 214,5% на пацієнта/рік (95% ДІ 171,0-258,1). Після курсу лікування Уромуне®-МВ140 лише 2,4% пацієнтів потребували госпіталізації зі значно меншою середньою тривалістю: 0,23 і 0,03 дня (p=0,001) у до- та поствакцинальний період відповідно [42]. За оцінками P. Carriуn-Lуpez et al. (2022), до призначення Уромуне®-МВ140 середні прямі річні витрати на пацієнта становили 1001,1 євро, переважно пов’язані з наданням консультацій (64,1%) та спеціалізованої допомоги (24,6%). Загалом витрати на лікування одного епізоду ІСШ до вакцинації оцінювалися в 161,8 євро. Після сублінгвальної вакцинації середньорічна вартість лікування значно знизилася (із 42,7 до 16,5 євро на пацієнта/рік залежно від типу антибіотика).
Раціональні превентивні заходи, а саме призначення вакцини Уромуне®-МВ140, дозволили зменшити навантаження на спеціалістів первинної та вторинної ланки, а також скоротити потребу пацієнтів у візитах до медичних закладів, у діагностичних обстеженнях та лікуванні повторних епізодів ІСШ.
Дієвий неантибіотичний підхід у менеджменті рІСШ є нагальною медичною потребою. Враховуючи значну поширеність рІСШ, клінічний вплив, високі кумулятивні витрати, пов’язані із захворюванням, а також глобальну проблему антибіотикорезистентністі, використання сублінгвальної вакцини Уромуне®-МВ140 є оптимальною стратегією для запобігання виникненню епізодів рІСШ, покращення якості життя пацієнтів і зменшення використання антибіотиків. Імуноактивна профілактика бактеріальною вакциною з метою зниження ризику рецидивів ІСШ рекомендована багатьма міжнародними науковими товариствами, у тому числі EAU, AWMF, SSGO, SEIMC і COMEGO. Високі профілі ефективності та безпеки дозволяють призначати Уромуне®-МВ140 дорослим для стимуляції імунної відповіді, спрямованої проти бактерій, що викликають ІСШ.
Література
- Medina M., Castillo-Pino E. An introduction to the epidemiology and burden of urinary tract infections. Ther Adv Urol. 2019 May 2;11:1756287219832172. doi: 10.1177/1756287219832172. PMID: 31105774; PMCID: PMC6502976.
- Kranz J., Schmidt S., Lebert C. et al. The 2017 update of the German clinical guideline on epidemiology, diagnostics, therapy, prevention, and management of uncomplicated urinary tract infections in adult patients: part 1. Urol Int 2018; 100: 263-270.
- Foxman B. Recurring urinary tract infection: incidence and risk factors. Am J Public Health. 1990 Mar;80(3):331-3.
- Aydin A., Ahmed K., Zaman I., Khan M.S., Dasgupta P. Recurrent urinary tract infections in women. Int Urogynecol J. 2015 Jun;26(6):795-804].
- Olson Patrick D., Hruska Keith A., Hunstad David A. Androgens Enhance Male Urinary Tract Infection Severity in a New Model. Journal of the American Society of Nephrology 27(6): p 1625-1634, June 2016.doi: 10.1681/ASN.2015030327.
- Renard J., Ballarini S., Mascarenhas T. et al. Recurrent lower urinary tract infections have a detrimental effect on patient quality of life: a prospective, observational study. Infect Dis Ther. Epub ahead of print 18 December 2014. doi: 10.1007/s40121-014-0054-6.
- Wagenlehner F., Wullt B., Ballarini S. et al. Social and economic burden of recurrent urinary tract infections and quality of life: a patient web-based study (GESPRIT). Expert Rev Pharmacoecon Outcomes Res 2018; 18: 107-117.
- Kwok M., McGeorge S., Mayer-Coverdale J., Graves B., Paterson D.L., Harris P.N.A. et al. Guideline of guidelines: management of recurrent urinary tract infections in women. BJU Int. 2022; 130(Suppl 3):11-22. Epub 20220517. https://doi.org/10.1111/bju.15756 PMID: 35579121; PubMed Central PMCID: PMC9790742.
- European Medicines Agency. (2014). Antimicrobial Resistance. Available online at: http://www.ema.europa.eu/ema/index.jsp?curl=pages/special_topics/general/general_content_000439.jsp.
- Food and Drug Administration U.S. (2014). Antimicrobial Resistance. Available online at: http://www.fda.gov/animalveterinary/safetyhealth/antimicrobialresistance/default.htm.
- World Health Organisation. Antimicrobial resistance: global report on surveillance 2014 (WHO, 2014).
- Bryce A. et al. Global prevalence of antibiotic resistance in paediatric urinary tract infections caused by Escherichia coli and association with routine use of antibiotics in primary care: systematic review and meta-analysis. BMJ 352, i939 (2016).
- Johnson J.R., Johnston B., Clabots C., Kuskowski M.A. & Castanheira M. Escherichia coli sequence type ST131 as the major cause of serious multidrug-resistant E. coli infections in the United States. Clin. Infect. Dis. 51, 286-294 (2010).
- Wang Y. et al. Prevalence, risk factors, outcomes, and molecular epidemiology of mcr‑1‑positive Enterobacteriaceae in patients and healthy adults from China: an epidemiological and clinical study. Lancet Infect. Dis. 17, 390-399 (2017).
- Blair J.M., Webber M.A., Baylay A.J., Ogbolu D.O. & Piddock L.J. Molecular mechanisms of antibiotic resistance. Nat. Rev. Microbiol. 13, 42-51 (2015).
- Munita J.M. & Arias C. A. Mechanisms of antibiotic resistance. Microbiol. Spectr. https://doi.org/10.1128/microbiolspec.VMBF‑0016-2015 (2016).
- Burrows L.L. (2024) It’s uncomplicated: Prevention of urinary tract infections in an era of increasing antibiotic resistance. PLoS Pathog 20(2): e1011930. https://doi.org/10.1371/journal.ppat.1011930.
- Prattley S., Geraghty R., Moore M., Somani B.K. Role of Vaccines for Recurrent Urinary Tract Infections: A Systematic Review. Eur Urol Focus. 2020; 6(3):593-604. Epub 20191202. https://doi.org/10.1016/j.euf.2019.11.002 PMID:1806578.
- Sihra N., Goodman A., Zakri R. et al. Nonantibiotic prevention and management of recurrent urinary tract infection. Nat Rev Urol 15, 750-776 (2018). https://doi.org/10.1038/s41585-018-0106‑x.
- Nickel J.C., Doiron R.C. An Effective Sublingual Vaccine, MV140, Safely Reduces Risk of Recurrent Urinary Tract Infection in Women. Pathogens. 2023;12(3). Epub 20230221. https://doi.org/10.3390/pathogens12030359 PMID: 36986281; PubMed Central PMCID: PMC10052183.
- Benito-Villalvilla C. et al. MV140, a sublingual polyvalent bacterial preparation to treat recurrent urinary tract infections, licenses human dendritic cells for generating Th1, Th17, and IL‑10 responses via Syk and MyD88. Mucosal Immunol. 10, 924-935 (2017).
- Nickel J.C. Could sublingual vaccination be a viable option for the prevention of recurrent urinary tract infection in Canada? A systematic review of the current literature and plans for the future. Can. Urol. Assoc. J. 2020, 14, 281-287.
- Lorenzo-Gomez, M.F. et al. Comparison of sublingual therapeutic vaccine with antibiotics for the prophylaxis of recurrent urinary tract infections. Frontiers Cell. Infect. Microbiol. 5, 50 (2015).
- Lorenzo-Gуmez M.F., Padilla-Fernбndez B., Garcнa-Criado F.J., Mirуn-Canelo J.A., Gil-Vicente A., Nieto-Huertos A., Silva-Abuin J.M. Evaluation of a therapeutic vaccine for the prevention of recurrent urinary tract infections versus prophylactic treatment with antibiotics. Int Urogynecol J. 2013 Jan;24(1):127-34. doi: 10.1007/s00192-012-1853-5. Epub 2012 Jul 18. PMID: 22806485; PMCID: PMC3536982.
- Yang B., Foley S. First experience in the UK of treating women with recurrent urinary tract infections with the bacterial vaccine Uromune®. BJU Int. 2018 Feb;121(2):289-292. doi: 10.1111/bju.14067. Epub 2017 Nov 23. PMID: 29171130.
- Ramнrez Sevilla C., Gуmez Lanza E., Manzanera J.L., Martнn J.A.R., Sanz M.B. Active immunoprophyilaxis with Uromune® decreases the recurrence of urinary tract infections at three and six months after treatment without relevant secondary effects. BMC Infect Dis. 2019 Oct 28;19(1):901. doi: 10.1186/s12879-019-4541‑y. PMID: 31660885; PMCID: PMC6819445.
- US National Library of Medicine. ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02543827. (2018).
- Lorenzo-Gуmez M.F., Martнnez-Huйlamo M., Valverde-Martinez L.S., Hernбndez-Hernбndez D., Garcнa-Garcнa M.A., Perбn-Teruel M., Garcнa-Cenador M.B. Quality of life in patients with chronic prostatitis treated with elaborated polybacterial vaccine. Int. Cont. Soc. 2018, 250.
- Ordaz-Jurado D.G., Bonillo-Garcнa M.A., Betancourt-Hernбndez J., Arlandis-Guzmбn S., Avargues-Pardo A., Broseta-Rico E., Boronat-Tormo F. Does bacterial vaccine become clinically significant in neurogenic bladder in patients at clean intermittent catheterization? Int. Cont. Soc. 2014, 567.
- Sбnchez-Ramуn S., Fernбndez-Paredes L., Saz-Leal P., Diez-Rivero C.M., Ochoa-Grullуn J., Morado C., Macarrуn P., Martнnez C., Villaverde V., de la Peсa A.R. et al. Sublingual Bacterial Vaccination Reduces Recurrent Infections in Patients with Autoimmune Diseases Under Immunosuppressant Treatment. Front. Immunol. 2021, 12, 675735.
- Garcнa Agudo R., Redondo Gonzбlez O., Cazalla Cadenas F., Pereira Pйrez E., Arias Arias A. Vacunaciуn sublingual con bacterias inactivadas en las infecciones urinarias de repeticiуn de pacientes nefrolуgicos: experiencia en nuestro centro. Congr. Nac. Soc. Espaсola Nefrol. 2015, 539, 78-84. 39.
- Garcнa-Ledesma P., Hernando A., Galan M., Bilbao S., Muсoz R.I., Vargas A., Olarte A., Neyra P., Martinez I. Anбlisis de nuestra experiencia en el tratamiento con la vacuna sublingual de bacterias inactivadas en pacientes con infecciones urinarias de repeticiуn. Congr. Nac. Soc. Espaсola Nefrol. 2016, 1637. 40.
- Castro-Alonso C., Ruiz Millo O., Galbis Bernacer A., Escudero Quesada V., Pantoja Perez J., Montomoli M., Conzalez-Moya M., Nogueira Coito J.M., Pallardo Mateu L.M. Efectividad de la vacunaciуn bacteriana individualizada para prevenir infecciones urinarias de repeticiуn en pacientes con ERC. In Proceedings of the Congreso Nacional de la Sociedad Espaсola de Nefrologнa, Oviedo, Spain, 8-11 October 2016. 41.
- Shabaka A., Zapata N., Santiago J.L., Pйrez-Flores I., Moreno-de la Higuera M.A., Sбnchez-Ramуn S., Sбnchez-Fructuoso A.I. Clinical and Immunological Response to Sublingual Vaccination for the Prevention of Recurrent Urinary Tract Infections in Kidney Transplant Patients: Results after 1 Year of Follow-up. Transplant. Soc. 2018, 102, S320.
- Ochoa-Grullуn J., Guevara K., Guzmбn-Fulgencio M., Benavente C.M., Martнnez R., Pйrez C., Peсa A., Rodrнguez-de la Peсa A., Llano-Hernбndez K., Rodrнguez-Frнas E. et al. Polybacterial mucosal stimulation in lymphoproliferative syndromes with recurrent infections: A new complementary strategy. Eur. Acad. Allergy Clin. Immunol. 2017, 576.
- Lorenzo-Gуmez M.F.; Padilla-Fernбndez B.; Flores-Fraile J.; Valverde-Martнnez S.; Gonzбlez-Casado I.; Hernбndez J.-M.D.D.; Sбnchez-Escudero A.; Arroyo M.-J.V.; Martнnez-Huйlamo M.; Criado F.H. et al. Impact of whole-cell bacterial immunoprophylaxis in the management of recurrent urinary tract infections in the frail elderly. Vaccine 2021, 39, 6308-6314.
- Padilla Fernandez B.; Gonzбlez Casado I.; de Dios Hernбndez J.M.; Sбnchez Escudero A.; Vicente Arroyo M.J.; Martнnez Huйlamo M.; Herrera Criado F.; Blanco Tarrнo E.; Mбrquez Sбnchez M.T.; Flores Fraile M.d.C. et al. Autovacuna frente a vacuna polibacteriana elaborada en el manejo de la infecciуn urinaria en el anciano frбgil. Confed. Am. De Urol. 2019.
- Martinez-Camacho M.A.; Escuer Morell M.J.; Royo Gomez G.F.; Asensio Llorente M.; Solй E. Profilaxis inmunoactiva para la prevenciуn de las infecciones del tracto urinario de repeticiуn, Asociaciуn Espaсola de Pediatrнa: Madrid, Spain, 2015; C110.
- Lorenzo Gomez M.F.; Collazos Robles R.E.; Virseda Rodriguez A.J.; Garcia Cenador M.B.; Miron Canelo J.A.; Padilla Fernandez, B. Urinary tract infections in women with stress urinary incontinence treated with transobturator suburethral tape and benefit gained from the sublingual polibacterial vaccine. Ther. Adv. Urol. 2015, 7.
- Carriуn-Lуpez P.; Martнnez-Ruiz J.; Librбn-Garcнa L.; Gimйnez-Bachs J.M.; Pastor-Navarro H.; Salinas-Sбnchez A. S. Analysis of the Efficacy of a Sublingual Bacterial Vaccine in the Prophylaxis of Recurrent Urinary Tract Infection. Urol. Int. 2020, 104, 293-300.
- Nickel J.C.; Kelly K.L.; Doiron R.C. A novel sublingual vaccine for recurrent urinary tract infection in women: Preliminary results from the pre-COVID‑19 cohort in the first North American Uromune early clinical experience study. Can. Urol. Assoc. J. 2021, 15, 55.
- Carriуn-Lуpez P., Martнnez-Ruiz J., Gimйnez-Bachs J.M., Fernбndez-Anguita P.J., Dнaz de Mera-Sбnchez Migallуn I., Legido-Gуmez O., Rico-Marco S., Lorenzo-Sбnchez M.V., Salinas-Sбnchez A.S. Cost-Effectiveness of a Sublingual Bacterial Vaccine for the Prophylaxis of Recurrent Urinary Tract Infections. Urol Int. 2022;106(7):730-736. doi: 10.1159/000521772. Epub 2022 Feb 7. PMID: 35130558; PMCID: PMC9393836.
Підготувала Дарина Чернікова