23 квітня, 2025
Доброякісні захворювання молочних залоз. Тактика ведення аномальних результатів обстеження молочних залоз
Стандарт медичної допомоги
Скарги з боку молочних залоз є однією з найбільш частих причин звернення по медичну допомогу. При цьому деякі доброякісні захворювання молочних залоз пов’язані зі збільшенням ризику раку молочної залози (РМЗ), що вимагає повного та всебічного обстеження з метою своєчасного виявлення та лікування доброякісної патології молочних залоз. Цей стандарт медичної допомоги призначений для забезпечення організації надання медичної допомоги пацієнтам із доброякісними захворюваннями молочних залоз на всіх етапах ведення.
Загальна частина
Коди стану або захворювання.
НК 025:2021 «Класифікатор хвороб та споріднених проблем охорони здоров’я»:
N60. Доброякісна дисплазія молочної залози
N60.0 Солітарна кіста молочної залози
N60.1 Дифузна кістозна мастопатія
N60.2 Фіброаденоз молочної залози
N60.3 Фібросклероз молочної залози
N60.4 Ектазія проток молочної залози
N60.8 Iнші доброякісні дисплазії молочної залози
N60.9 Доброякісна дисплазія молочної залози, неуточнена
N61. Запальні хвороби молочної залози
N63. Неуточнене утворення в молочній залозі
N64. Iнші хвороби молочної залози
N64.3 Галакторея, не пов’язана з пологами
N64.4 Мастодинія
N64.5 Iнші ознаки та симптоми, що стосуються молочної залози
N64.8 Iнші уточнені ураження молочної залози
N64.9 Ураження молочної залози, не уточнене
Панель 1
Збір анамнезу при скаргах, пов’язаних із молочними залозами. Оцінка факторів ризику злоякісної трансформації тканин молочної залози
При зборі анамнезу необхідно визначити наявність/відсутність факторів ризику
злоякісної трансформації тканин молочної залози, серед яких:
- сімейні/генетичні фактори:
- спадковий рак молочної залози та яєчників (BRCA1/2);
- синдром Лі – Фраумені (TP53);
- синдром Пейтца – Єгерса (STK11);
- синдром Коудена (PTEN);
- спадковий дифузний рак шлунка (CDH1);
- носійство мутацій низькопенетрантних генів (PALB2, CHEK2);
- особливості гінекологічного анамнезу:
- відсутність пологів;
- подовжений інтервал між менархе та віком першого живонародження (раннє менархе або пізній вік першого живонародження);
- менархе у більш молодому віці або пізня менопауза;
- наявність проліферативних уражень з атипією в анамнезі (атипова протокова гіперплазія, атипова лобулярна гіперплазія, LCIS);
- підвищена щільність молочної залози;
- раннє торакальне опромінення у віці до 30 років, що охоплює ділянку грудей/молочні залози;
- гіперпролактинемія (у жінок у постменопаузі – рівні пролактину по верхній межі
референтних значень та вище); - куріння;
- надмірне вживання алкоголю;
- високий індекс маси тіла та ожиріння;
- недостатня фізична активність, сидячий спосіб життя;
- незбалансоване харчування;
- недостатність і дефіцит вітаміну D3.
Розділ І. Організація надання медичної допомоги при доброякісних захворюваннях молочних залоз
Положення стандарту. Жінки з підозрою на доброякісні захворювання молочних залоз (ДЗМЗ) мають бути направлені до закладів охорони здоров’я (ЗОЗ), що надають спеціалізовану медичну допомогу. Діагностика, лікування та подальше спостереження за пацієнтками зі скаргами, пов’язаними з молочними залозами, здійснюються лікарем акушером-гінекологом та/або лікарем-онкологом, лікарем хірургом-онкологом або іншим підготовленим фахівцем (лікарем-ендокринологом, лікарем-хірургом) залежно від клінічної ситуації.
Обґрунтування. ДЗМЗ тривалий час знаходились в тіні сучасних алгоритмів попередження та зниження ризику раку і потребують сучасного регламентованого мультидисциплінарного підходу. Окрім ДЗМЗ прискіпливої уваги вимагають ураження молочної залози з невизначеним потенціалом злоякісності (ураження В3).
З огляду на малосимптомний перебіг багатьох ДЗМЗ і уражень В3, часто зазначені захворювання вперше можуть бути виявленні під час проведення скринінгу РМЗ відповідно до Порядку скринінгу і ранньої діагностики раку молочної залози та моніторингу стану здоров’я пацієнток із груп ризику, затвердженого наказом Міністерства охорони здоров’я України від 5 серпня 2024 року № 1368, зареєстрованого в Міністерстві юстиції України 20 серпня 2024 року за № 1273/42618.
Критерії якості медичної допомоги
Обов’язкові:
1) наявність узгодженого клінічного маршруту пацієнта (КМП), що координує та інтегрує медичну допомогу для забезпечення своєчасного направлення, діагностики та лікування пацієнтів із ДЗМЗ та зі знахідками при фізикальному та/або інструментальному обстеженні молочних залоз;
2) забезпечення інформованості пацієнтки щодо:
– її стану з акцентом на довгострокових наслідках для здоров’я;
– плану обстеження, лікування та подальшого спостереження, переваг і недоліків, пов’язаних із кожним методом, що застосовується при веденні пацієнток із ДЗМЗ;
– контактів для отримання додаткової інформації та консультації;
3) при виписці зі стаціонару пацієнткам із ДЗМЗ надаються рекомендації щодо подальшого спостереження;
4) у випадках виявлення осіб, постраждалих від домашнього насильства, або осіб, які, ймовірно, постраждали від домашнього насильства, насильства за ознакою статі, допомога надається відповідно до галузевих стандартів у сфері охорони здоров’я;
Бажані:
5) під час прийому пацієнток незалежно від причини звернення лікарем акушером-гінекологом проводиться клінічне обстеження молочних залоз;
6) ЗОЗ, що надають допомогу пацієнткам із ДЗМЗ, розміщують інформаційні матеріали стосовно факторів ризику і проявів захворювань молочної залози, методики самообстеження грудей і профілактики РМЗ.
Розділ ІІ. Діагностична тактика при аномальних результатах обстеження молочних залоз
Положення стандарту. Усі пацієнти зі скаргами з боку молочних залоз підлягають фізикальному та, за необхідності, інструментальному обстеженню. Під час діагностики є необхідним ретельний збір анамнестичних даних, який має включати визначення факторів ризику злоякісної трансформації тканин молочної залози.
Обсяг застосування спеціальних діагностичних методів залежить від статі та віку пацієнта і ґрунтується на виявленні ключових скарг і знахідок при обстеженні. До таких методів відповідно до показань належать:
- методи візуалізації: ультразвукове дослідження (УЗД) молочних залоз, мамографія, магнітно-резонансна томографія (МРТ) молочних залоз;
- морфологічні методи: тонкоголкова аспіраційна біопсія, товстоголкова біопсія, трепан-біопсія, ексцизійна біопсія.
Обґрунтування. При діагностиці ДЗМЗ застосовується синдромальний підхід, який враховує провідні скарги/знахідки з боку молочної залози – масталгія, наявність пальпованих утворень, виділення із сосків тощо. Дотримання чіткого алгоритму КМП дозволяє діагностувати ДЗМЗ та/або ураження ВЗ:
- непроліферативні ураження молочної залози;
- проліферативні ураження молочної залози без атипії, у тому числі фіброаденоми (ФА), помірна/виражена гіперплазія звичайного типу, внутрішньопротокова папілома (ВПП);
- радіальний рубець/комплексне склерозуюче ураження;
- атипія плоского епітелію;
- атипова гіперплазія;
- тубулярні аденоми;
- філоїдні пухлини;
- лобулярна карцинома in situ (LCIS);
- інші ураження, у тому числі запальні захворювання молочних залоз і зміни шкіри грудей.
ДЗМЗ можуть мати симптомний або безсимптомний перебіг, при цьому анамнестичним і фізикальним ознакам часто бракує чутливості та специфічності, що зумовлює застосування низького діагностичного порога до використання інструментальних методів обстеження при підозрі на доброякісні захворювання та/або ураження ВЗ.
Критерії якості медичної допомоги
Обов’язкові:
1) у всіх пацієнтів зі скаргами з боку молочних залоз під час збору анамнестичних даних слід визначити наявність факторів ризику злоякісної трансформації молочної залози (див. панель 1). Також визначити профіль безпеки використання лікарських засобів, що містять естрогени та гестагени (комбіновані оральні контрацептиви [КОК], менопаузальна гормональна терапія [МГТ]), наведені в табл. 1;
2) за наявності відповідних показань використовуються методи візуалізації молочних залоз. При формуванні заключення УЗД, мамографії і МРТ молочних залоз необхідно проводити оцінку за категоризацією BI-RADS (табл. 2);
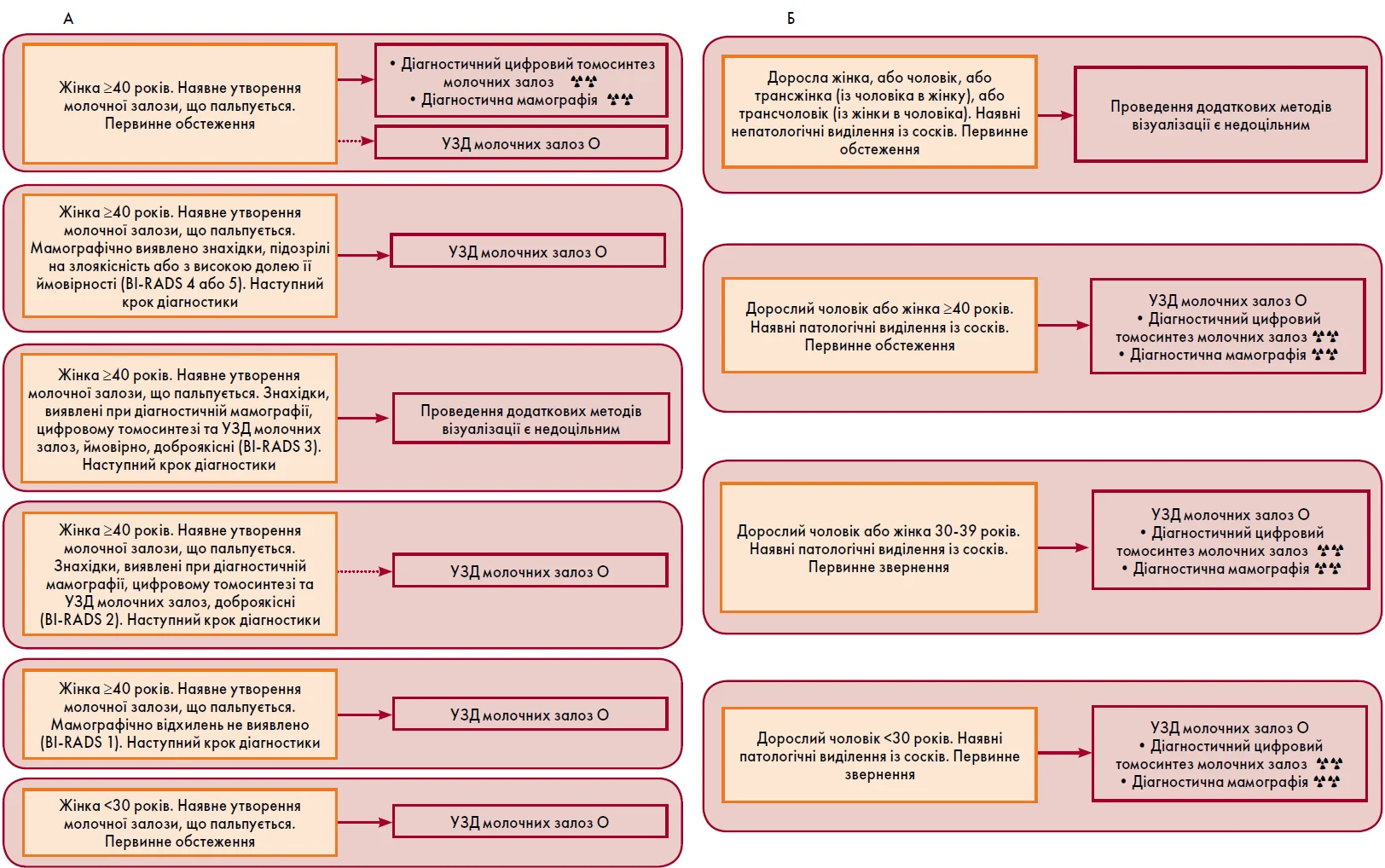
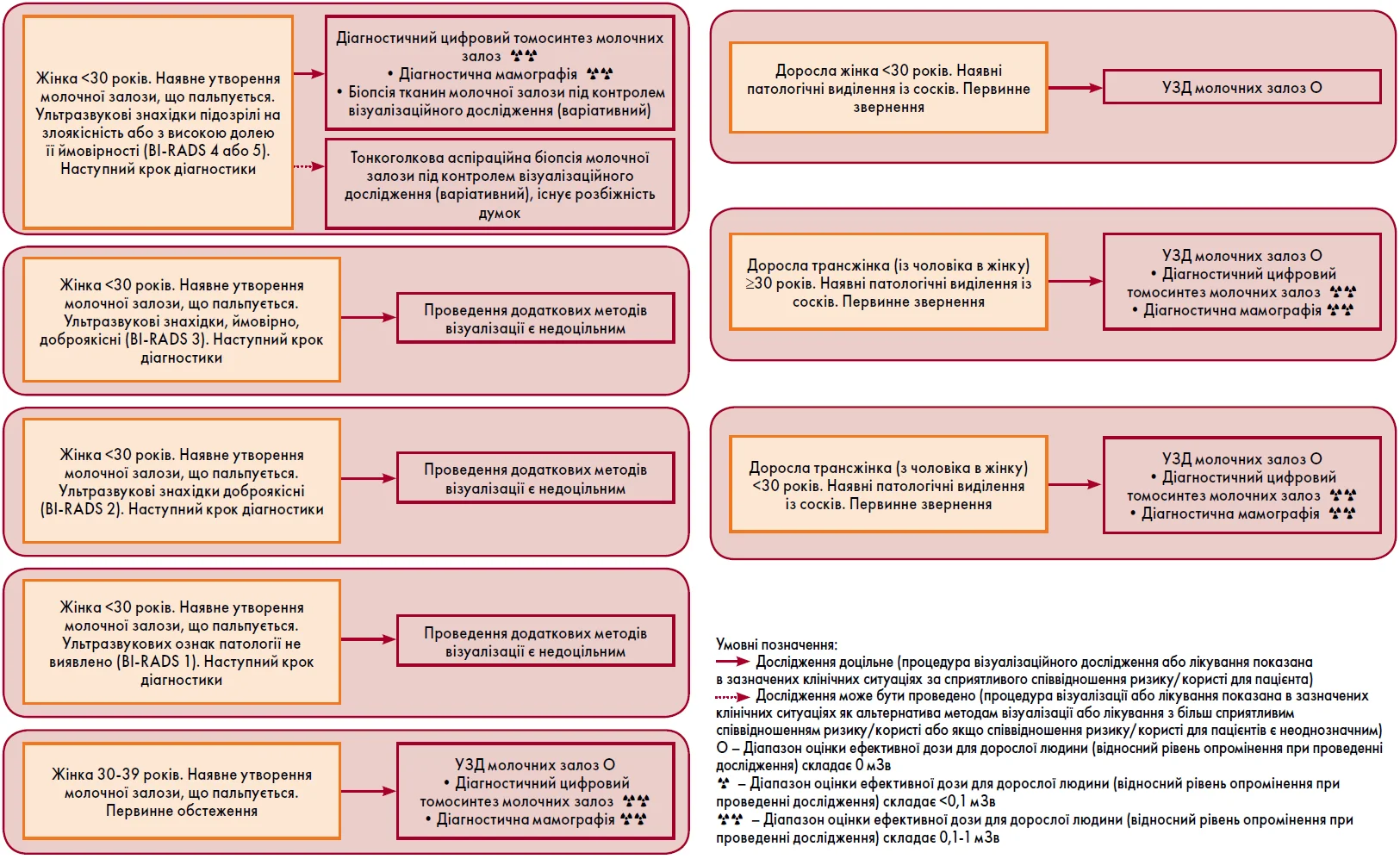
3) у випадках відповідності клінічній ситуації одному із варіантів, наведених на рис. 1 (А, Б), проводиться персоніфікований підбір методів візуалізації із використанням зазначених у ньому алгоритмів;
4) у разі наявності масталгії слід виключити медикаментозно опосередковані причини появи болю в грудях (прийом КОК, антидепресантів тощо). Подальший пошук причин масталгії (циклічна, нециклічна, вторинна) здійснюється відповідно до алгоритму, представленого на рис. 2;
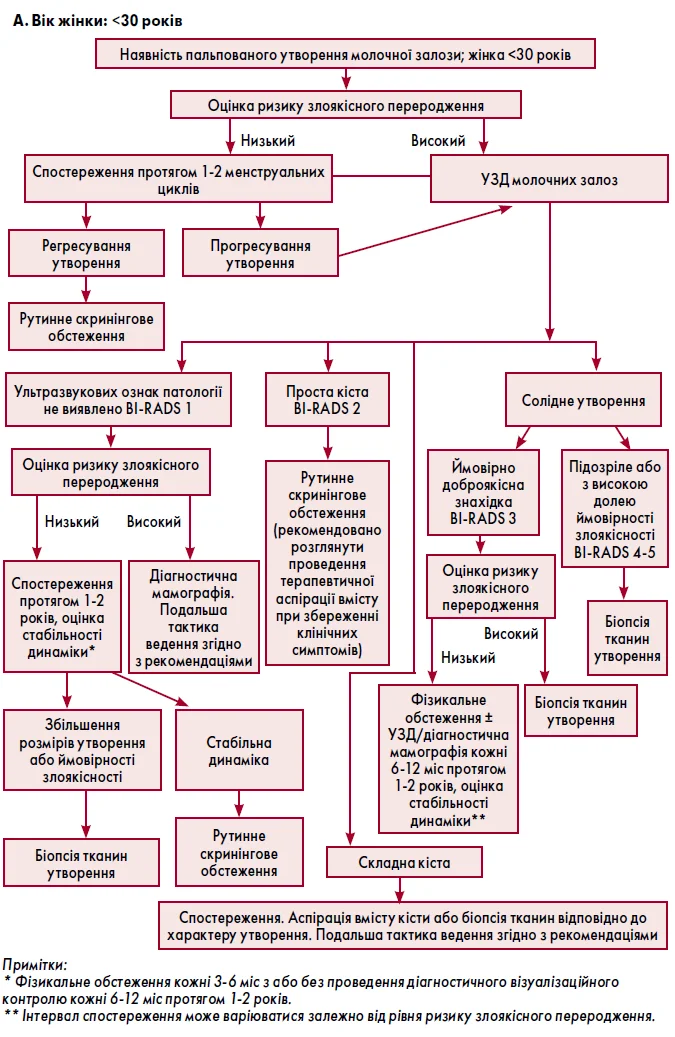
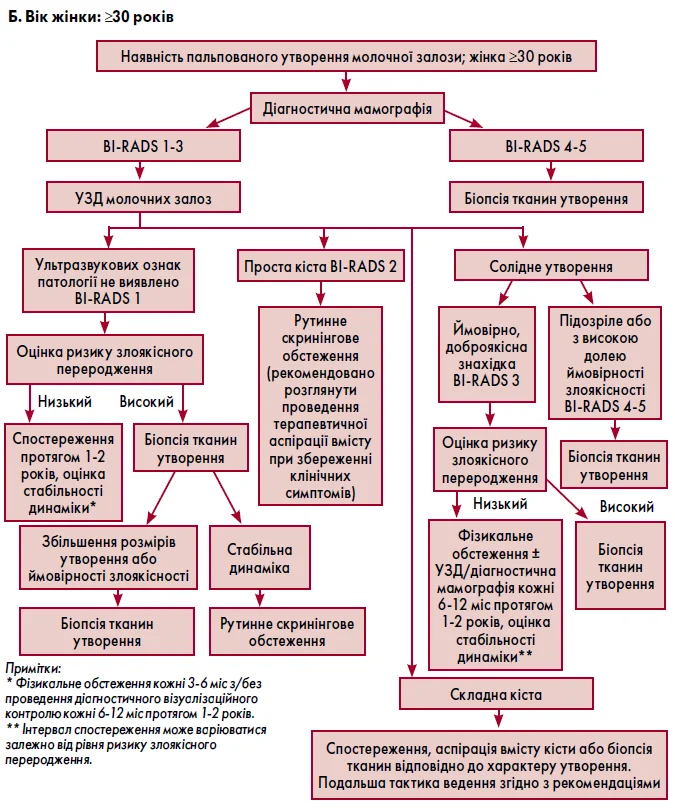
5) діагностична тактика за наявності пальпованих утворень молочної залози залежить від віку пацієнтки (<30 років або ≥30 років) та визначається алгоритмами, новеденими на рис. 3 (А, Б);
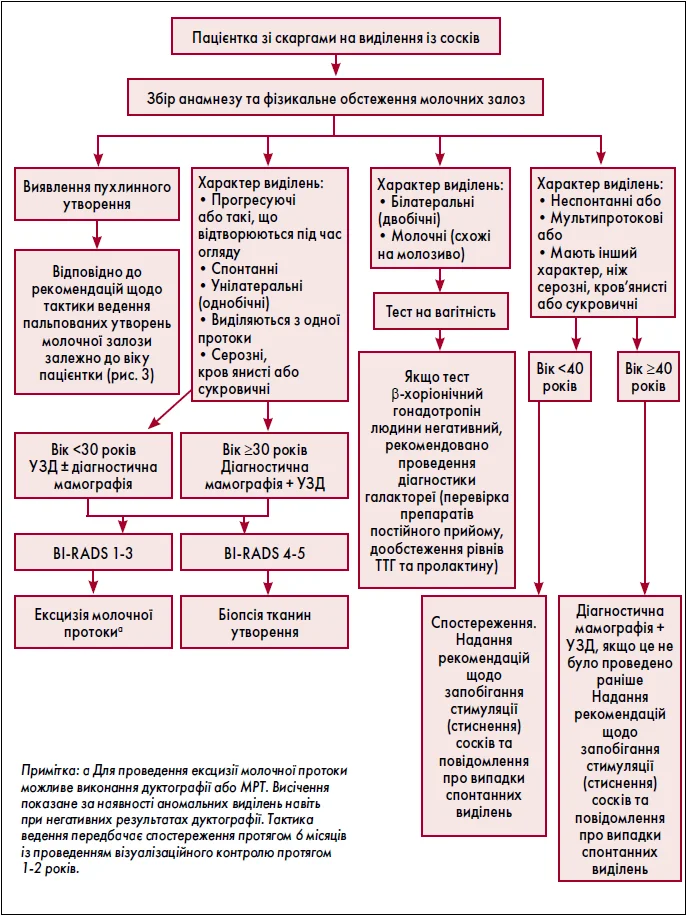
6) для діагностики виділень із молочних залоз залежно від їхнього характеру використовується алгоритм тактики ведення таких жінок (рис. 4);
7) у разі виконання біопсії пацієнти мають бути поінформовані, що відразу після закінчення втручання і протягом 1-2 діб після нього можливі незначний біль і поява синців. За необхідності доцільно розглянути адекватне знеболення;
8) диференціальна діагностика утворень молочної залози має враховувати виключення низки станів (табл. 3);
9) при діагностичному обстеженні слід виключити наявність запальних захворювань молочних залоз і змін шкіри грудей (табл. 4, 5);
Бажані:
10) за наявності виділень із молочних залоз доцільно розглянути можливість цитологічного дослідження виділень (стандартні препарати та препарати рідинної цитології, забарвлені за Папаніколау та Diff-Quick);
11) жінкам зі скаргами, пов’язаними з молочними залозами, слід рекомендувати лабораторне обстеження на визначення рівню пролактину та тиреотропного гормону (ТТГ) у крові.
Рис. 1. Персоніфікований підбір методів візуалізації у пацієнток зі скаргами, пов’язаними з молочними залозами: А – пальповані утворення молочної залози; Б – виділення із сосків
Рис. 2. Тактика ведення жінок із масталгією
Рис. 3. Тактика ведення жінок із наявним утворенням молочної залози, що пальпується
Рис. 4. Тактика ведення жінок із виділеннями із сосків
|
Таблиця 1. Профіль безпеки препаратів статевих гормонів щодо молочної залози |
|||
|
Лікарський засіб |
Безпека |
Побічні дії, пов’язані з молочною залозою |
Тактика ведення. Обмеження застосування |
|
КОК |
Обов’язкове консультування лікаря-гінеколога перед призначенням КОК |
Циклічна масталгія (незначна кореляція Галакторея (рідко) |
Застосування безперервного режиму дозування (пропуск тижня без гормонів) може полегшити симптоми циклічної масталгії |
|
МГТ |
Безпека застосування комбінованої МГТ залежить від гестагенного компонента: – найвищий ризик – похідні нортестостерону – найнижчий ризик – дидрогестерон, мікронізований прогестерон У жінок, які перенесли гістеректомію й отримують естрогени без протипоказань у якості МГТ, відсутній підвищений ризик РМЗ Використання лише естрогенної монотерапії та короткострокове (<5 років) використання комбінованих препаратів естрогену/прогестагену в минулому не пов’язане з підвищеним ризиком РМЗ |
МГТ має значно нижчі ризики щодо індукції РМЗ, ніж вважалося раніше Підвищена частота аномальних мамограм та подвоєння ризику доброякісних проліферативних захворювань молочної залози серед пацієнток, які отримують естрогени у якості монотерапії |
МГТ не рекомендована пацієнткам, які приймають тамоксифен, анастрозол або екземестан поза межами клінічних досліджень |
|
|
Тривалий прийом комбінованих препаратів МГТ не впливає на значне посилення болю з часом та на зміну характеру болю при пероральному або трансдермальному застосуванні |
Розвиток масталгії у жінок у постменопаузі з початком прийому МГТ |
Жінкам у постменопаузі, у яких розвинулася масталгія з початком МГТ, рекомендовано розглянути доцільність застосування гормональної терапії або зниження дози естрогену |
Розділ ІІІ. Ведення пацієнток із доброякісними захворюваннями молочних залоз
Положення стандарту медичної допомоги. Тактика ведення пацієнток із ДЗМЗ, у тому числі з ураженнями В3, залежить від віку та результатів клінічного й інструментального обстеження. Вибір алгоритмів лікування та подальшого спостереження має враховувати оцінку факторів ризику злоякісної трансформації виявлених утворень.
Обґрунтування. ДЗМЗ і ураження В3 включають гетерогенну групу станів, що пояснює відсутність єдиної тактики їх ведення. Необхідним є персоніфікований підбір лікування та подальшого спостереження таких пацієнтів з огляду на стать, вік і особливості клінічної картини захворювання.
Критерії якості медичної допомоги
Обов’язкові:
1) за наявності масталгії після визначення її причини використовуються підходи до етіотропного та/або симптоматичного лікування (рис. 2). У разі виключення всіх можливих причин масталгії з боку молочної залози пацієнток скеровують до лікарів суміжного профіля;
2) при визначенні пальпованого утворення молочної залози тактика лікування та подальшого спостереження обирається відповідно до віку пацієнтки (рис. 3);
3) у разі встановлення причини синдрому виділень із молочної залози використовується алгоритм тактики ведення відповідно до рис. 4;
4) верифікація інших ДЗМЗ вимагає підбору тактики подальшого ведення (табл. 3);
5) у разі виявлення запальних захворювань молочної залози та змін шкіри грудей пацієнток направляють до лікарів суміжних спеціальностей;
6) тактика ведення та обсяг хірургічного втручання у разі наявності показань до оперативного лікування ДЗМЗ і уражень В3 вимагає персоніфікованого підходу (панель 2);
7) пацієнткам надаються рекомендації щодо подальшого спостереження та вживання заходів, спрямованих на зниження ризику РМЗ;
Бажані:
8) з метою підтримки рекомендованого профілактичного режиму харчування доцільним є додавання до дієти вітамінів і мікронутрієнтів із антипроліферативною дією.
Дата оновлення стандарту – 2030 рік.
Затверджено наказом МОЗ України 26 березня 2025 року № 535.
|
Таблиця 2. Класифікація систем звітності даних візуалізаційних досліджень молочної залози та алгоритм подальшого ведення |
||||
|
Категорія оцінки BI-RADS |
Імовірність раку |
Ведення |
||
|
Мамографія* |
УЗД* |
МРТ* |
||
|
Категорія 0: Неповна — потрібна додаткова візуалізаційна оцінка (та/або попередні мамографії для порівняння у випадку мамографічного скринінгу) |
Дані відсутні |
Виклик на додаткове візуалізаційне дослідження, порівняння з попереднім(и) обстеженням(ями) або і те, й інше |
Виклик на додаткове візуалізаційне дослідження |
Рекомендувати додаткове обстеження: мамографію або прицільну ультразвукову діагностику |
|
Категорія 1: Негативна |
Практично 0% ймовірність злоякісних новоутвореньа |
Рутинний мамографічний скринінг |
Рутинний скринінг |
Рутинний МРТ-скринінг молочної залози, якщо кумулятивний ризик протягом життя ≥20% |
|
Категорія 2: Доброякісні |
Практично 0% ймовірність злоякісних новоутвореньа |
Рутинний мамографічний скринінг |
Рутинний скринінг |
Рутинний МРТ-скринінг молочної залози, якщо кумулятивний ризик протягом життя ≥20% |
|
Категорія 3: Імовірно доброякісні |
>0%, але ≤2% ймовірність злоякісного новоутворення |
Короткоінтервальна (6‑місячна) контрольна мамографія або мамографія для тривалого спостереження |
Короткострокове (6‑місячне) або тривале спостереження |
Короткострокове (6‑місячне спостереження |
|
Категорія 4: Підозрілі |
>2%, але <95% ймовірності злоякісного новоутворення |
Біопсія тканин |
||
|
б Категорія 4A: Низька підозра на злоякісність |
Ймовірність злоякісної пухлини від >2% до ≤10% |
|||
|
б Категорія 4В: Помірна підозра на злоякісність |
Ймовірність злоякісного новоутворення від >10% до ≤50% |
|||
|
бКатегорія 4C: Висока підозра на злоякісність |
Ймовірність злоякісних новоутворень від >50% до <95% |
|||
|
Категорія 5: Висока ймовірність злоякісної пухлини |
≥95% ймовірність злоякісного новоутворення |
Біопсія тканин |
||
|
Категорія 6: Відома злоякісна пухлина, підтверджена біопсією |
Дані відсутні |
Хірургічне видалення, коли це доцільно |
||
|
Примітки: *Виявлені результати візуалізаційних досліджень мають корелювати з даними клінічного обстеження, якщо ця система використовується для визначення тактики лікування. Якщо результати обстеження та візуалізаційної діагностики не узгоджуються, слід розглянути можливість подальшого обстеження, включаючи біопсію. Прикладами розбіжностей є пальповане утворення при візуалізації BI-RADS 1, виявлення BI-RADS 2 або BI-RADS 3 в іншому місці, ніж при обстеженні, а також підозріле утворення при обстеженні з результатом BI-RADS 2. аBI-RADS 1 і BI-RADS 2 вказують на те, що при візуалізаційному дослідженні не було діагностовано злоякісних новоутворень. Однак важливо зазначити, що чутливість візуалізації молочної залози для виявлення раку залежить від методу дослідження та щільності молочної залози. бBI-RADS 4A‑4C застосовуються лише до результатів мамографії та УЗД. |
||||
|
Таблиця 3. Діагностичний пошук і тактика ведення доброякісних утворень молочної залози та уражень В3 |
|||
|
Групи уражень |
Сутність уражень |
Діагностичний пошук. Методи візуалізації |
Тактика ведення |
|
Непроліферативні ураження молочної залози: – прості кісти – легка гіперплазія звичайного типу – апокринні зміни |
Переважно доброякісні, не пов’язані з підвищеним ризиком розвитку РМЗ. Можуть виявлятися як артефакт за результатами пункційної біопсії (виконаної за іншими показаннями) |
Огляд УЗД молочних залоз |
Рутинне клінічне спостереження (для простих кіст). Прийняття рішення щодо аспірації або візуалізаційного спостереження протягом 1-2 років після ретельного обговорення з пацієнткою, виходячи з її уподобань або переважаючих клінічних показань (для ускладнених кіст). Біопсія тканин утворення (для непростих кіст із кістозними та солідними компонентами та результатами візуалізації BI-RADS 4-5). |
|
Проліферативні ураження молочної залози без атипії: – помірна/виражена гіперплазія звичайного типу – внутрішньопротокова папілома |
Помірна гіперплазія звичайного типу має вогнищеве потовщення шарів епітеліальних клітин протоки (≤4), які не заповнюють протоку. Не пов’язана з підвищеним ризиком розвитку РМЗ. Гіперплазія звичайного типу – багатопротокові епітеліальні клітинні шари (>4), які заповнюють усю протоку, але не мають цитологічної атипії Асоціюється з низьким/помірно підвищеним ризиком розвитку РМЗ Усі ВПП – з/без АПГ – належать до уражень B3 |
||
|
Фіброаденоми (ФА) – параканалікулярні – змішані – прості – складні |
ФА – доброякісне невелике (1-2 см) щільне, чітко обмежене рухоме утворення з проліферацією епітеліальних і стромальних елементів. Виникає у жінок різного віку, переважно молодшого |
Огляд, фізикальне обстеження. УЗД молочних залоз. Біопсія (тонкоголкова або трепан-біопсія) з подальшою обов’язковою гістологічною верифікацією. Диференціальна діагностика з кістою/солідним утворенням |
Спостереження кожні 6 міс протягом принаймні 2 років. Хірургічне лікування – за нестабільності динаміки (збільшення розмірів >3 см, клінічна симптоматика), розглядається при розташуванні ФА за соском, близько до вивідних проток молочної залози. Хірургічна резекція – за наявності розбіжностей між даними візуалізаційного дослідження та клінічним обстеженням і результатами біопсії або якщо атипія, протокова карцинома in situ (DCIS), LCIS або інвазивна карцинома виявлені за допомогою трепан-біопсії |
|
– гігантська ФА |
Гігантська ФА – велике (10-11 см) щільне, чітко обмежене утворення з епітеліальних і стромальних елементів із розгалуженими залозистими елементами з великою клітинністю строми, що деформує молочну залозу. Виникає переважно у підлітків, становить 4% усіх діагностованих ФА у дорослих |
||
|
Ураження В3 |
|||
|
Радіальний рубець/комплексне склерозуюче ураження |
Радіальний рубець – додаткове псевдопроліферативне ураження, яке може приховувати або сприяти розвитку атипових проліферацій. Часто діагностується як артефакт (випадкова знахідка на біопсії, мамографії, томографії) |
Товстоголкова біопсія під ультразвуковим контролем. Вакуум-асистована біопсія під стереотаксичним контролем або томосинтезом (особливо за наявності мікрокальцинатів) МРТ молочних залоз (із метою виключення інвазивної злоякісної пухлини, пов’язаної з радіальним рубцем) |
Зазвичай хірургічне; подальше зниження ризику (тамоксифен) не показане. Ретельне рутинне спостереження в динаміці |
|
Склерозуючий аденоз |
Збільшення кількості або розміру залозистих компонентів у часточкових одиницях Асоціюється з низьким/помірно підвищеним ризиком розвитку РМЗ |
||
|
Внутрішньопротокова папілома |
Невеликі (від 2-4 мм до 5 см) утворення в молочній протоці, які можуть бути поодинокими й розташовуватися по центру біля отвору протоки або множинними й розташовуватися по периферії молочної залози |
Огляд Визначення виділень із сосків (прозорі, серозні, кров’янисті) Товстоголкова біопсія. Імуногістохімічна верифікація (р63, важкий ланцюг міозину гладкої мускулатури, кальпонін) |
Хірургічне лікування при виявленні атипових клітин при товстоголковій біопсії. Обсяг операції: – центральна ВПП із виділеннями із соска: відкрита резекція протоки з пухлиною(-ами), іноді з резекцією прилеглої дольки або секторальною резекцією; – периферична солітарна ВПП: відкрита операція або вакуум-асистована біопсія. Множинні ураження або такі, що охоплюють усю молочну залозу, – розглянути профілактичну мастектомію або підшкірну мастектомію з/без реконструкції |
|
Атипія плоского епітелію |
В ізольованій формі має низький ризик місцевого рецидиву та прогресування до карциноми |
УЗД молочних залоз Мамографія |
Мамографія щорічно. Хірургічне видалення лише у випадках патолого-рентгенологічної невідповідності, масивного ураження або залишкових кальцифікатів після біопсії |
|
Атипова гіперплазія: – атипова протокова гіперплазія (АПГ) – атипова лобулярна гіперплазія |
АПГ являє собою протокові або лобулярні елементи з однорідними клітинами та втратою апікально-базальної орієнтації клітин, гістологічно має вигляд невеликого вогнища моногенної епітеліальної внутрішньопротокової проліферації низького ступеня, що не перевищує максимальний діаметр 2 мм. Зазвичай є випадковою знахідкою під час патоморфологічної оцінки аномальних результатів мамографії або утворень молочної залози. Найчастіше асоціюється з кластерними кальцифікатами, утвореннями або асиметричною щільністю на мамографії. Асоційована з підвищеним ризиком інвазивного раку ураженої та контрлатеральної молочної залози |
УЗД молочних залоз. МРТ молочних залоз. Біопсія голкою 14G під візуалізаційним контролем або вакуум-асистована біопсія з використанням голки від 14G до 9G |
Хірургічне лікування, якщо АПГ діагностовано під час товстоголкової біопсії або вакуум-асоційованої біопсії. Вакуум-асистована ексцизія під візуалізаційним контролем при розмірах <15 мм. Динамічна тактика: – самообстеження Спостереження, клінічне обстеження молочних залоз кожні 6-12 міс Мамографія щорічно. Терапія зниження ризику – опціонально: – тамоксифен (у жінок у пізньому репродуктивному віці/постменопаузі); – інгібітори ароматази (у жінок у постменопаузі). Консультування щодо ведення здорового способу життя, включаючи збільшення обсягу фізичної активності, підтримку належної маси тіла, зменшення вживання алкоголю. Щорічну МРТ можна розглядати для скринінгу РМЗ у жінок з атиповою гіперплазією віком ≥30 років |
|
Лобулярна карцинома in situ – класична LCIS – квіткова LCIS – плеоморфна LCIS |
LCIS – це неопластичне ураження з неінвазивною проліферацією дискогезивних клітин, що виникають у кінцевій часточковій протоці, не має вигляду утворення |
Патоморфологічна знахідка, не має вигляду утворення або специфічних аномалій при візуалізації молочної залози |
Хірургічне видалення при діагностуванні LCIS під час біопсії, для окремої групи пацієнток методом вибору може бути спостереження. Пацієнтки з плеоморфною LCIS повинні проходити лікування згідно з рекомендаціями щодо РМЗ. Можливе проведення профілактичої мастектомії або хіміопрофілактики (хіміопревенції). Динамічна тактика: – мамографія щорічно – клінічне обстеження молочних залоз кожні 6-12 міс починаючи з моменту встановлення діагнозу, але не раніше 30 років – розглянути можливість МРТ щорічно Терапія зниження ризику – опціонально: – тамоксифен (у жінок у пізньому репродуктивному віці/постменопаузі); – інгібітори ароматази (у жінок у постменопаузі) |
|
Тубулярні аденоми |
Ущільнення молочної залози, патоморфологічно являють собою доброякісні залозисті клітини з мінімальною кількістю стромальних елементів. Лактуючі аденоми – пальповані ущільнення, що виникають в період вагітності та лактації |
Огляд, фізикальне обстеження. УЗД молочних залоз. Біопсія тканин утворення з подальшою верифікацією |
|
|
Філоїдні пухлини |
Рідкісні фіброепітеліальні пухлини щільної консистенції, обмежено рухомі, зі швидким ростом та широким діапазоном біологічної поведінки – від доброякісного утворення молочної залози зі схильністю до місцевих рецидивів до саркоми, здатної до виникнення віддалених метастатичних захворювань (5%) |
УЗД молочних залоз (визначення солідного характеру утворення, диференціальна діагностика ускладнена). Ексцизійна біопсія з висіченням широкого поля (>1 см) незміненої оточуючої тканини |
|
|
Таблиця 4. Діагностичний пошук і тактика ведення запальних захворювань молочної залози |
|||
|
Групи уражень |
Сутність уражень |
Діагностичний пошук. Методи візуалізації |
Тактика ведення |
|
Інфекційний мастит: — непологовий — післяпологовий |
Найчастіше виникає під час лактації, спричинений Staphylococcus spp. Інші мікроорганізми включають стрептококи та епідермальні стафілококи, ентерококи та анаероби |
Збір анамнезу для характеристики симптомів і виявлення факторів ризику РМЗ. Клінічне обстеження молочних залоз. Додаткова візуалізаційна діагностика (починаючи з УЗД) |
Рекомендовано лікування інфекцій молочних залоз у жінок, які не годують грудьми, емпірично амоксициліном і клавулановою кислотою або (у пацієнток з алергією на пеніцилін) еритроміцином і метронідазолом. При підозрі на абсцес або при стійких симптомах після емпіричної антибіотикотерапії слід виконати візуалізаційне дослідження молочної залози, щоб виключити іншу патологію, а за його результатами виконати біопсію |
|
Перидуктальний мастит |
Характеризується вогнищевим запаленням періареолярної ділянки, може супроводжуватись утворенням абсцесу/фістули протоки молочної залози. Виникає переважно у молодих жінок-курців і може мати рецидивуючий характер |
Емпірична антибіотикотерапія, включаючи анаеробне покриття, із переходом на етіотропну антибактеріальну терапію за результатами бактеріологічного дослідження. Хірургічне лікування з висіченням уражених проток при утворенні нориць/рецидивуванні |
|
|
Абсцес молочної залози |
Хірургічне лікування шляхом аспірації або розрізу та дренування з подальшим бактеріологічним дослідженням для призначення етіотропної антибіотикотерапії |
||
|
Таблиця 5. Діагностичний пошук і тактика ведення змін шкіри грудей |
|||
|
Групи уражень |
Сутність уражень |
Діагностичний пошук. Методи візуалізації |
Тактика ведення |
|
Дерматологічні захворювання: – псоріаз – екзема – контактний дерматит – кандидоз шкіри |
Кандидозні інфекції мають класичний вигляд запалення шкіри із супутніми ураженнями |
Збір анамнезу для характеристики симптомів і виявлення факторів ризику РМЗ. Клінічне обстеження молочних залоз. Додаткова візуалізаційна діагностика (починаючи з УЗД) |
Рекомендовано лікування шкірних інфекцій молочних залоз у жінок, які не годують грудьми, емпірично амоксициліном і клавулановою кислотою або (у пацієнток з алергією на пеніцилін) еритроміцином і метронідазолом. При підозрі на абсцес або стійких симптомах після емпіричної антибіотикотерапії слід виконати візуалізаційне дослідження молочної залози, щоб виключити іншу патологію, а за його результатами виконати біопсію |
|
Хвороба Педжета |
Рідкісний рак соска та ареоли, асоційований із DCIS або інвазивною карциномою (85% випадків) та іншими типами інвазивного РМЗ. Основні ознаки: виразки, кірки або лущення на соску, з поширенням на ареолу; сосок втягнутий/або гіперпігментований; біль, печіння або свербіж ураженої ділянки. Виразки шкіри на інших ділянках молочної залози викликають занепокоєння щодо інших злоякісних новоутворень молочної залози |
Збір анамнезу з визначенням часу, перебігу та тривалості симптомів, їх характеристикою; виявлення факторів ризику РМЗ. Клінічне обстеження молочних залоз. Діагностична візуалізаційна діагностика (УЗД, діагностична мамографія). Подальша тактика згідно з результатами дообстеження |
Оцінка ризику РМЗ. При ураженні В3 слід рекомендувати знизити вагу пацієнткам з надлишковою масою тіла/ожирінням; підвищити рівень фізичної активності (30 хв на день або 150 хв на тиждень помірних або інтенсивних фізичних навантажень). Подальша тактика згідно з результатами дообстеження: – BI-RADS 1-3 – пункційна біопсія аномальної шкіри або соска, якщо клінічне занепокоєння зберігається; – BI-RADS 4-5 – товстоголкова біопсія та, можливо, пункційна біопсія або хірургічне видалення ураження шкіри |
|
Поверхневий тромбофлебіт бічної грудної вени (хвороба Мондора) |
Рідкісне захворювання, яке викликає нециклічний біль і болісність молочних залоз, характеризується наявністю пальпованого тяжу, який спочатку є червоним і болісним, а згодом супроводжується лінійною шкірною ямочкою |
Збір анамнезу, характеристика симптомів, виявлення факторів ризику РМЗ. Клінічне обстеження молочних залоз. Додаткова візуалізаційна діагностика відповідно до віку |
Подальша тактика залежно від отриманих результатів |
Панель 2
Тактика ведення деяких граничних уражень молочної залози та утворень високого ризику
- Фіброепітеліальні ураження
– Фіброепітеліальні ураження, схожі на фіброаденоми, без мітозів у стромі, розростання строми, ядерного плеоморфізму, фрагментації, інфільтрації жирової тканини або наявність «коментаря патолога, що викликає занепокоєння» – можна безпечно спостерігати. Видалення можливе, але не є обов’язковим, якщо наявне прогресування симптомів, невизначеність діагнозу або бажання пацієнтки.
– Фіброепітеліальні ураження, що сприяють виникненню філоїдних пухлин, слід розглянути для хірургічного втручання.
- Папілярні утворення
– Через відсутність надійних клінічних та візуалізаційних характеристик, що прогнозують прогресування, більшість папілярних утворень слід запропонувати до видалення, особливо за наявності об’ємного ураження, що визначається пальпаторно, або невідповідності між морфологією та візуалізаційними характеристиками.
– Невеликі випадкові доброякісні папілярні ураження з візуалізаційною конкордант-
ністю можуть бути запропоновані для ретельного клінічного спостереження.
- Комплексні склерозовані ураження
– З огляду на типово підозрілу візуалізаційну картину та ймовірність прогресування, хірургічне втручання слід розглядати для більшості комплексних склерозованих уражень.
– Ці утворення можуть не потребувати висічення, якщо вони невеликі та за умови відповідності між морфологією та візуалізаційними характеристиками.
- Атипова протокова гіперплазія
– Хірургічне видалення рекомендоване для більшості випадків АПГ, діагностованих при товстоголковій біопсії.
– АПГ невеликого об’єму та така, що повністю видалена шляхом товстоголкової біопсії, може підлягати спостереженню, якщо результати візуалізаційного дослідження та морфологія узгоджуються. Врахування факторів ризику РМЗ та мультидисциплінарний підхід мають вирішальне значення для прийняття такого рішення.
- Лобулярна неоплазія, включаючи LCIS
– Лобулярна неоплазія, виявлена при товстоголковій біопсії, має бути видалена, якщо візуалізаційні та морфологічні характеристики є непереконливими або дискордантними.
– Для невеликих за об’ємом лобулярних неоплазій із відповідністю між візуалізаційними та морфологічними характеристиками та без інших атипових уражень або уражень високого ризику може бути запропоновано спостереження з використанням спільного з пацієнткою прийняття рішень.
– Для лобулярних уражень, які не були видалені, рекомендоване клінічне та візуалізаційне спостереження. Мультидисциплінарний підхід має вирішальне значення для прийняття цього рішення.
- Плеоморфні LCIS, LCIS із некрозом та інші некласичні ураження мають бути рекомендовані до хірургічного видалення.
- Стовпчастоклітинні ураження
– Хірургічне висічення рекомендоване при атипії плоского епітелію з АПГ, виявленій при товстоголковій біопсії.
– Спостереження та подальше лікування є розумним варіантом для атипії плоского епітелію без супутніх змін.
Друкується у скороченні.
Повна версія за посиланням: https://moz.gov.ua/storage/uploads/ef11e939-1e21-452a-bec2-524e57ba35af/2025_01_20_%D0%A1%D0%9C%D0%94-%D0%94%D0%97%D0%9C%D0%97-%D0%9C%D0%9E%D0%97.pdf
Текст адаптовано та уніфіковано відповідно до стандартів Тематичного випуску Медичної газети «Здоров’я України».
Тематичний номер «Акушерство. Гінекологія. Репродуктологія» № 1 (62) 2025 р.