21 липня, 2023
Сучасні аспекти діагностики ангіоневротичного набряку у дітей
Ангіоневротичний набряк (АН) – це транзиторна судинна реакція, яка супроводжується підвищенням проникності ендотелію, що призводить до екстравазації внутрішньосудинної рідини та набряку тканин підшкірної, підслизової клітковини і глибоких тканин у певній ділянці тіла (M. Maurer, 2022; M. Cicardi, 2013). Точна поширеність АН у педіатричній практиці невідома. Оскільки захворювання має значну варіабельність клінічної картини, це ускладнює встановлення правильного діагнозу та вибір терапевтичного підходу. Серед приблизно 6 тисяч пацієнтів дитячого алергологічного центру лише у 95 випадках (1,6%) було діагностовано АН без пухирів (H.I. Ertoy Karagol et al., 2013). Правильна діагностична тактика дозволяє обрати оптимальний шлях ведення пацієнта, призначення відповідної терапії та планування адекватного подальшого спостереження.
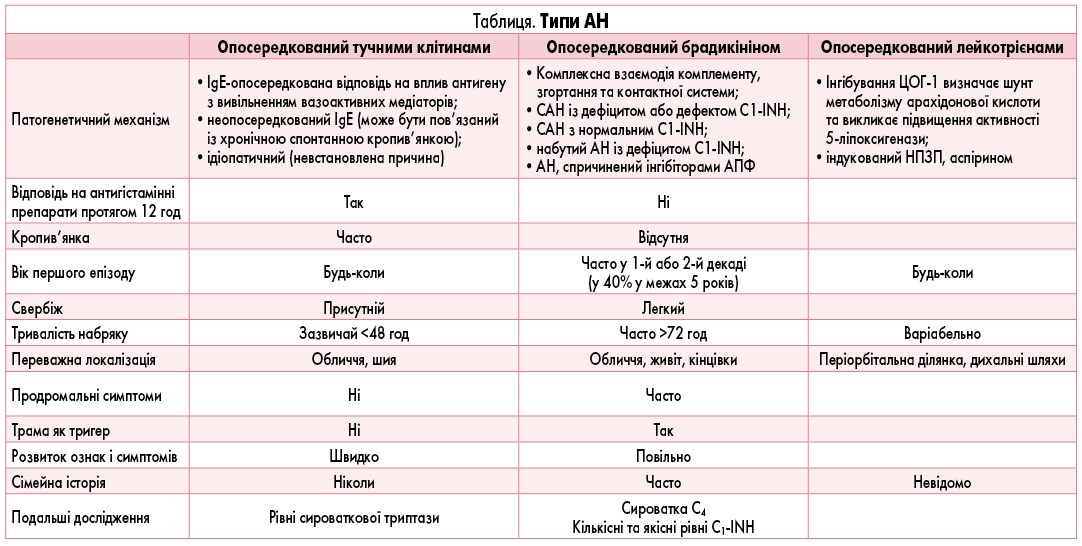
Патогенетичний механізм, відповідальний за АН, можна розділити на 3 шляхи: опосередкований тучними клітинами, опосередкований лейкотрієнами та опосередкований брадикініном. Кожен шлях має унікальну етіологію, імунопатологічні моделі та відповідь на лікування. АН, опосередкований тучними клітинами, запускається дегрануляцією тучних клітин і базофілів, що призводить до вивільнення вазоактивних речовин (таких як гістамін, простагландин D2, лейкотрієни C4, D4, фактор активації тромбоцитів) і активації кінінової системи. Це може статися через реакцію гіперчутливості типу I, опосередковану імуноглобуліном (Ig) E, після контакту з алергеном або викликану прямою дегрануляцією тучних клітин (фармакодинамічна дія, спричинена, наприклад, контрастною речовиною, опіоїдними препаратами). Найчастіше алергенами цього шляху є харчові продукти, ліки та укуси комах.
Другий шлях полягає в активації цистеїніл-лейкотрієнів, індукцію яких можуть викликати нестероїдні протизапальні препарати (НПЗП). Інгібування циклооксигенази (ЦОГ) 1 (R. Tachdjian, 2021; W. Stevens, 2015) спричиняє активацію метаболізму арахідонової кислоти та збільшення продукції прозапальних цистеїніл-лейкотрієнів, що призводить до АН.
У дослідженні за участю 1007 дітей з атопією у 4,1% пацієнтів повідомлялося про побічні ефекти на обличчі внаслідок прийому НПЗП, причому частота реакцій зростала з віком і досягла піку в 21% у віковій групі від 16 до 21 року порівняно з 2% у пацієнтів <5 років (E. Capriles-Behrens, 2000).
Третій патогенетичний механізм включає нерегульовану активацію кінінової системи, що призводить до надлишку брадикініну. Брадикінін є вазоактивним нанопептидом, який зв’язується з трансмембранним рецептором кініну B2 на ендотеліальних клітинах судин і викликає фосфорилювання з руйнуванням кадгерину судинного ендотелію (VE-кадгерин). VE-кадгерин є ключовим білком, який бере участь у формуванні щільних з’єднань ендотелію, отже, його втрата призводить до переміщення рідини з судинного простору в позаклітинний, викликаючи збільшення проникності судин, що клінічно проявляється АН (B.L. Zuraw, 2010). Основним регулятором контактної системи є інгібітор С1, серинова протеаза, здатна інгібувати низку ферментів, таких як фактори згортання крові XI і XII, калікреїн плазми та плазміноген, що беруть участь у метаболізмі брадикініну. Останній пов’язаний із розвитком таких патологічних станів, як спадковий ангіоневротичний набряк (САН), набутий АН, спричинений дефіцитом інгібітора C1-естерази (C1-INH), та АН, індукований інгібуванням ангіотензинперетворювального ферменту (АПФ) (D.M. Lang, 2012; J.S. Fok, 2015). Цікаво, що в останні роки були виявлені нові генетичні мутації, які викликають АН із нормальним C1-INH, що проливає нове світло на патогенез цих рідкісних форм САН.
Гормональні фактори (наприклад, використання контрацептивів, переважно естрогенів, менструація, вагітність та овуляція), а також загальні тригери, такі як травма або стрес, також можуть відігравати важливу патогенетичну роль в АН (А. Agostoni, 2004). У дитячому віці провокувальним фактором АН можуть бути інфекції (D. Pattanaik, 2017). Наприклад, простий герпес, Коксакі А і В, гепатит В, вірус Епштейна – Барр та інші вірусні захворювання, такі як інфекції верхніх дихальних шляхів, можуть продукувати імунні комплекси, що активують комплемент для вивільнення анафілатоксинів C3a, C4a та C5a, які взаємодіють із рецепторами тучних клітин і базофілів і призводять до дегрануляції тучних клітин із вивільненням гістаміну та інших вазоактивних факторів.
Диференційна діагностика
Порівняльна характеристика різних типів АН представлена у таблиці.
Набряк губ може імітувати синдром Мелькерсона – Розенталя – рідкісний стан невідомого походження, який клінічно характеризується тріадою: рецидивуючий периферичний параліч обличчя, рецидивуючий орофаціальний набряк і тріщини язика (G. Wehl, 2018). Зокрема, набряк губ не болючий і є найчастішою ознакою початкової стадії цього синдрому, який також називають гранулематозним хейлітом Мішера. Підтвердженням діагнозу є виявлення неказеозної гранульоми при біопсії слизової оболонки губ. Ще одним рідкісним захворюванням для диференційної діагностики є ідіопатичний системний капілярний синдром (ISCLS), або синдром Кларксона (K.M. Druey, 2017). Це потенційно летальний гострий стан, що характеризується рецидивуючими нападами гіперпроникності капілярів і судинного колапсу і супроводжується гіпоальбумінемією, гемоконцентрацією та підшкірним набряком обличчя, рук і стегон (L.C. Zingale, 2006). Хоча патогенетичний механізм цього синдрому невідомий, клінічна картина, в якій домінує екстравазація рідини, може ускладнити перебіг таких видів патології, як септичний шок, опіки або терапевтичні втручання, наприклад, лікування рекомбінантним інтерлейкіном-2, трансплантація кісткового мозку або серцево-легеневе шунтування.
Інші стани, що супроводжуються АН, включають гіпереозинофільний синдром, васкулітну кропив’янку, аутоімунні захворювання, реакції, подібні до сироваткової хвороби (SSLR), і медикаментозний висип з еозинофілією та системними симптомами (DRESS). Однак ці розлади рідко зустрічаються у дітей (J.S. Fok, 2015; A. Krishnamurthy, 2008). Клініцистам слід пам’ятати, що не всі набряки є ангіоневротичними, тому точний і детальний анамнез, ретельний об’єктивний огляд і цілеспрямовані діагностичні тести дуже важливі для правильної класифікації. Це дозволяє виключити форми псевдоАН, які також можуть виникати у дітей.
Діагностика
Першим етапом діагностики є розуміння того, чи пов’язаний АН із кропив’янкою та свербежем (H.I. Ertoy Karagol et al., 2013). Наступні кроки пов’язані з визначенням тривалості симптомів, характеристикою розташування набряку та наявністю АН у сімейному анамнезі. Крім того, слід провести спеціальне дослідження можливих провокувальних факторів, таких як їжа, ліки, зокрема НПЗП, укуси комах, вплив інгаляційних алергенів або фізичних агентів, таких як тиск або тепло, фізичні вправи, травми, емоційний стрес і вживання алкоголю. У пацієнтів слід уточнити нещодавно перенесені вірусні або бактеріальні інфекції та лихоманку. Крім того, важливо визначити реакцію на ліки, особливо антигістамінні та стероїди. Цей аспект необхідний для диференціації опосередкованого тучними клітинами або брадикініном АН. Зокрема, при опосередкованому тучними клітинами АН пацієнт зазвичай реагує на антигістамінні препарати та стероїди, на відміну від АН, опосередкованого брадикініном.
Діагностичні тести повинні ґрунтуватися на анамнезі та клінічних особливостях. Якщо це необхідно, слід провести алергологічну оцінку за допомогою шкірної прик-проби та дозування специфічного IgE для їжі, інгаляцій або перетинчастокрилих, щоб ідентифікувати етіологічний агент. Якщо є підозра на рецидив АН, ці тести менш цінні. У такому випадку варто припустити САН. При підозрі на САН першим кроком є визначення рівня C4 та C1-INH.
Ідіопатичний АН без пухирів
Ідіопатичний АН без пухирів є діагнозом виключення (А. Belbеzier et al., 2020). Дослідження серед дорослих повідомляють про частоту ідіопатичних АН від 33,5 до 46% (L.C. Zingale, 2006; S. Tai, 2010). У педіатричному дослідженні етіологічний фактор не був виявлений приблизно у 50% суб’єктів, незважаючи на належне діагностичне дослідження (H.I. Ertoy Karagol et al., 2013). Залежно від відповіді на фармакологічне лікування розрізняють 2 типи ідіопатичного АН без пухирів. Якщо є реакція на антигістамінні препарати, це ідіопатичний АН, опосередкований гістаміном, при другому типі реакція відсутня. Ідіопатичний неопосередкований гістаміном АН можна також диференціювати відповідно до відповіді на вищі дози H1-антигістамінних препаратів (до 4-кратної стандартної дози), омалізумабу та транексамової кислоти (А. Belbеzier, 2020; М. Mansi, 2015; рис.).
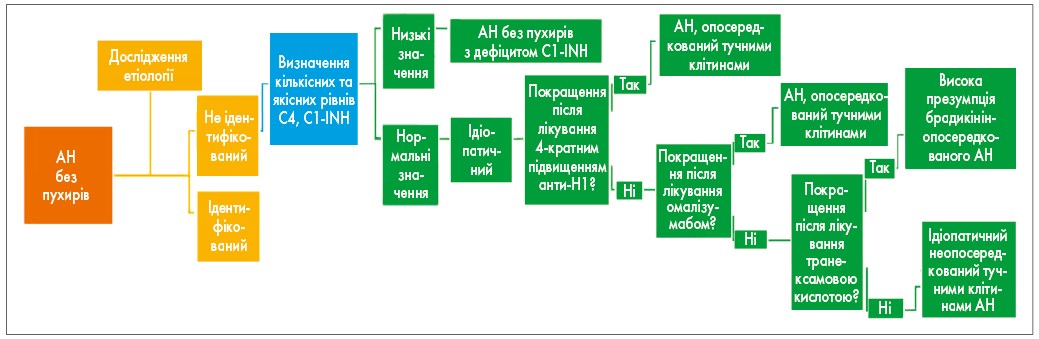 Рис. Діагностичні та терапевтичні підходи до лікування АН
Рис. Діагностичні та терапевтичні підходи до лікування АН
Сьогодні мало відомо про поширеність, клінічну картину, етіологію, лікування та спостереження за ідіопатичним гістамін-опосередкованим АН у педіатричних пацієнтів. Лише дослідження E. Karagol та співавт. (2013) і М. Ocak та співавт. (2021) вивчали суб’єктів, які постраждали від гістамін-опосередкованого АН без пухирів, включно з пацієнтами зі слабкою реакцією на антигістамінні препарати. Перехресні дослідження в педіатричній популяції визначили, що поширеність ізольованого АН становить 1,6% (H.I. Ertoy Karagol et al., 2013). Більшість випадків спостерігалася у пацієнтів чоловічої статі (42,9-71,6%), а початок першого епізоду захворювання в середньому становив 7-7,8 років (H.I. Ertoy Karagol, 2013; M. Ocak, 2021). Середня тривалість епізоду загострення АН становила 24 год. За 12 місяців у кожного пацієнта було зареєстровано 2-5 епізодів ізольованих загострень АН. Лише у 23,2% пацієнтів спостерігався тільки один епізод загострення. Найчастішими локалізаціями були повіки, губи, кінцівки, статеві органи, вуха, язик. Найпоширенішим супутнім захворюванням був алергічний риніт. Лише 11,9% пацієнтів повідомили про наявність принаймні одного члена родини з епізодами АН протягом їхнього життя. Щодо етіології, то у 51% випадків пацієнти страждали від епізодів АН невідомої причини. Найчастіше етіологія була представлена інфекційними факторами, потім йшли алергічні захворювання, гіперчутливість до НПЗП і захворювання щитоподібної залози.
Щодо профілактики епізодів ідіопатичного гістамін-опосередкованого АН без пухирів, тримісячне лікування антигістамінним препаратом дезлоратадином може бути варіантом вибору. Захворювання щитоподібної залози можуть бути фактором ризику, пов’язаним із продовженням антигістамінної профілактики (H.I. Ertoy Karagol et al., 2013). У короткостроковому періоді спостереження прогноз виглядає сприятливим.
L. Liotti et al. Pediatric Angiodema without Wheals: How to Guide the Diagnosis. Life, 2023. 13 (4); 1021.
Переклала з англ. Ольга Загора
Тематичний номер «Педіатрія» № 3 (69) 2023 р.