8 грудня, 2017
Долгосрочное использование эверолимуса у пациентов с комплексом туберозного склероза: обновление данных исследования EXIST‑2 после 4 лет наблюдения

Представлены результаты исследования долгосрочных эффектов эверолимуса у пациентов с почечной ангиомиолипомой (АМЛ), связанной с комплексом туберозного склероза (ТС) или спорадическим лимфангиолейомиоматозом (ЛАМ).
Введение
Туберозный склероз представляет собой генетическое заболевание с частотой 1 случай на 6 тыс. новорожденных, которое приводит к росту гамартом в таких органах, как мозг, почки, кожа, легкие, глаза и сердце. Около 20% пациентов страдают от развития в головном мозге субэпендимальных гигантоклеточных астроцитом (СЭГА), рост которых может привести к обструкции желудочков, острой гидроцефалии и смерти. Повреждения кожи различных типов, включая фибромы и лицевые ангиофибромы, развиваются у >90% пациентов с одним или несколькими поражениями. Ангиомиолипомы являются наиболее распространенными связанными с ТС почечными поражениями, которыми страдают до 80% пациентов. Они также наблюдаются у 33-50% больных ЛАМ. Обычно АМЛ проявляются как мультифокальное двустороннее бессимптомное поражение, но по мере разрастания новообразований до >3-4 см они стают симптомными, сопровождаются повышенным риском аневризм, что может привести к кровоизлиянию. В АМЛ почек, связанных с ТС или спорадическим ЛАМ (сЛАМ), выявляется повышенная активность мишени рапамицина млекопитающих (mTOR), вызванная мутациями в генах TSC1 или TSC2. Консенсусные рекомендации по лечению ТС предлагают ингибиторы mTOR в качестве первой линии терапии бессимптомных растущих АМЛ диаметром >3 см, в то время как селективная эмболизация и резекция почки являются приемлемыми подходами для второй линии терапии.
Исследование EXIST‑2 показало преимущество эверолимуса по сравнению с плацебо по частоте ответа АМЛ, времени до прогрессирования и скорости ответа со стороны поражений кожи у пациентов с АМЛ, связанными с ТС или сЛАМ. Промежуточный анализ результатов продленной фазы исследования продемонстрировал стабильность сохранения эффектов эверолимуса с течением времени. В настоящее время доступны данные окончательного анализа продленной фазы EXIST‑2.
Методы
EXIST‑2 – проспективное двойное слепое рандомизированное плацебо-контролируемое с параллельными группами многоцентровое исследование III фазы, посвященное изучению эверолимуса в дозе 10 мг/сут против плацебо.
Исследование не было остановлено 9 сентября 2011 г. после того, как запланированный промежуточный обзор показал высокую эффективность и безопасность эверолимуса, в то время как у пациентов, получавших плацебо, состояние продолжало ухудшаться.
В продленной фазе пациенты, рандомизированные в группу эверолимуса, продолжали открытое лечение препаратом в той же дозе. Снижение дозы до 5 мг/сут или 5 мг через день зависело от переносимости лечения. Пациенты из группы плацебо были переведены на эверолимус в дозе 10 мг/сут. Продленная фаза продолжалась в течение 4 лет после того, как последний пациент был рандомизирован, обеспечив период последующего наблюдения от 4 до 5 лет. Каждый пациент, прекративший терапию эверолимусом, прошел обследование через 28 дней после последнего получения препарата для оценки безопасности.
Текущий анализ EXIST‑2 охватывает все данные пациентов, получавших эверолимус во время основной либо продленной фазы исследования до 4 февраля 2015 г.
Первичной конечной точкой была частота ответа, определяемая как сокращение на 50% от исходного уровня в суммарном объеме целевых почечных АМЛ (>1 см в наибольшем диаметре) и отсутствие новых АМЛ, увеличения объема почек на >20% и кровотечений ≥2 степени, связанных с АМЛ. Первоначальный ответ требовал подтверждения повторным МРТ-сканированием. Все результаты МРТ-исследований анализировались централизованно независимыми радиологами. Дополнительные конечные точки включали продолжительность ответа, время до ответа и прогрессирования АМЛ, долю пациентов с ≥30% уменьшением объема АМЛ, долю пациентов, перенесших хирургическое удаление опухоли, а также частоту ответа со стороны поражений кожи. Кроме того, оценивалась частота ответа СЭГА (сокращение на ≥50% суммарного объема целевой опухоли при отсутствии новых СЭГА без ухудшения поражения и отсутствие новой или ухудшающейся гидроцефалии). У пациентов с ЛАМ проводился мониторинг функции легких. Оценка безопасности лечения включала регистрацию всех неблагоприятных событий и серьезных побочных эффектов (ПЭ).
Результаты
В общей сложности 112 пациентов получили по крайней мере одну дозу эверолимуса и были включены в этот анализ: 79 больных изначально были рандомизированы в группу эверолимуса и 33 перешли из группы плацебо на открытую терапию эверолимусом. По состоянию на 4 февраля 2015 г. 83 пациента (74,1%) завершили терапию по протоколу исследования. Женщины составляли 65,2%, средний возраст пациентов на момент включения в исследование – 32,2 года. Более пяти очагов АМЛ в начале исследования наблюдались у 59,8% пациентов, 29,5% имели почечную АМЛ размером 8 см. Общая сумма объемов очагов АМЛ составила 92,1 (диапазон 2,8-1611,5) см3. Более 1/3 пациентов (37,5%) подверглись операции в связи с осложнениями АМЛ до начала терапии эверолимусом; медиана уровня клубочковой фильтрации исходно составила 86 (диапазон 23-178) мл/мин/1,73 м2. У 50 пациентов (44,6%) имелся один очаг СЭГА.
Средняя продолжительность исследования составила 47,2 месяца, медиана длительности терапии эверолимусом – 46,9 месяца (диапазон 0,5-63,9). Средняя доза составляла 8,7 (диапазон 1,9-19,3) мг/сут при относительной интенсивности дозы (отношение вводимой дозы к запланированной) 0,86. Большинство (82,1%) пациентов получали эверолимус 2,8 года, 12,5% – 4,5 года. Десять (8,9%) пациентов прекратили исследование из-за ПЭ. Примерно 80% пациентов нуждались в одном прерывании приема и/или сокращении дозы, наиболее распространенной причиной чего были ПЭ. За 4 года исследования примерно 60% пациентов получали эверолимус в дозе 10 мг/сут, около 30% – от 5 до 10 мг/сут (в основном 5 мг/сут) и 10-15% пациентов принимали от 0 до <5 мг/сут (в основном 5 мг через день) – из 58 пациентов, которые получали эверолимус не менее 4 лет.
Почечные ангиомиолипомы
Из 112 пациентов с одной целевой АМЛ подтвержденный ответ достигнут у 65 (58%; 95% доверительный интервал, ДИ 48,3-67,3%). Среднее время до достижения ответа составило 2,89 месяца (95% ДИ 2,79-3,19). Лучший общий результат стабилизации АМЛ (между сокращением объема поражения <50% от исходного уровня и увеличением объема <25% от исходного) был зарегистрирован у 34 пациентов (30,4%; 95% ДИ 22,0-39,8%); у одного пациента заболевание прогрессировало в течение 18 нед после начала терапии эверолимусом. У 12 (10,7%) пациентов оценка ответа не проводилась, в основном из-за отсутствия исходных измерений объема почек.
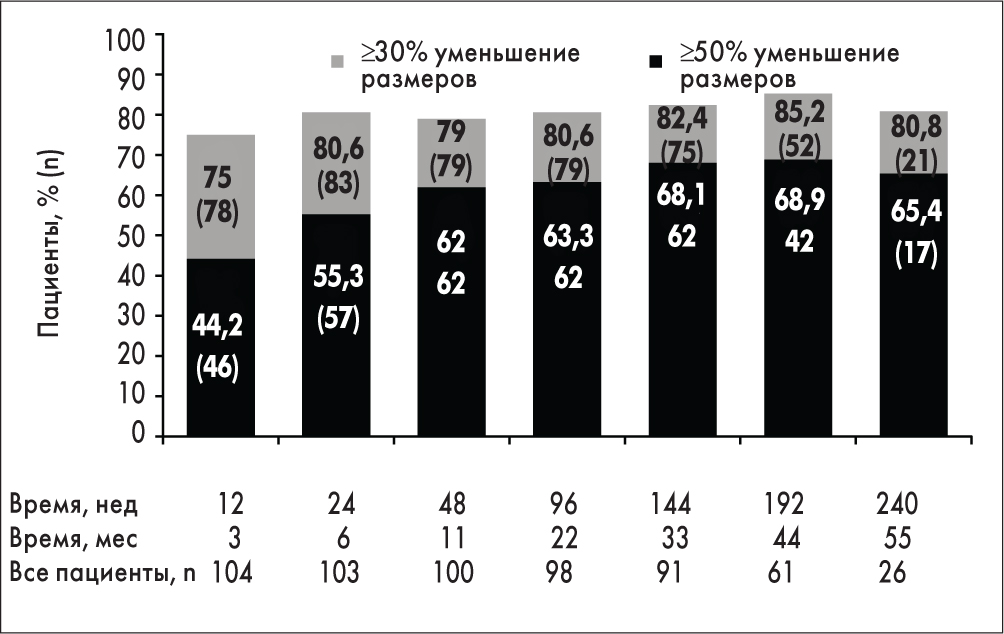
Рис. 1. Уровень ответа ангиомиолипомы почки на терапию эверолимусом с течением времени
По крайней мере одно сокращение от исходного уровня в сумме объемов поражений АМЛ наблюдалось у 98 (97%) из 101 оцениваемого пациента в период исследования. Снижение объема АМЛ на уровне 30% поддерживалось у 75% пациентов. Со временем доля пациентов, достигших сокращения объема на 50%, увеличилась (рис. 1). Анализ подтвердил, что более продолжительное лечение ассоциировалось со снижением общего объема очагов АМЛ, особенно в течение 3 мес после начала лечения. В течение первых 3 мес было зафиксировано снижение суммарного объема новообразований на 46% (95% ДИ 37-54%) по сравнению с исходным. Три последующих месяца лечения привели к небольшому – <2% – сокращению (95% ДИ <1-2%) в суммарном объеме по сравнению с исходным. Прогрессирование АМЛ наблюдалось у 16 пациентов (14,3%; 95% ДИ 8,4-22,2%) (рис. 2). Причинами прогрессирования были увеличение размера АМЛ (6 пациентов) и увеличение объема почек (10 пациентов); 9 участников продолжали терапию, несмотря на прогрессирование заболевания, из-за наличия клинической пользы. Прогрессированию заболевания предшествовало снижение дозы или прерывание терапии у 13 (81,3%) из 16 пациентов. Только у 2 из 65 пациентов, получивших исходно подтвержденный ответ АМЛ, в период исследования наблюдалось прогрессирование заболевания, зафиксированное по сравнению с минимальным достигнутым объемом АМЛ. Продолжительность периода от первого ответа до прогрессирования АМЛ или последней доступной рентгенологической оценки варьировалась от 3,0 до 55,5 месяца.
Рис. 2. Время до прогрессирования ангиомиолипомы почки
Субэпендимальные гигантоклеточные астроцитомы
Среди 50 пациентов с одним исходным поражением СЭГА размером 1 см частота ответа составила 48% (24/50; 95% ДИ 33,7-62,6%) и 42% пациентов (21/50; 95% ДИ 28,2-56,8%) достигли стабилизации заболевания (у 5 оценка не проводилась). Наблюдалось постепенное снижение средних объемов СЭГА с течением времени. Более половины пациентов перенесли сокращение объема СЭГА на 30% в различные периоды, доля пациентов со снижением объема СЭГА на 50% со временем увеличивалась (рис. 3). Среднее время до ответа СЭГА составило 8,31 месяца. Ни у одного из 24 пациентов, ответивших на лечение, СЭГА не прогрессировала во время исследования.
Рис. 3. Уменьшение объема СЭГА на фоне терапии эверолимусом с течением времени у пациентовс ангиомиолипомами почки
Изменение функции легких
У 29 пациентов с ЛАМ, которые получали эверолимус, объем форсированного выдоха за 1-ю секунду (FEV1), форсированная жизненная емкость (FVC) и DLCO со временем уменьшались незначительно. Среднее процентное изменение FEV1 составляло -3,45% от исходного на 24-й неделе, ±5,88% на 96-й и ±9,00% на 192-й неделе. Среднее процентное изменение в FVC было 0% на 24-й неделе, ±1,25% на 96-й и ±4,29% на 192-й неделе; среднее процентное изменение в DLCO составляло ±2,69, ±10,19 и ±10,62% соответственно. Кроме того, наблюдалось увеличение общего и остаточного объема легких.
Обсуждение
Текущий анализ результатов исследования EXIST‑2 подтверждает долгосрочную эффективность и безопасность эверолимуса у пациентов с АМЛ, связанной с ТC или сЛАМ. Реакция АМЛ на лечение продолжала улучшаться с 41,8% в основной фазе исследования (медиана продолжительности лечения 8,8 месяца) до 58% в продленной фазе (медиана 46,9 месяца). Клинически значимое сокращение размеров АМЛ сохранялось по мере продолжения лечения: анализ продемонстрировал значительное сокращение объема новообразований в первые 3 мес лечения и непрерывное, но менее выраженное снижение позже. Наблюдались низкие показатели прогрессирования в период исследования. За 4-летнюю продолжительность лечения эверолимусом осложнения, связанные с АМЛ, были редкими, ни один пациент не перенес связанное с АМЛ кровоизлияние.
Терапия эверолимусом также была связана с устойчивым сокращением объема СЭГА и уменьшением поражений кожи. В подгруппе пациентов с ТC-ассоциированным ЛАМ частота снижения функции легких была ниже ожидаемой. В плацебо-контролируемом двойном слепом исследовании у пациентов с ЛАМ показано, что ежегодное снижение FEV1 составляет 10% у пациентов, принимающих плацебо (n=43), тогда как в текущем исследовании сообщалось о снижении на 5,9% после почти двух лет лечения эверолимусом. Полученные данные подтверждают стабильное клиническое воздействие эверолимуса на различные проявления ТC.
Долгосрочный профиль безопасности эверолимуса был сопоставим с ранее описанным в клинических исследованиях, где эверолимус изучался при ТС. ПЭ имели место у большинства пациентов, но, как правило, подлежали устранению путем коррекции дозы. После прекращения приема плацебо было трудно отличить истинные ПЭ эверолимуса от проявлений ТС (например, инфекции были равно распространены как в группе плацебо, так и в группе эверолимуса в двойной слепой фазе исследования). Некоторые из них, однако, были предсказуемыми или известными ПЭ ингибиторов mTOR (например, аменорея, язвы во рту). Почти 3/4 пациентов завершили это долгосрочное исследование в соответствии с протоколом. Стоматит был наиболее частым ПЭ эверолимуса. Частота возникновения ПЭ всех типов уменьшалась с течением времени. Почечная функция оставалась стабильной у большинства пациентов, не сообщалось о случаях кровотечения, связанных с АМЛ. У одного пациента проведено ургентное хирургическое вмешательство с эмболизацией (в течение периода исследования), еще один пациент перенес нефрэктомию (после прекращения лечения).
Единственный случай эмболизации при медиане продолжительности терапии эверолимусом около 4 лет указывает на то, что лечение было успешным, и предполагает необходимость долгосрочного ингибирования mTOR для предотвращения или замедления роста опухоли, сохранения почечной функции и снижения потребности в эмболизациях. Сокращение частоты кровоизлияний может быть вызвано восстановлением более подходящей оси mTORC1 в мутантных сосудистых перицитах, тем самым позволяя предотвратить ремоделирование сосудов и образование аневризмы. Необходимы дополнительные ангиографические данные для оценки воздействия терапии эверолимусом на сосуды. Пациенты, включенные в это исследование, были подвержены высокому риску ухудшения состояния почек, поскольку у большинства из них имелись большие двусторонние АМЛ в начале исследования. Устойчивые клинические ответы на эверолимус со стороны АМЛ и других патологических проявлений TC, таких как поражения кожи, СЭГА и ЛАМ, подтверждают потенциал эверолимуса модифицировать течение заболевания у больных с ТС. Учитывая выраженный эффект эверолимуса, показанный при первичном анализе, продолжение приема плацебо в контрольной группе было неэтичным, что оправдывает отсутствие группы плацебо в продленной фазе.
Текущий анализ показал, что терапия эверолимусом оставалась эффективной и безопасной в течение примерно 4 лет. Общая оценка риска/преимуществ лечения подтверждает использование эверолимуса в качестве жизнеспособного варианта в терапии АМЛ, связанной с комплексом ТС или ЛАМ.
Список литературы находится в редакции.
Статья печатается в сокращении.
Bissler J.J., Kingswood J.Ch., Radzikowska E. et al. Everolimus
long-term use in patients with tuberous sclerosis complex:
four-year update of the EXIST‑2 study. PLoS ONE 12 (8): e0180939.
Перевела с англ. Катерина Котенко