4 квітня, 2018
Ингибиторы mTOR в медикаментозном лечении комплекса туберозного склероза и их потенциальная роль при других редких нарушениях нервно-психического развития

Комплекс туберозного склероза (КТС) представляет собой редкое генетическое заболевание, для которого характерно поражение многих органов и систем организма. Установлено, что при КТС имеет место дисрегуляция сигнального пути мишени рапамицина в клетках млекопитающих (mTOR), и накопленная к настоящему времени доказательная база поддерживает использование в лечении пациентов с данной патологией инновационных препаратов, принадлежащих к классу ингибиторов mTOR.
На сегодняшний день убедительно продемонстрировано, что применение ингибиторов mTOR эффективно при разных клинических проявлениях КТС, поэтому можно с уверенностью утверждать, что в скором времени данный терапевтический подход станет общепринятым. Кроме того, mTOR в настоящее время рассматривается как потенциальная цель для фармакологического воздействия и при ряде других редких заболеваний, в молекулярной патофизиологии которых также играют важную роль нарушения функционирования данного сигнального пути.
Введение
КТС – редкое аутосомно-доминантное заболевание, при котором отмечается развитие в разных органах узловых доброкачественных опухолевидных образований – гамартом [1-3]. Согласно экспертным оценкам, частота КТС составляет 1 на 6000 новорожденных, а в целом в мире данное заболевание зафиксировано примерно у 1,5 млн человек [1, 2, 4].
Хотя КТС может клинически манифестировать различным по степени тяжести поражением многих органов, прежде всего данное заболевание проявляется неврологической симптоматикой (включая судорожные припадки), нарушениями нервно-психического развития (такими, как умственная отсталость и аутизм) и опухолевидными поражениями головного мозга, легких, почек и кожи [1].
Обновленное консенсусное руководство по ведению пациентов с КТС, принятое в 2012 г., рекомендует использование системной терапии ингибиторами mTOR, поскольку данный подход дает возможность одновременно воздействовать на многочисленные клинические проявления этого заболевания [5].
Материалы и методы
Выполнен поиск опубликованных в базах данных PubMed/Medline ключевых клинических исследований по оценке эффективности ингибиторов mTOR в лечении субэпендимальных гигантоклеточных астроцитом (СЭГА), ангиомиолипом, лимфангиолейомиоматоза (ЛАЛМ), ангиофибром и эпилепсии у пациентов с КТС. Для поиска информации о применении этих препаратов при других редких заболеваниях использовались термины «mTOR», «ингибитор mTOR» и «ингибирование mTOR».
Клинические проявления, ассоциированные с КТС
Кортикальные туберсы, субэпендимальные узлы (СЭУ) и СЭГА представляют собой основные патологические опухолевидные образования, которые выявляют в головном мозге таких больных [1]. Кортикальные туберсы, которые формируются во время эмбриогенеза, могут обнаруживаться уже при рождении, их выявляют у 80-90% пациентов с КТС [1, 2, 6].
Считается, что наличие туберсов ассоциировано с судорожными припадками, умственной отсталостью, поведенческими отклонениями и аутизмом [6, 7]. СЭУ, которые представляют собой бессимптомные гамартомы, выступающие в просвет желудочков головного мозга, встречаются примерно у 90% лиц с КТС. При этом лишь примерно у 5-20% пациентов они могут трансформироваться в СЭГА [1, 8].
СЭГА представляют собой медленно растущие глионейронные опухоли, которые развиваются вблизи отверстия Монро и способны вызывать гидроцефалию, повышение внутричерепного давления и смертельный исход вследствие нарушения оттока цереброспинальной жидкости [1, 6].
До начала применения медикаментозной терапии, способной уменьшить объем опухоли, методом выбора в лечении растущих симптомных СЭГА являлась хирургическая резекция [9, 10].
Наиболее частым нарушением со стороны центральной нервной системы у пациентов с КТС является эпилепсия – ее диагностируют у 90% больных [11, 12]. Фокальные судорожные припадки и младенческие судороги представляют собой наиболее типичные виды судорог у пациентов с КТС. Младенческие судороги, как правило, возникают на первом году жизни примерно у трети детей с КТС [10, 11].
Раннее начало младенческих судорог ассоциировано с неутешительными исходами в плане психоневрологического развития и с неудовлетворительным контролем судорожной активности в будущем [1, 13, 14].
При КТС в патологический процесс вовлекаются многие органы и системы, в том числе головной мозг, почки, легкие, сердце и кожа.
Почечные проявления заболевания отмечаются примерно у 55-90% пациентов, в то время как ангиомиолипомы обнаруживаются у 75% пациентов [6]. Почечные ангиомиолипомы являются наиболее частой причиной смерти пациентов с КТС, поскольку потенциально способны приводить к почечной недостаточности и кровотечениям [15].
ЛАЛМ – наиболее распространенное легочное проявление КТС, характеризующееся кистозными поражениями легких. ЛАЛМ также спорадически встречается у лиц без данного генетического заболевания [16]. ЛАЛМ диагностируется примерно у 30-40% пациентов с КТС (почти исключительно у женщин) и может приводить к деструкции легочной паренхимы, вследствие которой развивается прогрессирующая одышка при физической нагрузке и рецидивирующий пневмоторакс [16-18].
Сердечные рабдомиомы представляют собой частое первоначальное клиническое проявление КТС, имеющее место у 33% пациентов.
Клиническое течение рабдомиом обычно бессимптомное, и они спонтанно регрессируют с возрастом [19, 20], однако в редких случаях эти опухоли ввиду своей локализации могут вызывать аритмию и сердечную недостаточность [21].
У большинства пациентов (>90%) имеются кожные проявления заболевания: гипомеланотические макулы, ангиофибромы и/или бляшки на коже головы, ногтевые или околоногтевые фибромы, участки «шагреневой кожи» и сочетание разнообразных поражений кожи в виде конфетти.
Ангиофибромы встречаются примерно у 80% лиц с КТС в возрасте старше 5 лет и в типичных случаях расположены на лице [3].
Характерные красные или розовые узлы часто формируются в первые годы жизни и с возрастом становятся более выраженными [22].
Несмотря на применение многочисленных методов дерматологического лечения (в некоторых случаях включающих хирургическое иссечение), ангиофибромы часто рецидивируют [22].
Значение сигнального пути mTOR в патогенезе КТС
В норме сигнальный каскад mTOR (также известный как путь фосфатидилинозитол‑3-киназы [PI3K]/протеинкиназы B [Akt]/mTOR) играет важную роль в процессах роста, пролиферации и выживаемости клеток (рис.) [23]. Разные стимуляторы, такие как факторы роста (например, инсулиноподобный фактор роста 1 [IGF‑1]), связываются с рецепторами тирозинкиназы (например, IGF‑1R), что приводит к фосфорилированию PI3K [23]. Результатом этой активации PI3K становится каскад событий фосфорилирования, вызывающий активацию протеинкиназы В (Akt), которая в свою очередь ингибирует комплекс TSC1/TSC2. Ингибирование комплекса TSC1/TSC2 обусловливает гиперактивацию mTOR, приводящую к избыточному клеточному росту и пролиферации [23-25].
Два дополнительных белка – кодируемый геном NF1 нейрофибромин и кодируемый геном NF2 мерлин (участвующий в подавлении развития опухолей) – также действуют как отрицательные регуляторы пути mTOR [26, 27]. mTOR образует два различных мультипротеиновых комплекса – mTORC1 и mTORC2, которые дифференцируются в зависимости от своих партнеров по взаимодействию (регуляторный ассоциированный белок mTOR [RAPTOR] для mTORC1 и рапамицин-нечувствительный партнер mTOR [RICTOR]/SIN1 для mTORC2), селективности по отношению к субстрату и чувствительности к рапамицину (сиролимус) и его аналогам (например, к эверолимусу) [25, 28].
Нисходящие регуляторные эффекты mTORC1 включают транскрипцию генов и трансляцию белков, пролиферацию и выживание клеток, а также ангиогенез, в то время как mTORC2, как считается, опосредует цитоскелетную динамику [28]. Дисрегуляция пути mTOR связана с развитием многих видов опухолей (включая КТС), а также ряда неврологических расстройств [23, 28].
КТС вызван мутацией в гене TSC1 или TSC2, «выключение» которых вызывает конститутивную активацию сигнального пути mTOR. Это приводит к аномальному клеточному росту/пролиферации и последующему образованию гамартомных поражений [25, 29]. Открытие взаимосвязи между TSC1/TSC2 и mTOR привело к такому важному клиническому достижению, как использование ингибиторов mTOR (в частности, сиролимуса и его аналога – эверолимуса) с целью лечения ряда клинических проявлений КТС. Сиролимус и эверолимус действуют путем связывания и формирования комплекса с FK506-связывающим белком‑12 (FKBP12), который затем ингибирует mTORCl (рис.) [24].
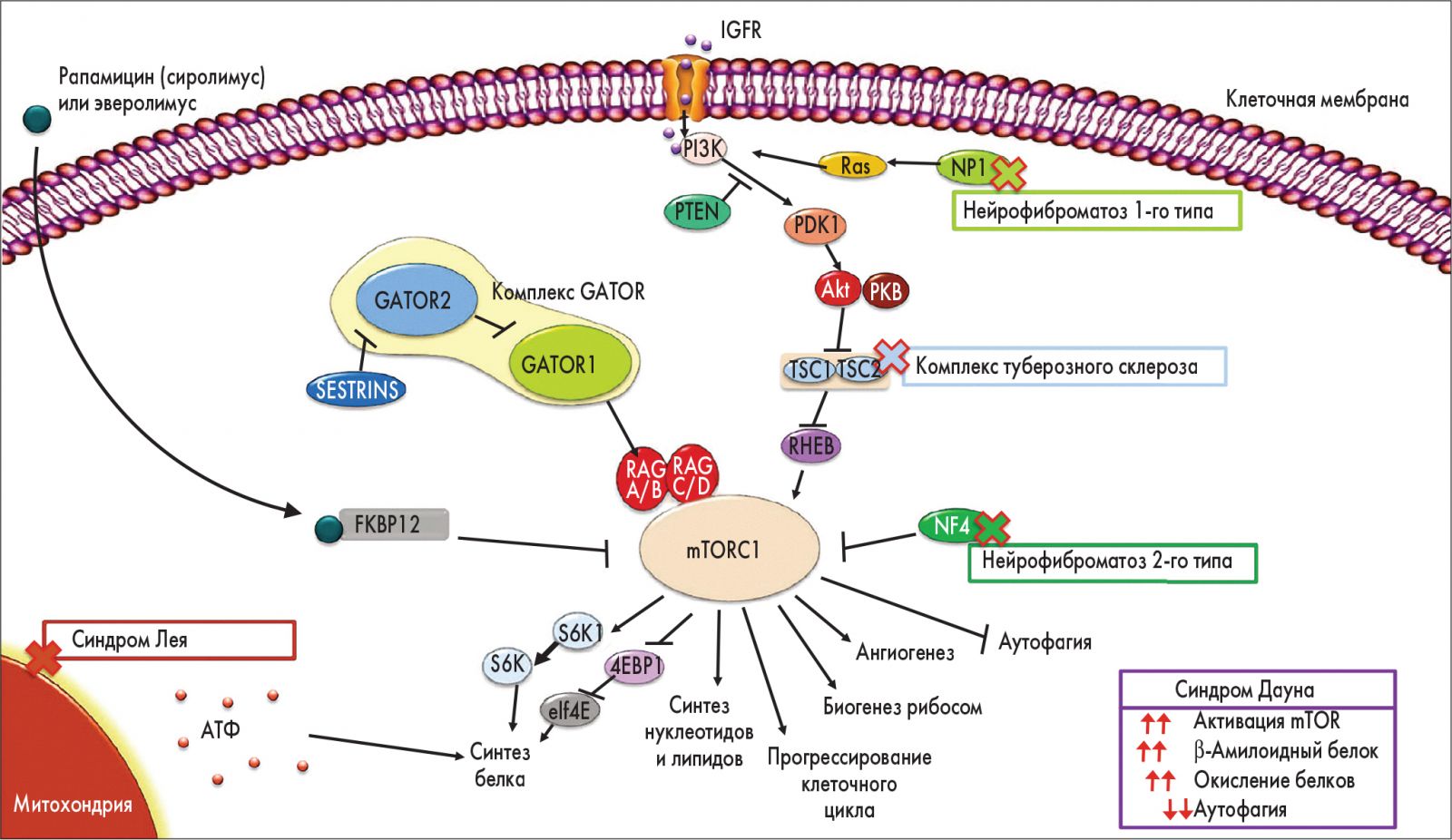 Рис. Сигнальный путь mTOR и его возможная роль при редких заболеваниях
Рис. Сигнальный путь mTOR и его возможная роль при редких заболеваниях
Стимуляторы, такие как IGF, связываются с рецепторами тирозинкиназы, что приводит к фосфорилированию PI3K [23]. Каскад последующих реакций фосфорилирования приводит к активации протеинкиназы B (Akt), которая в свою очередь фосфорилирует и ингибирует комплекс TSC1/TSC2 – отрицательный регулятор mTOR. Как следствие, ингибирование комплекса TSC1/TSC2 приводит
к активации mTOR [23-25]. NFI-кодируемый нейрофибромин и NF2-кодируемый белок мерлин также действуют как отрицательные регуляторы пути mTOR. Нейрофибромин функционирует как Ras-ГТФаза-активирующий протеин, который ингибирует эффекты, оказываемые Ras на PI3K [26], в то время как белок мерлин напрямую воздействует на комплекс mTOR1 (mTORC1) [27]. Сиролимус
и эверолимус формируют комплексы с FK506-связывающим протеином-12 (FKBP12), что приводит к подавлению активности mTORC1 [24]. Хотя данные механизмы являются сложными и не до конца ясными при синдромах Лея и Дауна, доказательства демонстрируют взаимосвязь между активностью mTOR и содержанием АТФ (синдром Лея) и между сниженной аутофагией, усиленной продукцией
белка и оксидацией с гиперактивацией mTOR (синдром Дауна) [62, 65, 66].
Ингибиторы mTOR в лечении клинических проявлений, ассоциированных с КТС
СЭГА, ассоциированные с КТС
Опыт применения сиролимуса в лечении СЭГА был проанализирован в серии сообщений о клинических случаях, а также оценен в качестве вторичной конечной точки в клиническом исследовании ІІ фазы с участием небольшого количества пациентов. Было показано, что применение сиролимуса обеспечивает очевидную регрессию СЭГА [30-32].
Эверолимус более широко изучали в лечении СЭГА – оценке его эффективности были посвящены долгосрочные исследования ІІ и ІІІ фазы [33-36]. В ходе 6-месячного открытого исследования ІІ фазы, включавшего 28 пациентов, на фоне лечения эверолимусом было продемонстрировано значимое уменьшение объема опухоли по сравнению с исходным: примерно у 75% пациентов – более чем на 30%, а у 32% пациентов – более чем на 50% [33]. Примечательно, что достигнутое уменьшение размеров опухоли оставалось стойким и в течение расширенной фазы исследования (медиана лечения – 5,65 года) [37].
В ходе рандомизированного двойного слепого плацебо-контролируемого исследования ІІІ фазы с участием 117 пациентов с СЭГА и КТС лечение эверолимусом (медиана – 9,6 мес) ассоциировалось с достоверно более высокой частотой достижения ответа со стороны СЭГА (уменьшение объема СЭГА более чем на 50%) по сравнению с плацебо (35% в сравнении с 0%; p <0,0001) [35].
Анализ данных 111 пациентов, которые получили как минимум одну дозу эверолимуса (во время двойной слепой или последующей открытой фазы исследования), выявил, что частота ответа со стороны СЭГА увеличилась до 57,7% в течение периода, медиана которого составила 47,1 мес (3,9 года), а достигнутое уменьшение размера СЭГА (медиана) сохранялось и даже незначительно продолжалось в течение всего исследования [38].
В целом клинические данные исследований ІІ и ІІІ фазы свидетельствуют о целесообразности применения эверолимуса при КТС-ассоциированных СЭГА, а результаты исследований ІІ фазы послужили основанием для одобрения Управлением по контролю за пищевыми продуктами и лекарственными препаратами (FDA) США использования эверолимуса с целью лечения СЭГА у взрослых и детей с КТС [39].
Почечная ангиомиолипома, ассоциированная с КТС
Эффективность применения эверолимуса в лечении пациентов с почечной ангиомиолипомой оценивали в ходе крупного клинического исследования ІІІ фазы EXIST‑2, а также в подгруппе участников исследования EXIST‑1, у которых имело место сочетание СЭГА и почечной ангиомиолипомы [40, 41].
В исследовании EXIST‑2 частота ответа со стороны ангиомиолипомы (уменьшение объема на 50% или больше при отсутствии других факторов) после примерно 8 мес лечения составила 42% у пациентов, получавших эверолимус, и 0% у пациентов, получавших плацебо (p <0,0001) [40]. Этот показатель увеличился до 54% у пациентов, получавших лечение эверолимусом в течение периода, медиана которого составляла 29 мес [42], и до 58% – на момент завершения открытой расширенной фазы (медиана длительности воздействия – 46,9 мес) [43]. На основании результатов основной фазы исследования EXIST‑2 эверолимус был одобрен FDA США для лечения взрослых пациентов с почечной ангиомиолипомой и КТС [39].
Аналогично результатам исследования EXIST‑2, в исследовании EXIST‑1 было сообщено, что частота ответа в подгруппе пациентов с СЭГА и ангиомиолипомой (преимущественно педиатрическая популяция) составила 53,3% для эверолимуса и 0% для плацебо после курса лечения, медиана длительности которого составляла 9,6 и 8,3 мес соответственно. У 80% пациентов было достигнуто уменьшение размера почечной ангиомиолипомы на 50% и более после 48 недель (11 мес) лечения [41].
Сиролимус не был одобрен для лечения почечной ангиомиолипомы, но его применение оценивалось в ходе нескольких небольших открытых клинических исследований ІІ фазы [32, 44-46]. Bissler и соавт. обнаружили, что введение сиролимуса способствовало уменьшению размера ангиомиолипомы и улучшению легочной функции в течение 12 мес лечения [44].
Однако через 12 мес, после прекращения терапии сиролимусом, размеры поражения и несколько показателей легочной функции приблизились к исходным, свидетельствуя о том, что необходимая продолжительность терапевтического ингибирования mTOR должна быть весьма долгой или неопределенной по длительности [44].
Davies и соавт. выполнили более длительное исследование и у 50% пациентов выявили сохранение положительного ответа со стороны ангиомиолипомы (исчезновение поражения или уменьшение его размеров на 30% и более от суммы максимальных диаметров целевых очагов поражения) в течение 2 лет [45].
В ходе одного многоцентрового клинического исследования ІІ фазы были оценены эффекты, оказываемые сиролимусом на многочисленные поражения у взрослых с КТС. В течение одного года лечения исследователи зафиксировали уменьшение размера почечных ангиомиолипом, размера СЭГА и ангиомиолипом печени, а также субъективное улучшение клинического течения кожных поражений и снижение уровня фактора роста эндотелия сосудов (VEGF) D в крови [32].
ЛАЛМ, ассоциированный с КТС
Применение как сиролимуса, так и эверолимуса оценивали в лечении ЛАЛМ в ходе ряда исследований, включавших преимущественно пациентов со спорадически возникшим заболеванием, хотя среди них было и незначительное количество пациентов с КТС-ассоциированным ЛАЛМ [47-50]. В ходе многоцентрового плацебо-контролируемого исследования MILES у 89 пациентов с ЛАЛМ (8 – с сопутствующим диагнозом КТС), получавших лечение сиролимусом (n=46) в течение 12 мес, были продемонстрированы улучшение форсированной жизненной емкости легких (ФЖЕЛ) и качества жизни, а также стабилизация объема форсированного выдоха за 1-ю секунду (ОФВ1) [47].
Эти результаты послужили основанием для одобрения FDA США применения сиролимуса с целью лечения ЛАЛМ [51].
Использование сиролимуса в лечении ЛАЛМ также оценивали в двух ретроспективных исследованиях [48, 49]: сообщалось об улучшении или стабилизации легочной функции даже при минимальных остаточных концентрациях препарата (<5 нг/мл) [48] наряду со стойкими клиническими эффектами в течение периода лечения продолжительностью примерно 3,5 года [49].
Недавно использование эверолимуса также было оценено в проспективном исследовании, которое включало 24 пациента с ЛАЛМ (из них 5 – с ЛАЛМ, ассоциированным с КТС). Было показано улучшение ОФВ1, стабилизация ФЖЕЛ и снижение уровней VEGF-D и коллагена IV в сыворотке крови; однако оптимальное дозирование эверолимуса при его применении по данному показанию нуждается в дальнейшем изучении [50].
Судорожные припадки, ассоциированные с КТС
Хотя ни один из ингибиторов mTOR в настоящее время не имеет специфических показаний к применению в качестве средства для лечения судорожных припадков, ассоциированных с КТС, недавно полученные клинические доказательства демонстрируют многообещающие перспективы использования препаратов этого класса при данной патологии.
Согласно нескольким сообщениям, сиролимус может быть эффективен в лечении судорог, ассоциированных с КТС [52-54]. Так, терапия сиролимусом, назначенная более чем на 10 мес 10-летней девочке, способствовала снижению ежедневной судорожной активности с 5-10 до 1-5 припадков в сутки и полному прекращению кластерных (серийных) судорожных припадков [52].
При анализе серии клинических случаев, включавшей 7 детей с КТС, было выявлено, что спустя 12 мес терапии сиролимусом у всех пациентов достигался контроль судорог [53].
По данным анализа второй серии случаев, также включавшей 7 детей с КТС и рефрактерными судорожными припадками, сообщалось, что у большинства пациентов отмечалось уменьшение их количества на 50-90% [54].
В недавно завершенном небольшом рандомизированном клиническом исследовании с участием 23 детей (в возрасте от 3 мес до 12 лет) с КТС лечение сиролимусом снизило общую частоту судорожных припадков на 41% в сравнении со стандартной терапией, но это изменение не достигло статистической значимости (p=0,11) [55].
Возможности использования эверолимуса также были оценены при КТС-ассоциированных судорожных припадках [33, 56]. Результаты проспективного исследования І/ІІ фазы, напрямую оценивавшего применение эверолимуса в лечении рефрактерных судорожных припадков, ассоциированных с КТС, продемонстрировали снижение их частоты на 50% и более у 12 из 20 пациентов через 12 недель лечения [56].
В исследовании ІІ фазы терапия эверолимусом ассоциировалась с клинически значимым снижением общей частоты клинически манифестных и субклинических судорог (медиана изменения, –1 судорожный припадок; p=0,02) у пациентов с СЭГА. Из 16 пациентов, данные электроэнцефалографии которых были доступны, частота судорог снизилась у 9 пациентов через 6 мес; у 5 пациентов вообще не отмечалось припадков [33].
Недавно были обнародованы результаты первого исследования ІІІ фазы по оценке применения ингибитора mTOR (эверолимуса) при рефрактерных судорожных припадках, ассоциированных с КТС (ClinicalTrials.gov NCT01713946) [57]. В этом проспективном рандомизированном двойном слепом многоцентровом исследовании сравнивали эффективность эверолимуса в двух различных диапазонах остаточных концентраций (низкие – 3-7 нг/мл; высокие – 9-15 нг/мл) с таковой плацебо в уменьшении частоты судорожных припадков (N=36) при их добавлении к уже получаемым противоэпилептическим препаратам.
Через 18 недель лечения выраженная в процентах медиана уменьшения частоты судорожных припадков оказалась достоверно выше при применении эверолимуса (29,3% – в низких концентрациях и 39,6% – в высоких концентрациях по сравнению с 14,9% на фоне приема плацебо; p=0,0028 и p <0,0001 соответственно), а количество лиц, у которых достигнут ответ на лечение (снижение частоты судорожных припадков на 50% или более), было достоверно больше на фоне терапии эверолимусом (28,2% – в низких концентрациях и 40% – в высоких концентрациях по сравнению с 15,1% при приеме плацебо; p=0,0077 и p <0,0001 соответственно) [57].
Эти предварительные результаты указывают, что дополнительное лечение эверолимусом может быть эффективным в снижении частоты рефрактерных судорожных припадков у пациентов с КТС.
Нейропсихические расстройства, ассоциированные с КТС
Ингибиторы mTOR также могут обоснованно рассматриваться в качестве вариантов для применения в лечении нейропсихических расстройств и нарушений психоневрологического развития, ассоциированных с КТС (TAND; в том числе – интеллектуальной недостаточности и аутизма).
В недавно завершенном доклиническом испытании у взрослых крыс с мутациями гена TSC2 и экспериментальным эпилептическим статусом, а также в описании клинического случая у пациента с КТС сообщалось об улучшении социального поведения (включая поведенческие стереотипы, связанные с аутизмом) после терапии ингибитором mTOR эверолимусом [58, 59].
Однако ингибиторы mTOR пока не были адекватно оценены либо одобрены для лечения нарушений психоневрологического развития при КТС, особенно у детей раннего возраста. Также крайне важно установить безопасность и общее влияние ингибиторов mTOR в педиатрической популяции еще до проведения более длительных и масштабных клинических исследований. В будущем ожидается получение дополнительной информации об эффектах, оказываемых ингибиторами mTOR при КТС-ассоциированных нейропсихических расстройствах, включая вторичный анализ результатов исследования EXIST‑3 и результатов нескольких исследований ІІ фазы (NCT01289912, NCT01954693).
Обоснование потенциального применения ингибиторов mTOR по другим инновационным показаниям
Помимо КТС, применение ингибиторов mTOR было изучено при ряде других редких заболеваний, при которых имеет место дисрегуляция сигнального пути mTOR.
Синдром Лея
Генетические дефекты, отмечаемые при синдроме Лея, приводят к нарушению функции митохондрий, что обусловливает развитие целого ряда серьезных проблем со здоровьем. У пациентов могут иметь место такие симптомы, как респираторные нарушения, паралич глазодвигательного и других черепных нервов, патологические непроизвольные движения, задержка развития моторики, умственная отсталость и судорожные припадки [60]. Хотя время дебюта заболевания может варьировать, оно, как правило, манифестирует уже на первом году жизни ребенка. Синдром Лея характеризуется диффузной мультифокальной спонгиозной дегенерацией различных участков головного мозга, и многие пациенты умирают в течение нескольких лет после появления первых симптомов заболевания [60].
В доклиническом испытании у мышей с «выключенным» геном Ndufs4 (белок, кодируемый геном Ndufs4, участвует в сборке, обеспечении стабильности и активности комплекса I митохондриальной цепи транспорта электронов) введение рапамицина улучшало состояние здоровья животных и повышало их выживаемость [61]. Механизм этого феномена пока не вполне понятен, однако считается, что снижение активности mTOR может «сдвигать» клеточный метаболизм в направлении катаболизма аминокислот и подавления гликолиза, и таким образом уменьшается накопление промежуточных продуктов гликолиза, которое ассоциировано с синдромом Лея [61].
Дополнительное исследование указывает, что ингибирование mTOR может помочь при синдроме Лея посредством сохранения в клетках аденозинтрифосфата (АТФ). Митохондрии обеспечивают клетки энергией благодаря синтезу АТФ, содержание которого, как было установлено, снижается при митохондриальных заболеваниях; это приводит к дегенерации нейронов, как при синдроме Лея [62].
В исследовании in vitro рапамицин вводили в нейроны с митохондриальными дефектами, что обеспечивало значимое повышение уровня АТФ на фоне замедления продукции белка [62]. Существует предположение, что снижение интенсивности энергозатратного процесса белкового синтеза при ингибировании mTOR позволяет сохранить в клетке большее количество АТФ [62].
Хотя исследования по оценке возможного применения ингибиторов mTOR при синдроме Лея находятся на очень ранней стадии, полученные на сегодня доклинические результаты являются весьма обнадеживающими, поскольку в настоящее время вообще отсутствует какое-либо эффективное лечение данного заболевания.
Синдром Дауна
Синдром Дауна представляет собой генетическое заболевание (трисомия по 21-й хромосоме), ассоциированное с интеллектуальной недостаточностью [63]. Синдром Дауна характеризуется нарушениями морфологии дендритных клеток и синаптической пластичности, а mTOR, как считается, участвуют в процессах роста и разветвления дендритов в гиппокампе [64]. На модели синдрома Дауна у мышей было показано, что активность mTOR в дендритах гиппокампа увеличена [64]. Это увеличение после введения рапамицина было обратимым. В настоящее время изучается, способен ли рапамицин устранять проблемы с обучением, ассоциированные с синдромом Дауна.
Гиперактивация пути PI3K/Akt/mTOR (по сравнению с контролем) также наблюдалась в образцах тканей, взятых при аутопсии тел пациентов с синдромом Дауна [65]. Выдвигается гипотеза о том, что причинным фактором синдрома Дауна может выступать трипликация гена, кодирующего β-амилоидный белок, которая приводит к его избыточному образованию.
В сочетании со сниженной аутофагией вследствие усиленной активации mTOR это может приводить к накоплению β-амилоидного пептида в головном мозге и способствовать развитию у пациентов с синдромом Дауна нейродегенеративных процессов и деменции альцгеймеровского типа [65].
Также считается, что при нейродегенеративных заболеваниях (в том числе – при синдроме Дауна) значимая роль принадлежит оксидативному стрессу. На модели синдрома Дауна у мышей продемонстрировано, что окисление белков было повышено ввиду снижения протективного эффекта аутофагии вследствие гиперактивации пути mTOR [66]. При введении рапамицина окисление белков в клетках уменьшалось [66].
Нейрофиброматоз 1-го и 2-го типов
Нейрофиброматоз представляет собой аутосомно-доминантное генетическое заболевание, которое классифицируется на 1-й и 2-й типы.
Нейрофиброматоз 1-го и 2-го типов вызван инактивирующими мутациями в генах NF1 и NF2 соответственно [67]. «Выключение» гена NF1, кодирующего белок нейрофибромин, приводит к развитию нейрофибром на периферических нервах или вокруг них, а также к образованию пигментированных опухолей кожи и радужной оболочки глаза [67].
Примерно у 1/3 пациентов с нейрофиброматозом 1-го типа отмечается плексиформная (гроздевидная) нейрофиброма, которая обезображивает внешность, может вызывать сдавление различных структур тела, неврологическую дисфункцию и болевой синдром [68].
Доказательная база свидетельствует о том, что нейрофибромин принимает участие в отрицательной регуляции пути mTOR. Результаты клинического исследования ІІ фазы, в которое были включены пациенты с прогрессирующими плексиформными нейрофибромами, продемонстрировали умеренно выраженное замедление прогрессирования заболевания на фоне лечения сиролимусом [68].
Однако данные аналогичного исследования II фазы, в котором оценивали применение сиролимуса при непрогрессирующих плексиформных нейрофибромах, показали, что препарат не вызывает какого-либо уменьшения размеров опухоли [69]. При анализе серии клинических случаев, включавшей пациентов с симптомными плексиформными нейрофибромами, было продемонстрировано, что сиролимус уменьшал выраженность болевого синдрома, хотя и не уменьшал размер опухоли [70]. Отсутствие противоопухолевого ответа при применении сиролимуса у пациентов с нейрофиброматозом 1-го типа может быть обусловлено альтернативными компенсаторными механизмами (например, усилением активности Akt по механизму обратной связи), включающимися после ингибирования mTOR [71].
При нейрофиброматозе 2-го типа (более редкий подтип заболевания) отмечается «выключение» гена NF2, который кодирует регуляторный белок мерлин, участвующий в подавлении развития опухолей. Отсутствие белка мерлина приводит к развитию доброкачественных опухолей, именуемых шванномами, которые могут расти по ходу слуховых нервов, приводя к глухоте, и сдавливать нервы, обусловливая повышение внутричерепного давления, дисфункцию нервов и болевой синдром [67].
Было установлено, что как и нейрофибромин, белок мерлин выступает отрицательным регулятором пути mTOR [72]. Рапамицин останавливал рост шванномы у мышей и на модели in vitro [72]. Однако в исследовании ІІ фазы, в котором оценивали применение эверолимуса в лечении прогрессирующих вестибулярных шванном, ни у одного из пациентов не было отмечено ответа на лечение (уменьшение размера опухоли на 15% и более) [73]. Ограниченная активность эверолимуса при вестибулярных шванномах также может объясняться активацией механизма отрицательной обратной связи после ингибирования mTOR [73].
Безопасность ингибирования mTOR при КТС
Имеющиеся в настоящее время данные исследований убедительно свидетельствуют, что ингибирование mTOR (в особенности – с помощью эверолимуса) остается эффективным и безопасным в течение весьма длительного лечения по поводу определенных проявлений КТС.
Однако при использовании сиролимуса либо эверолимуса все же следует принимать во внимание нежелательные явления (НЯ), рассматриваемые как классовые эффекты всех ингибиторов mTOR (включающие неинфекционный пневмонит, инфекции, изъязвление слизистой оболочки полости рта, нарушение процесса заживления ран и метаболические расстройства, такие как гипергликемия и дислипидемия) [39, 51].
Данные НЯ можно контролировать путем временного прекращения приема препарата либо коррекции его дозы в зависимости от степени тяжести того или иного НЯ [39]. В то время как данные о долгосрочном применении сиролимуса при КТС отсутствуют, клинический опыт использования эверолимуса у пациентов с КТС и почечными ангимиолипомами либо СЭГА указывает, что длительная терапия этим препаратом в целом хорошо переносится; большинство НЯ, зарегистрированных при его применении, были легкими либо умеренными по степени тяжести [36-38, 43, 74, 75].
Долгосрочное ингибирование mTOR при КТС
В то время как изучение терапии ингибиторами mTOR по вышеупомянутым инновационным показаниям в качестве возможного варианта продолжается, при КТС она уже одобрена в качестве современной стратегии лечения. При данном заболевании актуальным вопросом является оценка эффектов ее долгосрочного применения.
КТС представляет собой хроническое заболевание, которое может манифестировать уже в раннем возрасте, поэтому весьма вероятно, что пациенты (включая детей) будут нуждаться в пожизненной терапии ингибиторами mTOR. Выраженность некоторых более поздних проявлений КТС можно уменьшить либо предотвратить их возникновение посредством раннего назначения ингибитора mTOR. Однако начало терапии у детей и подростков может также иметь и другие последствия. Поэтому важно проанализировать эффективность и безопасность лечения ингибиторами mTOR у детей и подростков и его потенциальное долгосрочное воздействие на процессы роста и полового созревания.
Если пациенты получают долгосрочную терапию ингибиторами mTOR, важное значение приобретает стойкость терапевтического ответа.
Долгосрочные данные, недавно полученные в ходе исследований EXIST‑1 [38] и EXIST‑2 [43], продемонстрировали стойкое и более выраженное клиническое преимущество эверолимуса по сравнению с краткосрочными первичными анализами [35, 40]. При этом в подгруппе доступных для оценки участников исследования EXIST‑2, за которыми осуществлялось наблюдение и после прекращения терапии эверолимусом (n=7), было зафиксировано увеличение размера ангиомиолипом более чем на 50% в период от прекращения применения препарата до истечения 48 недель после завершения лечения [76]. Эти результаты подчеркивают необходимость длительного, постоянного лечения КТС.
Хотя данные о долгосрочном воздействии ингибиторов mTOR у детей и подростков, включая влияние этих препаратов на рост и половое созревание, являются ограниченными, в исследовании EXIST‑1 сообщалось о том, что эверолимус не оказывал значимого эффекта на течение пубертатного периода или развитие пациентов с КТС (медиана длительности воздействия составляла 47 мес) [38]. Кроме того, при ретроспективном анализе популяции пациентов, перенесших трансплантацию почки и также получавших ингибиторы mTOR, была оценена когорта из 31 пациента и сообщено, что долгосрочная терапия ингибиторами mTOR не влияла на рост и половое созревание (средняя длительность последующего наблюдения – 4,9 года) [77]. Дальнейшее запланированное наблюдение за популяцией участников исследования EXIST‑1 должно предоставить дополнительные доказательства в отношении влияния эверолимуса на рост и половое созревание детей и подростков.
Выводы и перспективы
Недавние исследования, посвященные КТС, в очередной раз подчеркнули особую ценность таргетной терапии, в основе которой лежит воздействие на молекулярные патофизиологические механизмы развития заболевания. КТС может служить моделью для демонстрации возможности модификации приобретенных и врожденных генетических дефектов, вызывающих дисфункцию головного мозга.
Цель проводимых в настоящее время исследований состоит в определении роли ингибирования mTOR при неврологических расстройствах и нарушениях развития, которые не связаны с КТС (например, при синдромах Лея, Дауна и нейрофиброматозе 1 и 2-го типов), но имеют с ним общую характеристику, а именно – гиперактивацию сигнального пути mTOR. Для достижения этой цели необходимо лучшее понимание фундаментальных особенностей молекулярной патофизиологии этих различных врожденных и приобретенных заболеваний. Кроме того, отдельной серьезной проблемой также остается отбор пациентов для участия как в фундаментальных научных, так и в клинических исследованиях.
Однако уже имеющиеся результаты исследований в этих областях показывают, что после дальнейшего изучения ингибирование mTOR вполне может стать вариантом терапии при вышеуказанных неврологических нарушениях, для лечения которых в настоящее время имеется крайне мало возможностей.
Помимо дальнейшего изучения ингибирования mTOR при редких неврологических расстройствах, дальнейшие исследования также будут сфокусированы на определении оптимального использования ингибиторов mTOR при КТС, включая дозирование при краткосрочном и долгосрочном применении, а также установлении того возраста, в котором наиболее целесообразно начинать терапию.
В последнее время отмечается существенный интерес к определению стратегий лечения тех пациентов с КТС, у которых это заболевание было диагностировано в раннем детском возрасте, т.е. в тот период, когда потенциальные эффекты ингибиторов mTOR или других лекарственных средств (при условии их максимально раннего применения) могут радикально уменьшить или даже предотвратить развитие ряда клинических проявлений заболевания (включая судорожные припадки, задержку развития, аутизм, заболевание почек, опухоли кожи и другие поражения).
Ингибиторы mTOR все шире используют в лечении не только гамартомных и онкологических проявлений КТС, но и в качестве вспомогательной терапии при эпилепсии и интеллектуальной недостаточности. Ожидается, что проводимые в настоящее время исследования будут способствовать лучшему пониманию роли этих препаратов в лечении и накоплению большего массива данных о профиле их токсичности. Как следствие этого, стратегия ингибирования mTOR при КТС (в том числе – с целью предотвращения долгосрочных отрицательных последствий, таких как умственная отсталость, аутизм и рефрактерные судорожные припадки) уже в ближайшие годы может быть широко внедрена в клиническую практику.
Литература
1. Franz D.N. Everolimus: an mTOR inhibitor for the treatment of tuberous sclerosis. Expert Rev Anticancer Ther. 2011; 11: 1181-92.
2. Baskin Jr H.J. The pathogenesis and imaging of the tuberous sclerosis complex. Pediatr Radiol. 2008; 38: 936-52.
3. Curatolo P., Bombardieri R., Jozwiak S. Tuberous sclerosis. Lancet. 2008; 372: 657-68.
4. Osborne J.P., Fryer A., Webb D. Epidemiology of tuberous sclerosis. Ann N Y Acad Sci. 1991; 615: 125-7.
5. Krueger D.A., Northrup H. Tuberous sclerosis complex surveillance and management: recommendations of the 2012 International Tuberous Sclerosis Complex Consensus Conference. Pediatr Neurol. 2013; 49: 255-65.
6. Crino P.B., Nathanson K.L., Henske E.P. The tuberous sclerosis complex. N Engl J Med. 2006; 355: 1345-56.
7. Kwiatkowski D.J., Manning B.D. Tuberous sclerosis: a GAP at the crossroads of multiple signaling pathways. Hum Mol Genet. 2005; 14 (spec N 2): R251-8.
8. Goh S., Butler W., Thiele E.A. Subependymal giant cell tumors in tuberous sclerosis complex. Neurology. 2004; 63: 1457-61.
9. Adriaensen M.E., Schaefer-Prokop C.M., Stijnen T., Duyndam D.A., Zonnenberg B.A., Prokop M. Prevalence of subependymal giant cell tumors in patients with tuberous sclerosis and a review of the literature. Eur J Neurol. 2009; 16: 691-6.
10. Krueger D.A. Management of CNS-related disease manifestations in patients with tuberous sclerosis complex. Curr Treat Options Neurol. 2013; 15: 618-33.
...
77. Kranz B., Wingen A.M., Vester U., Knig J., Hoyer P.F. Long-term side effects of treatment with mTOR inhibitors in children after renal transplantation. Pediatr Nephrol. 2013; 28: 1293-8.
Полный список литературы находится в редакции.
Статья печатается в сокращении.
Franz D.N., Capal J.K. mTOR inhibitors in the pharmacologic management of tuberous sclerosis complex and their potential role
in other rare neurodevelopmental disorders. Orphanet Journal of Rare Diseases 2017; 12: 51.
Перевела с англ. Елена Терещенко
Тематичний номер «Педіатрія» №1 (44), березень 2018 р.




