4 січня, 2018
Клінічні аспекти недостатності та дефіциту вітаміну D у тиреоїдології
 Останніми роками спостерігається лавиноподібне зростання кількості публікацій у медичній науковій літературі, присвячених потенційному значенню порушень обміну вітаміну D у різноманітній патології й оцінці ефектів лікування препаратами вітаміну D. Причиною такого сплеску інтересу є нові дані про фізіологічну роль похідних цього вітаміну.
Останніми роками спостерігається лавиноподібне зростання кількості публікацій у медичній науковій літературі, присвячених потенційному значенню порушень обміну вітаміну D у різноманітній патології й оцінці ефектів лікування препаратами вітаміну D. Причиною такого сплеску інтересу є нові дані про фізіологічну роль похідних цього вітаміну.
Вітамін D3 (холекальциферол) надходить до організму людини здебільшого внаслідок фотосинтезу в шкірі під дією ультрафіолетового випромінювання. Надалі холекальциферол гідроксилюється в печінці з утворенням 25(OH)D3 – кальцидіолу, вітаміну, який є основною депонованою і транспортною формою.
Незначна частина кальцидіолу під дією ферменту 1-альфа-гідроксилази перетворюється на активний гормон кальцитріол – 1,25(OH)2D3. Рівень циркулюючого кальцитріолу визначається в основному його синтезом у клітинах ниркових канальців (M.F. Holick, 2013).
Згідно з класичними уявленнями основні фізіологічні функції кальцитріолу полягають у посиленні абсорбції кальцію і фосфору в кишечнику, посиленні реабсорбції кальцію в дистальних ниркових канальцях, пришвидшенні мінералізації кістки й індукції синтезу ліганда рецептора ядерного чинника kВ (Receptor activator of nuclear factor kappa-B ligand, RANKL), який стимулює диференціювання преостеокластів в остеокласти. Ефективна дія кальцитріолу переважно пов’язана з його з’єднанням в цитоплазмі клітини із специфічним рецептором – VDR (vitamin D receptor). Комплекс D3-VDR переміщується в ядро, з’єднується з ретиноїдним рецептором X (RXR) з утворенням гетеродимера D3-VDR-RXR. Останній шляхом поєднання зі специфічними послідовностями ДНК (VDRE – елементами, що відповідають на вітамін D), керує транскрипцією відповідних генів (M.R. Haussler et al., 2011).
Нещодавні дослідження констатують важливі факти. Так, 1-альфа-гідроксилаза активна в багатьох клітинах різних органів і тканин, серед яких прищитоподібні залози, кістки, тимус, яєчники, плацента, простата, головний мозок, молочні залози, легені, острівці підшлункової залози, гладкі міоцити та ендотеліальні клітини судин, адипоцити, хондроцити, епітелій кишечника, гепатоцити, клітини тубулярного епітелію нирок, T- і B-лімфоцити, макрофаги, дендритні клітини, стромальні клітини кісткового мозку, кератиноцити шкіри (J. Li et al., 2008).
Це означає, що вказані клітини синтезують кальцитріол. Однак у зв’язку з тим, що кількість синтезованого гормона невелика, він справляє вплив переважно на клітину, що виробляє його, а також на її найближчих «сусідів» (автокринний і паракринний ефекти).
У всіх зазначених органах і тканинах, а також у низці інших (сім’яники, міокард, стравохід, шлунок, скелетні м’язи) виявляють рецептори до кальцитріолу (G. Verhave et al., 2010). Наявність цих рецепторів у тканинах свідчить про те, що гормон бере участь у регуляції діяльності відповідних структур. Послідовності нуклеотидів, відповідальних за зв’язування активованого рецептора вітаміну D, виявлено у більш ніж 200 генах. До продуктів генів, безпосередньо регульованих VDR, належать чинники росту, гормони, медіатори запалення і регулятори кальцієвого обміну (M.H. de Borst et al., 2011).
Отже, на сьогодні з’ясовано, що кальцитріол як один з прадавніх представників суперсімейства стероїдних ядерних гормонів у людському організмі регулює широке коло процесів, серед яких, крім обміну кальцію і фосфору, клітинний ріст і диференціювання, гістогенез, реакції вродженого і адаптивного імунітету, вуглеводний обмін і, ймовірно, ще багато інших.
Компоненти метаболізму вітаміну D та VDR поєднуються, утворюючи ендокринну систему вітаміну D. Її функції полягають у генеруванні біологічних реакцій у більш ніж 40 тканинах-мішенях за рахунок регуляції VDR-транскрипції генів (геномний механізм) і швидких позагеномних реакцій, здійснюваних у процесі взаємодії з VDR, які локалізуються на поверхні низки клітин. За рахунок геномних і позагеномних механізмів D-ендокринна система бере участь у регуляції мінерального гомеостазу (насамперед в обміні кальцію і фосфору), концентрації електролітів й обміну енергії, пригнічує клітинну проліферацію та індукцію кінцевого диференціювання, інгібує ангіогенез, стимулює синтез інсуліну, пригнічує секрецію реніну та підвищує синтез кателіцидину в макрофагах (D.D. Bikle, 2010).
Значущість цієї ендокринної системи для здоров’я людини підтвердилася у багатьох епідеміологічних дослідженнях (J.K. Virtanen et al., 2011). Так, дефіцит вітаміну D у найрізноманітніших популяціях асоціюється зі зростанням загальної смертності. У дослідженні NHANES III (2008) за результатами аналізу даних понад 13 тис. учасників співвідношення ризиків смерті від будь-якої причини між верхнім і нижнім квартилями рівня вітаміну D у крові становило 1,26. Більше того, результати метааналізу рандомізованих клінічних досліджень демонструють достовірне зниження ризику смерті від будь-яких причин у хворих, що отримували лікування вітаміном D, на 7% (M.L. Melamed et al., 2008).
Можливість дістати такі результати шляхом простого, безпечного і недорогого втручання розглядається з оптимізмом. Крім того, розуміння механізмів цього позитивного впливу могло б виявитися дуже корисним у різних галузях медицини.
Аутоімунні захворювання – одна з основних причин інвалідності і смертності в промислово розвинутих країнах після онкологічних і серцево-судинних захворювань. Етіологія і патогенез більшості аутоімунних розладів залишаються нез’ясованими. На патогенез аутоімунної патології впливає велика кількість чинників, до яких віднедавна відносять і порушення обміну вітаміну D. Клінічні дослідження підтверджують, що вітамін D має важливе значення для модуляції імунних відповідей при різних запальних та аутоімунних захворюваннях.
Виявлення VDR практично в усіх клітинах імунної системи, особливо антигенпрезентуючих клітинах (макрофагах і дендритних клітинах) і активованих Т-клітинах, зробило необхідним дослідження вітаміну D як імуномодулятора (A. Mackawy, 2014). Крім того, відомо, що активація ядерного VDR впливає на транскрипцію, проліферацію і диференціювання клітин імунної системи.
Попри те що сучасні огляди припускають вплив низьких рівнів вітаміну D на розвиток аутоімунних захворювань, зв’язок між вітаміном D й аутоімунними тиреоїдними захворюваннями, до яких належать дифузний токсичний зоб (ДТЗ) і аутоімунний тиреоїдит (АІТ), досі не встановлений.
Щитоподібна залоза (ЩЗ) – найбільший за розмірами ендокринний орган, одна з невід’ємних частин нейроімуноендокринної системи, інтегруюче значення якої проявляється на всіх етапах життя людини, починаючи з найбільш ранніх стадій ембріогенезу. Підвищення інтересу до проблеми тиреоїдної патології в останні роки пояснюється її зростаючою поширеністю серед населення України, високою частотою спричинюваною нею тимчасової і стійкої непрацездатності, що визначає соціальну значущість цих захворювань. У результаті прогресу теоретичної і практичної тиреоїдології уявлення про сутність захворювань ЩЗ зазнали істотних змін. Збільшення частоти патології ЩЗ зумовлене впливом несприятливих факторів довкілля, погіршенням загальної екологічної обстановки на тлі зниження імунологічного захисту організму. Радіаційний удар унаслідок Чорнобильської катастрофи вражав насамперед ЩЗ, що зумовлено масивним викидом радіоізотопів йоду. Нагромадження останніх саме в ЩЗ визначає їх «органотропність» як можливих і реальних патогенетичних чинників тиреоїдної патології в найближчі й віддалені терміни після опромінення. Як відомо, захворювання ЩЗ посідають одне з перших місць у структурі ендокринопатій, при цьому аутоімунна тиреоїдна патологія трапляється найчастіше серед аутоімунних захворювань. Поширеність аутоімунної тиреоїдної патології, включаючи АІТ, ДТЗ, післяпологовий тиреоїдит, оцінюється в 5% у загальній популяції (D.S. McLeod, D.S. Cooper, 2012).
В одному з останніх метааналізів було оцінено взаємозв’язок між рівнями вітаміну D й аутоімунними захворюваннями ЩЗ на підставі даних систематичних літературних оглядів. Були відібрані роботи, в яких оцінювали зв’язок між рівнями вітаміну D та аутоімунними тиреоїдними захворюваннями за базами даних PubMed, Embase, CENTRAL і China National Knowledge Infrastructure. Порівняно з групою контролю у пацієнтів з аутоімунними захворюваннями ЩЗ відзначалися нижчі рівні й частіший дефіцит 25(ОН)D. Крім того, аналіз підгруп показав, що ДТЗ і АІТ частіше траплялися у пацієнтів з низьким рівнем і дефіцитом 25(ОН)D. Тому можна припустити, що недостатність 25(ОН)D пов’язана з розвитком аутоімунних тиреоїдних захворювань (J. Wang et al., 2015).
У дослідженні E.E. Mazokopakis і співавт. (2015) було оцінено статус вітаміну D шляхом визначення рівня 25(ОН)D у 218 пацієнтів (180 жінок і 38 чоловіків) з АІТ у стані еутиреозу, які проживають і працюють на острові Кріт (Греція). Серед них дефіцит вітаміну D (<30 нг/мл) відзначався у 186 (85,3%) осіб. Пацієнтам з АІТ на тлі дефіциту вітаміну D призначали холекальциферол перорально в дозі 1200-4000 МО щоденно впродовж 4 міс. Результати дослідження показали наявність значущої зворотної кореляції між рівнями 25(ОН)D і титром антитіл до тиреоїдної пероксидази (ТПО). Крім того, рівні антитіл до ТПО були достовірно вищі серед хворих на АІТ з дефіцитом вітаміну D порівняно з пацієнтами з нормальним вмістом вітаміну D у сироватці крові. Додаткове призначення холекальциферолу сприяло зниженню на 20,3% рівня антитіл до ТПО.
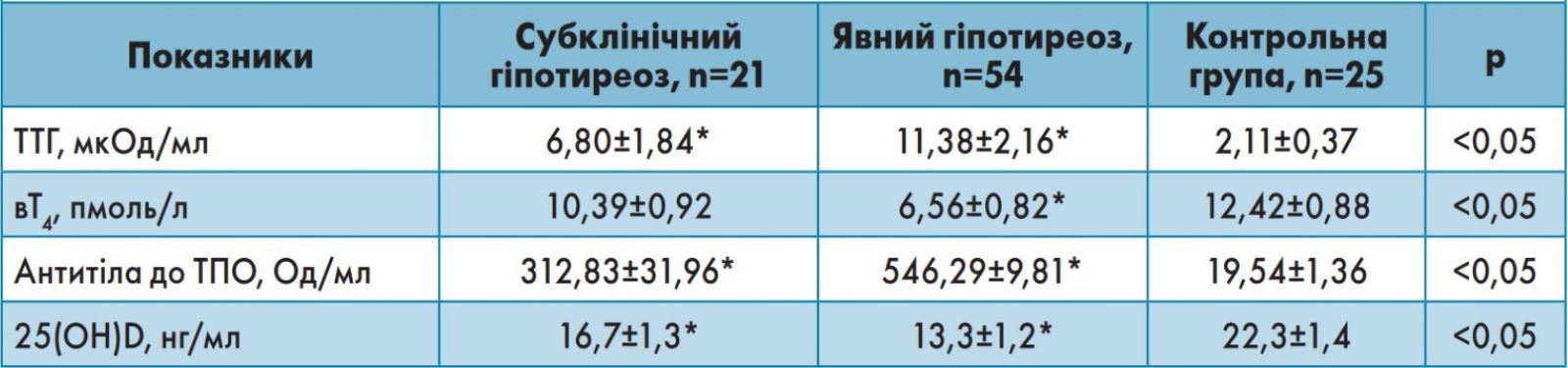
У проведеному в Україні дослідженні (В.В. Поворознюк, І.В. Паньків, 2014) було визначено рівень 25(ОН)D у 75 хворих (59 жінок і 16 чоловіків) на АІТ із явним і субклінічним гіпотиреозом. Відповідно до рівнів тиреотропного гормона (ТТГ), вільного тироксину (вТ4) і вільного трийодтироніну (вТ3) хворі на АІТ були розподілені на дві групи: субклінічний гіпотиреоз (підвищений рівень ТТГ за нормальних показників вТ4 і вТ3) і явний гіпотиреоз (підвищений рівень ТТГ за знижених показників вТ4 і вТ3). У таблиці 1 наведено показники рівня вітаміну D і функціонального стану ЩЗ у зазначених хворих. Рівень 25(OH)D у сироватці крові був достовірно нижчим при субклінічному (16,7±1,3 нг/мл) і явному гіпотиреозі (13,3±1,2 нг/мл) порівняно з контрольною групою (22,3±1,4 нг/мл; p<0,05). Рівень антитіл до ТПО був достовірно вищим у пацієнтів з АІТ порівняно з контрольною групою. Вміст 25(ОН)D у крові перебував у позитивній кореляції з об’ємом ЩЗ і у зворотній – із рівнем антитіл до ТПО. Достовірна негативна кореляція також встановлена між вмістом у крові ТТГ і вітаміну D. Ці дані свідчать про потенційну роль вітаміну D у розвитку і прогресуванні гіпотиреозу.
Таблиця 1. Показники функціонального стану ЩЗ, титру антитіл до ТПО і вітаміну D у крові хворих на гіпотиреоз
(В.В. Поворознюк, І.В. Паньків, 2014)
Два механізми дають можливість пояснити низькі рівні вітаміну D у хворих на АІТ з гіпотиреозом: по-перше, низькі рівні вітаміну D можуть бути спричинені зниженою абсорбцією вітаміну D з кишечника, по-друге, організм належним чином не активує вітамін D (G. Effraimidis et al., 2012).
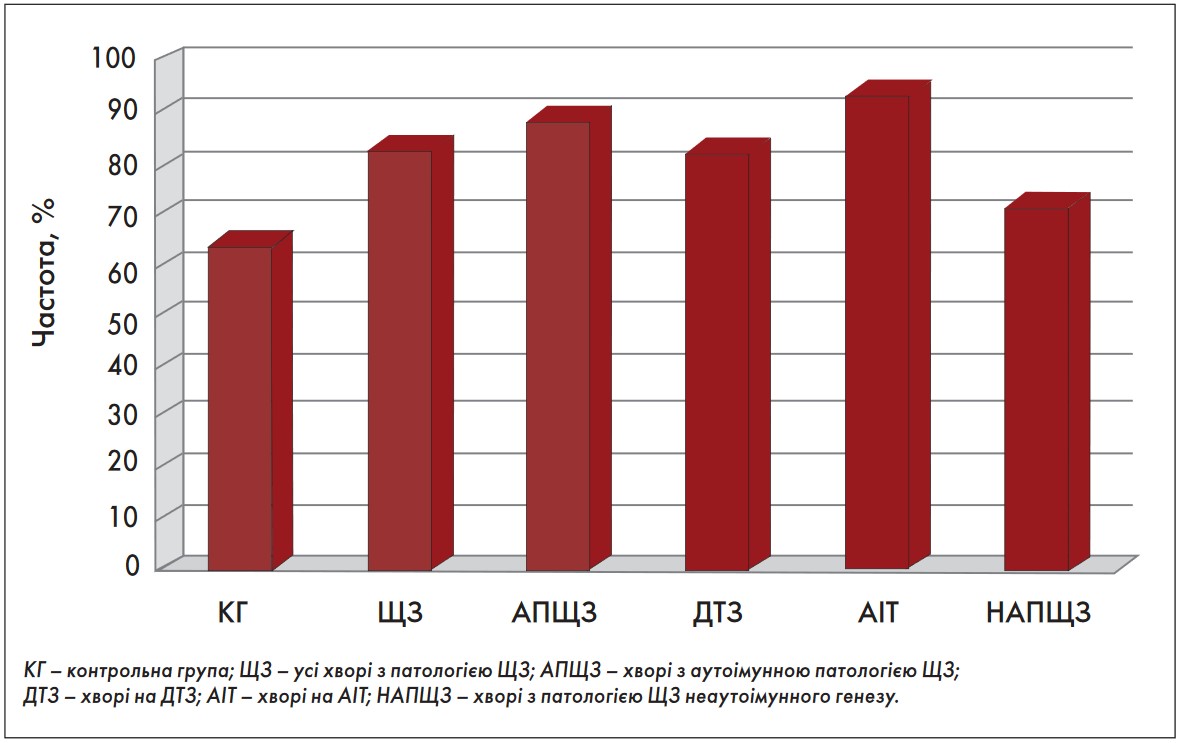
У ході подальшого дослідження (В.В. Поворознюк, І.В. Паньків, 2015) було встановлено взаємозв’язок між дефіцитом вітаміну D та аутоімунною патологією ЩЗ. В одномоментному дослідженні обстежено 119 осіб: 62 хворі з аутоімунною тиреоїдною патологією (ДТЗ та АІТ), 32 хворі без аутоімунної тиреоїдної патології (дифузний вузловий нетоксичний зоб) і 25 здорових осіб. Підтвердженням аутоімунної патології ЩЗ була наявність ДТЗ або АІТ з підвищеними титрами антитіл до ТПО i/або до рецептора ТТГ. Дефіцит вітаміну D встановлено у 82,9% (78/94) пацієнтів із захворюваннями ЩЗ різного генезу. Водночас серед осіб контрольної групи цей показник становив 64% (16/25). При цьому серед хворих з аутоімунною патологією ЩЗ частота дефіциту вітаміну D сягала 88,7% (55/62). Найчастіше дефіцит вітаміну D спостерігався у хворих на АІТ – у 94,1% (32/34). Серед хворих на ДТЗ дефіцит вітаміну D зафіксовано у 82,1% (23/28). Частота дефіциту вітаміну D показана на рисунку 1. Наявність антитиреоїдних антитіл достовірно частіше спостерігалася у пацієнтів з дефіцитом вітаміну D, ніж в осіб з нормальним вмістом вітаміну D у крові (70,5 проти 43,8%; р<0,05).
Рис. 1. Частота дефіциту вітаміну D у пацієнтів із тиреоїдною патологією порівняно з контрольною групою (В.В. Поворознюк, І.В. Паньків, 2015)
Автори також встановили безпосередній зв’язок між рівнями ТТГ і забезпеченням організму вітаміном D. Так, рівень ТТГ при АІТ становив 7,8 мМО/л за умов дефіциту вітаміну D (<20 нг/мл) і 3,4 мМО/л – за умов адекватного забезпечення вітаміном D. У хворих на ДТЗ відповідні показники ТТГ становили 0,07 мМО/л за вмісту вітаміну D <20 нг/мл і 2,9 мМО/л – за вмісту вітаміну D >20 нг/мл. У пацієнтів без аутоімунної тиреоїдної патології не спостерігали залежність між рівнями ТТГ і вмістом вітаміну D у крові. При цьому не встановлено кореляції між рівнем вТ4 і забезпеченням організму вітаміном D у всіх обстежених.
Отримані результати щодо ролі вітаміну D у патогенезі аутоімунних захворювань ЩЗ указують на доцільність проведення скринінгу вмісту вітаміну D у крові пацієнтів з такою патологією.
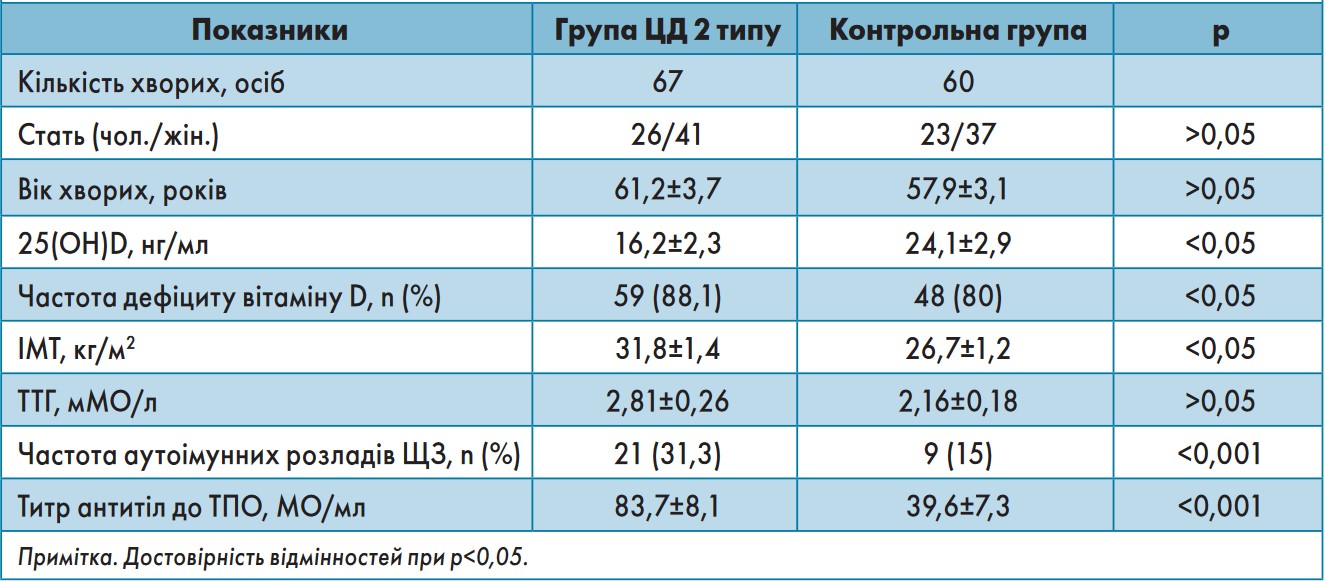
Таблиця 2. Частота аутоімунних розладів ЩЗ у хворих на ЦД 2 типу
(І.В. Паньків, 2015)
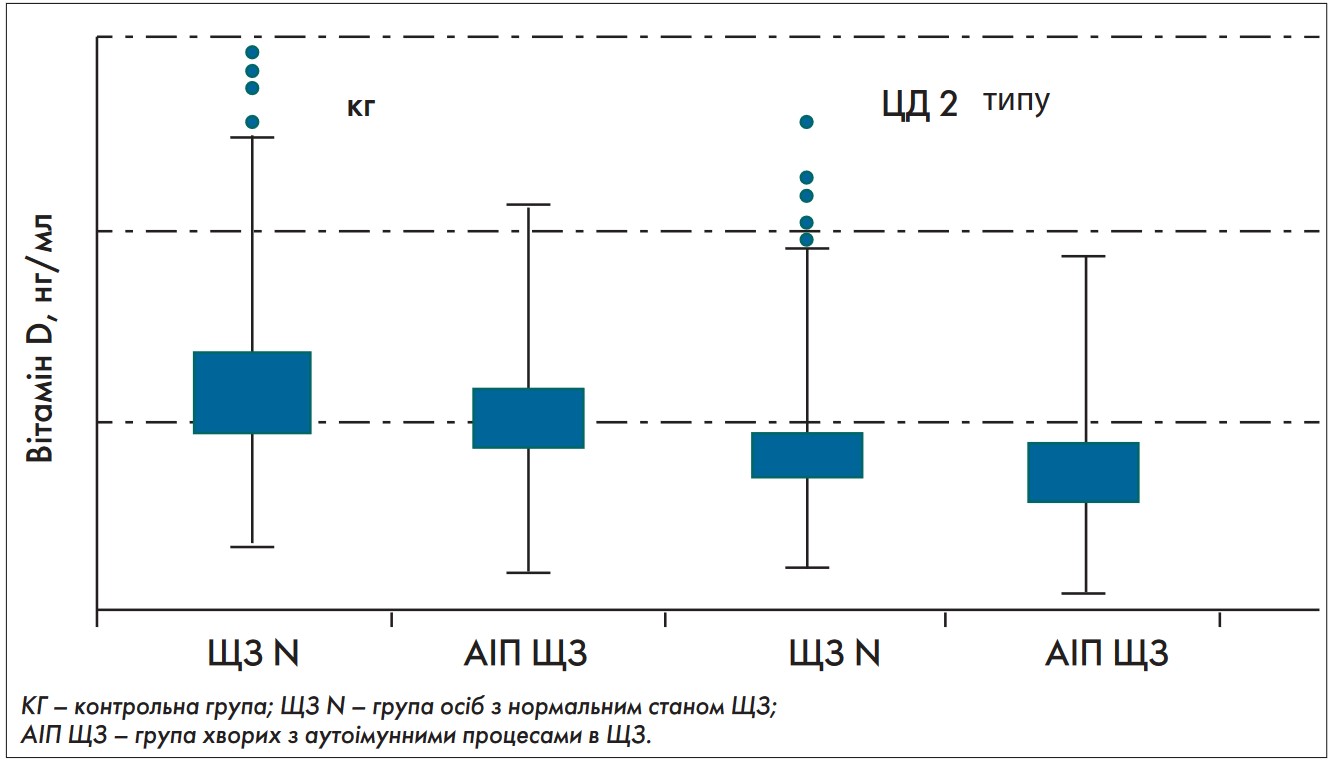
Взаємозв’язок між цукровим діабетом (ЦД) 2 типу та аутоімунною патологією ЩЗ залишається предметом дискусій. В окремих публікаціях указано на відсутність прямих асоціацій між ними (P.S. George et al., 2012), однак в інших дослідженнях встановлено збільшення частоти аутоімунних тиреоїдних розладів у хворих на ЦД 2 типу (J.J. Doez, P. Iglesias, 2012). В українському дослідженні (І.В. Паньків, 2015) вивчали взаємозв’язок між ЦД 2 типу й аутоімунною патологією ЩЗ на тлі дефіциту вітаміну D. Спостереженням було охоплено 67 хворих на ЦД 2 типу і 60 осіб контрольної групи (без порушень вуглеводного обміну). Середня тривалість ЦД 2 типу становила 8,2±1,4 року, рівень глікованого гемоглобіну – 7,3±0,7%. Пацієнти з ЦД 2 типу мали достовірно більшу масу тіла, менший вміст вітаміну D у крові й вищий титр антитіл до ТПО порівняно з контрольною групою (табл. 2). Частота тиреоїдних аутоімунних розладів була вдвічі більшою у пацієнтів із ЦД 2 типу. Частота дефіциту вітаміну D була достовірно більшою серед хворих на ЦД 2 типу (88,1%) порівняно з контрольною групою. Рівні вітаміну D та показники аутоімунних тиреоїдних розладів в обстежених осіб наведено на рисунку 2.
Рис. 2. Аналіз вмісту вітаміну D у крові в різних групах обстежених залежно від наявності тиреоїдної аутоімунної патології (І.В. Паньків, 2015)
Багатофакторний логістичний регресійний аналіз показників віку, статі, індексу маси тіла (ІМТ) показав, що наявність ЦД 2 типу (відносний ризик, ВР 2,69; 95% довірчий інтервал, ДІ 1,24-5,35) і рівень вітаміну D (ВР 1,44; 95% ДІ 1,02-1,69) достовірно асоційовані з наявністю аутоімунних процесів у ЩЗ.
Результати інтерпретації даних аналізу в клінічних термінах показують, що зниження рівня вітаміну D на одну одиницю в осіб із ЦД 2 типу асоціюється із збільшенням майже на 25% частоти виникнення аутоімунних процесів у ЩЗ. Тому можна припустити наявність взаємозв’язку між вмістом вітаміну D у крові і виникненням аутоімунних процесів у ЩЗ на тлі ЦД 2 типу. Отримані авторами результати підтверджують такі припущення. По-перше, асоціація між аутоімунним процесами в ЩЗ і ЦД 2 типу встановлена на підставі даних про те, що в осіб із ЦД 2 типу істотно зростає ризик виникнення аутоімунних тиреоїдних розладів порівняно із здоровими особами. По-друге, рівні вітаміну D достовірно асоційовані з наявністю антитиреоїдних антитіл в осіб з ЦД 2 типу, але не з показниками контрольної групи. По-третє, встановлено, що нижчий рівень вітаміну D у крові пов’язаний зі збільшенням частоти виявлення антитіл до ТПО у хворих на ЦД 2 типу.
Нещодавно було проведено дослідження вмісту вітаміну D у крові, а також його можливого впливу на перебіг захворювання у 57 пацієнток із ДТЗ (І.В. Паньків, 2015). Обстежених розподілили на дві групи залежно від стану компенсації тиреотоксикозу. Першу групу було сформовано з 23 жінок із ДТЗ у стані тривалої (понад 6-9 міс) компенсації тиреотоксикозу. До другої групи увійшли 34 пацієнтки в стані декомпенсації ДТЗ. Тривалість захворювання в обох групах не відрізнялася і становила від 6 міс до 3 років. Протягом того самого періоду були обстежені 25 практично здорових жінок без порушення функції ЩЗ і без підвищених титрів антитіл до рецептора ТТГ.
Пацієнтки із ДТЗ не відрізнялися за віком і тривалістю захворювання. Водночас у жінок у стані декомпенсації тиреотоксикозу спостерігався знижений рівень ТТГ (0,008±0,003 мМО/л) і підвищений рівень вТ4 (2,27±0,39 нг/дл) порівняно з обстеженими особами двох інших груп. Крім того, в жінок з некомпенсованим тиреотоксикозом спостерігався достовірно вищий рівень антитіл до рецептора ТТГ (11,8±2,3 МО/л).
У ході дослідження встановлено, що вміст вітаміну D у крові виявився достовірно нижчим у пацієнток із ДТЗ у стані декомпенсації на час обстеження порівняно з групою жінок із ДТЗ у стані стабільної компенсації тиреотоксикозу і контрольною групою. При цьому не встановлено достовірних відмінностей між рівнем вітаміну D у жінок із ДТЗ у стані компенсації і контрольною групою. Результати кореляційного аналізу свідчать про наявність у пацієнток із ДТЗ у стані декомпенсації тиреотоксикозу значущого зворотного зв’язку між вмістом вітаміну D і рівнем антитіл до рецептора ТТГ у крові (r= -0,47; р<0,05).
Отримані результати вказують на асоціацію між дефіцитом вітаміну D і тиреоїдною дисфункцією, спричиненою аутоімунним процесом.
Низький рівень вітаміну D, можливо, є первинним феноменом, залученим до патогенезу хвороби. З іншого боку, він може бути наслідком такої патології. Низький вміст вітаміну D у крові при інших аутоімунних хворобах можна пояснити мальабсорбцією (наприклад, при розсіяному склерозі) або відсутністю інсоляції через ураження шкіри (наприклад, при дерматоміозиті). Однак хворі з підвищеною функцією ЩЗ у більшості випадків не страждають на захворювання шкіри чи мальабсорбцію. Можливим поясненням низького вмісту вітаміну D у крові може бути пришвидшений кістковий метаболізм при гіпертиреозі, що призводить до підвищеного рівня кальцію і негативного зворотного зв’язку із вмістом паратгормона і синтезом 1,25(OH)2D3. Тому потрібні подальші дослідження для встановлення первинної ролі дефіциту вітаміну D у патогенезі аутоімунних захворювань ЩЗ, однак результати досліджень вказують, що низький рівень вітаміну D може впливати на клінічний перебіг ДТЗ.
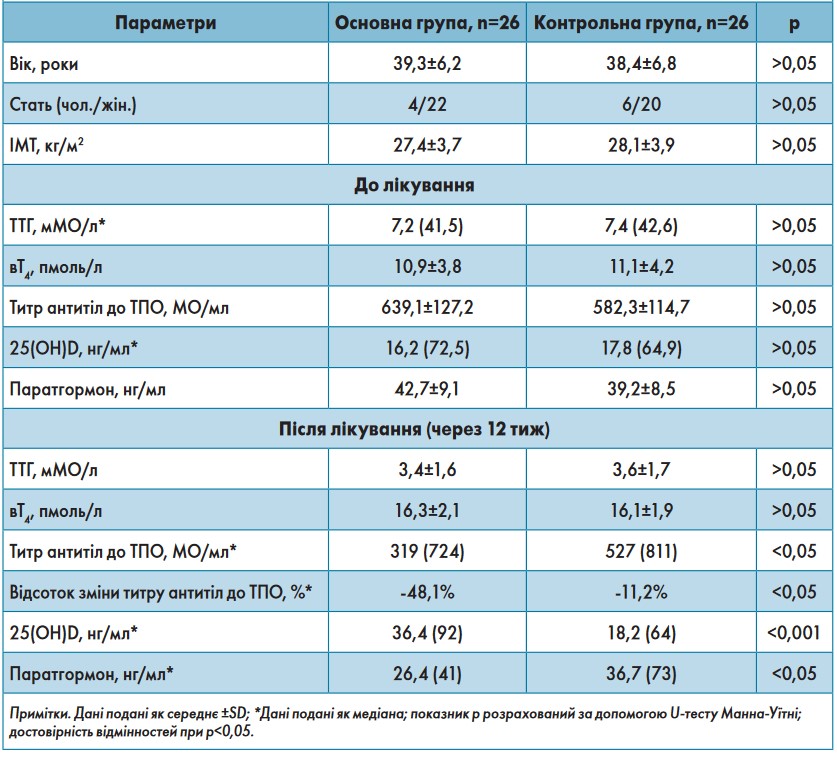
Ще в одному дослідженні (І.В. Паньків, 2016) було вивчено ефективність додаткового призначення холекальциферолу з метою нормалізації рівня 25(ОН)D у сироватці крові та зниження титру антитіл до ТПО у хворих на АІТ. Холекальциферол у дозі до 4000 МО/добу (до 28 000 МО/тиж) отримували 26 пацієнтів. Обстеження проводили на початку і наприкінці 12-тижневого лікування. Позитивним результатом лікування вважали зниження титру антитіл до ТПО принаймні на 25%. У всіх пацієнтів відзначався дефіцит вітаміну D (вміст 25(ОН)D у сироватці крові <20 нг/мл), а рівень антитіл до ТПО перевищував 102 МО/мл. При цьому найвищі титри антитіл до ТПО спостерігали в пацієнтів з більш низькими показниками 25(ОН)D. На тлі терапії впродовж 3 міс не спостерігалося жодних несприятливих ефектів і відмови хворих від лікування. Після лікування зафіксовано достовірну різницю в титрах антитіл до ТПО у пацієнтів з АІТ порівняно з контрольною групою. Відсоток змін медіани титру антитіл до ТПО становили -48,1% у групі лікування і -11,2% – у контрольній групі (p=0,032). Загалом зменшення титру антитіл до ТПО на 25% і більше досягнуто у 73,1% пацієнтів основної групи і у 23,1% пацієнтів контрольної групи (р=0,025). Призначення препарату вітаміну D привело до достовірного підвищення вмісту 25(OH)D у сироватці крові (табл. 3). Це одне з перших досліджень, яке демонструє ефективність призначення вітаміну D у терапевтичних дозах хворим на АІТ з достовірним зниженням титру антитіл до ТПО.
Таблиця 3. Порівняльна характеристика функціонального стану ЩЗ і титру антитіл до ТПО в процесі лікування холекальциферолом (І.В. Паньків, 2016)
Як бачимо, роль вітаміну D виходить далеко за межі кісткового метаболізму. Вітамін D належить до одного з найголовніших чинників розвитку життя на планеті і людської еволюції (The Scientific Advisory Committee on Nutrition – SACN, 2016). Шкіра є ключовим органом людського організму: вона є місцем синтезу цього вітаміну і тканиною-мішенню для біологічно активних метаболітів вітаміну D. Сьогодні інтенсивно вивчається роль вітаміну D не лише в регуляції рівня кальцію, а й у патогенезі хронічного системного запалення, порушенні чутливості тканин до інсуліну. З’являється дедалі більше доказів його потенційної ролі в профілактиці різних хронічних неінфекційних захворювань – від онкологічних до серцево-судинних, аутоімунних і метаболічних розладів. Установлено, що адекватний вміст вітаміну D у крові здатний знижувати ризик розвитку ЦД 2 типу, ожиріння, а також аутоімунної деструкції β-клітин підшлункової залози і деяких кардіометаболічних чинників ризику і серцево-судинних захворювань (ССЗ) (D. Dutta et al., 2014). Препарати вітаміну D у найближчому майбутньому можуть стати додатковими і необхідними компонентами корекції інсулінорезистентності, хронічного запалення, а також профілактики порушень вуглеводного обміну і ССЗ (F. D’Aurizio et al., 2015). Нові настанови директиви Public Health England рекомендують достатнє вживання вітаміну D кожним мешканцем Великої Британії для забезпечення нормального стану кістково-м’язової системи.
Результати епідеміологічних досліджень свідчать, що значна частина населення різних країн і континентів страждає від D-гіповітамінозу, але через відсутність клінічних симптомів і незацікавленість лікарів більшість цих випадків залишаються без належної уваги. Необхідно враховувати, що навіть клінічно не виражений D-гіповітаміноз може сприяти розвитку вищезгаданих імунологічних розладів, підвищенню сприйнятливості до багатьох захворювань і пухлинного переродження клітин різних органів і тканин. Оскільки в географічних умовах України поширеність D-гіповітамінозу є високою, його виявлення, профілактика і лікування мають надзвичайне значення для здоров’я нашого населення.
Слід згадати, що радянська система охорони здоров’я приділяла цій важливій проблемі велику увагу, і було нагромаджено значний досвід з її розв’язання, принаймні в дитячого населення. Сьогодні необхідно враховувати попередні досягнення і, крім того, задіяти нові сучасні можливості, знання і технології. Слід створювати програми епідеміологічних, клінічних, експериментальних досліджень, проводити скринінг рівня вітаміну D у крові для виявлення D-гіповітамінозу, впроваджувати нові, досконаліші препарати вітаміну D для перорального застосування.
Оскільки на сьогодні доведено позитивний вплив оптимального рівня 25(OH) D у сироватці крові як у дітей, так і в дорослих, доцільно підтримувати його для здорової популяції в межах 30-50 нг/мл згідно з Методичними рекомендаціями для країн Центральної Європи (2013). Роль дефіциту та недостатності вітаміну D у порушеннях регуляції багатьох систем організму людини та розвитку різних патологічних станів обґрунтовує доцільність ширшого використання методів корекції статусу вітаміну D. Попри необхідність проведення масштабних рандомізованих клінічних випробувань для визначення схем використання препаратів вітаміну D, уже зараз не викликає сумніву той факт, що нормалізація рівня 25(ОН)D у сироватці крові потрібна на всіх вікових етапах онтогенезу.
Література
1. Поворознюк В.В. Фактичне харчування, вітамін D-дефіцит та мінеральна щільність кісткової тканини у дорослого населення різних регіонів України / В.В. Поворознюк, Н.І. Балацька, Ф.В. Климовицький, О.В. Синенький // Травма. – 2012. – № 4. – С. 12-16.
2. Thacher T.D. Vitamin D Insufficiency / T.D. Thacher, B.L. Clarke // Mayo Clin Proc. – 2011. – Vol. 86, № 1. – P. 50-60.
3. Endocrine Society: Evaluation, treatment, and prevention of vitamin D deficiency: an Endocrine Society clinical practice guideline / M.F. Holick, N.C. Binkley, H.A. Bischoff-Ferrari et al. // J. Clin Endocrinol Metab. – 2011. – Vol. 96. – Р. 1911-1930.
4. Vitamin D and cardiovascular disease / K. Kienreich, A. Tomaschitz, N. Verheyen et al. // Nutrients. – 2013. – Vol. 5 (8). – P. 3005-3021. doi: 10.3390/nu5083005.
5. Ginde A.A. Demographic differences and trends of vitamin D insufficiency in the US population, 1988-2004 / A.A. Ginde, M.C. Liu, C.A. Camargo // Arch Intern Med. – 2009. – Vol. 169 (6). – P. 626-632.
6. Vitamin D and mortality: meta-analysis of individual participant data from a large consortium of cohort studies from Europe and the United States / B. Schuttker, R. Jorde, A. Peasey еt al. // BMJ. – 2014. – Vol. 348.
7. Kriegel M.A. Does vitamin D affect risk of developing autoimmune disease? A Systematic review / M.A. Kriegel, J.A. Manson, K.H. Costenbader // Semin. Arthritis Rheum. – 2011. – Vol. 40 (6). – P. 512-531.
8. Дефіцит та недостатність вітаміну D у жителів України / В.В. Поворознюк, Н.І. Балацька, В.Я. Муц, О.А. Вдовіна // Біль. Суглоби. Хребет. – 2011. – № 4 (04). – С. 3-8.
9. Комісаренко Ю.І. Корекція вітаміном D порушень метаболічних процесів у пацієнтів із цукровим діабетом 1-го та 2-го типів / Ю.І. Комісаренко // Ukrainian Biochemical Journal. – 2014. – Т. 86, № 1. – С. 111-116.
10. Clinical research of serum vitamin D in early Graves’ disease. / Y.-B. Li, X.-H. Xue, S.-W. Liu et al. // Chin. Rem. Clin. – 2014. – Vol. 14. – P. 242-243.
11. Association between vitamin D receptor gene polymorphisms (Fok1 and Bsm1) and osteoporosis: a systematic review / Z. Mohammadi, F. Fayyazbakhsh, M. Ebrahimi et al. // J Diabetes Metab Disord. – 2014. – Vol. 13. doi: 10.1186/s40200-014-0098-x; 98.
12. Evaluation, treatment and prevention of vitamin D deficiency: an Endocrine Society clinical practice guideline / M.F. Holick, N.C. Binkley, H.A. Bischoff-Ferrari et al. // J Clin Endocrinol Metab. – 2011. – Vol. 96. – P. 1911-1930.
13. Роль витамина D в патогенезе хронических неинфекционных заболеваний / Л.В. Егшатян, Е.Н. Дудинская, О.Н. Ткачева, Д.А. Каштанова // Остеопороз и остеопатии. – 2014. – № 3. – С. 27-30.
14. Yin K. Vitamin D and inflammatory diseases / K. Yin, D.K. Agrawal // Journal of Inflammation Research. – 2014. – Vol. 7. – P. 69-87.
15. Querfeld U. Vitamin D and inflammation / U. Querfeld // Pediatr Nephrol. – 2013. – Vol. 28. – P. 605-610.
16. Holick M.F. Vitamin D deficiency / M.F. Holick // N Engl J Med. – 2007. – Vol. 357. – P. 266-281.
17. Дефіцит та недостатність вітаміну D: епідеміологія, діагностика, профілактика та лікування / За редакцією проф. В.В. Поворознюка, проф. П. Плудовські. – Донецьк: Видавець Заславський О.Ю., 2014. – 262 с.
18. A systematic review of vitamin D status in populations worldwide. / J. Hilger, A. Friedel, R. Herr et al. // Br J Nutr. – 2014. – Vol. 111. – P. 23-45.
19. Rosen C.J. Clinical practice. Vitamin D insufficiency / C.J. Rosen // N Engl J Med. – 2011. – Vol. 364. – P. 248-254.
20. Vitamin D deficiency and risk of cardiovascular disease / T. Wang, M. Pencina, S. Booth et al. // Circulation. – 2008. – Vol. 117. – P. 503-511.
21. Vaidya A. Vitamin D and cardio-metabolic disease / A. Vaidya // Metabolism. – 2013. – Vol. 62. – P. 1697-1699.
22. Meta-analysis of the association between vitamin D and autoimmune thyroid disease. / J. Wang, S. Li, G. Chen et al. // Nutrients. – 2015. – Vol. 7. – P. 2485-2498.
23. Паньків В.І. Практична тиреоїдологія / В.І. Паньків. – Донецьк: Видавець Заславський О.Ю., 2011. – 224 с.
24. Serum vitamin D levels are decreased and associated with thyroid volume in female patients with newly onset Graves’ disease. / T. Yasuda, Y. Okamoto, N. Hamada et al. // Endocrine. – 2012. – Vol. 42 (3). – P. 739-741.
25. Zhang H. Low vitamin D status is associated with increased thyrotropin-receptor antibody titer in Graves’ disease. / H. Zhang, L. Liang, Z. Xie // Endocr Pract. – 2015. – Vol. 21. – P. 258-263.
26. Герасименко Л.В. Изменения костной ткани и их возрастные различия у женщин, больных диффузным токсическим зобом / Л.В. Герасименко // Міжнародний ендокринологічний журнал. – 2015. – № 72 (8). – С. 107-112.
27. Анварова Ш.С. К оценке состояния костной ткани у женщин, больных тиреотоксикозом, в условиях йодного дефицита / Ш.С. Анварова, Н.Ф. Ниязова // Доклады Академии наук Республики Таджикистан. – 2010. – Т. 53, № 11. – С. 889-892.
28. Методичні рекомендації з лікування та профілактики дефіциту вітаміну D у населення країн Центральної Європи: рекомендовані дози препаратів вітаміну D для здорової популяції та груп ризику / P. Pіudowski, E. Karczmarewicz, M. Bayer еt al. // Боль. Суставы. Позвоночник. – 2013. – № 3 (11). – С. 2-7.
29. Molecular mechanisms of vitamin D action / M.R. Haussler, G.K. Whitfield, I. Kaneko et al. // Calcif Tissue Int. – 2013. – Vol. 92 (2). – P. 77-98.
30. Non-classical mechanisms of transcriptional regulation by the vitamin D receptor: insights into calcium homeostasis, immune system regulation and cancer chemoprevention / V. Dimitrov, R. Salehi-Tabar, B.S. An, J.H. White // J Steroid Biochem Mol Biol. – 2014. – Vol. 144. – P. 74-80.
31. Pleiotropic activities of vitamin D receptors – adequate activation for multiple health outcomes / J.W. Ryan, P.H. Anderson, H.A. Morris // Clin Biochem Rev. – 2015. – Vol. 36 (2). – P. 53-61.
32. DIPART (Vitamin D Individual Patient Analysis of Randomized Trials) Group. Patient level pooled analysis of 68 500 patients from seven major vitamin D fracture trials in US and Europe // BMJ. – 2010. – Vol. 340. – P. 5463-5472.
33. Vitamin D with calcium reduces mortality: patient level pooled analysis of 70,528 patients from eight major vitamin D trials / L. Rejnmark, A. Avenell, T. Masud et al.] // J Clin Endocrinol Metab. – 2012. – Vol. 97 (8). – P. 2670-2681.
34. Vitamin D: modulator of the immune system. / F. Baeke, T. Takiishi, H. Korf [et al.] // Curr. Opin Pharmacol. – 2010. – Vol. 10 (4). – P. 482-496.
35. Relative vitamin D insufficiency in Hashimoto’s thyroiditis. / G. Tamer, S. Arik, I. Tamer, D. Coksert // Thyroid. – 2011. – Vol. 21 (8). – P. 891-896.
36. Vitamin D and autoimmune thyroid diseases. / S. Kivity, N. Agmon-Levin, M. Zisappl et al. // Cell Mol Immunol. – 2011. – Vol. 8 (3). – P. 243-247.
37. Prevalence of vitamin D deficiency and its relationship with thyroid autoimmunity in Asian Indian: a community – based survey. / R. Goswami, K. Raman, G. Nandita et al. // British Journal of Nutrition. – 2009. – Vol. 102. – P. 382-386.
38. Vitamin D deficiency is not associated with early stages of thyroid autoimmunity. / G. Effraimidis, K. Badenhoop, J.G. Tijssen, W.M. Wiersinga // Eur. J. Endocrinol. – 2012. – Vol. 167 (1). – P. 43-48.
39. Bizzaro G. Vitamin D and autoimmune thyroid diseases: facts and unresolved questions / G. Bizzaro, Y. Shoenfeld // Immunol Res. – 2015. – Vol. 61 (1-2). – P. 46-52.
40. Vitamin D and thyroid disease: to D or not to D? / G. Muscogiuri, G. Tirabassi, G. Bizzaro et al. // Eur J Clin Nutr. – 2015. – Vol .69 (3). – P. 291-296.
41. Vitamin D and autoimmune thyroid diseases / S. Kivity, N. Agmon-Levin, M. Zisappl et al. // Cell Mol Immunol. – 2011. – Vol. 8 (3). – P. 243-247.
42. Dіez J.J. An analysis of the relative risk for hypothyroidism in patients with Type 2 diabetes. / J.J. Dіez, P. Iglesias // Diabetic Medicine. – 2012. – Vol. 29 (12). – P. 1510-1514.
43. Duntas L.H. The interface between thyroid and diabetes mellitus. /L.H. Duntas, J. Orgiazzi, G. Brabant // Clinical Endocrinology. – 2011. – Vol. 75 (1). – P. 1-9.
44. Поворознюк В.В. Дефіцит вітаміну D у населення України та чинники ризику його розвитку / В.В. Поворознюк, Н.І. Балацька // Репродуктивная эндокринология. – 2013. – № 5 (13). – С. 7-13.
45. Vitamin D and Health // The Scientific Advisory Committee on Nutrition (SACN) 2016.
46. The nonskeletal effects of vitamin D: an Endocrine Society scientific statement / C.J. Rosen, J.S. Adams, D.D. Bikle et al. // Endocr Rev. – 2012. – Vol. 33. – P. 456-492.
47. Vitamin-D supplementation in prediabetes reduced progression to type 2 diabetes and was associated with decreased insulin resistance and systemic inflammation / D. Dutta, S.A. Mondal, S. Choudhuri et al. // Diabetes Res Clin Pract. – 2014. – Vol. 103. – P. 18-23.
48. Is vitamin D a player or not in the pathophysiology of autoimmune thyroid diseases? / F. D’Aurizio, D. Villalta, P. Metus et al. // Autoimmun Rev. – 2015. – Vol. 14 (5). – P. 363-369.
49. Meta-analysis of the association between vitamin D and autoimmune thyroid disease / J. Wang, S. Li, G. Chen et al. // Nutrients. – 2015. – Vol. 7. – P. 2485-2498.
50. Low levels of serum Vitamin D3 are associated with autoimmune thyroid disease in pre-menopausal women / Y.M. Choi, W.G. Kim, T.Y. Kim et al. // Thyroid. – 2014. – Vol. 24. – P. 655-661.
51. Mazokopakis E.E., Papadomanolaki M.G., Tsekouras K.C. et al. Is vitamin D related to pathogenesis and treatment of Hashomoto’s thyroiditis? // Hell J Nucl Med. – 2015. – Vol. 18 (3). – P. 222-227.
52. Поворознюк В.В. Вміст вітаміну D у хворих на аутоімунний тиреоїдит із зниженою функцією щитоподібної залози / В.В. Поворознюк, І.В. Паньків // Міжнародний ендокринологічний журнал. – 2014. – № 5 (61). – С. 27-30.
53. Паньків І.В. Взаємозв’язок дефіциту вітаміну D та аутоімунної патології щитоподібної залози / І.В. Паньків // Буковинський медичний вісник. – 2015. – Т. 19. – № 4 (76). – С. 132-136.
54. Паньків І.В. Вплив призначення вітаміну D на рівень антитіл до тиреоїдної пероксидази у хворих на гіпотиреоз аутоімунного генезу / І.В. Паньків // Міжнародний ендокринологічний журнал. – 2016. – № 5 (77). – С. 78-82.
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (40), грудень 2017 р.