16 березня, 2018
Доцільність застосування Декасану при санації черевної порожнини у хворих із розповсюдженим гнійним перитонітом
Інтенсивність і вид інтраабдомінального інфекційного забруднення при поширеному гнійному перитоніті суттєво впливають на ефективність лікування пацієнтів. Адекватність та своєчасність проведеного хірургічного втручання є вирішальними в перебігу захворювання. Метою дослідження було вивчення доцільності застосування декаметоксину як розчину для санації черевної порожнини (ЧП) у хворих із гнійним перитонітом. 
У дослідженні проведено аналіз результатів лікування 50 хворих із поширеним гнійним перитонітом, спричиненим різними видами гострої абдомінальної патології. У 58% випадків основним фактором розвитку перитоніту була перфорація порожнистого органа. Усім хворим проводили бактеріологічне дослідження ексудату з ЧП на наявність мікроорганізмів та їх чутливість до антибіотиків. З метою санації ЧП використовували розчини антисептиків – декаметоксину та октенідину дигідрохлориду. Під час бактеріологічного дослідження ексудату, отриманого інтраопераційно при первинному оперативному втручанні, у 24% випадків було виявлено ріст бактеріальної флори. Застосування декаметоксину та октенідину дигідрохлориду як антисептиків під час виконання санації ЧП продемонстрували ефективну елімінацію збудника й статистично зіставні показники післяопераційного ліжко-дня (р<0,05).
Інтраабдомінальна інфекція усе ще залишається однією з головних проблем загальної хірургії. [4] Аналіз літературних джерел і результати власних клінічних спостережень підтверджують актуальність твердження, що перитоніт та внутрішньочеревна інфекція не є синонімами. В ранні терміни виконання оперативного втручання при перфорації виразки шлунка, дванадцятипалої кишки ми спостерігаємо стерильне запалення очеревини, тобто розповсюджений перитоніт, викликаний хімічними чинниками. На відміну від цього, внутрішньочеревна інфекція (intraabdominal infection) означає запалення очеревини, спричинене мікроорганізмами. Оскільки в клінічній практиці переважна більшість випадків перитоніту є бактеріальним, ці два терміни використовують взаємозамінно [2]. Внутрішньочеревна інфекція охоплює всі форми бактеріального перитоніту, внутрішньочеревних абсцесів та інфекцій внутрішньочеревних органів [4].
Існує декілька класифікаційних систем для перитоніту та внутрішньочеревних інфекцій відповідно. Проте ані феноменологічні класифікації, ані класифікаційні системи щодо етіології бактеріального забруднення не є вирішальними для клінічного перебігу цього захворювання. Крім того, більшість досліджень, що стосуються перитоніту або внутрішньочеревних інфекцій, погано порівнюються через те, що критерії включення суттєво різняться. Отже, справжню поширеність бактеріального перитоніту складно оцінити. Що стосується його етіології, то перфорація порожнистого органа є основною причиною розвитку післяопераційного перитоніту, ішемічного ураження стінки кишечника, інфекції внутрішньочеревних органів і транслокації в небактеріальному перитоніті. До основних предикторів результатів лікування не відноситься анатомічне походження бактеріального забруднення й мікробіологічних знахідок [4].
Патогенез внутрішньоабдомінальних інфекцій визначається бактеріальними факторами, які впливають на перехід від забруднення до інфекції. Бактеріальні агенти призводять до майже рівномірної реакції запалення, яка викликається відповіддю на них мезотеліальних клітин і черевних мезотеліальних макрофагів, а також включає плазматичні системи, ендотеліальні клітини, поза- та внутрішньосудинні лейкоцити. Місцевими наслідками такої активації є трансміграція гранулоцитів з очеревинних капілярів на мезотеліальну поверхню й розширення перитонеальних кровоносних судин, що призводить до підвищення проникності та набряку очеревини, утворення насиченого білками перитонеального ексудату [4].
Уперше дані про хірургічне лікування перитоніту з’явилися в XIX столітті (Mikulicz, 1889; Krоnlein, 1885; Kоrte, 1892). М. Кіршнеру в 1926 році одному з перших вдалося знизити рівень смертності від перитоніту з 80-100 до 60% завдяки впровадженню хірургічного лікування. Однак на той час існували упередження, що осушення ЧП при перитоніті «фізично та фізіологічно неможливе» (Yates, 1905). З 1926 року смертність від перитоніту зменшилася в середньому на 30-40% завдяки впровадженню нових оперативних методик, застосуванню антибіотиків та проведенню інтенсивної терапії у цієї категорії хворих. Збудники, які зазвичай виявляються при бактеріальному перитоніті, є грамнегативними (наприклад, E. coli) та анаеробами (наприклад, Bacteroides fragilis) [1]. Однак визначити чіткий спектр мікрофлори, яка є чинником розвитку розповсюдженого перитоніту, доволі складно. Це зумовлено широкою варіацією патології, що є первинним джерелом розвитку запального деструктивного процесу в ЧП, а також часом виконання оперативного втручання від моменту початку захворювання та діагностичними можливостями бактеріологічної лабораторії, у якій вивчається отриманий інтраопераційно з ЧП ексудат.
При подальшому розвитку перитоніту може бути виявлений більш широкий спектр патогенних мікроорганізмів (наприклад, Рseudomonas aeruginosa, Enterobacter spp., Enterococcus spp.). Протимікробна резистентність бактеріальної флори, отриманої інтраопераційно, здатна визначати тяжкість післяопераційної інфекції та ускладнень [1].
Наразі погляди фахівців щодо впливу виду патогенів на результат лікування змінилися, порівняно з початком 80-х років минулого століття. Сьогодні відомо, що імунна відповідь, спричинена вторгненням патогенів, є вирішальним елементом для досягнення позитивного результату лікування інтраабдомінальної інфекції. У випадках, коли запальна реакція стає погано контрольованою, провокуючи розвиток поліорганної недостатності, операція вже не здатна обмежити імунну відповідь. Це свідчить про необхідність своєчасного виконання оперативного втручання та санації черевної порожнини у разі підозри на перитоніт [1].
Хірургія залишається наріжним каменем лікування перитоніту. Під час виконання будь-якого виду операції при розповсюдженому перитоніті має бути обов’язково дотримано два основних принципи лікування внутрішньочеревних інфекцій:
- ранній та остаточний контроль джерела інфекції;
- елімінація бактеріального забруднення й токсинів із ЧП [3].
Прогностичними чинниками ефективного лікування розповсюдженого перитоніту є передопераційний стан хворого, своєчасність та адекватність хірургічної санації джерела інфекції і відповідь на лікування [4].
В умовах поширеного гнійного перитоніту техніка «відкритого» ведення рани з повторними програмованими санаціями ЧП є надзвичайно ефективною [3]. Інтраопераційний лаваж ЧП – традиційний етап оперативного втручання у хворих на розповсюджений перитоніт у сучасній хірургічній практиці, однак він поки що не продемонстрував суттєвого зниження показників клінічної летальності [1]. Показаннями до здійснення планового повторного лаважу ЧП є неможливість досягти адекватного контролю над джерелом інфекції при первинному оперативному втручанні, дифузний каловий перитоніт, нестабільність гемодинамічних показників та внутрішньочеревна гіпертензія. Велика кілька повторних програмованих санацій ЧП може бути пов’язана із суттєвим зростанням ризику післяопераційних ускладнень, у тому числі за рахунок гіперактивації імунної запальної реакції, розвитку порушень електролітного обміну, гіпотонії. Саме тому важливо визначити оптимальну частоту та кількість санаційних релапаротомій, ураховуючи ризик продовження некротичного та інфекційного процесу в ЧП [3].
Результати представлених у літературі досліджень щодо ефективності, специфічних показань та особливостей виконання програмованих санацій ЧП у хворих із розповсюдженим перитонітом є недостатньо конкретними або ж містять статистично незіставну вибірку цих пацієнтів [3].
Немає абсолютної достовірності того, що додавання антибіотиків до інтраопераційного лаважу збільшує виживання хворих (клас доказів В і С) [1]. Саме тому вибір розчину для санації, а також його ефективність у процесі елімінації бактеріального збудника з ЧП відіграють важливу роль у досягненні позитивних результатів лікування та зменшенні відсотка необхідності виконання інтраабдомінального лаважу.
Метою дослідження було вивчення доцільності застосування декаметоксину як розчину для санації ЧП у хворих на розповсюджений гнійний перитоніт.
Матеріали і методи
У клініці кафедри загальної хірургії № 2 Національного медичного університету ім. О.О. Богомольця на базі хірургічного відділення Міської клінічної лікарні м. Києва у період із січня 2015 по лютий 2018 року перебувало на лікуванні 50 хворих із розповсюдженим гнійним перитонітом. Середній вік пацієнтів становив 64±12,5 року (чоловіків – 34, жінок – 16). Усім хворим проводили оперативне втручання в ургентному порядку. Об’єм оперативного втручання залежав від типу виявленої нозології, що спричинила розвиток розповсюдженого гнійного перитоніту. Хворим були виконані такі основні етапи: лапаротомія, ревізія ЧП, інтраопераційний лаваж і дренування ЧП. Усім пацієнтам проводили бактеріологічне дослідження ексудату з ЧП на наявність мікроорганізмів та їх чутливість до антибіотиків. З метою санації ЧП використовували розчини антисептиків – декаметоксину (препарат Декасан, ТОВ «Юрія-Фарм», Україна) та октенідину дигідрохлорид (препарат Октенісепт, «Шюльке і Майр ГмбХ», Німеччина). Також хворим проводили парентеральну антибактеріальну терапію. Вибір антибактеріального препарату залежав від «поверху» локалізації джерела інфекції в ЧП, виду первинної патології, а також чутливості виявленої бактеріальної мікрофлори. Перевагу віддавали препаратам групи карбапенемів.
Статистичну обробку результатів досліджень здійснювали за допомогою пакета програм «Statisticа 10.0» та «Microsoft Office Exсel 2010».
Результати та їхнє обговорення
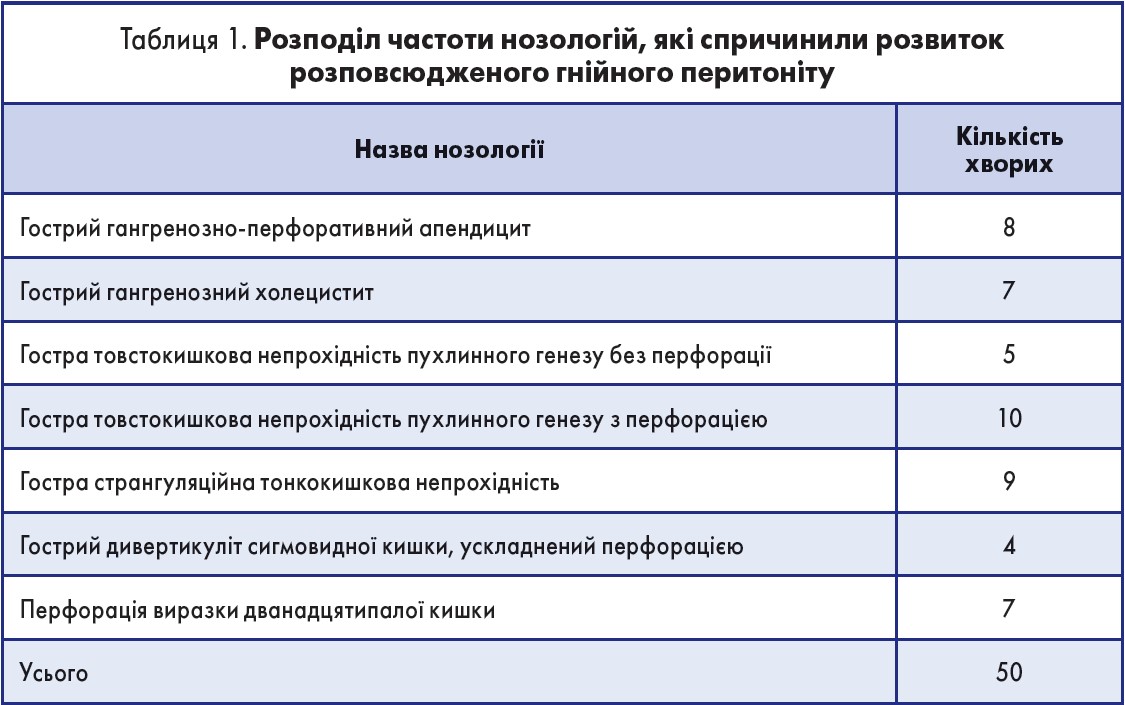
Під час аналізу результатів дослідження було встановлено, що в усіх хворих перитоніт був спричинений деструктивним процесом органів ЧП. У таблиці 1 представлено спектр нозологій, які виявилися джерелом розвитку розповсюдженого гнійного перитоніту.
З таблиці 1 видно, що у 58% випадків основним фактором розвитку перитоніту була перфорація порожнистого органа. При цьому в 54% випадків спостерігався патологічний деструктивний процес різних відділів товстої кишки. З огляду на дані літератури, саме транслокація мікрофлори товстої кишки стає провідним фактором у розвитку розповсюдженого гнійного перитоніту [2].
Пацієнти були розподілені на дві групи, зіставні за типом нозології та її структурою (р<0,05). У дослідній групі (n=24) санацію порожнини виконували розчином декаметоксину об’ємом 1000 мл з експозицією 10 хв. У контрольній групі (n=26) лаваж ЧП здійснювали розчином октенідину дигідрохлориду, розведеним у теплому ізотонічному 0,9% розчині натрію хлориду у співвідношенні 1:4 загальним об’ємом 1000 мл.
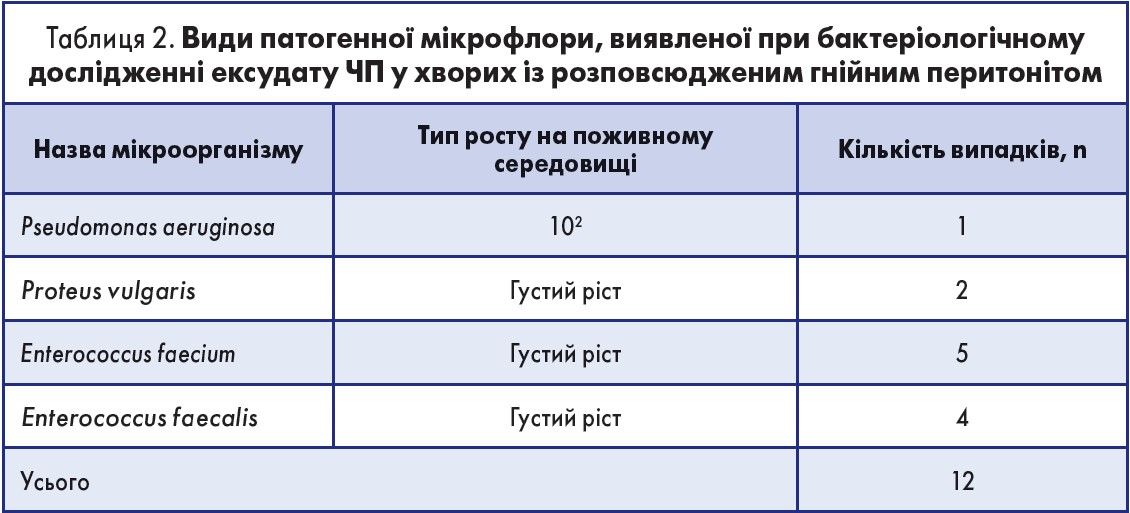
Варіабельність патології, що спричинила розвиток розповсюдженого перитоніту, а також різні терміни діагностики патології й проведення оперативного втручання не дають змоги провести кореляцію між інтраопераційною картиною та особливостями перебігу захворювання (р<0,05). З огляду на вищезазначене, було вирішено проаналізувати тип і ступінь бактеріального забруднення ексудату з ЧП. Під час бактеріологічного дослідження ексудату, отриманого інтраопераційно при первинному оперативному втручанні, у 38 (76%) випадках не було виявлено росту бактеріальної флори. У 12 (24%) випадках встановлено ріст колоній патогенних мікроорганізмів, перелік яких представлений у таблиці 2.
Під час аналізу даних, наведених у таблиці 2, встановлено, що в більшості випадків (92%) бактеріальне забруднення ЧП представлено мікрофлорою товстого кишечника. Виявлені мікроорганізми входили до спектра антимікробної активності декаметоксину та октенідину дигідрохлориду.
У 8 (16%) випадках виникла необхідність у проведенні програмованих санацій ЧП. При цьому спостерігалося зіставне співвідношення в групах – 4 (16,6%) випадки в дослідній і 4 (15,3%) випадки в контрольній (р<0,05). Усі ці хворі ввійшли до групи, у яких при первинному оперативному втручанні в ексудаті виявлено ріст патогенної мікрофлори, представленої в таблиці 2. У контрольній та дослідній групах повторну санацію ЧП виконували за допомогою розчину антисептика відповідно до обраної групи. У 3 (6%) випадках клінічний перебіг захворювання потребував проведення повторного інтраопераційного лаважу розчинами антисептиків через 48 год. В усіх 8 випадках контрольної та дослідної груп під час повторних санацій ЧП у наявному ексудаті ріст бактеріальної флори не виявлено. Це може свідчити про адекватність ліквідації джерела інфекції при первинному оперативному втручанні та превалювання реактивних запальних змін очеревини в патогенезі розвитку продовженого перитоніту.
При порівнянні тривалості перебування в стаціонарі у післяопераційному періоді статистично значущої різниці в контрольній та дослідній групах не виявлено (р<0,05). Утім, варіабельність видів патології, що спричинила розвиток розповсюдженого гнійного перитоніту, віку, наявності супутніх соматичних захворювань та обмежена кількість спостережень не дають змогу провести статистично достовірну кореляцію показників відповідно до післяопераційного ліжко-дня.
! Отже, аналізуючи вищенаведені результати дослідження, необхідно звернути увагу на те, що вивчати особливості лікування розповсюдженого гнійного перитоніту надзвичайно складно. Це зумовлено широким спектром патологій, які спричиняють бактеріальне забруднення ЧП. При цьому лабораторне підтвердження бактеріального компонента й чутливість мікрофлори до антибактеріальних препаратів мають бути пріоритетними у визначенні обсягу подальшої консервативної терапії. Застосування антисептиків при виконанні інтраабдомінального лаважу дозволяє ліквідувати мікробну контамінацію перитонеального ексудату. Однак варіабельність призначеної антибактеріальної терапії обмежує достовірність результатів дослідження й першочергове значення в елімінації бактеріальних патогенів.
Застосування декаметоксину та октенідину дигідрохлориду як антисептиків під час виконання санації ЧП продемонструвало ефективну елімінацію збудника й статистично зіставні показники післяопераційного ліжко-дня. Тому доцільним є вивчення економічної ефективності використання різних видів антисептиків, у тому числі декаметоксину, при наданні медичної допомоги хворим із розлитим гнійним перитонітом.
Висновок
Застосування декаметоксину – антисептика з числа четвертинних амонієвих сполук – під час виконання санації черевної порожнини дає змогу ефективно ліквідувати бактеріальне забруднення інтраабдомінального ексудату при лікуванні хворих на розповсюджений гнійний перитоніт.
Література
1. Holzheimer R.G., Mannick J.A. Surgical Treatment: Evidence-Based and Problem-Oriented. Munich: Zuckschwerdt; 2001; https://www.ncbi.nlm.nih.gov/books/NBK6950/.
2. Schein M. Peritonitis: Contamination and Infection – Principles of Treatment. In: Schein’s Common Sense Emergency Abdominal Surgery. Springer, Berlin, Heidelberg. 2000.
3. Ruben Peralta. Surgical Approach to Peritonitis and Abdominal Sepsis. https://emedicine.medscape.com/article/1952823-overview (Publication date: Jul 21, 2017).
4. Farthmann E.H., Schоffel U. Epidemiology and pathophysiology of intraabdominal infections (IAI). Infection (1998) 26: 329. September 1998, Volume 26, Issue 5, p. 329-334; https://doi.org/10.1007/BF02962266.