2 жовтня, 2018
Преимущества и недостатки различных спазмолитиков в лечении синдрома раздраженной кишки
 Синдром раздраженной кишки (СРК) – гастроэнтерологическое заболевание, распространенность которого во взрослой популяции в разных странах варьирует в пределах 10-15%. Это наиболее частое проявление функциональной гастроинтестинальной патологии. СРК не представляет угрозы для жизни пациента, однако, будучи хроническим состоянием, значительно ухудшает ее качество.
Синдром раздраженной кишки (СРК) – гастроэнтерологическое заболевание, распространенность которого во взрослой популяции в разных странах варьирует в пределах 10-15%. Это наиболее частое проявление функциональной гастроинтестинальной патологии. СРК не представляет угрозы для жизни пациента, однако, будучи хроническим состоянием, значительно ухудшает ее качество.
Точные причины СРК до конца не известны, в связи с чем этиотропное лечение отсутствует. На сегодня установлено, что в патогенезе СРК играют роль генетические факторы, расстройства моторики, нарушение висцеральной чувствительности, дисрегуляция ЦНС, психологические расстройства и психосоциальные факторы, нарушение барьерной функции кишечника и изменения кишечной микробиоты, постинфекционное воспаление и иммунная дисфункция, пищевая аллергия и пищевая непереносимость.
В подавляющем большинстве случаев у лиц до 50 лет при отсутствии тревожных симптомов первичный диагноз СРК с вероятностью 93-97% устанавливается на основании характерных проявлений. Согласно Римским критериям IV, СРК рассматривается как функциональное кишечное расстройство, при котором рецидивирующая абдоминальная боль ассоциируется с дефекацией или изменениями стула.
Кроме таких нарушений стула, как диарея, запор или их сочетание, при СРК часто присутствуют вздутие и чувство растяжения живота, которые, тем не менее, не являются специфичными. Подразделение СРК на подтипы основывается на консистенции стула (согласно Бристольской шкале). При этом выделяют СРК с диареей (около 39% случаев), СРК с запорами (31% случаев), СРК смешанного (6% случаев) и неопределенного типа (24% случаев).
Лечение СРК, как и любого другого функционального заболевания, представляет собой сложную задачу. Стойкий клинический эффект даже при удачно подобранной терапии отмечается не более чем у 25% больных. Учитывая достаточно хорошую изученность основных патогенетических факторов и клинических особенностей СРК, его лечение в настоящее время проводится с учетом преобладающего клинического синдрома/симптома и ведущего патофизиологического механизма, то есть носит симптоматический характер.
При СРК с диареей медикаментозное лечение в основном сводится к применению противодиарейных препаратов, при СРК с запорами преимущественно используют пищевые волокна, набухающие и осмотические слабительные, 5-HT4-агонисты и пробиотики. У пациентов с преобладанием болевого синдрома применяют спазмолитики и антидепрессанты. Для многих используемых в лечении СРК препаратов нет убедительных доказательств их превосходства над плацебо.
Наиболее часто для симптоматического лечения СРК применяются спазмолитики. Длительное время считалось, что нарушение двигательной активности кишки и кишечной перистальтики является центральным в развитии СРК и главной его причиной. В последние годы эта точка зрения пересматривается: предполагается, что указанные нарушения скорее носят вторичный характер. Тем не менее дисмоторные нарушения со стороны как толстой, так и тонкой кишки при СРК обнаруживаются очень часто.
Таким образом, они участвуют в формировании основных клинических проявлений СРК, что обосновывает широкое применение спазмолитков в лечении данной патологи.
Хотя этот класс является фармакологически разнообразным, считается, что механизм действия, благодаря которому спазмолитические средства, как полагают, облегчают симптомы СРК (в частности, боли в животе и спазмы), реализуется через уменьшение сокращений гладкой мускулатуры. Кроме того, спазмолитики также могут воздействовать на повышенную висцеральную чувствительность.
Спазмолитики можно разделить на 3 группы: антихолинергические препараты, прямые релаксанты гладкомышечной ткани (миотропные спазмолитики) и мятное масло. Представители этих групп обладают как преимуществами, так и определенными недостатками, ограничивающими их клиническое применение.
Среди всех спазмолитиков особняком стоит масло мяты перечной, спазмолитический эффект которого реализуется вследствие блокады калий-ассоциированной деполяризации и кальциевых каналов. Кроме того, масло мяты перечной оказывает антиноцицептивный (прямое антагонистическое действие на κ-опиоидные рецепторы кишки), антиэметический (опосредованное действие через гистаминовые, ацетилхолиновые и серотониновые рецепторы), антибактериальный и противовоспалительный эффекты. Масло мяты перечной также улучшает ритмичность перистальтики гладкомышечных волокон кишечника и замедляет кишечный транзит, в связи с чем более эффективно при СРК с диареей.
В настоящее время на рынке Украины появился Капсумен – натуральное средство в форме капсул для приема внутрь, которое использует хорошо изученное воздействие мяты перечной на работу кишечника. Капсумен рекомендуется в качестве добавки к рациону питания как дополнительный источник L-ментола, который содержится в масле мяты перечной, с целью устранения дискомфорта в кишечнике (вздутия, спазма и т. п.) и нормализации функции кишечника (секреторной, моторной и опорожнения) в условиях эмоциональной перегрузки, при несбалансированном режиме питания, изменениях режима питания или применении отдельных категорий лекарственных средств.
Нами проведено открытое сравнительное исследование эффективности Капсумена у больных СРК (n=56) в возрасте от 23 до 60 лет (средний возраст – 38±16 лет) без запора. У всех участников органическая кишечная патология исключена при проведении колоноскопии; диагноз СРК установлен в соответствии с Римскими критериями IV; отсутствовали клинические признаки лактазной недостаточности. Целиакия исключалась на основании негативных результатов на антиглиадиновые и антитрансглутаминазные антитела.
Все больные СРК были рандомизированы на 2 группы – основную (n=26) и контрольную (n=30). В контрольной группе больные СРК получали базисную терапию (индивидуальная диета с ограничением ферментируемых олиго- и моносахаридов, лоперамид по требованию, спазмолитик (мебеверин) в течение 1 мес). Пациенты основной группы на фоне базисной терапии вместо мебеверина получали Капсумен (1 капсула 3 р/день после еды в течение 1 мес).
Эффективность лечения оценивали через 1 мес по количеству респондеров – пациентов, которые сообщили о ≥30% уменьшении среднего количества случаев наиболее сильной боли в животе и о ≥50% уменьшении количества дней в неделю, в которые как минимум один стул имел консистенцию типа 6 или 7 в соответствии с Бристольской шкалой формы стула в сравнении с исходным уровнем.
Важные положительные результаты включали также адекватное общее улучшение, улучшение консистенции стула, нормализацию императивных позывов или вздутия живота. Отрицательными результатами считались сохранение диареи, требующее прекращения или изменения лечения, и побочные эффекты, приводящие к отмене лечения.
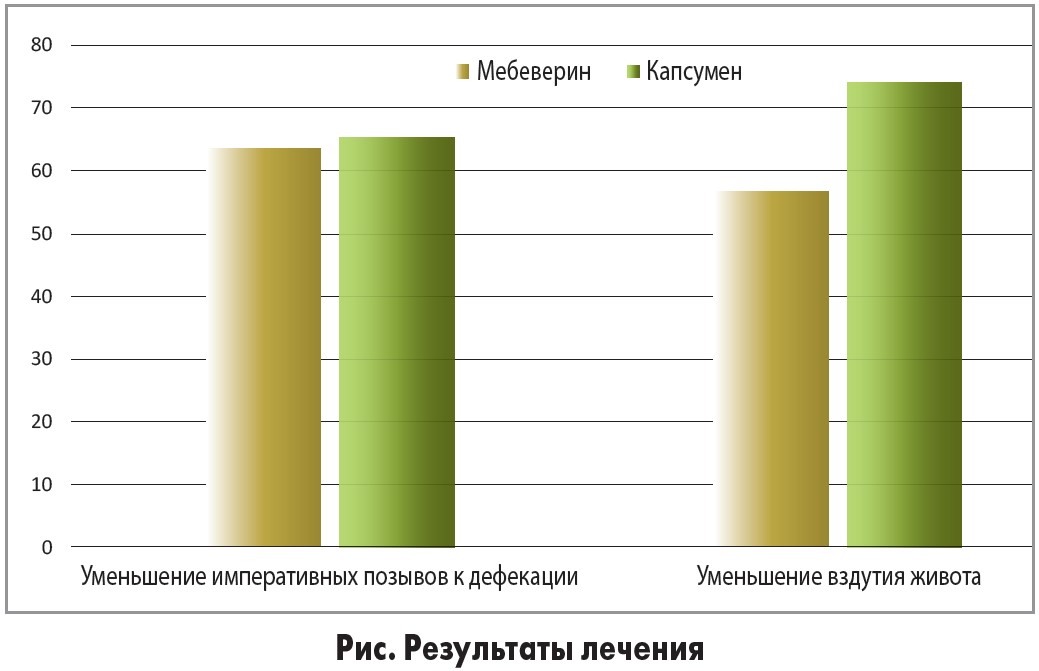
В основной группе число респондеров (16 из 26 пациентов, 61,5%) достоверно не отличалось от такового в контрольной (18 из 30, 60%; р>0,05). Улучшение консистенции стула и уменьшение или нормализация императивных позывов к дефекации в основной группе отмечались у 17 (65,4%) больных, что также достоверно не отличалось от аналогичных показателей в контрольной группе (63,3%).
В то же время количество больных СРК в основной группе, отметивших существенное уменьшение вздутия живота (n=9, 73,1%), достоверно превышало аналогичный показатель в контрольной группек (n=17, 56,6%; р<0,01). Каких-либо существенных неблагоприятных побочных эффектов при приеме Капсумена выявлено не было. Таким образом, наше исследование свидетельствует об эффективности и безопасности базисной терапии с включением Капсумена у больных СРК (рис.).
В литературе многократно обсуждались особенности, преимущества и недостатки применения различных спазмолитиков при СРК. Какой группе препаратов отдать предпочтение, решает клиницист с учетом конкретной клинической ситуации. Однако несомненно то, что при сравнимой клинической эффективности препараты с селективным действием на гладкие мышцы пищеварительной системы (мебеверин, отилония бромид, пинаверия бромид) предпочтительнее, поскольку лишены побочных эффектов холинолитиков (ощущение сухости во рту, нарушение зрения, задержка мочеиспускания, рефлекторная гипотония кишечника) и системного вазодилатирующего действия, свойственного дротаверину и папаверину.
Кроме того, при СРК пероральный прием неселективных препаратов в терапевтических дозах чаще всего малоэффективен, что диктует необходимость увеличения дозы или парентерального введения. В свою очередь, это может вызывать головокружение, понижение возбудимости миокарда, нарушение желудочковой проводимости вплоть до развития атриовентрикулярной блокады. В связи с этим антихолинергические препараты и неселективные спазмолитики в лечении СРК применяются все реже, тогда как селективные спазмолитики по-прежнему широко используются.
Справедливости ради следует сказать, что и селективные спазмолитики эффективны далеко не у всех пациентов с СРК. Отдельно отметим, что в отличие от других стран в США спазмолитики не популярны, из них там применяются только гиосцин, дицикломин и масло мяты перечной.
В техническом обзоре Американской гастроэнтерологической ассоциации проанализированы 12 различных спазмолитических средств, исследованных в 22 рандомизированных клинических испытаниях (РКИ; 1983 пациента с СРК; спазмолитики принимали 1008, плацебо – 1975). Показаны значительные различия между испытаниями, в целом качество исследований было низким. Тем не менее спазмолитики продемонстрировали улучшение в сравнении с плацебо относительно общего облегчения и боли в животе, хотя последнее не удовлетворяло современным критериям клинической значимости.
Проведенный Кокрановский обзор выявил благоприятное влияние спазмолитических средств в сравнении с плацебо на облегчение боли в животе и улучшение общего состояния. Общая эффективность спазмолитиков составила 61%, плацебо – 44%, относительный риск сохранения симптомов равнялся 0,68 (ДИ 057-0,81).
К сожалению, согласно последним данным, мебеверин, тримебутин, пирензепин, альверин, прифиний не показали статистически значимых эффектов в отношении симптоматики СРК, кроме того, количество участников в соответствующих исследованиях было небольшим.
Достоверную эффективность, по данным последних РКИ, продемонстрировали только гиосцин, циметоприм, пинаверия бромид, дицикломина гидрохлорид (уровень доказательств 2С), отилония бромид (1В) и масло мяты перечной. Неясно, являются ли спазмолитические средства более эффективными при отдельных подтипах СРК, однако их регулярное применение при запоре может быть ограничено вследствие антихолинергических эффектов.
Поскольку кардинальным симптомом СРК является абдоминальная боль, связанная с кишечной дисмоторикой, на сегодня спазмолитики остаются одними из наиболее востребованных и применяемых препаратов для лечения СРК. Среди наиболее безопасных и эффективных спазмолитиков как для краткосрочного, так и для длительного лечения СРК следует рассматривать масло мяты перечной, позволяющее эффективно уменьшать или полностью устранять основные симптомы СРК.
Несомненными преимуществами масла мяты перечной являются эффективность, сравнимые с плацебо безопасность и переносимость, отсутствие системных побочных эффектов. Благодаря этому диетическая добавка Капсумен практически не имеет противопоказаний и в отличие от других спазмолитиков может применяться в период беременности и лактации, а также у пациентов с сопутствующими кардиоваскулярными заболеваниями, болезнями печени и почек.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 17 (438), вересень 2018 р.