21 листопада, 2018
Особенности предменструального синдрома у женщин с эндометриозом: варианты терапевтических подходов
 Актуальной проблемой в гинекологии является предменструальный синдром (ПМС), характеризующийся физическими и психоэмоциональными проявлениями, которые нарушают соматическое и психическое состояние женщин, приводят к снижению их работоспособности, усложняют коммуникацию в профессиональных и личных отношениях, а со временем создают условия для нервно-психической дезадаптации. ПМС относится к широко распространенным (отмечается у 20-80% женщин репродуктивного возраста, у 5-10% пациенток – в тяжелой форме), но наименее изученным состояниям [7].
Актуальной проблемой в гинекологии является предменструальный синдром (ПМС), характеризующийся физическими и психоэмоциональными проявлениями, которые нарушают соматическое и психическое состояние женщин, приводят к снижению их работоспособности, усложняют коммуникацию в профессиональных и личных отношениях, а со временем создают условия для нервно-психической дезадаптации. ПМС относится к широко распространенным (отмечается у 20-80% женщин репродуктивного возраста, у 5-10% пациенток – в тяжелой форме), но наименее изученным состояниям [7].
Согласно последним данным, ПМС можно рассматривать как функциональное расстройство центральной нервной системы (ЦНС) вследствие действия неблагоприятных внешних факторов на фоне врожденной или приобретенной лабильности гипоталамо-гипофизарно-овариальной системы [1].
ПМС представляет собой многогранный симптомокомплекс, включающий более 150 симптомов и проявляющийся нервно-психическими, вегетососудистыми и обменно-эндокринными нарушениями в лютеиновую фазу ментруального цикла.
В возникновении ПМС определенную роль играют личностные факторы, факторы внешней среды и преморбидный фон. По мнению некоторых исследователей, в возрасте до 29 лет ПМС наблюдается у 20% женщин, 30-39 лет – у 47% и в 40-50 лет у 55% женщин [2].
По данным некоторых авторов, ПМС фиксируют у 28,8% практически здоровых женщин [2]. По данным С.М. Шардина, ПМС встречается у 92% женщин с хроническими заболеваниями желудочно-кишечного тракта и 72,4% – с сахарным диабетом. Часто наблюдается ПМС у женщин с психическими заболеваниями: при маниакально-депрессивном психозе – у 86,4% пациенток, при психопатиях – у 68,3%, при неврозах – у 81,4%, при алкоголизме – у 72,2%; он встречается у 41,5% больных с пороками сердца. ПМС имеет место у 95% пациенток с генитальным эндометриозом, и его лечение наряду с купированием симптомов эндометриоза приобретает особое значение [2, 3, 6, 7].
Клинические проявления эндометриоза, как правило, характеризуются различной степенью выраженности болевых ощущений, зачастую трансформирующихся в хроническую тазовую боль. При этом хроническая патологическая болевая импульсация обеспечивает высокий уровень невротизации больных, влечет за собой особенности поведения и изменения личности, формирует условия для развития депрессивных состояний и астенизации [5, 7, 8]. Таким образом, само наличие эндометриоза уже формирует предпосылки для развития различных клинических проявлений ПМС.
Согласно гормональной теории, ПМС – следствие относительной или абсолютной гиперэстрогении в лютеиновой фазе цикла, что является абсолютно характерным для женщин с эндометриозом. Повышение уровня эстрогенов в сыворотке крови вызывает задержку натрия, это приводит к накоплению межклеточной жидкости и отекам.
Кроме того, дополнительный синергичный эффект достигается вследствие влияния эстрогенов на секрецию альдостерона путем изменения дофаминэргической передачи или обмена дофамина. Прогестерону присуще натрий-диуретическое действие, способствующее повышению диуреза.
При гиполютеинизме, характерном для ПМС, жидкость задерживается в тканях, что клинически проявляется периферическими отеками, масталгией, вздутием живота, увеличением массы тела, артралгиями. Раздражительность, головную боль и некоторые другие неврологические и психические проявления ПМС можно объяснить как отечностью головного мозга, так и особенностями метаболизма прогестерона в ЦНС [3, 7].
При нормальном метаболизме прогестерона в ЦНС образуется аллопрегненолон, обладающий способностью стимулировать А-рецепторы гамма-аминомасляной кислоты (ГАМК) и повышать активность хлоридных ионных канальцев нейронных мембран, обеспечивая анксиолитический (седативный) эффект.
В случае нарушения метаболизма прогестерона образуются прегненолон и прегненолона сульфат, являющиеся антагонистами как А-, так и В-ГАМК рецепторов. Наличие В-ГАМК рецепторов не только в ЦНС, но и в других системах и органах, может в некоторой степени объяснить полиморфизм клинических проявлений ПМС.
Во время лютеиновой фазы эндометрий выделяет простагландины, а нарушение их секреции приводит к дисменорее и ПМС [3]. Изменение гемодинамики малого таза в виде гипертензии и спазма сосудов или длительной вазодилатации и венозного застоя, вызванного недостатком магния и повышением концентрации простагландина F2a, обусловливает гипоксию клеток, накопление аллогенных веществ, раздражение нервных окончаний и возникновение боли внизу живота перед менструацией и в ее первые дни [3].
Отмечено, что у здоровых женщин перед менструацией количество магния в эритроцитах увеличивается [3, 9]. Имеются данные, что у женщин с ПМС концентрация ионизированного магния во 2-ю фазу цикла снижена, а коэффициент Са2+/Mg2+ повышен [3]. Дефицит магния и витамина В6 часто сочетаются – дефицит пиридоксина сопровождается клиническими симптомами, которые часто наблюдаются при недостаточности магния [4].
Некоторые авторы указывают на связь возникновения симптомов ПМС с недостатком витамина В6 в лютеиновую фазу (теория циклического авитаминоза) [3]. При дефиците магния и витамина В6 развиваются недостаток прогестерона и относительная гиперэстрогения [3]
. Выявлено, что, в свою очередь, избыток эстрогенов может привести к недостатку витамина В6, который является коферментом в заключительной стадии образования дофамина и серотонина [3, 6].
Причиной недостаточности дофамина в мозге может быть и дефицит магния. Поэтому прием магния и витамина В6 дает возможность изменить ситуацию, приводит к увеличению уровня дофамина и серотонина, что уменьшает выраженность симптомов ПМС. Магний и витамин В6 способствуют увеличению выработки простагландина E1 и снижению таковой простагландина Е2 из ненасыщенных жирных кислот, поступающих с пищей, тем самым положительно влияя на симптомы депрессии и мигрени при ПМС [3].
Магний приводит к снижению выработки простагландина F2а клетками эндометрия, его релаксации и уменьшению выраженности циклического болевого синдрома [3, 6, 9]. Магний вызывает гипертрофию гломерулярной зоны коры надпочечников, секретирующей альдостерон, что ведет к задержке жидкости.
В клинической практике дефицит магния чаще всего становится очевидным не только при ПМС, но и при миоме матки, эндометриозе, патологическом климаксе и дисменорее (состояниях, имеющих особую выраженность у женщин с эндометриозом).
Учитывая высокую частоту развития ПМС на фоне эндометриоза, его полиэтиологичность, противоречивость теорий патогенеза, вариабельность клинической картины, целью данного исследования стала оптимизация способов терапии ПМС с учетом его особенностей при генитальном эндометриозе [6].
Материалы и методы
В исследование включены 64 женщины репродуктивного возраста от 19 до 40 лет (средний возраст составил 32,2±5,4 года) с ПМС легкой и средней степени выраженности, которые были распределены на две клинические группы. Группы исследования были сравнимы по возрасту, формам ПМС и степени выраженности генитального эндометриоза.
Все пациентки перед обследованием и лечением подписали информированное согласие на участие в исследовании.
Первую группу исследования составили 30 пациенток, получающие дидрогестерон в дозе 10 мг 2 раза в день в сочетании с Гамалате В6 по 2 таблетки 3 раза в день. Во 2-ю группу вошли 34 пациентки, получающие дидрогестерон согласно рекомендациям нормативних документов – по 10 мг 2 раза в день.
Препарат Гамалате В6 был выбран с учетом его состава. Он содержит комбинацию активних веществ: ГАМК, g-амино-b-оксимасляную кислоту, витамин В6, которые являются естественными компонентами тканей головного мозга, а также магния глутамата гидробромид. Препарат оказывает нейрорегулирующее воздействие на процессы в головном мозге, легкий седативный и церебротонический эффект.
Прием Гамалате В6 обеспечивает экзогенное поступление ГАМК в нервную систему. Высокий уровень ГАМК выполняет нейротрансмиттерную функцию и подавляет процессы возбуждения, участвует в транспортировке и использовании глюкозы в мозге, в клеточном дыхании и оксидативном фосфорилировании, регуляции синтеза протеинов в головном мозге.
Предложен следующий режим лечения Гамалате В6: по 2 таблетки 3 раза в день в течение 3 месяцев. Схема терапии дидрогестероном: по 10 мг 2 раза в день с 16-го по 25-й день менструального цикла в течение 3 циклов. Выбранная терапия продолжалась 3 месяца.
С целью мониторинга эффективности назначенной терапии нами проводилась субъективная и объективная оценка динамики клинических симптомов по специально разработанной анкете через 3 и 6 месяцев лечения. Независимая оценка болевого синдрома осуществлялась по методу многомерной семантической дескрипции с применением Мак-Гилловского опросника (McGill Pain Questionnaire; В.В. Кузьменко и соавт., 1986).
Полученные цифровые данные обрабатывали с использованием современных методов медицинской статистики с помощью программы Microsoft Office Excel и применением критерия Стьюдента. Разницу между сравниваемыми величинами считали достоверной при p <0,05.
Результаты и их обсуждение
Клиническая картина ПМС у участниц исследования характеризовалась следующими симптомами: дисменорея имела место у 46 (69,14%) пациентoк, раздражительность – у 49 (74,26%), депрессия – у 28 (44,18%), слабость – у 22 (35,72%), нарушение пищевого поведения – у 23 (36,17%), мастодиния – у 41 (64,86%) пациентки, отечность век, лица, пальцев рук – у 22 (35,72%), увеличение массы тела во 2-й фазе цикла – у 19 (30,08%), головная боль – у 21 (32,9%), акне – у 11 (17,86%), повышение температуры тела – у 5 (4,7%) пациенток исследуемых групп. Вышеперечисленные симптомы относятся преимущественно к нервно-психической и отечной формам ПМС.
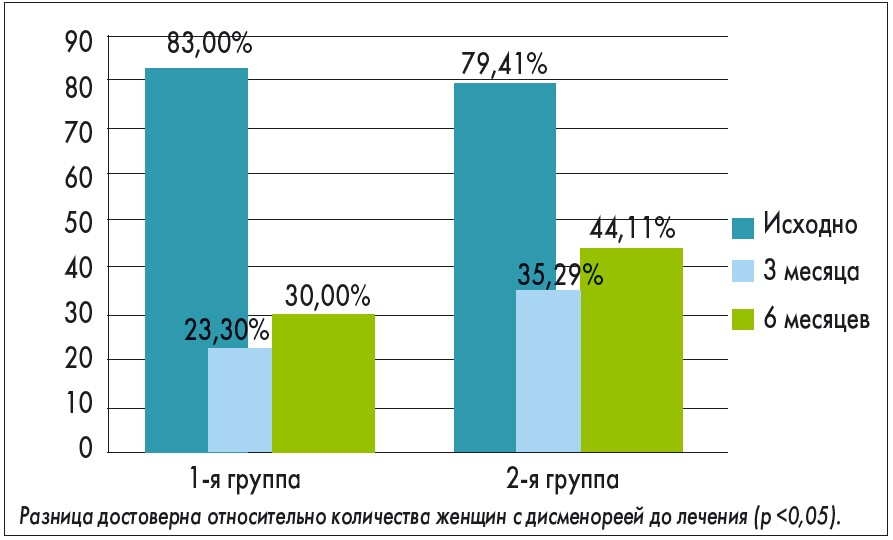
Через 3 месяца терапии в обеих исследуемых группах отмечено существенное уменьшение количества женщин с дисменореей по сравнению с показателем до лечения (рис. 1).
Рис. 1. Динамика проявления дисменореи у женщин с ПМС и эндометриозом на фоне проводимой терапии
При этом разница между количеством женщин с дисменореей в 1 и 2-й группах была статистически достоверна (23,30 и 35,29% соответственно; p<0,05). Через 6 месяцев от начала терапии количество женщин с дисменореей в обеих группах существенно не изменилось по сравнению с таковым через 3 месяца лечения (30,0% в 1-й группе и 44,11% во 2-й группе; p <0,05).
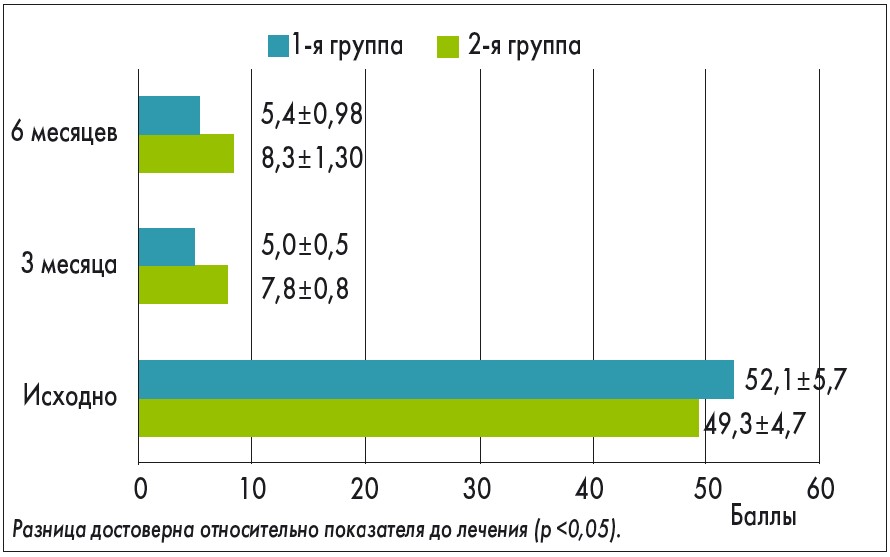
При оценке выраженности дисменореи согласно Мак-Гилловскому опроснику нами обнаружено снижение среднего рангового индекса боли у женщин 1 и 2-й групп через 3 месяца терапии (c 52,1±5,7 до 5,0±0,5 и c 49,3±4,7 до 7,8±0,8 балла соответственно; p <0,05). Через 6 месяцев после начала лечения результаты сохранились, при этом более стойкий эффект отмечался в 1-й группе (5,4±0,98 против 8,3±1,30 балла соответственно; p >0,05; рис. 2).
Рис. 2. Средний индекс боли у участниц исследования согласно Мак-Гилловскому опроснику
Болевые ощущения при ПМС у участниц исследования, которые оценивали по среднему значению количества выбранных дескрипторов, стали также существенно слабее через 3 месяца лечения (cнижение с 15,7±1,1 до 2,7±0,4 балла в 1-й группе и c 13,9±0,8 до 4,3±0,6 балла во 2-й группе; p <0,05). Через 6 месяцев после начала терапии отмечалось сохранение ее результатов, при этом более стойкий эффект выявлен у пациенток 1-й группы (3,1±0,30 балла в 1-й группе и 5,5±0,73 – во 2-й; p >0,05; рис. 3).
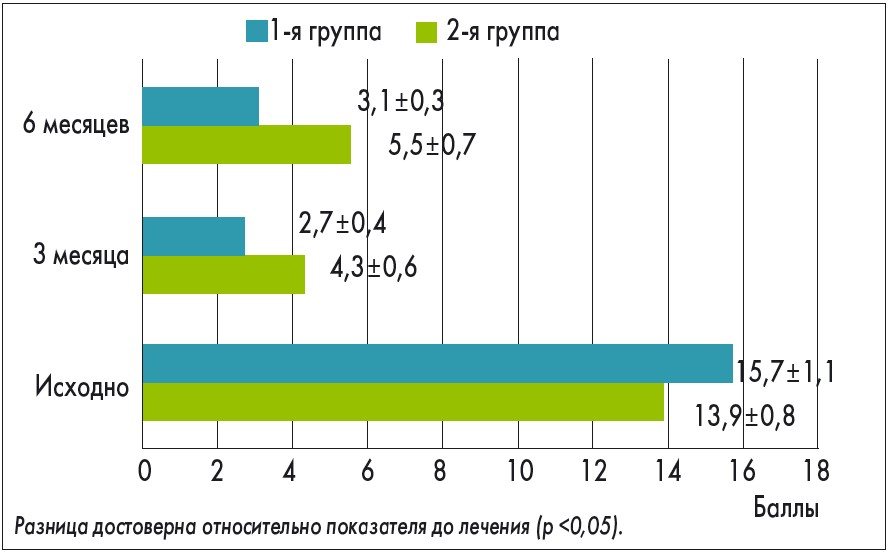 Рис. 3. Среднее количество дескрипторов у участниц исследования согласно Мак-Гилловскому опроснику
Рис. 3. Среднее количество дескрипторов у участниц исследования согласно Мак-Гилловскому опроснику
Таким образом, мониторинг клинических симптомов через 6 месяцев от начала терапии дал возможность выявить более стойкие результаты лечения у пациенток 1-й группы. Это свидетельствует в пользу эффективности лечения дисменореи по схеме, включающей Гамалате В6 по 2 таблетки 3 раза в день в течение 3 месяцев на фоне приема дидрогестерона по 10 мг 2 раза в день с 16-го по 25-й день цикла.
Нами выявлена положительная динамика симптомов негативной аффектации (раздражительности и депрессии) у женщин обеих групп. Так, в обеих группах доля женщин с проявлениями раздражительности имела тенденцию к уменьшению через 3 месяца терапии в сравнении с исходной (36,6 и 41,1% против 86,6 и 73,5% до начала терапии в 1 и 2-й группах соответственно).
Через 6 месяцев от начала лечения доля женщин с симптомами раздражительности и депрессии в группах исследования значимо не изменилась относительно таковой через 3 месяца лечения и составила 43,3% в 1-й и 47,1% – во 2-й группе.
В ходе исследования выявлена статистически значимая положительная динамика симптомов, вызванных задержкой жидкости у женщин с ПМС (отечности, масталгии). Так, доля женщин с симптомами отечности ощутимо уменьшилась через 3 месяца терапии в сравнении с исходной в группах наблюдения (23,3 и 23,5% против 56,6 и 52,9% до начала терапии в 1 и 2-й группах соответственно; p <0,05) Через 6 месяцев после начала терапи эффект лечения сохранялся (33,3 и 35,3% в 1 и 2-й группах соответственно).
Отмечена положительная динамика в результате использования предложеных схем лечения и в отношении уменьшения выраженности масталгии (26,6 и 29,4% через 3 месяца лечения против 46,6 и 47,0% до начала терапии в 1 и 2-й группе соответственно; p >0,05).
Выводы
- Клиническая картина ПМС на фоне генитального эндометриоза характеризуется доминированием симптомов отечной и нервно-психической форм ПМС.
- Полученные нами данные свидетельствуют о клинической целесообразности использования Гамалате В6 в комплексной терапии женщин с эндометриозом и симптомами ПМС.
Литература
1. Татарчук Т.Ф., Венцковская И.Б., Шевчук Т.В. Предменструальный синдром – междисциплинарная проблема // Мистецтво лікування. – 2004. – № 4 (10). – С. 36-43.
2. Пересада О.А. Предменструальный синдром: патогенез, клинические проявления, лечение // Медицинские новости. – 2010. – № 8. – С. 15-18.
3. Прилепская В.Н., Межевитинова Е.А., Сасунова Р.А., Иванова Е.В. Роль магния в патогенезе предменструального синдрома // Российский вестник акушера-гинеколога. – 2012. – № 3.
4. Майоров М.В., Жученко С.И. Применение препаратов магния в амбулаторной гинекологии // Медицинские аспекты здоровья женщины. – 2011. – № 1. – С. 14-18.
5. Татарчук Т.Ф., Захаренко Н.Ф., Маноляк І.П., Ковбасій В.П. Удосконалення лікувальної тактики ведення жінок з ендометріозом // Репродуктивна ендокринологія. – 2014. – № 4(18). – С. 24-27.
6. Захаренко Н.Ф., Ковбасий В.П., Маноляк И.П. Особенности терапии передменструального синдрома у женщин с эндометриозом // Репродуктивна ендокринологія. – 2014. – № 3(17). – С. 80-87.
7. Zukov I., Ptacek R., Raboch J. et al. Premenstrual dysphoric disorder-review of actual findings about mental disorders related to menstrual cycle and possibilities of their therapy. Prague Med Rep. 2010; 111(1): 12-24.
8. Direkvand-Moghadam A., Sayehmiri K., Delpisheh A., Kaikhavandi S. Epidemiology of Premenstrual Syndrome (PMS)-A Systematic Review and Meta-Analysis Study. J Clin Diagn Res. 2014 Feb; 8(2): 106-109.
9. Garalejic E., Bojovic-Jovic D., Damjanovic A., Arsic B., Pantic I., Turjacanin-Pantelic D., Perovic M. Hamilton anxiety scale (HAMA) in infertile women with endometriosis and its correlation with magnesium levels in peritoneal fluid. Psychiatr Danub. 2010 Mar; 22(1): 64-67.
Тематичний номер «Акушерство, Гінекологія, Репродуктологія» № 3 (31), жовтень 2018 р.