29 листопада, 2018
Оцінка лікувального та профілактичного потенціалу препарату Канефрон® Н при веденні вагітних з хронічними запальними захворюваннями верхніх сечовидільних шляхів
 Загострення хронічного пієлонефриту (ХП) – одне з найбільш поширених та серйозних захворювань у вагітних, яке належить до основних причин неакушерської допологової госпіталізації [4, 6].
Загострення хронічного пієлонефриту (ХП) – одне з найбільш поширених та серйозних захворювань у вагітних, яке належить до основних причин неакушерської допологової госпіталізації [4, 6].
Симптоматика загострення ХП подібна до клініки гострого пієлонефриту (ГП), однак вона менш виражена порівняно з ГП [6, 7]. Для перебігу захворювання характерні періодичні загострення. Підозра на загострення ХП є показанням для госпіталізації вагітної до урологічного стаціонару з метою проведення детального урологічного обстеження та лікування.
Необхідно визначити функціональний стан нирок і сечовидільних шляхів, а також встановити або виключити інші можливі причини пієлонефриту – аномалії сечовидільної системи, туберкульоз, камені у нирках та ін. Слід зауважити, що ХП негативно впливає на організм не лише матері, а й плода: він може призвести до розвитку гіпотрофії плода, зменшення маси тіла новонародженого, підвищує ризик мертвонародження.
Сучасне лікування ХП у вагітних є досить агресивним, оскільки усі пацієнтки підлягають госпіталізації до стаціонару і отримують курс антибіотикотерапії для досягнення афебрильних показників протягом 24 год та покращення клінічної симптоматики [14], що дозволяє мінімізувати ризик ураження нирок та негативний вплив на розвиток плода.
У 20% жінок після перенесеного гострого епізоду пієлонефриту функція нирок залишається зниженою [4]. Під час гестації важливо застосовувати засоби, які не чинять ембріотоксичної дії. Такими засобами є препарати рослинного походження [2, 6].
У розпорядженні лікарів – препарат Канефрон® Н, який має такі переваги: рослинне походження, хороша переносимість, комплексний механізм дії (атибактеріальний, протизапальний, спазмолітичний, діуретичний та нефропротекторний ефекти), відсутність негативного впливу на плід, а також досить широкий та значний досвід його використання в акушерській практиці [3].
Метою нашого дослідження було оцінити ефективність застосування фітопрепарату Канефрон® Н у комплексі з антибактеріальними засобами для покращення лікування та профілактики загострення ХП у вагітних.
Матеріали та методи. Ми провели відкрите моноцентрове проспективне порівняльне (у паралельних групах) дослідження, в якому під спостереженням перебувало 60 вагітних із запальними захворюваннями верхніх сечовидільних шляхів – загостренням ХП.
Залежно від обраної тактики лікування пацієнтки були розподілені на 2 групи: пацієнтки основної групи (n=30) з метою купірування клінічної симптоматики та нормалізації лабораторних показників отримували антибактеріальну терапію протягом 7 днів у комплексі з Канефрон® Н у стандартних дозах із подальшим переходом на монотерапію препаратом Канефрон® Н протягом 3 місяців для профілактики рецидиву інфекційно-запального процесу.
Пацієнтки групи порівняння (n=30) отримували тільки стандартну антибактеріальну терапію з метою купірування клінічної симптоматики та нормалізації лабораторних показників протягом 7 днів.
Канефрон® Н призначали у формі крапель для перорального прийому – по 50 крапель 3 р/добу або у таблетованій формі – по 2 таблетки 3 р/добу протягом 30 днів.
Критеріями включення у дослідження були: встановлений діагноз ХП у стадії загострення, вік пацієнток – 18-45 років.
Критеріями виключення були: вади розвитку сечовидільної системи, індивідуальна непереносимість компонентів препарату Канефрон® Н, наявність коралоподібних каменів та конкрементів у сечовому міхурі чи сечовидільних шляхах, що призводить до порушення уродинаміки, цукровий діабет, хронічна ниркова недостатність, відсутність згоди на участь у дослідженні.
Рандомізацію пацієнток на групи проводили методом сліпої вибірки. З метою оцінки ефективності реабілітаційно-профілактичних заходів у дослідження включені вагітні з загостренням ХП, яке виникло до 30-го тижня вагітності.
Групи дослідження були порівнянні за віком (вік пацієнток – від 19 до 35 років), паритетом, наявністю соматичної патології, терміном госпіталізації. Усі вагітні отримали консультацію терапевта, уролога, гінеколога, нефролога. Лікування проводилось в умовах стаціонару.
Клінічними методами обстеження були: загальноклінічні аналізи крові та сечі, визначення рівня креатиніну та сечовини у сироватці крові, ультразвукове дослідження (УЗД). Бактеріологічні дослідження проводили на момент госпіталізації, 14, 35 та 90-й день після початку терапії. Сечу для бактеріального посіву та визначення чутливості до антибактеріальних препаратів отримували за допомогою катетера Нелатон 6 Fr. Клінічно значимими показниками бактеріурії вважали >105 колонієутворюючих одиниць (КУО) уропатогену в 1 мл сечі.
Ультрасонографічне дослідження нирок здійснювали з реєстрацією пульсаційного індексу (PI) та індексу резистентності (RI) у нирковій артерії та сегментарних, міждолевих та дугових артеріях нирки. УЗД та за необхідності магнітно-резонансна томографія рекомендовані Європейською асоціацією урологів (EAU, 2015, клас В) для обстеження вагітних через мінімальний вплив цих методик на розвиток плода.
Рентгенологічні та радіоізотопні дослідження у вагітних протипоказані через можливість їх негативного впливу на розвиток плода. З цієї причини не рекомендовано також проводити ендоскопічні дослідження.
 Статистична обробка варіаційних рядів включала підрахунок середніх величин (М) і середніх помилок (м). Для порівняння варіаційних рядів використовували критерій Стьюдента.
Статистична обробка варіаційних рядів включала підрахунок середніх величин (М) і середніх помилок (м). Для порівняння варіаційних рядів використовували критерій Стьюдента.
Результати дослідження. Середній вік вагітних на момент встановлення діагнозу становив 23±6,23 роки (± середнє стандартне відхилення). У 39 жінок (65%) це була перша вагітність.
Вагітні із загостренням запального процесу в нирках (60 пацієнток) були госпіталізовані до стаціонару у терміні гестації: 12-16 тижнів –10 (17,5%), 16-22 тижні – 23 (36,7%), 23-30 тижнів – 27 (45,8%). Усі пацієнтки на момент госпіталізації отримували антибактеріальні препарати цефалоспоринового ряду, а за результатами бактеріального посіву продовжили курс або протягом 7 днів були переведені на інший антибактеріальний препарат згідно з визначеною чутливістю до нього збудника.
Найбільш поширеними скаргами на момент госпіталізації до стаціонару були: біль у попереку (96,2%), дизурія (70,2%), підвищення температури тіла вище 38 °С (64,4%), озноб (31,9%) та інші (50,3%). У загальному аналізі сечі у 100% випадків була піурія, а у 38,2% – мікроскопічна гематурія. Середні показники гемоглобіну були 111±6,7 г/л. Середній показник лейкоцитів у крові – 12,1±4,6×109/л.
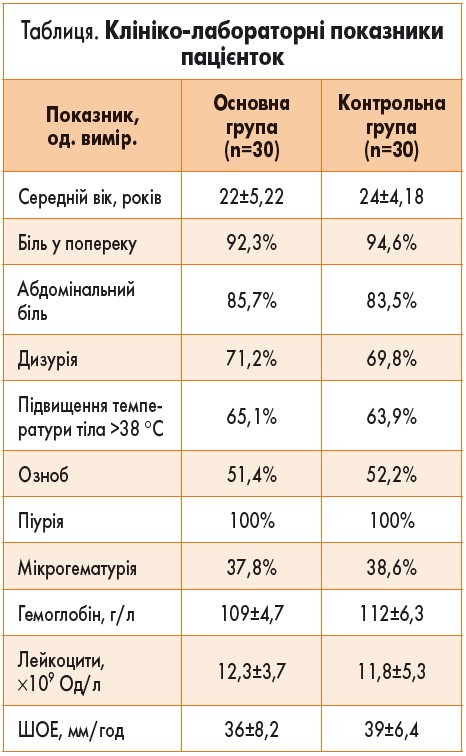
Середня температура тіла становила 37,5±0,9 °С. Симптом Пастернацького спостерігався здебільшого з правого боку – у 38 пацієнток (63,3%), ніж з лівого боку (15 жінок, 25%), був двобічним у 15 жінок (25%). Клініко-лабораторні показники пацієнток наведено у таблиці.
Усім жінкам при госпіталізації до стаціонару проводили акушерське УЗД, у всіх вагітних його результати були в нормі. У 39 (65%) пацієнток за результатами УЗД спостерігалася нормальна прохідність сечоводів, у 21 (35,8%) – уретерогідронефроз, 12 з них було поставлено ниркові стенти до кінця пологів, у решті випадків уретерогідронефрозу було достатньо займати колінно-ліктьову позу.
 Бактеріурію виявлено у 100% пацієнток із загостренням ХП з переважанням Escherichia coli (84,2% випадків), іншими мікроорганізмами були Klebsiella spp. (9,17%,) і Proteus spp. (6,67%), які мали найвищу чутливість до цефтріаксону (81,55% випадків), цефазоліну (79,5%), амоксициліну/клавуланату (77,1% випадків), цефотаксиму (72,6%), гентаміцину (60,57% випадків).
Бактеріурію виявлено у 100% пацієнток із загостренням ХП з переважанням Escherichia coli (84,2% випадків), іншими мікроорганізмами були Klebsiella spp. (9,17%,) і Proteus spp. (6,67%), які мали найвищу чутливість до цефтріаксону (81,55% випадків), цефазоліну (79,5%), амоксициліну/клавуланату (77,1% випадків), цефотаксиму (72,6%), гентаміцину (60,57% випадків).
У нашому дослідженні у 84,2% (101 з 120) випадків була висіяна E. coli з 82% чутливістю до цефтріакcону, що відповідає попереднім даним міжнародних досліджень A. Faundes та співавт. (2008) та Y.D. Fan та співавт. (2011) [7, 18].
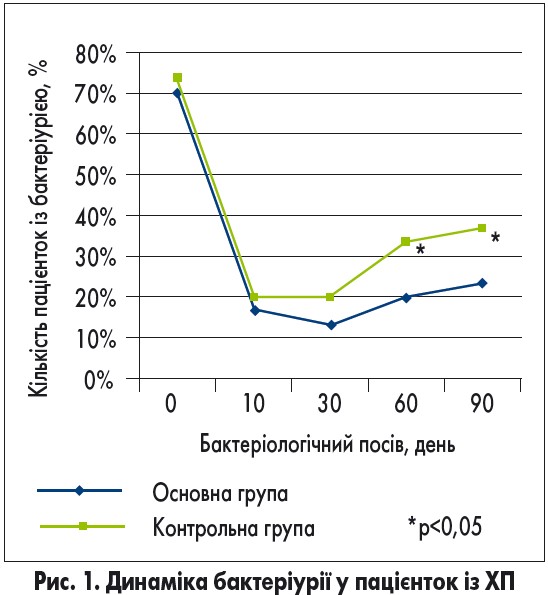
На 10-ту добу лікування у пацієнток основної групи бактеріурію виявлено у 5 (16,7%), у контрольній групі – у 6 (20%) жінок із ХП (p>0,05), на 30-ту добу в основній групі – у 4 (13,3%), у контрольній групі – у 6 (20%) (p>0,05), на 60-й день в основній групі – в 6 (20%), у контрольній групі – у 10 (33,3%) (p<0,05), на 90-й день – у 7 (23,3%) і 11 (36,7%) жінок відповідно (p<0,05).
Динаміку бактеріурії у пацієнток із ХП в групах представлено на рисунку 1. Рівень бактеріурії у пацієнток із ХП основної групи був достовірно нижчим на 60 та 90-й день після госпіталізації до стаціонару (p<0,05).
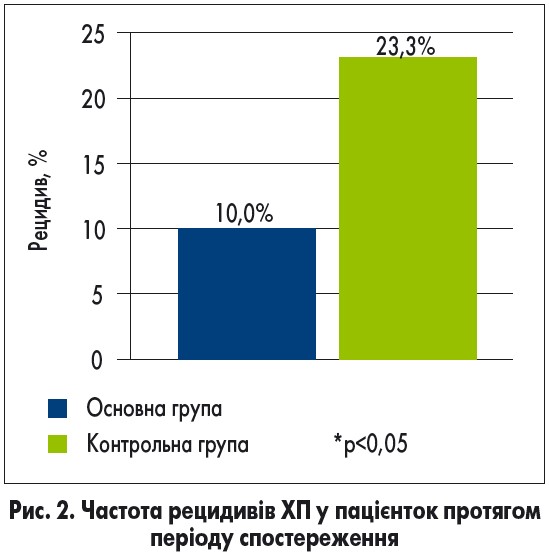 Рецидиви захворювання виникли у 3 (10%) пацієнток основної групи з ХП та 7 (23,3%) пацієнток контрольної групи протягом періоду спостереження (p<0,05). Частоту рецидивів ХП представлено на рисунку 2. Наведений графік демонструє, що частота рецидивів ХП була достовірно нижчою у пацієнток основної групи порівняно з контрольною (p<0,05).
Рецидиви захворювання виникли у 3 (10%) пацієнток основної групи з ХП та 7 (23,3%) пацієнток контрольної групи протягом періоду спостереження (p<0,05). Частоту рецидивів ХП представлено на рисунку 2. Наведений графік демонструє, що частота рецидивів ХП була достовірно нижчою у пацієнток основної групи порівняно з контрольною (p<0,05).
За даними доплерографічного дослідження ниркових артерій у вагітних із ХП відзначено істотне підвищення пульсаційного індексу (ПІ) (1,63±0,15) та індексу резистентності (ІР) (0,73±0,12), збільшення швидкості об’ємного кровотоку на рівні ниркової артерії (417±29 мл/хв).
Проведення антибактеріальної терапії забезпечило відновлення ниркового кровотоку і нормалізацію ПІ та ІР у пацієнток обох досліджуваних груп (р>0,5). Через 30 днів від початку лікування в основній групі ПІ (1,12±0,13) та ІР (0,59±0,04) нормалізувалися, у той час як у групі порівняння ПІ (1,33±0,12) та ІР (0,71±0,09) істотно перевищували показники основної групи, що зумовило високий ризик рецидиву (p<0,05). Швидкість об’ємного кровотоку на рівні ниркової артерії у пацієнток основної групи, які отримували Канефрон® Н, становила 283±28 мл/хв, натомість у жінок групи порівняння – 302±32 мл/хв (р>0,5).
Після перенесеного ХП загрозою викидня ускладнилися 9 (7,5%) вагітностей, загрозу передчасних пологів діагностовано у 14 (11,7%) жінок, які відбулися в 3 випадках (2,5%). Побічних явищ у вагітних під час прийому препарату Канефрон® Н не зареєстровано, пацієнтки відзначали хорошу переносимість препарату.
Обговорення результатів. За даними T.F. Patterson та співавт. (1997), частота безсимптомної бактеріурії не збільшується під час вагітності порівняно з невагітними [4], але фізіологічні та анатомічні зміни, що спричиняють сечовий стаз у цей період, підвищують ймовірність появи симптомів захворювання [17], особливо в середині вагітності [16] і здебільшого з правого боку [7].
Враховуючи особливості патогенезу захворювання, можна стверджувати, що головну роль у виникненні гіпотонії сечових шляхів та порушенні уродинаміки відіграють нейрогуморальні фактори на фоні механічного натискання збільшеної матки на сечоводи. Гіпотонія сечоводів у поєднанні з їх обструкцією збільшеною маткою призводить до уростазу, застою сечі у сечоводах та чашечко-мисковій системі нирок і створює сприятливі умови для інфікування [14, 15].
Дослідження, які провели L.C. Gilstrap та співавт. (2001) і L.K. Millar та співавт. (2003), присвячені вивченню захворюваності матері та плода [8, 11], асоційованої з пієлонефритом. За їх результатами, зокрема, встановлено, що лихоманка у I триместрі вагітності під час органогенезу пов’язана з тератогенним ефектом, викиднем і передчасними пологами.
Лікування загострення ХП у вагітних починають із відновлення відтоку сечі з нирки. Для цього застосовують позиційну терапію: пацієнтці рекомендовано лежати на «здоровому» боці, з припіднятим краєм ліжка, на якому розташовані ноги, займати колінно-ліктьову позу. Іноді навіть цієї простої процедури достатньо для того, щоб знизити вираженість запального процесу у нирці за рахунок зменшення тиску збільшеної матки на сечовід.
Якщо вказана консервативна терапія неефективна, а при обстеженні виявлено порушення відтоку сечі з ураженої нирки, можна виконати стентування сечоводу. Як правило, катетер-стент вдається провести без перешкод через увесь сечовід до ниркової миски, причому виділення з нього сечі частими краплинами або навіть струменем починається на висоті 13-20 см від сечового міхура, тобто саме над тим рівнем, де матка притискає сечовід до найвужчого місця кісткового кільця таза. Катетер-стент доцільно залишати на декілька тижнів після пологів.
Водночас за необхідності вагітній проводять антибактеріальну терапію, для якої обирають найменш токсичні антибактеріальні препарати, особливо до 12‑го тижня вагітності. Потім можна більш широко застосовувати антибактеріальні препарати, зокрема аміноглікозиди. Це пов’язано з тим, що до 12-го тижня закінчується закладка основних органів та систем організму плода.
Для лікування ГП або загострення захворювання у вагітних EAU (2017, клас А) рекомендує застосовувати: цефтріаксон у дозі 1-2 г в/в або в/м кожні 24 год, азтреонам у дозі 1 г в/в кожні 8-12 год, піперацилін-тазобактам 3,375-4,5 г в/в кожні 6 год, цефепім 1 г в/в кожні 12 год, іміпенем-циластатин 500 мг в/в кожні 6 год, ампіцилін 2 г в/в кожні 6 год, гентаміцин 3-5 мг/кг/добу в/в у 3 прийоми.
Таким чином, сьогодні навіть ГП або загострення ХП у вагітних із тяжким перебігом можуть бути ліквідовані та не вважаються перешкодою для сприятливого завершення і розрішення вагітності.
Отже, вагітні, які перенесли загострення ХП, значно більше схильні до розвитку ниркових захворювань внаслідок тривалого порушення уродинаміки. У 25‑30% таких пацієнток виявляють післяпологовий пієлонефрит [16, 19]. Основними факторами ризику розвитку післяпологового пієлонефриту є: «гормони вагітності» (3 міс) та розширення сечових шляхів (приблизно 1,5 міс); запальні захворювання статевих органів; ускладнення післяпологового періоду (гіпотонія матки, кровотечі та ін.).
При післяпологовому пієлонефриті проводять детальне урологічне обстеження, включаючи рентгенологічне і радіоізотопне дослідження, мета якого полягає у визначенні стану нирок і сечових шляхів, а також у виявленні або виключенні будь-яких інших можливих причин пієлонефриту – аномалій сечової системи, туберкульозу, каменів у нирках.
Досить показові дані наведені N. Pazos Otero та співавт. (2007), які проаналізували дані 4700 вагітних за 2004 рік. Частота захворюваності пієлонефритом становила 0,21%, єдиний збудник, висіяний у всіх випадках, – E. colі. У всіх пацієнток прогноз захворювання був сприятливий [17].
Заходи профілактики загострення хронічного пієлонефриту у вагітних мають подвійну спрямованість: з метою превентивного лікування хронічної інфекції сечовидільних шляхів та покращення відтоку сечі з нирок за допомогою позиційних вправ. Позиційна терапія передбачає рекомендації пацієнтці періодично займати колінно-ліктьову позу, лежати лише на «здоровому» боці, з припіднятим краєм ліжка, на якому розташовані ноги.
Для регулярного виконання таких позиційних вправ важливе значення має фаховий інструктаж пацієнтки лікарем та акушеркою, які спостерігають вагітну. У всіх вказаних положеннях знижується тиск матки на сечоводи, покращується відтік сечі, значно зменшується розширення ниркових мисок. Це підтверджують результати ультрасонографії, під контролем якої бажано проводити профілактику пієлонефриту у вагітних.
L.C. Gilstrap та співавт. (2001) повідомляють, що рецидив захворювання виникає у третини вагітних із хронічними інфекціями сечовидільної системи [9]. У нашому дослідженні рецидиви спостерігалися у 10% пацієнток із ХП протягом періоду спостереження, який тривав 90 днів.
Отже, препарат Канефрон® Н завдяки поєднанню протимікробного та протизапального ефектів забезпечує достовірне зниження рівня бактеріурії та зменшення кількості рецидивів у пацієнток із загостренням ХП. Канефрон® Н – оптимальний рослинний засіб для лікування запальних захворювань сечовидільних шляхів у вагітних, оскільки має стандартизований склад та низку необхідних ефектів.
Комплексний влив препарату Канефрон® Н на сечовидільну систему полягає у пригніченні факторів патогенності бактерій (антиадгезивній, бактеріостатичній дії), зменшенні запального процесу, нормалізації відтоку сечі завдяки сечогінному та спазмолітичному ефектам; нефропротекції за рахунок зниження виділення білку при протеїнурії.
Вкрай важливо, що різноманітний та широкий спектр рослинних речовин, які чинять антибактеріальну дію, запобігає розвитку антибіотикорезистентності, що також зумовлює доцільність застосування препарату Канефрон® Н для проведення тривалої профілактики. Проте основною перевагою цього фітопрепарату є висока безпека його застосування у пацієнток з інфекціями сечовидільних шляхів, у тому числі вагітних.
Висновки
1. Отримані у нашому дослідженні результати підтверджують ефективність препарату Канефрон® Н у зменшенні бактеріурії у пацієнток із загостренням ХП. На 30-ту добу у групі вагітних, які отримували препарат, бактеріурію виявлено у 4 (13,3%) пацієнток, а у контрольній групі – у 6 (20%) (p>0,05), на 60-й день в основній групі – у 6 (20%), у контрольній групі – у 10 (33,3%) (p<0,05), на 90-й день – у 7 (23,3%) та 11 (36,7%) жінок відповідно (p<0,05).
2. Фітопрепарат Канефрон® Н достовірно зменшує частоту рецидивів ХП, згідно з даними нашого дослідження, у 2,3 раза у пацієнток основної групи (10,0%) порівняно з контрольною (23,3%; p<0,05).
3. Застосування фітопрепарату Канефрон® Н у вагітних із загостренням ХП продемонструвало високу ефективність, безпеку та високий лікувально-профілактичний ефект засобу.
4. Препарат Канефрон® Н характеризується доброю переносимістю у вагітних із загостренням ХП, побічних явищ у пацієнток, які брали участь у дослідженні та отримували цей препарат, не зареєстровано.
5. Висока частота рецидивів ХП зумовлює необхідність у подальших дослідженнях, результати яких допоможуть у розробленні нових, більш ефективних, схем та алгоритмів лікування цієї патології у вагітних.
Література
1. Айламазян Э.К. Акушерство. Национальное руководство / Э.К. Айламазян, В.И. Кулаков, В.Е. Радзинский, Г.М. Савельева. – М.: «ГЭОТАР-Медиа», 2009. – 1200 с.
2. Кулакова В.И. Лекарственные средства, применяемые в акушерстве и гинекологии / В.И. Кулакова, В.Н. Серов. – М: «ГЭОТАР-Медиа», 2006. – 384 с.
3. Сафронова Л.А. Пиелонефрит и беременность // Русский медицинский журнал. – 2000. – № 8(18). – С. 778-781.
4. Сидельникова В.М. Преждевременные роды. Недоношенный ребенок / В.М. Сидельникова, А.Г. Антонов. – М: «ГЭОТАР-Медиа», 2006. – 448 с.
5. Шиховцева С.В. Допплерографическое исследование почечного кровотока при диффузной патологии почек / С.В. Шиховцева, Л.М. Меркулова // Материалы IX симпозиума с международным участием «Новые диагностические технологии в лучевой диагностике» (г. Москва, 26-27 сентября 2006 г.).
6. Dalal S. Long-term Escherichia coli asymptomatic bacteriuria among women with diabetes mellitus / S. Dalal, L. Nicolle, C.F. Marrs, L. Zhang, G. Harding, B. Foxman. Clinical Infectious Diseases. 2009; 49(4): 491-497.
7. Geerlings S.E. Urinary tract infections in patients with diabetes mellitus: epidemiology, pathogenesis and treatment / S.E. Geerlings. International Journal of Antimicrobial Agents. 2008; 31(suppl. 1): 54-57.
8. Gilstrap L.C. Acute pyelonephritis in pregnancy: an anterospective study / L.C. Gilstrap, F.G. Cunningham, P.J. Whalley. Obstetrics and Gynecology. 1981; 57(4): 409-413.
9. Gilstrap L.C. Urinary tract infections during pregnancy / L.C. Gilstrap, S.M. Ramin. Obstetrics and Gynecology Clinics of North America. 2001; 28(3): 581-591.
10. Hanchard N.A. The frequency of the sickle allele in Jamaica has not declined over the last 22 years / N.A. Hanchard, I. Hambleton, C.A. Harding, R.M. McKenzie. British Journal of Haematology. 2005; 130(6): 939-942.
11. Hill J.B. Acute pyelonephritis in pregnancy / J.B. Hill, J.S. Sheffield, D.D. McIntire, G.D. Wendel. Obstetrics and Gynecology. 2005; 105(1): 18-23.
12. Kokrdova Z. Septic shock in pregnancy on the basis of an acute pyelonephritis / Z. Kokrdova, A. Parizek, M. Koucky, A. Paskov, B. Boudov. Ceska Gynekol. 2016; 81(4): 286-288.
13. Kumar S. Urinary tract infections / S. Kumar, A. Dave, B. Wolf, E.V. Lerma.Dis Mon. 2015 Feb; 61(2): 45-59.
14. Oktar S.O. Doppler sonography of renal obstruction: value of venoue impedance index measurements / Oktar S.O. et al. J Ultrasound Med. 2004 Jul; 23(7).
15. Matuszkiewicz-Rowinska J. Urinary tract infections inpregnancy: old and new unresolved diagnostic and therapeutic problems / J. Matuszkiewicz-Rowinska, J. Malyszko, M. Wieliczko. Arch Med Sci. 2015 Mar 16; 11(1): 67-77.
16. Patterson T.F. Detection, significance, and therapy ofbacteriuria in pregnancy / T.F. Patterson, V.T. Andriole. Update in the managed health care era. Infectious Disease Clinics of North America. 1997; 11(3): 593‑608.
17. Pazos Otero N. Pyelonephritis and pregnancy. Our experience in a general hospital / N. Pazos Otero, L. Fuentes Ricoy, B. Ferrandez Perez, C. Martinez Vazquez, M. Martinez Poch, J. L. Osuna Diaz. Anales de Medicina Interna. 2007; 24(12): 585-587.
18. Sheiner E. Asymptomatic bacteriuria during pregnancy/ E. Sheiner, E. Mazor-Drey, A. Levy. Journal of Maternal-Fetal and Neonatal Medicine. 2009; 22(5): 423-427.
19. Smaill F.M. Antibiotics for asymptomatic bacteriuria in pregnancy // F.M. Smaill, J.C. Vazquez. Cochrane Database Syst Review. 2015 Aug 7; (8).


