10 грудня, 2018
Еверолімус у комбінації з ендокринною терапією у жінок в постменопаузі з поширеним ER-позитивним HER2‑негативним раком молочної залози
Моно- або комбінована ендокринна терапія є стандартом лікування жінок у постменопаузі з поширеним гормон-рецепторпозитивним (HR+) HER2-негативним (HER2-) раком молочної залози (РМЗ). Проте в більшості випадків на фоні ендокринної терапії розвивається стійкість до лікування, відбувається рецидив і прогресування захворювання. Подвійне інгібування сигнального шляху mTOR (мішень рапаміцину ссавців) і рецепторів естрогенів може відновити чутливість пацієнтів із поширеним РМЗ до ендокринної терапії. Доклінічні дослідження також показали, що раннє застосування інгібіторів mTOR у комбінації з ендокринною терапією може сповільнити розвиток або запобігти резистентності до ендокринної терапії, попереджуючи появу гормоннезалежних клітин.
Еверолімус є пероральним потужним селективним інгібітором mTOR, який діє синергічно з летрозолом. У дослідженнях ІІ фази, у яких еверолімус вивчався в комбінації з ендокринними препаратами, такими як тамоксифен (тамоксифен у комбінації з еверолімусом; дослідження TAMRAD), летрозол або фулвестрант (дослідження PrECOG 0102), повідомлялося про підвищення ефективності лікування порівняно з лише ендокринною терапією в неоад’ювантному та ад’ювантному режимі в жінок у постменопаузі з поширеним HR+ РМЗ. У дослідженні ІІІ фази BOLERO‑2 еверолімус у комбінації з екземестаном значно збільшував медіану виживаності без прогресування (ВБП) порівняно з плацебо в комбінації з екземестаном у жінок із поширеним HR+ HER2- РМЗ, прогресування якого відбулося на фоні прийому нестероїдних інгібіторів ароматази (7,8 проти 3,2 міс; відносний ризик – ВР – 0,45; 95% довірчий інтервал – ДІ – 0,38-0,54), результатом чого стало затвердження комбінації еверолімусу та екземестану за цим показанням. При пошуковому аналізі дослідження BOLERO‑2 медіана ВБП також була вищою у пацієнтів, які отримували еверолімус у поєднанні з екземестаном у першій лінії при рецидиві захворювання після ад’ювантної терапії (ВР 0,39; 95% ДІ 0,25-0,62). Послідовні докази ефективності еверолімусу у цих дослідженнях підтверджують доцільність поєднання еверолімусу з ендокринною терапією у першій лінії лікування поширеного HR+ РМЗ.
У цьому дослідженні вивчали ефективність еверолімусу в комбінації з летрозолом в першій лінії у жінок в постменопаузі з поширеним естроген-рецепторпозитивним (ER+) HER2- РМЗ, а також можливість продовження лікування еверолімусом в поєднанні з екземестаном у пацієнток, в яких хвороба прогресувала на фоні першої лінії терапії.
Методи дослідження
BOLERO‑4 – це відкрите багатоцентрове дослідження ІІ фази, яке було проведено в 56 центрах 13 країн. У ньому взяли участь пацієнтки в постменопаузі з поширеним ER+ HER2- РМЗ. Ці пацієнтки мали вимірювані вогнища захворювання за критеріями оцінки відповіді солідних пухлин (RECIST, версія 1.0) або ураження кісток (літичні чи змішані). Іншими критеріями включення були функціональний статус за шкалою ECOG від 0 до 2, відсутність порушення функції кісткового мозку, печінки і нирок, а також відсутність відхилень у коагулограмі. Крім того, у дослідження були включені пацієнтки, які припинили отримувати неоад’ювантну ендокринну терапію 1 рік тому або більше. Хворі, що раніше отримували інгібітор mTOR, гормональну чи іншу системну терапію на пізніх стадіях захворювання, були виключені з дослідження.
Пацієнтки в першій лінії терапії отримували перорально еверолімус 10 мг/добу і летрозол 2,5 мг/добу до прогресування захворювання, розвитку неприйнятних токсичних ефектів або відкликання згоди. Пацієнтки, які припинили лікування у зв’язку з прогресуванням захворювання, на розсуд дослідників могли отримувати еверолімус (10 мг/добу) та екземестан (25 мг/добу) у другій лінії до подальшого прогресування захворювання, неприйнятних токсичних ефектів або відкликання згоди на лікування. Дозволялася також модифікація дози.
Дослідники та/або лікар-рентгенолог оцінювали пухлини за критеріями RECIST (версія 1.0), переважно за допомогою комп’ютерної томографії або магнітно-резонансної томографії, кожні 8 тижнів (±1 тиждень) до припинення першої лінії лікування; оцінювання також проведилося кожні 8 тижнів у пацієнток у другій лінії терапії. Скан- або фотопідтвердження для вимірюваного ураження шкіри були отримані принаймні через 4 тижні після первинної відповіді.
Первинною кінцевою точкою була ВБП у першій лінії терапії за оцінкою дослідника згідно з критеріями RECIST (версія 1.0). Вторинні кінцеві точки включали загальну виживаність (ЗВ) у першій лінії терапії, ВБП у другій лінії терапії за критеріями RECIST (версія 1.0), загальну відповідь (повну або часткову), клінічний ефект (повна/часткова відповідь або стабілізація захворювання тривалістю ≥24 тижнів) в обох групах (RECIST, версія 1.0). Безпечність терапії першої та другої лінії оцінювали за частотою виникнення несприятливих подій відповідно до критеріїв CTCAE (версія 4.0).
Результати
У період з 7 березня 2013 р. до 17 грудня 2014 р. 245 пацієнток були перевірені щодо відповідності вимогам включення у дослідження. Із них 202 жінки були включені у дослідження та отримували еверолімус у комбінації з летрозолом в першій лінії терапії (рис. 1). Середній вік пацієнток становив 64 роки (58-70 років). Більшість хворих мали метастатичну (n=194; 96%), а не місцевопоширену (n=8; 4%) форму РМЗ, а також 3 або більше метастатичних вузлів (n=137; 67,8%) і вісцеральні метастази, крім локалізації у центральній нервовій системі (n=123; 60,9%). Медіана часу з моменту останнього рецидиву до початку терапії першої лінії склала 1,2 міс (0,76‑1,84 міс); дата останнього рецидиву могла збігатися за часом із вперше встановленим діагнозом метастатичного захворювання. Дата збору даних для аналізу – 17 грудня 2016 року, що відповідає 24 міс після першого візиту останньої пацієнтки.
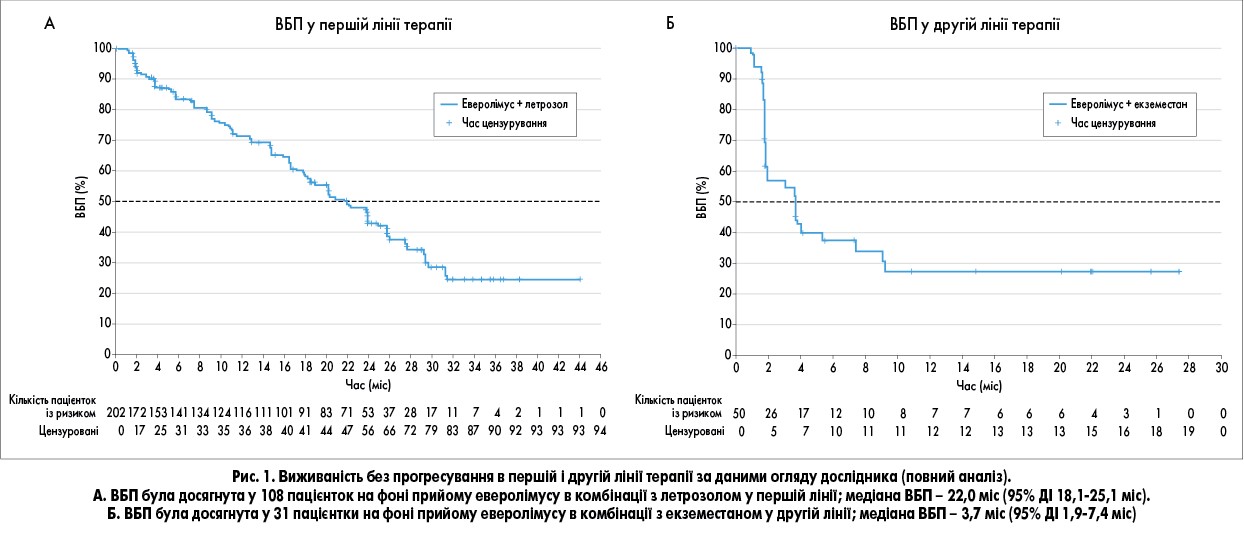 Терапію першої лінії продовжували отримувати 50 (24,8%) пацієнток, тоді як 152 (75,2%) припинили лікування. Найбільш поширеними причинами припинення лікування були прогресування захворювання (n=104; 51,5%) і розвиток побічних явищ (n=32; 15,8%). Медіана експозиції еверолімусу і летрозолу склала 64,2 та 75,1 тижня відповідно; середня фактична інтенсивність дози еверолімусу становила 8,5 мг/добу (6,0-9,9 мг/добу). Після прогресування захворювання на фоні першої лінії терапії 50 (24,8%) хворих отримували еверолімус у комбінації з екземестаном у другій лінії відповідно до рішення дослідників.
Терапію першої лінії продовжували отримувати 50 (24,8%) пацієнток, тоді як 152 (75,2%) припинили лікування. Найбільш поширеними причинами припинення лікування були прогресування захворювання (n=104; 51,5%) і розвиток побічних явищ (n=32; 15,8%). Медіана експозиції еверолімусу і летрозолу склала 64,2 та 75,1 тижня відповідно; середня фактична інтенсивність дози еверолімусу становила 8,5 мг/добу (6,0-9,9 мг/добу). Після прогресування захворювання на фоні першої лінії терапії 50 (24,8%) хворих отримували еверолімус у комбінації з екземестаном у другій лінії відповідно до рішення дослідників.
У другій лінії терапії середній вік пацієнток склав 62 роки (57-66 років). У більшості пацієнток на фоні терапії еверолімусом у комбінації з летрозолом розмір пухлини зменшувався в порівнянні з вихідним рівнем. Медіана ЗВ у пацієнток, які отримували еверолімус з летрозолом, не була досягнута (рис. 2).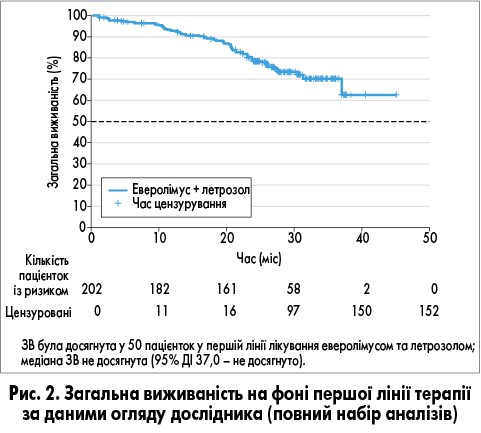
Загалом було зареєстровано 50 (24,8%) летальних випадків, дані 152 (75,2%) пацієнток підлягали перевірці. Розрахункова ЗВ для інтервалу у 24 міс склала 78,7%.
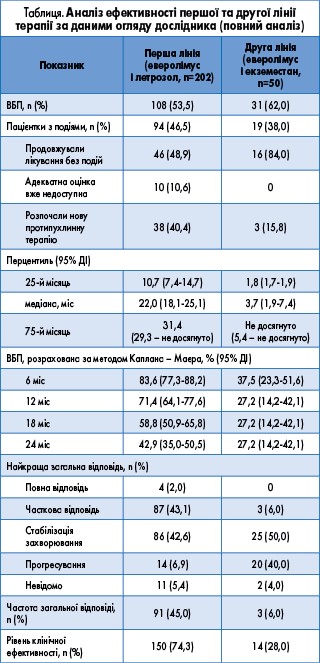
У другій лінії терапії ВБП оцінили у 31 пацієнтки. Медіана ВБП на фоні терапії еверолімусом у комбінації з екземестаном склала 3,7 міс (табл., рис. 1). Загальна відповідь і рівень клінічної ефективності становили 6 та 28% відповідно.
Обговорення результатів дослідження
Сучасні настанови рекомендують проведення ендокринної терапії у першій лінії для пацієнтів із поширеним HR+ HER2- РМЗ, за винятком захворювання, яке безпосередньо загрожує життю. У цьому дослідженні ІІ фази медіана ВБП у жінок в постменопаузі з поширеним ER+ HER2- РМЗ при застосуванні еверолімусу в комбінації з летрозолом у першій лінії становила 22,0 міс; медіана ЗВ не була досягнута при медіані спостереження 29,5 міс. Схоже покращення ВБП спостерігалось у дослідженні BOLERO‑2, у якому еверолімус в комбінації з екземестаном порівнювався з плацебо в комбінації з екземестаном (за даними дослідників: 7,8 проти 3,2 міс; ВР 0,45; за даними незалежного центру: 11,0 проти 4,1 міс; ВР 0,38).
 Результати BOLERO‑4 підтвердили обґрунтованість подвійного інгібування сигнального шляху mTOR і рецепторів естрогену в першій лінії терапії. Медіана ВБП, досягнута в цьому дослідженні, була особливо вражаючою з огляду на занедбаність захворювання у пацієнток: 96% мали метастази, 67,8% мали 3 і більше метастатичних вузлів, 60,9% мали вісцеральні метастази. Аналіз чутливості, проведений без цензурування пацієнток, які почали нову протипухлинну терапію, продемонстрував медіану ВБП, подібну до такої при первинному аналізі.
Результати BOLERO‑4 підтвердили обґрунтованість подвійного інгібування сигнального шляху mTOR і рецепторів естрогену в першій лінії терапії. Медіана ВБП, досягнута в цьому дослідженні, була особливо вражаючою з огляду на занедбаність захворювання у пацієнток: 96% мали метастази, 67,8% мали 3 і більше метастатичних вузлів, 60,9% мали вісцеральні метастази. Аналіз чутливості, проведений без цензурування пацієнток, які почали нову протипухлинну терапію, продемонстрував медіану ВБП, подібну до такої при первинному аналізі.
Останніми роками можливості лікування поширеного HR+ HER2- РМЗ значно розширилися за рахунок застосування інгібіторів циклінзалежних кіназ. У клінічних дослідженнях була встановлена перевага додавання палбоциклібу або рибоциклібу до ендокринної терапії в першій лінії. Незважаючи на ці нові варіанти лікування, доклінічні та клінічні дані показують, що комбінація інгібіторів mTOR та ендокринної терапії залишається важливим й ефективним варіантом лікування. Еверолімус продемонстрував синергізм відносно летрозолу в доклінічних моделях, а також у неоад’ювантному режимі при лікуванні хворих на РМЗ. Стосовно другої лінії терапії дослідження TAMRAD також показало, що додавання еверолімусу до тамоксифену підвищує ефективність лікування порівняно з застосуванням тільки тамоксифену, тоді як дослідження PrECOG 0102 підтвердило клінічну ефективність комбінації еверолімусу з фулвестрантом. Дослідження, представлене в цій статті, додатково підтверджує, що подвійне інгібування еверолімусом у поєднанні з ендокринною терапією є важливою терапевтичною опцією при поширеному HR+ HER2- РМЗ.
У цьому дослідженні не було отримано нових даних щодо безпечності препарату. Загалом профіль безпеки еверолімусу не відрізнявся від такого у попередніх дослідженнях, і випадки смерті внаслідок пневмонії або септичного шоку на фоні лікування узгоджуються з даними дослідження BOLERO‑2. Редукція дози або перерва в лікуванні еверолімусом у першій лінії були відносно частим явищем, у більшості випадків – унаслідок розвитку несприятливих подій. Однак більшість небажаних явищ мали 1-2 ступінь тяжкості, небажані явища 3-4 ступеня траплялись відносно нечасто.
Список літератури знаходиться в редакції.
Стаття друкується в скороченні.
Royce M. et al. Еverolimus plus endocrine therapy for postmenopausal women with estrogen receptor‑positive, human epidermal growth factor receptor 2-negative advanced breast cancer a clinical trial. JAMAOncology. 2018
Переклала з англ. Катерина Марушко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 4 (55), жовтень 2018 р


