31 січня, 2019
Титрування дози інсуліну та новий підхід до інтенсифікації терапії цукрового діабету 2 типу
21 вересня у м. Києві відбулося засідання експертної ради за участю провідних ендокринологів України за підтримки компанії Санофі. Засідання охопило декілька актуальних тем, що стосуються інсулінотерапії, а саме ситуацію з глікемічним контролем, невирішені проблеми у лікуванні хворих на цукровий діабет (ЦД), результати нових клінічних досліджень.
Засідання відбулося у вузькому колі провідних вітчизняних спеціалістів і відрізнялося динамічністю та спрямованістю на вирішення злободенних проблем менеджменту ЦД в Україні з огляду на дані доказової медицини, відображені на сторінках світових рекомендацій.
 Необхідність вирішення ключових питань, які стосуються інтенсифікації терапії ЦД, базується на останніх епідеміологічних даних, які представили увазі присутніх член-кореспондент НАМН України, доктор медичних наук, професор Б.М. Маньковський та кандидат медичних наук, доцент І.М. Кондрацька.
Необхідність вирішення ключових питань, які стосуються інтенсифікації терапії ЦД, базується на останніх епідеміологічних даних, які представили увазі присутніх член-кореспондент НАМН України, доктор медичних наук, професор Б.М. Маньковський та кандидат медичних наук, доцент І.М. Кондрацька.
Професор Б.М. Маньковський зазначив, що ЦД наразі є найпоширенішим ендокринологічним захворюванням у світі, при цьому 90% хворих страждають на ЦД 2 типу, 6-7% – на ЦД 1 типу й 3% – на ЦД інших типів. Незважаючи на величезні економічні затрати й постійні наукові розробки в даній галузі медицини, близько половини цих пацієнтів залишаються в стані декомпенсації.
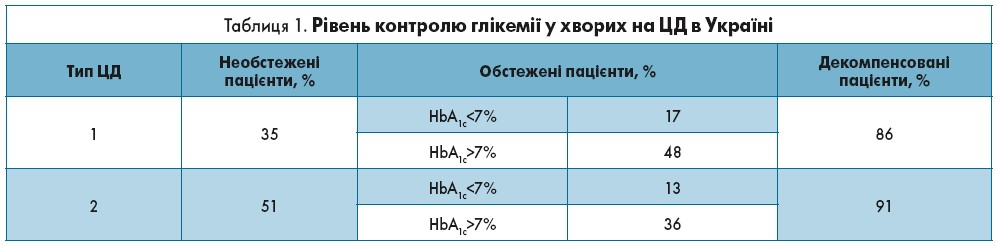
 Доцент І.М. Кондрацька розповіла, що, згідно з даними українського електронного реєстру пацієнтів, які отримують інсулін, майже 49% хворих становлять люди старше 60 років, які є економічно вразливою групою. Щодо стану глікемічного контролю, то ситуація в Україні невтішно відрізняється від світових тенденцій. Аналіз показників електронного реєстру серед пацієнтів, що перебувають на інсулінотерапії, відображений у таблиці 1.Якщо проаналізувати дані пацієнтів, які отримують аналоги інсуліну, ситуація виглядає значно кращою: лише 33% мають рівень глікозильованого гемоглобіну (HbA1c) вище 8%, однак у деяких регіонах компенсація на аналогових інсулінах дещо гірша – так, у Закарпатській області даний показник становить 56,8%.
Доцент І.М. Кондрацька розповіла, що, згідно з даними українського електронного реєстру пацієнтів, які отримують інсулін, майже 49% хворих становлять люди старше 60 років, які є економічно вразливою групою. Щодо стану глікемічного контролю, то ситуація в Україні невтішно відрізняється від світових тенденцій. Аналіз показників електронного реєстру серед пацієнтів, що перебувають на інсулінотерапії, відображений у таблиці 1.Якщо проаналізувати дані пацієнтів, які отримують аналоги інсуліну, ситуація виглядає значно кращою: лише 33% мають рівень глікозильованого гемоглобіну (HbA1c) вище 8%, однак у деяких регіонах компенсація на аналогових інсулінах дещо гірша – так, у Закарпатській області даний показник становить 56,8%.
Ситуація є близькою до критичної в пацієнтів з ЦД 2 типу, які приймають пероральні (таблетовані)цукрознижувальні препарати (ПЦЗП). У Києві рівень декомпенсації таких хворих становить 99%, що можна екстраполювати на ситуацію в країні в цілому. Отримані результати явно вказують на потребу в інтенсифікації лікування та вирішенні питання про призначення інсулінотерапії даній категорії пацієнтів, адже на сьогодні її отримують лише 11% хворих на ЦД 2 типу, що не відповідає світовим тенденціям.
На думку експертів, вже сьогодні в нашій країні необхідно провести зріз та оцінити реальність наданих даних, особливо стосовно вікової структури пацієнтів із ЦД, які отримують інсулін. Ще одним важливим моментом є оцінка зміни показників контролю глікемії у пацієнтів, що перейшли на аналоги інсуліну, яку на сьогодні оцінити вкрай важко, оскільки відсутні вихідні показники HbA1c та існує проблема фальсифікації результатів показників глікозильованого гемоглобіну, що необхідно вирішити найближчим часом.
 Доповідь керівника відділу діабетології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМНУ» доктора медичних наук Л.К. Соколової стосувалася незадоволених потреб у лікуванні пацієнтів із ЦД.
Доповідь керівника відділу діабетології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМНУ» доктора медичних наук Л.К. Соколової стосувалася незадоволених потреб у лікуванні пацієнтів із ЦД.
Сьогодні усім відомими є спільні рекомендації ADA/EASD стосовно поетапного підходу до лікування ЦД 2 типу, наявна велика кількість препаратів, ефективність яких підтверджена клінічними дослідженнями. Чому ж тоді так гостро стоїть проблема досягнення глікемічного контролю?
Для відповіді на це питання необхідно визначити труднощі, які існують сьогодні на кожному етапі інсулінотерапії.
1. Старт та титрування дози. Інсулінотерапію необхідно розпочинати у випадку, якщо цільовий рівень HbA1c не досягнутий через 3 міс після початку потрійної цукрознижувальної терапії. Стартова доза базального інсуліну становить 0,1-0,2 ОД/мл з послідуючим титруванням дози кожні 2-3 дні на 2 ОД до досягнення цільового рівня глікемії, який для більшості пацієнтів складає HbA1c<7%, глюкоза натще та перед їдою має бути у межах встановлених цільових показників.
Період титрування дози інсуліну протягом клінічних випробувань часто визначається як перші 8-12 тижнів після початку терапії. У реальній клінічній практиці неможливо госпіталізувати пацієнта на такі тривалі терміни, а амбулаторний комплаєнс до лікування не завжди є достатньо високим, що потребує тісної співпраці між лікарем та пацієнтом, а також кооперації між лікарями різних ланок (ендокринологами, сімейними лікарями тощо). Незважаючи на труднощі титрування дози інсуліну в умовах реальної амбулаторної практики, саме ефективне й безпечне титрування є ключовим процесом для досягнення коротко- і довгострокових результатів лікування. І про це мають пам’ятати абсолютно всі лікарі, що мають справу з хворими на ЦД.
Це твердження яскраво ілюструється даними останніх клінічних досліджень. Так, у ретроспективному когортному дослідженні пацієнтів із рівнем HbA1c≥7% 12-місячна затримка інтенсифікації лікування була пов’язана з підвищеним ризиком розвитку інфаркту міокарда, інсульту й серцевої недостатності (Paul S.K. et al., 2015). Ця «дисглікемічна спадщина» може впливати на якість життя пацієнта. Глікемічна відповідь протягом перших 3 міс терапії базальним інсуліном (БІ) є показником не лише глікемічного контролю в найближчій і поточній перспективі, а й довгострокового ризику гіпоглікемій, адже погане самопочуття, викликане початком інсулінотерапії, негативно впливає на комплаєнс до лікування.
Відповідно, алгоритми титрування та дози мають бути безпечними, простими й враховувати наступне:
- обмеження ризику гіпоглікемії або збільшення ваги;
- допомога в досягненні стабільного глікемічного контролю;
- базальний інсулін має забезпечити стабільний профіль зниження рівня глюкози;
- титрування дози має бути простим для навчання і застосування.
2. Підтримуючий період. Часто визначається як період, коли доза інсуліну зберігається стабільною, якщо тільки не потребує коригування з міркувань безпеки (гіпоглікемія). У цей період необхідний контроль досягнення цільових рівнів глікемії, а у разі відсутності такого необхідним є перехід на етап інтенсифікації лікування.
3. Інтенсифікація лікування. Один із найскладніших моментів інсулінотерапії, що супроводжується значною клінічною інерцією. Він полягає у додаванні до базального інсуліну інсуліна короткої дії, або перехід на терапію інсулінами премікс, або агоніста рецепторів глюкагоноподібного пептиду‑1 (АР ГПП‑1).
 Проблеми етапу інтенсифікації демонструє цікаве клінічне дослідження. У ретроспективному когортному дослідженні, проведеному у Великій Британії, в якому оцінювалися 81 573 пацієнти з ЦД 2 типу в період з січня 2004 по грудень 2006 року (спостереження до квітня 2011 року), середній рівень HbA1c у момент інтенсифікації за допомогою ПЦЗП або інсуліну в людей, які приймають один, два або три ПЦЗП, був відповідно 8,7%, 9,1% і 9,7%, що явно вказує на затримку в старті інтенсифікації (Khunti K. et al., 2013). У подальшому це негативно вплине на досягнення контролю глікемії. Відсутність своєчасної інтенсифікації призводить до збільшення ризику довгострокових мікро- і макросудинних ускладнень. Відстрочення інтенсифікації також пов’язане з небажанням пацієнтів вводити інсулін, поганою прихильністю до терапії і побоюваннями, пов’язаними з гіпоглікемією та збільшенням ваги.
Проблеми етапу інтенсифікації демонструє цікаве клінічне дослідження. У ретроспективному когортному дослідженні, проведеному у Великій Британії, в якому оцінювалися 81 573 пацієнти з ЦД 2 типу в період з січня 2004 по грудень 2006 року (спостереження до квітня 2011 року), середній рівень HbA1c у момент інтенсифікації за допомогою ПЦЗП або інсуліну в людей, які приймають один, два або три ПЦЗП, був відповідно 8,7%, 9,1% і 9,7%, що явно вказує на затримку в старті інтенсифікації (Khunti K. et al., 2013). У подальшому це негативно вплине на досягнення контролю глікемії. Відсутність своєчасної інтенсифікації призводить до збільшення ризику довгострокових мікро- і макросудинних ускладнень. Відстрочення інтенсифікації також пов’язане з небажанням пацієнтів вводити інсулін, поганою прихильністю до терапії і побоюваннями, пов’язаними з гіпоглікемією та збільшенням ваги.
Фактори, які мають впливати на вибір лікування згідно з консенсусом ADA/EASD – 2018:
- індивідуальний цільовий рівень HbA1c;
- вплив на вагу і гіпоглікемію;
- профіль безпеки препарату;
- складність режиму (частота призначення, шлях введення);
- режим для оптимізації прихильності й утримання на терапії;
- доступ до лікування, ціна і наявність препарату.
Основним аспектом, на якому було наголошено після обговорення усіх етапів інсулінотерапії, стала саме швидкість і зручність періоду титрування дози та своєчасність інтенсифікації, а також необхідність формату стаціонарного лікування хворих на ЦД. Експерти зійшлися на думці, що необхідною є оптимізація лікування, яка б, з одного боку, забезпечила належне обстеження та початок терапії пацієнтів, але з іншого – скорочення невиправданих витрат на стаціонарне лікування, яке може бути проведене в амбулаторних умовах при певній готовності цієї ланки надання допомоги хворим.
 Доктор медичних наук, професор В.В. Полторак представила увазі присутніх нещодавно опубліковані результати дослідження BRIGHT (2018), яке стало першим head-to-head рандомізованим клінічним дослідженням з порівняння ефективності та безпеки гларгіну, 300 ОД/мл (Gla‑300) і деглюдеку, 100 ОД/мл (IDeg‑100) у пацієнтів із ЦД 2 типу, які раніше не отримували інсулін.
Доктор медичних наук, професор В.В. Полторак представила увазі присутніх нещодавно опубліковані результати дослідження BRIGHT (2018), яке стало першим head-to-head рандомізованим клінічним дослідженням з порівняння ефективності та безпеки гларгіну, 300 ОД/мл (Gla‑300) і деглюдеку, 100 ОД/мл (IDeg‑100) у пацієнтів із ЦД 2 типу, які раніше не отримували інсулін.
У дослідженні взяли участь 929 пацієнтів. Критерії включення: вік ≥18 років; тривалість ЦД 2 типу ≥1 року; показник HbA1c – від ≥7,5 до ≤10,5% на момент скринінгу; ІМТ – від ≥25 до ≤40 кг/м2; застосування стабільної дози ПЦЗП ± АР ГПП‑1 (протягом ≥3 міс); незастосування інсуліну в минулому (інсулін-наївні пацієнти). Вихідні показники були однаковими в обох групах лікування.
Тривалість лікування склала 24 тижні. Пацієнти були розділені на дві групи. Перша отримувала в другій половині дня Gla‑300 (n=466), а друга – IDeg‑100 (n=463). Основною кінцевою точкою ефективності була зміна HbA1c від вихідного рівня до 24-го тижня, яка аналізувалася змішаним методом повторних вимірів (ЗМПВ) з поправкою на коваріати, в тому числі HbA1c на вихідному рівні. Межа мінімальної ефективності становила 0,3% (в одиницях HbA1c).
Вторинні кінцеві точки ефективності включали зміну від вихідного рівня до 24-го тижня показників глюкози в плазмі крові натще (ГПН), самостійно виміряний рівень глюкози в плазмі (СВРГ) натще і СВРГ у 8 контрольних точках та варіабельність СВРГ у 8 контрольних точках.
Кінцеві точки безпеки включали інцидентність та приведену до річного показника частоту підтверджених епізодів гіпоглікемії (≤70 і <54 мг/дл) протягом всього 24-тижневого періоду, а також протягом тижнів 0-12 (період титрування дози) і тижнів 13-24 (період підтримання дози) та небажані реакції, що виникли протягом лікування (НРВПЛ).
Амплітуда коливань глюкози (глікемічна варіабельність), згідно з сучасними даними, є більш важливим предиктором несприятливих наслідків ЦД, ніж HbA1c. У зв’язку з високими кореляціями між рядом метрик (індексів) глікемічної варіабельності, при її дослідженні можна обмежитися невеликою кількістю метрик без істотної втрати інформації.
Визначення міжденної варіабельності свідчить про те, що індивідуально вона характеризується стабільністю і майже абсолютно відтворює патерн на їжу, фізичну активність і лікування в наступні дні, що можливо за дуже обмежених умов клінічних досліджень, але не в реальному житті амбулаторної групи. За цих умов перевагу слід віддати синхронізуванню рівнів глюкози, отриманих з використанням 8-точкового глюкозного профілю (до і після їди, перед сном і вночі [3:00-4:00]), що і було зроблено в поточному дослідженні.
 Використання 8-точкового СВРГ-профілю, що включав у себе визначення ще однієї точки в нічний час, забезпечило релевантність оцінки глікемічної варіабельності й прогнозування патерна асоційованих гіпоглікемічних подій у реальній клінічній практиці при введенні аналогів базального інсуліну другої генерації.
Використання 8-точкового СВРГ-профілю, що включав у себе визначення ще однієї точки в нічний час, забезпечило релевантність оцінки глікемічної варіабельності й прогнозування патерна асоційованих гіпоглікемічних подій у реальній клінічній практиці при введенні аналогів базального інсуліну другої генерації.
При загальному низькому рівні гіпоглікемічних подій після ініціації інсулінотерапії в інсулін-наївних пацієнтів із ЦД 2 типу встановлено значущо більш виражене зниження ризику нічних гіпоглікемій у період титрування з Gla‑300 порівняно з IDeg‑100 при нейтральному або мінімально вираженому підвищувальному впливі на глікемічну варіабельність, що характеризується фізіологічним рівнем у початковий період (коефіцієнт варіації (CV) <25%).
Протягом усього дослідження і періоду підтримання дози інцидентність і частота виникнення підтверджених епізодів гіпоглікемії (≤70 і <54 мг/дл) у будь-який час доби (24 год) і в нічний час (00:00-06:00) статистично не відрізнялася в обох групах лікування. Протягом періоду титрування дози (тижні 0-12) інцидентність і частота виникнення підтверджених епізодів гіпоглікемії (≤70 і <54 мг/дл) у будь-який час доби (24 год), а також частота підтверджених епізодів гіпоглікемії (≤70 мг/дл) у нічний час (00:00-06:00) були нижчими в групі застосування Gla‑300.
Менші частота і річні темпи в будь-який час доби (24 год) підтвердженої гіпоглікемії (≤70 і ≤54 мг%) спостерігалися у групі Gla‑300 порівняно з IDeg‑100 під час початкового періоду титрування (тижні 0-12), незважаючи на те що в тимчасовому аспекті це був період інтенсивного нарощування дози інсуліну. Менша частота гіпоглікемії при використанні Gla‑300 порівняно з IDeg‑100 протягом періоду інтенсивного титрування інсуліну могла б допомогти в кращому комплаєнсі пацієнта, забезпечивши належне ініціювання та титрування базального інсуліну з меншим страхом гіпоглікемії.
Загалом, дослідження BRIGHT продемонструвало наступне:
- однаковий глікемічний контроль при застосуванні Gla‑300 і IDeg‑100 для зниження показників HbA1c і глюкози натще;
- однакова варіабельність добового показника глюкози натще при застосуванні обох препаратів;
- незначний і порівнянний набір маси тіла на момент завершення дослідження в обох групах лікування, незважаючи на дещо вищу середньодобову дозу інсуліну Gla‑300.
Впродовж усього дослідження і періоду підтримування дози інцидентність і частота виникнення підтверджених епізодів гіпоглікемії (≤70 і <54 мг/дл) у будь-який час доби (24 год) і в нічний час (00:00-06:00) були порівнянними в обох групах лікування.
 Впродовж періоду титрування дози (тижні 0-12) інцидентність і частота виникнення підтверджених епізодів гіпоглікемії (≤70 і <54 мг/дл) у будь-який час доби (24 год), а також частота підтверджених епізодів гіпоглікемії (≤70 мг/дл) у нічний час (00:00–06:00) були нижчими в групі застосування Gla-300.
Впродовж періоду титрування дози (тижні 0-12) інцидентність і частота виникнення підтверджених епізодів гіпоглікемії (≤70 і <54 мг/дл) у будь-який час доби (24 год), а також частота підтверджених епізодів гіпоглікемії (≤70 мг/дл) у нічний час (00:00–06:00) були нижчими в групі застосування Gla-300.
Отримані дані є унікальними та значущими при виборі лікувальної тактики у рутинній клінічній практиці, однак необхідні додаткові дослідження, які б порівняли Gla‑300 і IDeg‑100 у пацієнтів із більш тяжким ЦД 2 типу, для визначення того, чи можна відмінності між двома інсулінами, виявлені в дослідженні BRIGHT, також застосувати у пацієнтів із більш високим ризиком гіпоглікемії (ті, хто отримує тривалий час базальну або базисно-болюсну інсулінову терапію).
! Експертна рада дійшла висновку, що результати дослідження BRIGHT є переконливими й більш значущими, ніж дані, отримані в дослідженні DEVOTE, яке показувало переваги деглюдеку (100 ОД/мл) порівняно з гларгіном (100 ОД/мл) у частоті епізодів гіпоглікемій.
Переваги Gla‑300 при застосуванні полягають також у тому, що, згідно з обговореними вище епідеміологічними даними, основна маса пацієнтів, які перебувають на інсулінотерапії, відносяться до вікової групи >55 років, а чутливість до епізодів гіпоглікемії у цих пацієнтів значно знижується, тому Gla‑300 має переваги у даній популяції, зменшуючи кількість епізодів гіпоглікемії, особливо в період титрування.
 Ще одним моментом, на який звернули увагу експерти, стало те, що незважаючи на більшу дозу Gla‑300 метаболічні ефекти (збільшення маси тіла) були порівнянними в обох групах, а отже, з точки зору безпеки Gla‑300 не поступається IDeg‑100, однак цю різницю у дозах слід враховувати при формуванні цінової політики та оцінці фармекономічної вигоди для пацієнта.
Ще одним моментом, на який звернули увагу експерти, стало те, що незважаючи на більшу дозу Gla‑300 метаболічні ефекти (збільшення маси тіла) були порівнянними в обох групах, а отже, з точки зору безпеки Gla‑300 не поступається IDeg‑100, однак цю різницю у дозах слід враховувати при формуванні цінової політики та оцінці фармекономічної вигоди для пацієнта.
Наступна доповідь професора Б.М. Маньковського була присвячена препарату Соліква, принципово новій фіксованій комбінації базального інсуліну (інсулін гларгін 100 ОД/мл) і АР ГПП‑1 (ліксисенатид) у вигляді ін’єкції 1 раз на день для пацієнтів із ЦД 2 типу, яка не має аналогів в Україні.
Дія Солікви зумовлена синергічними ефектами компонентів, що входять до її складу. Базальний інсулін (гларгін 100 ОД/мл) знижує рівень глюкози в крові, підшкірні ін’єкції 1 раз на день призводять до тривалої дії інсуліну, а також він зменшує надлишкове продукування глюкози печінкою шляхом зниження глюконеогенезу. АР ГПП‑1 (ліксисенатид) зменшує постпрандіальний рівень глюкози шляхом глюкозозалежної секреції інсуліну, пригнічення секреції глюкагону та уповільнення випорожнення шлунка.
Ефективність такої комбінації була підтверджена двома рандомізованими відкритими контрольованими дослідженнями: LixiLan-O, в якому препарат Соліква продемонстрував перевагу в зниженні рівня HbA1c у пацієнтів, які отримували метформін у комбінації з іншими ПЦЗП, та LixiLan-L, де була продемонстрована перевага Солікви в зниженні рівня HbA1c у пацієнтів, які отримували гларгін. В обох дослідженнях показники безпеки в групі, яка отримувала Солікву, не відрізнялися від таких у групах, що приймали гларгін та ліксисенатид.
Основні результати по двом дослідженням представлені в таблиці 2.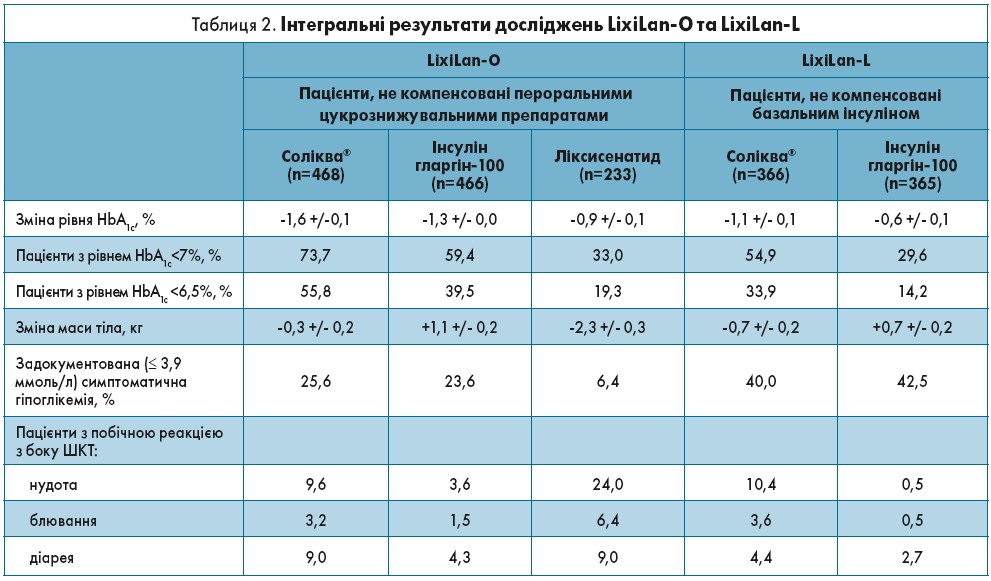 Отже, основними перевагами препарату Солікв є:
Отже, основними перевагами препарату Солікв є:
- контроль рівнів глюкози плазми натще та постпрандіальної глюкози плазми;
- ефективне зниження рівня HbA1c;
- більша кількість пацієнтів, які досягли цільових значень глікемії;
- менше збільшення ваги, ніж при застосуванні базального інсуліну;
- відсутність додаткового ризику гіпоглікемії порівняно з базальним інсуліном;
- краща переносимість з боку шлунково-кишкового тракту порівняно з АР ГПП-1.
Експертна рада оцінила результати, відображені у дослідженнях LixiLan-O та LixiLan-L, та дійшла висновку, що технічна зручність застосування препарату є величезною перевагою у пацієнтів з ЦД 2 типу, які потребують інсулінотерапії, оскільки більшість з них мають когнітивні порушення та деменцію. Використання препарату у вигляді 1 ін’єкції на день у поєднанні з кращою переносимістю, ніж базальний інсулін та АР ГПП-1, є ідеальним варіантом для досягнення цілі лікування та високого ступеня комплаєнсу, тому Соліква може розглядатися як препарат вибору у даної категорії пацієнтів.
Засідання експертної ради вкотре підтвердило свій статус одного з найбільш важливих заходів у сфері вітчизняної діабетології. Були не лише озвучені основні проблеми менеджменту й контролю хворих на ЦД, а й запропоновані шляхи їх подолання. Насамперед - це поява на ринку нових, зручних у використанні комбінацій, що корелює зі світовими рекомендаціями у лікуванні та досягненні компенсації у найбільш складних категорій пацієнтів. Таким чином, українська ендокринологія, незважаючи на велику кількість перешкод, рухається шляхом досягнення світового рівня у забезпеченні медичної допомоги пацієнтів із ЦД.
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (43) жовтень 2018 р.