13 лютого, 2019
Дослідження впливу таліглюцерази альфа на кістковий мозок у пацієнтів з хворобою Гоше 1 типу
Хвороба Гоше (ХГ) є найпоширенішою лізосомальною хворобою накопичення. Недостатня активність ферменту глюкоцереброзидази призводить до накопичення глюкоцереброзиду в макрофагах [1]. Ці макрофаги, перевантажені накопиченим матеріалом, так звані клітини Гоше, в основному акумулюються в селезінці, печінці та кістковому мозку. ХГ 1 типу є найпоширенішою формою і характеризується відсутністю симптомів з боку центральної нервової системи.
Ураження скелета є важливою причиною інвалідності та зниження якості життя, але його патофізіологія ще недостатньо зрозуміла. Може розвиватися біль у кістках і гострі кісткові кризи, (асептичний) остеомієліт, інфаркти та аваскулярний некроз. Зрештою, у деяких пацієнтів можуть виникати важкі прогресуючі деструктивні захворювання кісток, що вимагають заміни суглобів [2, 3]. Слід зазначити, що важкість цитопенії та ступінь органомегалії, інші важливі симптоми ХГ не завжди співвідносяться з тяжкістю захворювання кісток [4, 5]. Цей факт потребує окремої оцінки ураження кісток для оцінки важкості захворювання і ризику ускладнень.
Ферментна замісна терапія (ФЗТ) іміглюцеразою (Cerezym™; Джензайм, MA, США) та велаглюцеразою альфа (Vpriv™; ШайєрХДжТ, MA, США) продемонструвала високу ефективність у нормалізації кількості тромбоцитів і гемоглобіну та зменшенні розмірів органів [6]. Крім того, тривалий вплив іміглюцерази, яку вже використовують більше 15 років, приводить до поліпшення зрілості кісток у дітей та зменшення частоти аваскулярного некрозу та неспецифічного болю в кістках [7, 8]. Однак ФЗТ не може відновити наявні ушкодження кісток, зокрема переломи і колапс суглоба, що виникають внаслідок інфаркту кісток або локального остеолізу. Оскільки ураження кісткового мозку передує виникненню незворотних кісткових ускладнень, оцінка ефекту лікування повинна складатися з чутливих методів для виявлення інфільтрації кісткового мозку. Використання простих рентгенівських знімків або КТ-сканування має обмежене значення з цього боку. Магнітно-резонансна томографія (МРТ) вважається методом вибору для оцінки порушень кісткового мозку. За ХГ МРТ може адекватно визначати ранні зміни кісткового мозку до появи якихось клінічних симптомів [9]. Нормальний жовтий кістковий мозок продукує сигнал щодо високої інтенсивності на Т1- і T2-зважених зображеннях. Коли адипоцити замінюються клітинами Гоше, інтенсивність сигналу зменшується на Т1- та Т2-зважених зображеннях [9, 10]. Після терапії, коли жовтий кістковий мозок повертається, поступово збільшується інтенсивність сигналу на Т1- та Т2-зважених зображеннях [11]. Цей метод також застосовували для порівняння впливу доз. Дійсно, ураження кісткового мозку методом МРТ усувалися швидше і вираженіше в групі вищих доз [12].
Для кращої кількісної оцінки жирової фракції кісткового мозку (Ff) застосовували кількісну візуалізацію хімічного зсуву (QCSI), і вона виявилася значно нижчою у пацієнтів з ХГ порівняно зі здоровими дорослими та збільшувалася після лікування [11, 13, 14]. Середні показники для популяції здорових дорослих у цих дослідженнях коливаються від 0,29 [13] до 0,37 [15] і залежать від віку. Кісткові ускладнення передусім спостерігаються у пацієнтів з Ff <0,23. Одномірний логістичний регресійний аналіз показав, що для кожного зменшення Ff на 0,1 ризик кісткових ускладнень збільшувався на 85% [16]. Гістологічні дослідження довели, що інфільтрація клітинами Гоше пов’язана зі зменшенням кількості адипоцитів [17] і що ферментна замісна терапія призводить до зменшення числа клітин Гоше і відновлення жирової та нормальної гемопоетичної тканини [18].
Хоча спостерігаються варіації, коли неліковані пацієнти з низькою жировою фракцією можуть не мати симптомів протягом багатьох років [19], вважається, що в цілому посилена інвазія клітин Гоше в кістковий мозок створює підвищений ризик аваскулярного некрозу, інфарктів та криз [20]. Отже, оцінка кісткового мозку стала частиною міжнародних рекомендацій [21, 22] і застосовується під час досліджень нових препаратів.
Таліглюцераза альфа (Елелісо, ПроталіксБіотерапьютікс, Кармель, Ізраїль/Пфайзер Інк., Нью-Йорк, США) – це рекомбінантна β-глюкоцереброзидаза людини, що виробляється за допомогою клітин моркви, яка нещодавно була зареєстрована в Управлінні з контролю за якістю продуктів харчування та лікарських засобів США (FDA) як нова замісна ферментна терапія для пацієнтів з ХГ. Подвійне сліпе рандомізоване клінічне дослідження фази ІІІ в паралельних групах дозування (30 та 60 одиниць/кг кожні два тижні) було завершено. Результати цього 9-місячного клінічного дослідження 20 інфузій (номер NCT: 00376168) продемонстрували статистично значущі поліпшення порівняно з вихідним рівнем показників селезінки та всіх вторинних кінцевих точок ефективності (розмір печінки, рівні гемоглобіну та тромбоцитів) з більш швидкою відповіддю на дозу 60 одиниць/кг [23], Ff, яку вимірювали методом QCSI, була включена в експлораторні параметри в цьому реєстраційному дослідженні оцінки відповіді кісткового мозку у підгрупі пацієнтів з ХГ, що бра віді з боку Ff на терапію таліглюцеразою альфа упродовж періоду до 36 місяців, а також їхнє відношення до загальних відповідей у цих пацієнтів. Дані Ff порівнюються з результатами у нелікованих пацієнтів з бази даних АМЦ Гоше.
Матеріали і методи
Пацієнти, які отримували таліглюцеразу альфа
Вісім із 10 пацієнтів з вищезазначеного реєстраційного дослідження [23], які погодилися на експлораторний аналіз Ff в АМЦ Амстердама, продовжили участь у протоколі довгострокового спостереження. Відбір здійснювався тільки на основі згоди приїзду до Амстердама.
Чотири пацієнти отримували 30 одиниць/кг кожні два тижні (група низької дози) і чотири отримували 60 одиниць/кг кожні два тижні (група високої дози). Вихідні результати Ff та результати через 12, 24 та 36 місяців після початку лікування отримані для всіх 8 пацієнтів. Результати Ff після 9 місяців отримані у 7 з 8 пацієнтів (втрачені для одного пацієнта через технічну помилку).
Неліковані контрольні пацієнти
Дані цих 8 пацієнтів порівнювали з нелікованими контрольними пацієнтами. Для порівняння відповіді Ff через 12 місяців (медіана 12,2, діапазон 8,4-14 місяців) включені результати 15 голландських пацієнтів з ХГ. З цих 15 пацієнтів у 9 отримані результати після 24 місяців спостереження без лікування (медіана 24,1, діапазон 19,1-28,3 місяця), а у 6 пацієнтів отримані результати після 36 місяців спостереження без лікування (медіана 36, діапазон 33,5-41,4).
Жирові фракції кісткового мозку
МРТ виконували на апараті GeneralElectricSignaHorizon до серпня 2009 року і надалі на апараті SiemensAvanto. Сигнал отримували з використанням 2-точкової спін-ехо послідовності Діксона (TE/TR:22/2500), а Ff розраховували за допомогою внутрішнього алгоритму [24].
Зміна сканера не мала системного ефекту [25].
Особливі зусилля були спрямовані на перепозиціювання зрізу зображення на зображеннях середньосагітального локалізатора для кожного послідовного вимірювання у одного пацієнта якомога точніше і отримання досліджуваних зон L3, L4 і L5 стандартизованим способом. При отриманні зображень за цим протоколом відтворюваність становить 0,01-0,03 для Ff [15].
Співвідношення із загальною відповіддю
Для вивчення співвідношення між відповіддю в вимірах Ff і загальною відповіддю на лікування таліглюцеразою альфа були застосовані такі параметри:
- рівень гемоглобіну та число тромбоцитів;
- розміри печінки та селезінки за оцінкою МРТ;
- активність хітотріозидази, виміряна з використанням субстрату 4МО-деоксихітобіозиду, за методикою [26] з незначною модифікацією [27].
Дані про активність хітотріозидази були доступними після 24 місяців спостереження.
Оцінка антитіл
Антитіла до таліглюцерази альфа визначали (anti-drugantibody-ADA), використовуючи метод аналізу антитіл до препарату, заснований на ELISA, згідно з проектом рекомендацій FDA.
Зразки пацієнтів з позитивним ADA далі характеризували за нейтралізуючою активністю, використовуючи антитіла антиталіглюцерази альфа для позитивного контролю. Перший аналіз є аналізом нейтралізуючої активності in vitro, де зменшення ферментної активності вимірювали в присутності сироватки пацієнта. Другий аналіз є клітинним аналізом, який вимірював рівень активної таліглюцерази альфа, що поглинається макрофагами після інкубації культивованих макрофагів з таліглюцерази альфа в присутності сироватки пацієнта. Цей аналіз об’єднує виявлення зниженого поглинання препарату клітинами-мішенями та зменшення внутрішньоклітинної активності препарату. Знижена внутрішньоклітинна активність вимірюється у випадках, коли таліглюцераза альфа та ADA-комплекси впливають на клітинне поглинання або внутрішньоклітинну ферментну активність.
Статистичні методи
Для статистичних розрахунків використовували пакет програмного забезпечення PASW statistics‑18.
Були розраховані абсолютні зміни Ff. Різні групи порівнювали за відповіддю, Ff. Порівняння проводили між пацієнтами, які отримували таліглюцеразу альфа незалежно від дози, і нелікованими пацієнтами. Крім того, було проведено порівняння між таліглюцеразою альфа в дозі 30 одиниць/кг кожні два тижні та таліглюцеразою альфа 60 одиниць/кг кожні два тижні і нелікованими пацієнтами.
Відмінності в Ff порівняно з вихідним рівнем у пацієнтів, що отримували таліглюцеразу альфа, було перевірено з використанням критерію знакових рангів по Вілкоксону. Відмінності між лікованими та нелікованими групами, а також між групами різних доз відносно абсолютної зміни значення Ff були перевірені на статистичну значущість за допомогою U-критерію Манна-Уітні.
Результати
Схвалення інституційної контрольної ради для проведення реєстраційного дослідження було отримано в кожному центрі (Єрусалим, Хайфа, Белград) [23]. Усі учасники підписали інформовану згоду.
У таблиці 1 надана характеристика пацієнтів.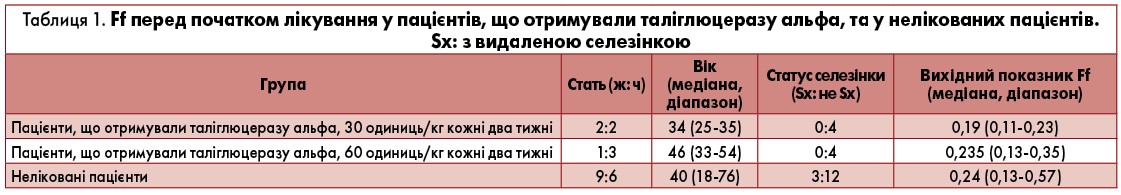
П’ять пацієнтів, що отримували таліглюцеразу альфа, мали вихідні показники Ff <0,23. Медіана вихідного Ff (n=8) становила 0,19 (діапазон 0,11-0,35) (табл. 2).
Усі пацієнти, які отримували таліглюцеразу, мали збільшення Ff, з середньою абсолютною різницею відносно вихідного рівня 0,10 (діапазон 0,03-0,19) після 1 року лікування, 0,095 (діапазон 0-0,28) через 2 роки лікування і 0,135 (діапазон 0,05-0,29) після 3 років лікування (табл. 2). Результати після 9 місяців (n=7 з 8) показують збільшення Ff, порівнювано з відповіддю після 1 року.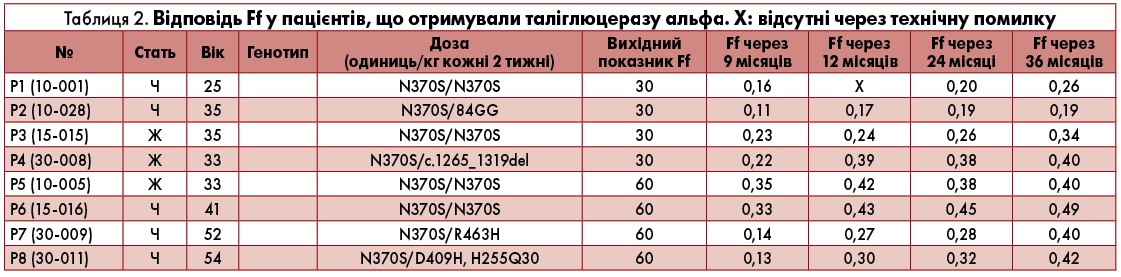
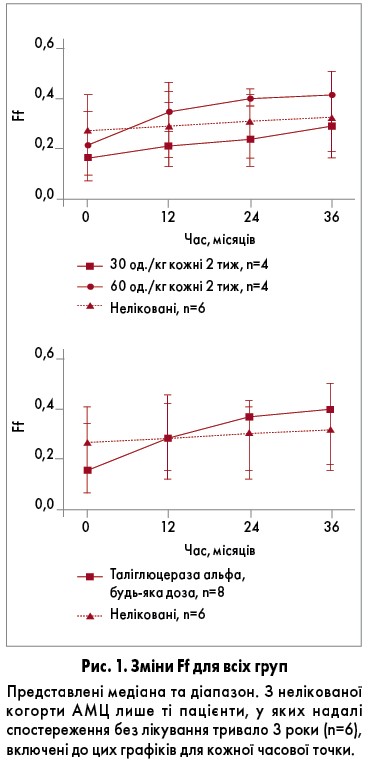 Пацієнтів, які отримували таліглюцеразу альфа, розділили відповідно до дози: 30 і 60 одиниць/кг кожні два тижні і порівняли з групою нелікованих пацієнтів. Показник Ff значно збільшився порівняно з вихідним рівнем (р=0,012) і порівняно з нелікованими пацієнтами (n=15, p=0,005) вже після 1-го року спостереження з подальшим покращенням протягом періоду до 36 місяців. На рисунку 1 зображені середні значення Ff упродовж 36 місяців спостереження пацієнтів, що отримували таліглюцеразу альфа, у порівнянні з підгрупою шести пацієнтів, які не одержували лікування, для котрих можливо було отримати результати спостереження до 36 місяців без лікування.
Пацієнтів, які отримували таліглюцеразу альфа, розділили відповідно до дози: 30 і 60 одиниць/кг кожні два тижні і порівняли з групою нелікованих пацієнтів. Показник Ff значно збільшився порівняно з вихідним рівнем (р=0,012) і порівняно з нелікованими пацієнтами (n=15, p=0,005) вже після 1-го року спостереження з подальшим покращенням протягом періоду до 36 місяців. На рисунку 1 зображені середні значення Ff упродовж 36 місяців спостереження пацієнтів, що отримували таліглюцеразу альфа, у порівнянні з підгрупою шести пацієнтів, які не одержували лікування, для котрих можливо було отримати результати спостереження до 36 місяців без лікування.
Доза не мала істотного впливу, але чотири пацієнти з найнижчим Ff (пацієнти 1, 2, 7 та 8 в таблиці 1), два з них отримували вищу дозу (пацієнти7 і 8), досягли збільшення вище 0,23 вже через 1 рік, тоді як для двох пацієнтів, що отримували 30 одиниць/кг кожні два тижні, це зайняло більше часу.
Кольорові кодовані зображення типового прикладу результатів Ff для нелікованого пацієнта та пацієнта, який отримував таліглюцеразу альфа, представлені на рисунку 2.
Відношення до загальної відповіді
Індивідуальні результати Ff та інших показників захворювання представлені на рисунку 3.
Пацієнти 1 (суб’єкт 10-001 реєстраційного дослідження) та 2 (10-028) показали порівняно помірне підвищення Ff у відповідь на лікування. Незважаючи на вихідні значення <0,23, абсолютні зміни у цих пацієнтів були відповідно 0,10 та 0,08 порівняно з вихідним рівнем.
Показник Ff підвищився до значень >0,23 у пацієнта 1, але збільшення є незначним у порівнянні з пацієнтами 7 і 8 відносно вихідного рівня Ff. Це відповідає загальній більш помірній відповіді, виявленій у цього пацієнта, незважаючи на чітке зменшення розміру селезінки, з 21 кратних нормі (КН) до 12 КН після 36 місяців лікування.
Пацієнт 2 є єдиним пацієнтом у цій когорті, який не продемонстрував збільшення Ff до значень >0,23 упродовж 36 місяців після лікування. Подібні результати отримані у деяких пацієнтів, які одержували іміглюцеразу (особистий досвід). Однак загальна відповідь у цього пацієнта задовільна з (майже) нормалізацією кількості тромбоцитів і різким зниженням активності хітотріозидази (через 24 місяці) і (більш незначним) зменшенням розмірів органів.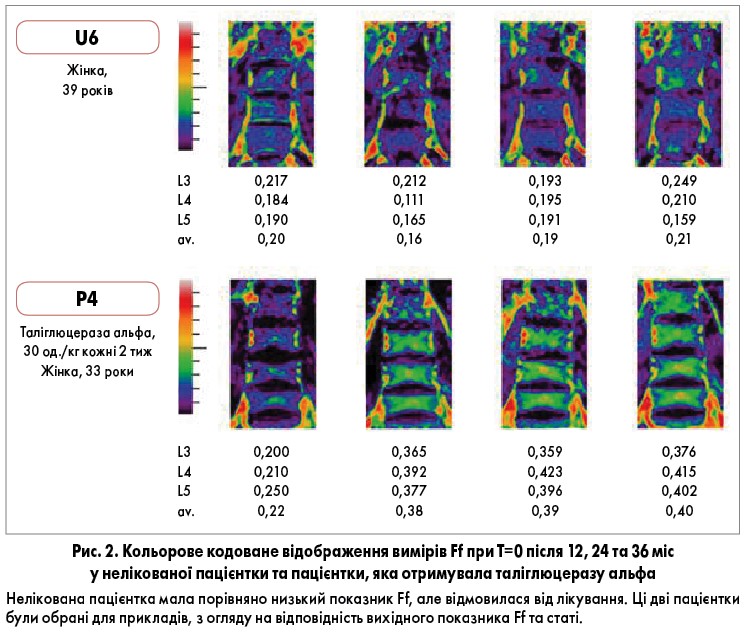
 Формування антитіл та побічні реакції
Формування антитіл та побічні реакції
Сім пацієнтів були позитивними на IgG-антитіла (3 пацієнти отримували 30 одиниць/кг кожні два тижні і 4-60 одиниць/кг кожні два тижні), з них 2 мали позитивний результат на нейтралізуючу активність (пацієнти 4 та 6) в аналізі на нейтралізуючу активність в сироватці крові, але жодний в клітинному аналізі. Пацієнт 3 виявився єдиним пацієнтом, у якого аналіз на антитіла залишався негативним упродовж всього дослідження. У пацієнта 8 після четвертої інфузії був позитивний результат на IgG-антитіла, які не мали негативного впливу, та надалі не виявлялись.
Усього було зареєстровано 112 побічних явищ (ПЯ) у 8 пацієнтів, з яких 20 ПЯ були зареєстровані як пов’язані з лікуванням. До них відносяться один пацієнт з гіперчутливою реакцією під час інфузії 23, один пацієнт з інтермітуючим фіксованим медикаментозним дерматитом через 15 місяців, який з’явився останнього разу через 14 місяців після першої інфузії, та один пацієнт з реакціями, пов’язаними з інфузією (запаморочення, озноб, нудота і біль у місці інфузії). Обидва пацієнти продовжують лікування таліглюцеразою альфа, і навіть пацієнт, що мав гіперчутливу реакцію, при повільній інфузії у поєднанні з премедикацією (лоратадин і ранітидин за 12 та 2 години до інфузії).
Обговорення
Дане наукове дослідження демонструє, що лікування таліглюцеразою альфа приводить до значного збільшення жовтого кісткового мозку, що відображає кліренс клітин Гоше у пацієнтів з ХГ 1 типу. Порівняно з нелікованими пацієнтами, показник Ff значно підвищився, що відповідає загальній задовільній відповіді у пацієнтів, які отримували таліглюцеразу альфа.
Незважаючи на те що для остаточних відповідей Ff не було встановлено статистичної різниці між дозами 30 та 60 одиниць/кг кожні два тижні, у пацієнтів з найнижчим показником Ff у групі з високою дозою відповідь досягалася швидше порівняно з двома пацієнтами з найнижчим показником Ff у групі пацієнтів з низькою дозою. Хоча це свідчить про дозозалежний ефект, також слід зазначити, що ці два пацієнти, які демонстрували швидку відповідь, були найстарішими пацієнтами в когорті. Оскільки Ff збільшується з віком, низька вихідна жирова фракція у цих двох пацієнтів могла відображати більш серйозну інфільтрацію (оскільки очікуваний показник Ff, що відповідає їхньому віку, є вищим) з наступною швидшою відповіддю.
Збільшення до рівня >0,23 було досягнуто у 7 з 8 пацієнтів. Цей поріг відсікання раніше використовували як показник ризику для кісток на основі попередніх досліджень в AMЦ [16]. Один пацієнт у групі низької дози (Р2) ще не досяг цього порога після 36 місяців лікування. Повільна відповідь кісткового мозку зазвичай просто відображає варіацію можливих відповідей і рідше може бути пов’язана із загальною повільною або відсутньою відповіддю в результаті нейтралізуючих антитіл або, можливо, локальних аномалій, як-от фіброз кісткового мозку. Оскільки цей пацієнт демонстрував адекватне зниження розмірів печінки та селезінки та позитивну відповідь на хітотріозидазу, навряд чи ефект наявності антитіл був значущим. Крім того, у цього пацієнта була відсутня нейтралізуюча активність антитіл. Досі ми не змогли визначити конкретні прогностичні показники для пацієнтів з низьким рівнем відповіді [4].
Два дослідження раніше повідомляли про відповідь Ff на замісну ферментну терапію іміглюцеразою [8, 14]. Розенталь (Rosenthal) і співавт. аналізували відповідь у 11 з 12 пацієнтів після 42 місяців лікування в початкових дозах 60 одиниць/кг кожні два тижня і встановили середнє абсолютне збільшення на 17,7% (діапазон 5,5-24,6%) [8]. Прямому порівнянню поточних результатів з результатами цього дослідження заважає той факт, що їхня популяція складалася з 8 дітей. З віком перетворення червоного кісткового мозку у жовтий починається в термінальних фалангах і прогресує від периферичного (апендікулярного) до центрального (осьового) скелета. Коли людина досягає 25 років, конверсія кісткового мозку завершена, і досягається модель дорослого зі збільшенням жирової фракції в довгих кістках, а також у хребцях [28, 29].
У дослідженні [14] вивчали відповідь Ff у 12 дорослих пацієнтів з ХГ під час лікування. Середнє абсолютне збільшення у цих пацієнтів після 48-60 місяців становило 17,5% (діапазон 8-29%) з нормалізацією Ff у 11 з 12 пацієнтів. Важлива різниця з цим дослідженням полягає в тому, що пацієнти в даній когорті отримували препарат у значно нижчих початкових дозах (середня доза 7,5 одиниць/кг кожні два тижня, діапазон 7,5-30 одиниць/кг кожні два тижня).
Було б дуже цікаво порівняти відповіді Ff у пацієнтів, що отримували таліглюцеразу альфа та іміглюцеразу. Голландська база даних Гоше містить досить великий обсяг спостережень щодо показників Ff (в основному) у пацієнтів, які отримували іміглюцеразу. Однак порівняння не було доцільним, оскільки голландська когорта пацієнтів, як правило, отримувала різні дози ферменту.
Обмеженням цього дослідження є той факт, що нелікована голландська когорта і пацієнти, які отримували таліглюцеразу альфа, не були уставлені за віком, статтю та вихідним рівнем Ff. Однак статистично значущої різниці у вихідному рівні Ff не було. Хоча не всі неліковані пацієнти мали дані на кожну часову точку, ми розрахували відносні зміни порівняно з вихідними показниками для кожного учасника, які демонструють, що загалом Ff залишається незмінним у нелікованих пацієнтів, як про це вже повідомлялося раніше [19].
Хоча у 7 пацієнтів виявлялись антитіла до таліглюцерази альфа, не було виявлено жодних побічних реакцій відносно клінічних результатів. Не було чіткого контрасту в клінічній відповіді між двома пацієнтами, у яких спостерігалася нейтралізуюча активність (пацієнти 4 та 6), у порівнянні з іншими пацієнтами, які отримували таліглюцеразу альфа. Хоча це підтверджує попередні спостереження, що антитіла до рекомбінантних ферментів, що використовуються для лікування ХГ, загалом мало впливають на клінічну ефективність [30], важко порівняти результати тесту з даними літератури. Оскільки чутливість аналізів може широко відрізнятися, не можна зробити ніяких висновків щодо імуногенності у порівнянні з іншими ферментами, які застосовуються для ФЗТ.
Отже, лікування таліглюцеразою альфа приводить до задовільного збільшення Ff, що відповідає (загалом) позитивній загальній динаміці, яка спостерігається у цих пацієнтів.
Список літератури знаходиться в редакції.
За матеріалами статті: van Dussen L., Zimran A., Akkerman E.M. et al. Taliglucerase alfa leads to favorable bone marrow responses in patients with type I Gaucher disease. Blood Cells, Molecules and Diseases 2013; 50: 206-211.
PP-ELE-UKR-0010
Статтю надруковано за підтримки представництва компанії «Пфайзер Eкспорт Бі. Ві.» в Україні.
Фахова думка
 Свій погляд на лікування хвороби Гоше представила завідувач Центру орфанних захворювань Національної дитячої спеціалізованої лікарні «Охматдит» Миністерства охорони здоров’я України, кандидат медичних наук Н.О. Пічкур.
Свій погляд на лікування хвороби Гоше представила завідувач Центру орфанних захворювань Національної дитячої спеціалізованої лікарні «Охматдит» Миністерства охорони здоров’я України, кандидат медичних наук Н.О. Пічкур.
– Клінічні форми лізосомних хвороб накопичення (ЛХН) були описані упродовж XIX століття когортою видатних клініцистів та патоморфологів, чиїми прізвищами були пізніше названі відповідні нозологічні форми: Уоррен Tей, Бернард Сакс, Філіп Гоше, Йоханес Фабрі, Альберт Німан, Людвіг Пік і Йоханес Помпе.
Хвороба Гоше (ХГ) – це спадкове панетнічне захворювання, яке належить до групи сфінголіпідозів і є яскравим представником даної групи макромолекулярних порушень спадкових орфанних метаболічних хвороб. ХГ успадковується за аутосомно-рецесивним типом, причиною захворювання є дефіцит лізосомального ферменту глюкоцереброзидази (кислої β-глюкозидази). Це призводить до накопичення субстрату глюкоцереброзиду (глюкозилцераміду) в макрофагах лізосом та інших клітинах організму, наприклад, в остеобластах. Клінічна картина ХГ характеризується мультисистемними ураженнями та зазвичай має прогресуючий хронічний перебіг. У пацієнтів спостерігається затримка росту і статевого дозрівання, ранній початок остеопенії, значна спленомегалія, гепатомегалія, тромбоцитопенія, анемія, сильний кістковий біль, гострі кісткові кризи та переломи. Приблизно 80% дітей з ХГ мають щонайменше одну кісткову патологію на момент діагнозу.
Завдяки розробці сучасних високоспецифічних методів лікування пацієнти з рідкісними спадковими захворюваннями, якими є ЛХН, отримали ефективні засоби корекції патологічного стану і суттєвого покращення якості життя. І саме ХГ стала в прямому сенсі піонером щодо ефективного застосування перших лікарських засобів для ферментозамісної терапії.
Замісна терапія ферментами забезпечується екзогенним введенням рекомбінантних ферментів з метою заміни дефектних лізосомальних ферментів.
Золотим стандартом лікування хвороби Гоше І типу та ненейропатичних проявів ІІІ типу є лікарський засіб, глюкоцереброзидаза, що містить залишки манози та впливає на макрофаги (іміглюцераза). Багаторічні дані Реєстру пацієнтів з ГХ (ICGG Gaucher Registry) вказують на те, що ферментна замісна терапія іміглюцеразою дозволяє нівелювати гематологічні та вісцеральні прояви захворювання і зменшити навантаження клітинами Гоше кісткового мозку. У результаті спостерігається зменшення остеопенії, болю в кістках, ризику переломів та загальне поліпшення якості життя хворих. Деякі прояви патології кісток, наприклад, остеонекроз, остеофіброз та літичні ураження, ліквідувати не можна, але своєчасно встановлений діагноз та вчасно розпочата терапія запобігає розвитку цих незворотних ускладнень.
Інші варіанти ферментної замісної терапії, що впливають на макрофаги, наразі завершили клінічні випробування та зареєстровані в розвинутих країнах: велаглюцераза, людський фермент, який виробляють фібробласти, та фермент рослинного походження – таліглюцераза альфа.
В Україні на сьогодні зареєстровано всі три лікарські засоби, що з одного боку дозволяє розширити лікарській арсенал, але з другого ставить складне питання щодо вибору найбільш ефективного препарату. Зазвичай рідкісність захворювання, що впливає на кількість пацієнтів, складність порівняння груп пацієнтів завдяки їхній неоднорідності, вплив генетичних та неспецифічних факторів на формування індивідуального фенотипу, а також відповіді на лікування суттєво ускладнюють оцінку ефективності різних лікарських засобів при орфанних захворюваннях. Але важливість розробки нових препаратів є надзвичайно актуальною і економічно обґрунтованою. І тому дослідження щодо впливу нового препарату – таліглюцерази альфа – на кістковий мозок і позитивні зміни з боку кісткової тканини, дають надію на те, що хворі з ХГ та лікарі отримають ще один ефективний препарат.
Медична газета «Здоров’я України 21 сторіччя» № 21 (442), листопад 2018 р.


