19 березня, 2019
Коли монотерапії недостатньо: вибір другого препарату в пацієнтів з артеріальною гіпертензією
Відповідно до рекомендацій з лікування артеріальної гіпертензії (АГ) Європейського товариства кардіологів та Європейського товариства з боротьби з артеріальною гіпертензією (ESC/ESH, 2018), β-блокатори застосовуються з першого кроку комбінованої медикаментозної терапії за наявності в пацієнтів з АГ певної супутньої патології, а саме ішемічної хвороби серця (ІХС), серцевої недостатності та миготливої аритмії. Кількість таких пацієнтів сягає 40% у загальній популяції осіб з АГ. З 2009 р. усі Європейські рекомендації (2009, 2013, 2018) виділяють конкретні переваги вазодилатуючих β-блокаторів перед звичайними кардіоселективними. В останньому документі 2018 року зазначено: «β-блокатори не є однорідним класом. Останніми роками збільшилося використання судинорозширювальних β-блокаторів, таких як лабеталол, небіволол, целіпролол і карведилол. Дослідження небівололу показали, що він має більш сприятливий вплив на центральний артеріальний тиск (АТ), аортальну жорсткість, дисфункцію ендотелію тощо. Він не має негативного впливу на ризик розвитку нових випадків цукрового діабету та має більш сприятливий профіль переносимості, ніж класичні β-блокатори, включаючи меншу побічну дію на сексуальну функцію».
Нещодавно група американських учених представила результати дослідження в умовах реальної клінічної практики, метою якого було оцінити ефективність і переносимість 4 часто застосовуваних антигіпертензивних препаратів: небівололу, амлодипіну, метопрололу та гідрохлортіазиду (ГХТЗ) – у пацієнтів з АГ, не контрольованою на фоні монотерапії (Ayyagari R. et al., 2018).
У дослідженні взяли участь 1600 пацієнтів з АГ, які перебували під спостереженням терапевтів, сімейних лікарів або кардіологів державних чи приватних медичних установ США. Середній вік хворих становив 56 років, чоловіків було 62%. Значна частина пацієнтів мала супутні захворювання або фактори ризику, як-от гіперліпідемію (47%), ожиріння (35%), куріння (24%) або діабет (21%).
Раніше як початкове лікування АГ пацієнти приймали лише один антигіпертензивний препарат – переважно інгібітори ангіотензинперетворювального ферменту (ІАПФ; 44%), діуретик (24%), блокатор рецепторів ангіотензину II (БРА; 18%) або β-блокатор (11%), проте через недостатню ефективність монотерапії (АТ >150/90 мм рт. ст.) потребували додаткового лікування. Залежно він обраного другого препарату (небіволол, амлодипін, метопролол, ГХТЗ) пацієнтів розділили на 4 рівні групи.
Після 2 міс комбінованої терапії всі препарати значно знижували систолічний (САТ) і діастолічний АТ (ДАТ) порівняно з вихідними показниками. Небіволол забезпечував контроль АТ у значно більшої кількості пацієнтів (70%), ніж амлодипін, ГХТЗ та метопролол (59, 62 і 58% відповідно; р<0,05 для всіх порівнянь). Суттєва перевага небівололу збереглася й після поправки на супутні фактори (рис.).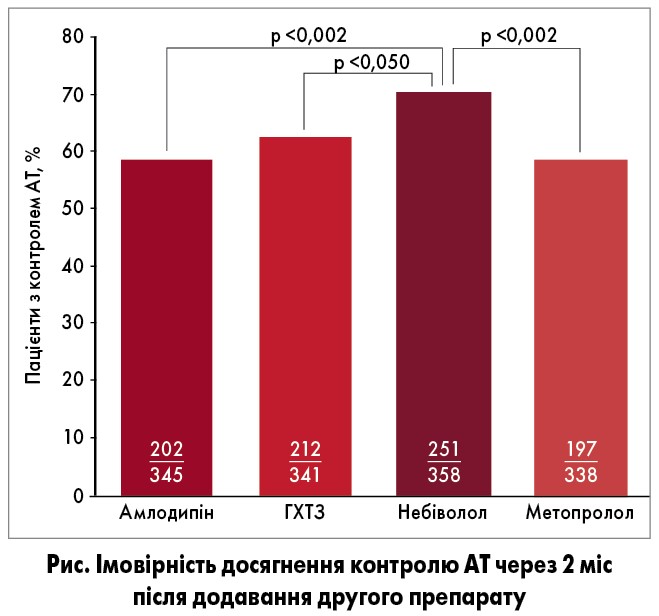
Крім вибору другого препарату, на контроль АТ впливали вік, вихідний рівень АТ, спостереження кардіологом чи лікарем загальної практики, вибір першого препарату, наявність діабету або хронічної хвороби нирок. Зокрема, ймовірність досягнення цільового АТ була вищою в пацієнтів старшого віку з менш високими початковими рівнями АТ, що починали лікування з ІАПФ/БРА та спостерігалися лікарями первинної ланки.
Частота побічних ефектів, пов’язаних із лікуванням, у групах небівололу, амлодипіну, ГХТЗ та метопрололу становила 7,0, 18,8, 10,5 та 15,0 подій на 100 пацієнтів відповідно. Хворих, які відзначили принаймні один пов’язаний з терапією побічний ефект, було найменше в групі небівололу – 5,25% порівняно з 16,25%, 7,75% та 10,25% для амлодипіну, ГХТЗ та метопрололу відповідно.
Порівняно з групою небівололу в групі амлодипіну частота пов’язаних із лікуванням побічних ефектів була вищою на 167% (р<0,001), у групі метопрололу – на 85% (р=0,012). У групі ГХТЗ побічні ефекти реєструвалися на 61% частіше порівняно з групою небівололу, проте різниця не досягла статистичної значимості (р=0,075).
Загалом частота побічних ефектів була нижчою в пацієнтів з менш тривалим анамнезом АГ (<1 року) і в чоловіків порівняно з жінками. Наявність ІХС була пов’язана з підвищенням імовірності побічних ефектів майже в 3 рази (p<0,001).
Найчастішими побічними явищами, пов’язаними з лікуванням досліджуваними препаратами, були периферичні набряки в групі амлодипіну (12,8%), гіперкаліємія в групі ГХТЗ (2,5%) та втомлюваність у групах метопрололу й небівололу (6,3 та 3,3% відповідно). У групах амлодипіну, ГХТЗ та метопрололу також було більше пацієнтів з будь-якими побічними ефектами (18,3, 10,3 та 11,1% відповідно) порівняно з групою небівололу (6,8%).
Тяжкі побічні явища спостерігалися в 7 пацієнтів: 2 (0,5%) – у групі амлодипіну (госпіталізація внаслідок гіпотензії, функціональні обмеження через периферичні набряки), 3 (0,8%) – у групі ГХТЗ (госпіталізації з приводу гіперкаліємії та гіпотензії, еректильна дисфункція), 1 (0,3%) – у групі метопрололу (госпіталізація внаслідок гіперглікемії та брадикардії) та 1 (0,3%) – у групі небівололу (госпіталізація через нудоту).
Пацієнти, які приймали небіволол, рідше потребували зменшення дози чи переривання терапії через побічні ефекти (1,3%) порівняно з хворими, що лікувалися амлодипіном (5,0%), ГХТЗ (2,8%) або метопрололом (5,8%), а також нижчу частоту відміни терапії внаслідок небажаних явищ (1,0 vs 6,0, 1,5 та 3,8% відповідно).
Проведене дослідження показало, що в пацієнтів з АГ, не контрольованою на фоні монотерапії, призначення небівололу як другого препарату забезпечує найліпші контроль АТ і переносимість порівняно з амлодипіном, ГХТЗ та метопрололом.
Більший відсоток пацієнтів у групі небівололу, які досягли цільових рівнів АТ через 2 міс лікування, дає змогу розраховувати на більш істотне зниження кардіоваскулярного ризику порівняно з трьома іншими препаратами. Раніше в дослідженні VALUE було доведено, що раннє досягнення контролю АТ асоціюється з ліпшою ефективністю профілактики кардіоваскулярних подій.
Кращі антигіпертензивна ефективність і переносимість небівололу в проведеному дослідженні добре узгоджуються з раніше отриманими даними. Так, результати рандомізованих досліджень свідчать, що небіволол у монотерапії є так само або більш ефективним порівняно з іншими антигіпертензивними препаратами та водночас переноситься ліпше, ніж інші β1-селективні блокатори (атенолол, бісопролол), блокатори кальцієвих каналів і навіть БРА лосартан (Van Bortel L. M. et al., 2008; Amrosioni E., Borghi C., 2005). У рандомізованому дослідженні в пацієнтів, які отримували лікування інгібіторами ІАПФ, БРА, діуретиками або комбінаціями цих препаратів, додаткове призначення небівололу забезпечувало високу антигіпертензивну ефективність і переносимість, подібну до такої плацебо (Neutel J. M. et al., 2010). Постмаркетингові дослідження, що проводилися в умовах реальної клінічної практики, засвідчили, що небіволол асоціюється з надійним антигіпертензивним ефектом, низькою частотою небажаних подій, поліпшенням метаболічних параметрів і якості життя пацієнтів (Hermans M. P. et al., 2009; Ladage D. et al., 2010; Schmidt A. C. et al., 2007).
Клінічні переваги небівололу в лікуванні АГ, ІХС та серцевої недостатності
Небіволол – це високоселективний блокатор β1-адренорецепторів із NO‑опосередкованими судинорозширювальними властивостями. На відміну від β-блокаторів без судинорозширювальної дії, які знижують АТ шляхом зменшення серцевого викиду, небіволол знижує опір периферичних судин і зберігає серцевий викид.
Підвищення продукції оксиду азоту (NO), яке небіволол індукує шляхом активації β3-адренорецепторів, не лише спричиняє вазодилатацію, а й має інші корисні ефекти, як-от: відновлення ендотеліальної функції, забезпечення гомеостазу позаклітинної рідини, зменшення агрегації тромбоцитів, підвищення скоротливості серця, покращення функцій центральної нервової системи (Amiri F. S., 2015). NO також відіграє ключову роль в ерекції. Нещодавній огляд продемонстрував, що небіволол значно поліпшує еректильну функцію або принаймні не погіршує її на відміну від інших β-блокаторів (Sharp R. P., Gales B. J. 2017).
Завдяки високій селективності до β1-адренорецепторів (кардіоселективності), яка є найвищою серед β1-селективних препаратів, небівололу властива добра переносимість. У терапевтичних дозах небіволол практично не впливає на β2-рецептори бронхів, печінки та підшлункової залози, що дозволяє його безпечно застосовувати в пацієнтів з бронхіальною астмою, цукровим діабетом і метаболічним синдромом.
З’являється все більше доказів того, що клінічні переваги небівололу пов’язані передусім з його унікальною здатністю діяти як агоніст β3-адренорецепторів.
Протягом багатьох років вважалося, що гемодинаміка та серцева функція регулюються двома типами β-рецепторів на рівні міокарда (β1 та β2) та α-рецепторами на рівні судин за участю нейрогуморальних ефектів ренін-ангіотензин-альдостеронової системи. Ендогенні катехоламіни (адреналін та норадреналін) діють на β1/β2-рецептори міокарда, регулюючи частоту та силу серцевих скорочень. За певних умов, наприклад при АГ або серцевій недостатності, рівні катехоламінів зростають, що підвищує серцеву активність. Цей компенсаторний механізм з часом стає шкідливим через цитотоксичність й апоптоз, що є наслідками активації та «гіперстимуляції» β1-рецепторів міокарда.
Відкриття β3-адренорецепторів у передсердях і шлуночках (Gauthier C. et al., 1996) змусило переглянути цю модель. Спочатку β3-рецептори були знайдені в жировій тканині, сечовому та жовчному міхурах. Щодо міокарда, було встановлено, що експресія β3-рецепторів збільшується у відповідь на підвищення рівнів катехоламінів. Активація міокардіальних β3-рецепторів послаблює інотропізм і в такий спосіб урівноважує шкідливу надмірну активацію β1-рецепторів. Отже, агонізм до β3-рецепторів може мати захисний ефект на рівні міокарда, захищаючи його від гіпертрофії, фіброзу й апоптозу (Arazi H. C., Gonzalez M., 2017). Активація β3-рецепторів периферичних і коронарних судин викликає NO‑опосередковану вазодилатацію, що поліпшує розслаблення шлуночків і попереджує їх ремоделювання (Balligand J.-L., 2013; 2016).
β3-рецептори розглядаються як важлива терапевтична мішень при багатьох патологічних станах, зокрема АГ, ІХС, серцева недостатність, гіперактивний сечовий міхур, синдром подразненого кишечнику, ожиріння тощо. Для клінічного застосування наразі доступні лише два β3-агоністи – небіволол і препарат для лікування гіперактивного сечового міхура мірабегрон.
Як продемонстрували результати дослідження, у пацієнтів з АГ, що не контролюється монотерапією, призначення небівололу як другого препарату дає змогу швидко та безпечно досягти цільових рівнів АТ. Іншим раціональним варіантом може бути відміна препарату, що не забезпечив достатнього зниження АТ у монотерапії, з подальшим призначенням фіксованої комбінації небівололу та ГХТЗ. Ця комбінація ефективно знижує АТ, добре переноситься, чинить нейтральний вплив на метаболізм глюкози та ліпідів, а завдяки спрощеному режиму прийому поліпшує прихильність пацієнтів до лікування.
За матеріалами статті: Ayyagari R., Xie J., Cheng D. et al. A retrospective study evaluating the tolerability and effectiveness of adjunctive antihypertensive drugs in patients with inadequate response to initial treatment. J Clin Hypertens (Greenwich). 2018 Jun; 20 (6): 1058-1066.
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 3 (448), лютий 2019 р.


