2 квітня, 2019
Нові можливості в терапії рефрактерного метастатичного колоректального раку
Колоректальний рак (КРР) є третім найпоширенішим злоякісним новоутворенням у чоловіків і жінок. У значної кількості пацієнтів на момент встановлення діагнозу вже присутні метастази, що значно погіршує прогноз. Варіанти лікування хворих на метастатичний КРР (мКРР) обмежені, особливо в разі прогресування після 1-ї та 2-ї ліній терапії. Новим можливостям лікування рефрактерного мКРР була присвячена науково-практична конференція, що відбулася 25 січня цього року у готелі Hilton Kyiv за підтримки компанії «Серв’є Україна».
 З вітальним словом перед учасниками конференції виступив генеральний директор «Серв’є Україна» Мішель Ешенбреннер. Він зазначив, що останніми роками Servier нарощує інвестиції в онкологічний та гематологічний напрями, їх розвиток є пріоритетним для компанії. У листопаді 2018 року на фармацевтичному ринку України з’явився Лансурф® – препарат для лікування пацієнтів з мКРР. Нещодавно Servier завершила придбання онкологічного підрозділу американської фармацевтичної компанії Shire, що дозволило розширити онкологічний портфель препаратами Oncaspar® (пегаспаргаза) та Onivyde® (пегільований ліпосомальний іринотекан). За словами М. Ешенбреннера, «Серв’є Україна» добре усвідомлює непросту ситуацію, яка склалася стосовно онкопатології в нашій країні, і докладе максимальних зусиль, щоб виправдати сподівання пацієнтів і лікарів на нове, більш ефективне та безпечне лікування раку.
З вітальним словом перед учасниками конференції виступив генеральний директор «Серв’є Україна» Мішель Ешенбреннер. Він зазначив, що останніми роками Servier нарощує інвестиції в онкологічний та гематологічний напрями, їх розвиток є пріоритетним для компанії. У листопаді 2018 року на фармацевтичному ринку України з’явився Лансурф® – препарат для лікування пацієнтів з мКРР. Нещодавно Servier завершила придбання онкологічного підрозділу американської фармацевтичної компанії Shire, що дозволило розширити онкологічний портфель препаратами Oncaspar® (пегаспаргаза) та Onivyde® (пегільований ліпосомальний іринотекан). За словами М. Ешенбреннера, «Серв’є Україна» добре усвідомлює непросту ситуацію, яка склалася стосовно онкопатології в нашій країні, і докладе максимальних зусиль, щоб виправдати сподівання пацієнтів і лікарів на нове, більш ефективне та безпечне лікування раку.
 Конференцію відкрила директор Національного інституту раку, доктор медичних наук Олена Олександрівна Колеснік (м. Київ). У своїй доповіді Олена Олександрівна зазначила, що особливістю проблеми КРР в Україні є порівняно низька захворюваність при високій смертності. Це зумовлено передусім відсутністю належного скринінгу. На жаль, протягом останніх 5 років збільшилася кількість пацієнтів, у яких захворювання діагностується на III‑IV стадіях, коли можливості лікування є обмеженими. Однорічна смертність пацієнтів з пізніми стадіями КРР становить 31‑37%. Близько 50% пацієнтів із КРР мають метастатичне ураження печінки, у 25% виявляють синхронні метастази. Основна стратегія лікування таких хворих включає активну хірургічну тактику, розширення можливостей комбінованого лікування та адекватне діагностичне обстеження. Поява нових препаратів з доведеною ефективністю розширює можливості лікування.
Конференцію відкрила директор Національного інституту раку, доктор медичних наук Олена Олександрівна Колеснік (м. Київ). У своїй доповіді Олена Олександрівна зазначила, що особливістю проблеми КРР в Україні є порівняно низька захворюваність при високій смертності. Це зумовлено передусім відсутністю належного скринінгу. На жаль, протягом останніх 5 років збільшилася кількість пацієнтів, у яких захворювання діагностується на III‑IV стадіях, коли можливості лікування є обмеженими. Однорічна смертність пацієнтів з пізніми стадіями КРР становить 31‑37%. Близько 50% пацієнтів із КРР мають метастатичне ураження печінки, у 25% виявляють синхронні метастази. Основна стратегія лікування таких хворих включає активну хірургічну тактику, розширення можливостей комбінованого лікування та адекватне діагностичне обстеження. Поява нових препаратів з доведеною ефективністю розширює можливості лікування.
 Завідувач відділення хіміотерапії КНП ЛОР «Львівський онкологічний регіональний лікувально-діагностичний центр», кандидат медичних наук Ярослав Васильович Шпарик нагадав, що фторпіримідини, серед яких найвідомішим є 5‑фторурацил, з метою паліативної терапії при пізніх стадіях КРР почали застосовувати з кінця 1950‑х років. Препарати цієї групи дотепер залишаються важливою складовою різних схем лікування хворих на КРР. З 1970‑х років для модуляції дії 5‑фторурацилу використовують лейковорин (кальцію фолінат). Останніми роками замість внутрішньовенного введення 5‑фторурацилу все частіше перорально призначають фторпіримідини, які забезпечують подібні показники виживаності, проте є зручнішими у застосуванні. Важливим досягненням 1990‑х років було впровадження двох нових цитостатиків – іринотекану й оксаліплатину, а також різних комбінацій, що включають один із цих засобів разом з 5‑фторурацилом і лейковорином. Останнє десятиліття відзначилося впровадженням у клінічну практику препаратів таргетної дії, зокрема моноклональних антитіл проти фактора росту ендотелію судин (VEGF) та рецептора епідермального фактора росту (EGFR), а також імунотерапії.
Завідувач відділення хіміотерапії КНП ЛОР «Львівський онкологічний регіональний лікувально-діагностичний центр», кандидат медичних наук Ярослав Васильович Шпарик нагадав, що фторпіримідини, серед яких найвідомішим є 5‑фторурацил, з метою паліативної терапії при пізніх стадіях КРР почали застосовувати з кінця 1950‑х років. Препарати цієї групи дотепер залишаються важливою складовою різних схем лікування хворих на КРР. З 1970‑х років для модуляції дії 5‑фторурацилу використовують лейковорин (кальцію фолінат). Останніми роками замість внутрішньовенного введення 5‑фторурацилу все частіше перорально призначають фторпіримідини, які забезпечують подібні показники виживаності, проте є зручнішими у застосуванні. Важливим досягненням 1990‑х років було впровадження двох нових цитостатиків – іринотекану й оксаліплатину, а також різних комбінацій, що включають один із цих засобів разом з 5‑фторурацилом і лейковорином. Останнє десятиліття відзначилося впровадженням у клінічну практику препаратів таргетної дії, зокрема моноклональних антитіл проти фактора росту ендотелію судин (VEGF) та рецептора епідермального фактора росту (EGFR), а також імунотерапії.
Загальноприйнятою стандартною практикою лікування при мКРР є підтримувальна терапія до прогресування захворювання або розвитку неприйнятної токсичності. З цією метою використовують різні стратегії, зокрема stop-and-go, реінтродукцію, «хіміотерапевтичні канікули», інтермітивну терапію та ін.
Значне покращення виживаності пацієнтів з мКРР за останнє десятиліття зумовлене не стільки досягненнями в терапії 1‑ї лінії, скільки додатковими ефектами від подальших ліній лікування. Доведено, що медіана виживаності подовжується при збільшенні кількості ліній терапії. Щоб максимізувати результати, пацієнти мають отримати всі можливі активні агенти. Актуальною є проблема резистентності до лікування та дослідження критеріїв чутливості до різних груп препаратів, особливо нових терапевтичних засобів. Одним із досягнень останніх років стало впровадження для пізніх ліній лікування мКРР препарату з групи антиметаболітів TAS‑102, або Лансурф®. Він складається з трифлуридину (аналог нуклеозиду, який включається в ДНК, перешкоджаючи її синтезу, внаслідок чого пригнічується клітинна проліферація) і типірацилу (інгібітор ферменту тимідинфосфорилази, який у звичайних умовах сприяє швидкому метаболізму трифлуридину).
 Доповідь завідувача кафедри онкології Запорізької медичної академії післядипломної освіти, доктора медичних наук, професора Олексія Олексійовича Ковальова була присвячена новим можливостям у лікуванні рефрактерного мКРР, які надає інноваційний препарат Лансурф®.
Доповідь завідувача кафедри онкології Запорізької медичної академії післядипломної освіти, доктора медичних наук, професора Олексія Олексійовича Ковальова була присвячена новим можливостям у лікуванні рефрактерного мКРР, які надає інноваційний препарат Лансурф®.
До 1990 року вважалося, що мКРР є абсолютно резистентним до дії цитостатиків. З 1970 по 1985 рік клінічні випробування пройшли 75 хіміопрепаратів для лікування цієї патології, і 5‑фторурацил був єдиним, що продемонстрував ефективність. Перші комбінації з 5‑фторурацилом включали інтерферон‑α, метотрексат, семустин, вінкристин та левамізол. У 2000‑х роках з’явилися ефективніші схеми з іринотеканом (FOLFIRI) та оксаліплатином (FOLFOX), а також комбіновані хіміотерапевтичні режими з включенням таргетних препаратів. Завдяки цим схемам медіана загальної виживаності хворих на мКРР збільшилась до 30 міс.
Однак стратегія лікування пацієнтів з КРР на пізніх стадіях потребувала оптимізації. З огляду на головні завдання терапії на цьому етапі, а саме тривалий контроль хвороби та підтримання якості життя, був розроблений новий препарат для перорального застосування у формі проліків – трифлуридин/типірацилу гідрохлорид. Після потрапляння всередину ракових клітин трифлуридин вбудовується у ДНК, що викликає її дволанцюжкові розриви та пригнічує ріст пухлини. У перших дослідженнях трифлуридин забезпечував зменшення розмірів пухлини у пацієнтів з раком грудної залози та раком товстої кишки. Проте вже тоді стало зрозуміло, що ця речовина має неоптимальний фармакокінетичний профіль (дуже короткий період напіввиведення – 12 хв) і викликає тяжкі побічні ефекти, зокрема тяжку й тривалу супресію кісткового мозку, що не дозволяло досягати терапевтичних концентрацій. Швидка деградація трифлуридину після перорального прийому зумовлена його активним метаболізмом під дією тимідинфосфорилази в печінці. Щоб вирішити цю проблему, трифлуридин поєднали з типірацилом – інгібітором тимідинфосфорилази з додатковими антиангіогенними властивостями. Ефективність і безпека трифлуридину/типірацилу (Лансурф®) у пацієнтів з рефрактерним мКРР уперше були продемонстровані в дослідженнях, що проводилися у Японії. Щоб розширити ці результати на глобальну популяцію, було ініційовано дослідження III фази RECOURSE, до участі в якому було залучено 800 пацієнтів зі 101 клінічного центру Європи, США, Австралії та Японії. Основними критеріями включення були добрий функціональний статус (ECOG 0‑1); задовільна функція кісткового мозку, печінки та нирок; попереднє застосування не менше двох ліній стандартної терапії (зокрема фторпіримідинами, іринотеканом, оксаліплатином, бевацизумабом, цетуксимабом або панітумумабом); прогресування пухлини впродовж 3 міс після останнього курсу хіміотерапії (6 міс у разі ад’ювантної терапії), а також клінічно значимі побічні реакції на тлі стандартних схем хіміотерапії, які унеможливлювали їх повторне застосування. Пацієнтів рандомізували 2:1 для лікування препаратом Лансурф® або плацебо 4‑тижневими циклами. Додатково всім пацієнтам призначали найкращу підтримувальну терапію, за винятком інших протипухлинних засобів, гормональної та імунотерапії. Пацієнтів обстежували через кожні 2 тижні під час лікування і через кожні 8 тижнів після припинення терапії. Первинною кінцевою точкою була загальна виживаність; вторинні кінцеві точки включали виживаність без прогресування, частоту відповіді, частоту контролю хвороби та безпеку.
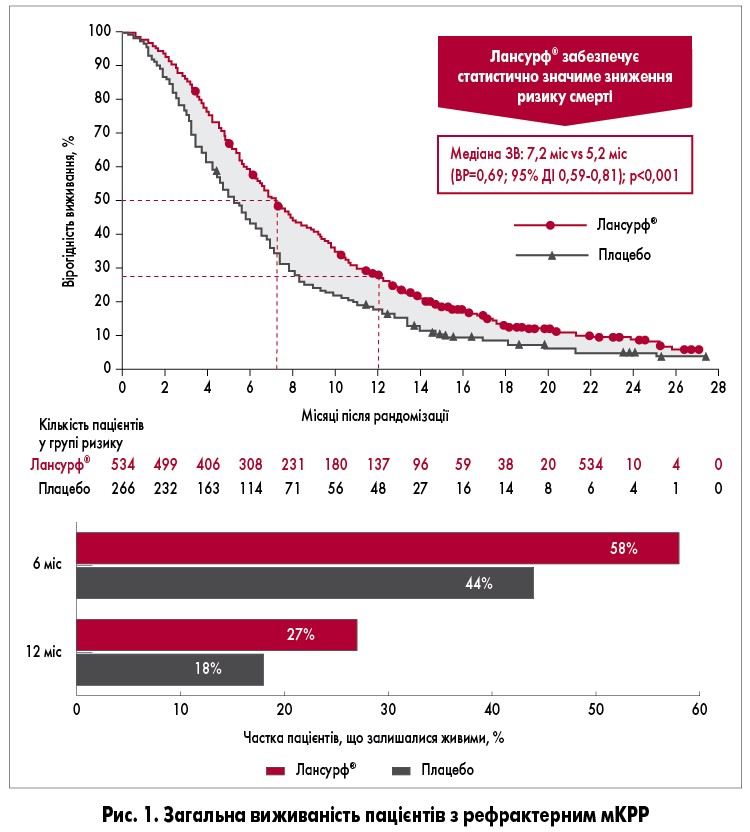
У групі пацієнтів, які застосовували Лансурф®, медіана загальної виживаності становила 7,2 міс проти 5,2 міс у групі плацебо, що відповідало зниженню ризику смерті від будь-яких причин на 32% (р<0,001); однорічна загальна виживаність становила 27 та 18% відповідно (рис. 1).
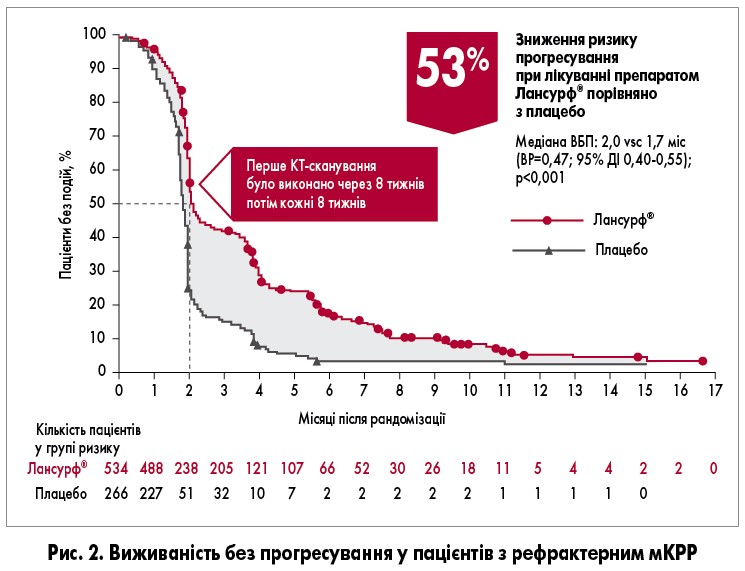
Медіана виживаності без прогресування також була значно вищою при лікуванні препаратом Лансурф® (рис. 2). Крім того, Лансурф® сприяв збереженню функціонального статусу пацієнтів: медіана часу від початкової оцінки ECOG 0-1 до ECOG ≥2 становила 5,7 міс у групі хворих, що приймали Лансурф®, порівняно з 4,0 міс у групі плацебо (р<0,001).
Аналіз даних по підгрупах пацієнтів підтвердив ефективність препарату Лансурф® в усіх підгрупах незалежно від віку, географічного регіону чи статусу KRAS. Важливо, що Лансурф® продемонстрував ефективність у пацієнтів з мКРР, рефрактерним до попередньої терапії 5-фторурацилом або регорафенібом.
Частота тяжких небажаних подій у групах досліджуваного препарату та плацебо була порівнянною (30 vs 34% відповідно). Найчастішим побічним ефектом, пов’язаним із лікуванням трифлуридином/типірацилом, була нейтропенія, яка спостерігалася у 38% пацієнтів. Слід зазначити, що за даними дослідження Pashtoon і співавт. (2016) розвиток нейтропенії після 1 міс лікування препаратом Лансурф® є предиктором кращої загальної виживаності. Імовірно це пояснюється тим, що, з одного боку, активовані пухлиною нейтрофіли стимулюють міграцію, інвазію та метастазування, а з іншого – Лансурф® вбудовується у ДНК як ракових клітин, так і нейтрофілів. Отже, у пацієнтів з високим пухлинним навантаженням і, відповідно, високим початковим рівнем нейтрофілів стандартної дози трифлуридину/типірацилу може бути недостатньо для проявлення нейтропенії, і таким хворим для досягнення кращих результатів, можливо, слід призначати препарат у вищій дозі.
Результати дослідження RECOURSE стали підставою для схвалення препарату Лансурф® як стандартної 3-ї лінії терапії пацієнтів з рефрактерним мКРР. Іншим препаратом, який також можна застосовувати в 3-й лінії терапії, є мультикіназний інгібітор регорафеніб. Порівняно з трифлуридином/типірацилом регорафеніб забезпечує зіставні переваги у виживаності, проте характеризується гіршою переносимістю.
На завершення виступу О.О. Ковальов зазначив, що реєстрацію препарату Лансурф® разом із впровадженням радіоемболізації метастазів у печінці можна визнати найбільшими досягненнями у лікуванні пацієнтів з рефрактерним мКРР. Наразі тривають дослідження трифлуридину/типірацилу в комбінації з іншими протипухлинними препаратами в 1-й і 2-й лініях терапії мКРР.
 Про безпеку терапії хворих із рефрактерним мКРР докладно розповіла доцент кафедри онкології Національної медичної академії післядипломної освіти ім. П.Л. Шупика, кандидат медичних наук Ольга Володимирівна Пономарьова (м. Київ). Вона зазначила, що в 3-й і наступних лініях терапії КРР на перший план виходить збереження якості життя пацієнтів, тому профіль побічних ефектів терапії є дуже важливим. Порівняно з іншими схемами, використання яких оцінювалося в пацієнтів із рефрактерним мКРР, застосування регорафенібу і трифлуридину/типірацилу ґрунтується на доказах високого рівня, і їх профілі безпеки є добре вивченими.
Про безпеку терапії хворих із рефрактерним мКРР докладно розповіла доцент кафедри онкології Національної медичної академії післядипломної освіти ім. П.Л. Шупика, кандидат медичних наук Ольга Володимирівна Пономарьова (м. Київ). Вона зазначила, що в 3-й і наступних лініях терапії КРР на перший план виходить збереження якості життя пацієнтів, тому профіль побічних ефектів терапії є дуже важливим. Порівняно з іншими схемами, використання яких оцінювалося в пацієнтів із рефрактерним мКРР, застосування регорафенібу і трифлуридину/типірацилу ґрунтується на доказах високого рівня, і їх профілі безпеки є добре вивченими.
Основними побічними ефектами трифлуридину/типірацилу є анемія, нудота та блювання, а також нейтропенія, яка слугує маркером хорошої відповіді. Натомість регорафеніб часто спричиняє неприємні для пацієнтів долонно-підошовний синдром, слабкість, діарею та гіпертензію. Останній побічний ефект особливо небезпечний з огляду на те, що більшість пацієнтів з мКРР є особами похилого віку і зазвичай мають супутню патологію та високий ризик кардіоваскулярних подій.
Після отримання обнадійливих результатів застосування препарату Лансурф® у дослідженні RECOURCE з метою забезпечення раннього доступу пацієнтів до життєво важливого лікування було розпочато відкрите міжнародне дослідження IIIb фази PRECONNECT, що проводиться в умовах клінічної практики. Головне завдання цього дослідження – більш детально вивчити профіль безпеки трифлуридину/типірацилу, зокрема зумовлені ним побічні ефекти, лабораторні показники, фізичний стан і вітальні симптоми. Крім того, у PRECONNECT оцінюються виживаність без прогресування, частота об’єктивної відповіді, час до погіршення ECOG ≥2, а також якість життя за питальниками EQ‑5D та EORTC QLQ-C30.
Загалом у PRECONNECT було включено 462 пацієнти з європейських країн та Австралії, які отримали принаймні 1 дозу препарату Лансурф®. У дослідження залучили, зокрема, 9 пацієнтів із 4 клінічних центрів України. Середній вік хворих становив 64 роки, у більшості пацієнтів з часу виявлення перших метастазів минуло ≥18 міс.
Пацієнти отримали від 1 до 12 циклів лікування препаратом Лансурф® (медіана – 3 цикли) із середньою дозовою інтенсивністю 89%. Зменшення дози через небажані події потребували лише 8% хворих.
На час запланованого проміжного аналізу 357 (77,3%) пацієнтів припинили лікування внаслідок прогресування хвороби. Серед небажаних подій, які стали причиною відміни терапії у 31 (2,2%) пацієнта, 10 (2,2%) були безпосередньо пов’язані з лікуванням. Найчастішою небажаною подією була нейтропенія, її зафіксовано у 51,3% пацієнтів. Загалом профіль безпеки препарату Лансурф® був прийнятним і відповідав такому в дослідженні RECOURSE та інших рандомізованих дослідженнях. Примітно, що медіана ВБП при застосуванні препарату Лансурф® в умовах клінічної практики становила 2,8 міс, а у дослідженні RECOURSE – 2,2 міс. Крім того, Лансурф® забезпечував збереження хорошого функціонального статусу пацієнтів (ECOG 0-1) протягом медіани часу 8,7 міс і досягнення контролю хвороби у 36,8% випадків. Результати щодо оцінювання якості життя пацієнтів планують отримати вже цього року.
***
Після закінчення основної частини конференції фахівці Лікарні ізраїльської онкології Lisod представили три клінічні випадки застосування препарату Лансурф® у 3-й та 4-й лініях терапії пацієнтів з рефрактерним мКРР. Один клінічний випадок було представлено з Київського міського клінічного онкологічного центру.
Лансурф® забезпечував певний контроль хвороби, характеризувався хорошою переносимістю, не викликав гематологічної чи гепатологічної токсичності, обтяження супутньої патології (ішемічної хвороби серця, артеріальної гіпертензії, цукрового діабету).
Під час обговорення учасники погодилися, що Лансурф® має перспективи у 3-й і наступних лініях терапії мКРР. Про застосування препарату в ад’ювантній терапії, 1-й і 2-й лініях терапії говорити поки що рано, хоча вже отримані обнадійливі результати в дослідженнях II фази.
До початку лікування трифлуридином/типірацилом (Лансурф®) профілактику колонієстимулювальними факторами застосовувати не потрібно, оскільки частота фебрильної нейтропенії є порівняно низькою. Немає також потреби визначати молекулярний профіль пухлини через відсутність предикторних біомаркерів ефективності трифлуридину/типірацилу.
Особливостями лікування мКРР в Україні є те, що більшість пацієнтів звичайних онкологічних клінік не отримують стандартного лікування у 1-й і 2-й лініях через фінансові труднощі, зокрема дуже високу вартість таргетних препаратів. Це потрібно враховувати під час перенесення результатів міжнародних клінічних досліджень в українські реалії.
Підбиваючи підсумки конференції, О.О. Ковальов зазначив, що мКРР поступово перетворюється на хронічне захворювання, на що вказує збільшення кількості ліній терапії з доведено ефективними опціями. Впровадження препарату Лансурф® у клінічну практику є свідченням того, що потенціал хіміотерапевтичних засобів в еру таргетної та імунотерапії зберігається.
Підготував Олексій Терещенко
Від редакції
- 22 лютого цього року Управління з контролю якості харчових продуктів і лікарських препаратів США (FDA) cхвалило застосування трифлуридину/типірацилу (Лансурф®) за новим показанням – 3-я лінія терапії пацієнтів з метастатичною аденокарциномою шлунка або шлунково-стравохідного з’єднання. Рішення FDA ґрунтується на результатах міжнародного дослідження TAGS, у якому Лансурф® порівняно з плацебо покращував загальну виживаність і виживаність без прогресування на 31 та 44% відповідно.
- У дослідженні II фази TASCO1 Лансурф® + бевацизумаб порівнювали з іншим фторпіримідином для перорального застосування – капецитабіном (також у комбінації з бевацизумабом) у 1-й лінії терапії пацієнтів з нерезектабельним мКРР, які були рефрактерними до стандартної хіміотерапії або не могли її отримувати. Виживаність без прогресування становила 9,23 міс у групі трифлуридину/типірацилу проти 7,82 міс у групі капецитабіну. Це відповідало зниженню ризику прогресування або смерті на 29% пр и лікуванні трифлуридином/типірацилом + бевацизумабом.
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (57), лютий 2019 р