2 квітня, 2019
GOLD‑2019: что нового?
Сегодня хроническое обструктивное заболевание легких (ХОЗЛ) занимает 4-е по значимости место в структуре причин смерти в мире и, по прогнозам, к 2020-му году поднимется на 3-е. Кроме того, вследствие постоянного воздействия факторов риска и старения населения социально-экономическая составляющая ХОЗЛ становится все более тяжелым бременем.
В 2001 г. Глобальная инициатива по ХОЗЛ (Global Initiative for Chronic Obstructive Lung Disease, GOLD) впервые представила стратегию диагностики, лечения и профилактики этого заболевания, которая в дальнейшем регулярно пересматривалась и обновлялась по мере публикации результатов новых клинических исследований. Так, в консенсусе 2015 года было добавлено положение по синдрому перекреста (оверлап-синдром) бронхиальной астмы и ХОЗЛ, подготовленное совместно научными комитетами GOLD и GINA.
Одним из преимуществ отчетов GOLD являются цели лечения: ослабление симптомов и уменьшение их воздействия на пациента; снижение риска обострений. Второе преимущество заключается в разработке простой, интуитивно понятной классификации тяжести ХОЗЛ, основанной на показателях объема форсированного выдоха за 1-ю секунду (ОФВ1) и системе стадирования, при которой тяжесть заболевания коррелирует со степенью ограничения воздушного потока. При этом необходимо отметить, что для некоторых пациентов ОФВ1 не служит надежным маркером тяжести одышки, снижения толерантности к физическим нагрузкам и ухудшения здоровья.
На момент составления первоначального отчета целью лечения было улучшение симптомов и состояния пациента. Предложенная GOLD оценка ХОЗЛ основывалась на симптоматике, риске обострений, степени ограничения воздушного потока, отклонениях значений спирометрии и выявлении сопутствующих заболеваний. Однако оценка симптомов не имела прямого отношения к менеджменту ХОЗЛ, а мониторинг состояния пациента был сложным процессом, в основном применявшимся в клинических исследованиях. Сегодня в рутинной клинической практике для мониторинга состояния пациента используются простые и надежные опросники, разработанные с учетом как оценки состояния пациента, так и факторов риска развития обострений, что позволяет применять новые подходы к менеджменту ХОЗЛ в любой клинической обстановке, а также сфокусироваться на индивидуальных потребностях пациента.
Предложенный в 2011 г. инструмент оценки ABCD стал значительным шагом вперед по сравнению с простой системой ранжирования, основанной на изменениях спирометрических данных, поскольку включил в себя многофакторный подход в менеджменте ХОЗЛ, учитывающий как бремя симптомов, так и важность профилактики обострений. Однако первоначальный вариант инструмента оценки ABCD не показал преимуществ относительно прогнозирования смертности или других исходов ХОЗЛ по сравнению с учетом спирометрических данных. Для решения этой проблемы (при одновременном сохранении простоты применения метода в клинической практике) в отчете‑2017 инструмент ABCD усовершенствован и отделен от спирометрической оценки состояния пациента; рекомендации по фармакотерапии основываются исключительно на симптомах, истории обострений, а также индивидуальных потребностях пациента. Такой пересмотр признает влияние ограничений ОФВ1 на выбор варианта терапии в менеджменте ХОЗЛ. При этом спирометрия остается ключевым методом диагностики и прогнозирования результатов при выборе нефармакологических методов лечения ХОЗЛ.
Версия 2019 года представляет собой Доклад рабочей группы GOLD и включает в себя пересмотр отчетов 2013-2018 гг., основанный на обновленных данных научной литературы, опубликованных после завершения работы над документом 2011 года, и сохраняет ту же парадигму лечения. Литература, включенная в обновленный консенсус, содержит дополнительные данные, полученные в ходе исследований по ведению ХОЗЛ, опубликованные с января 2017 по июль 2018 года.
Учитывая отзывы клиницистов, использующих рекомендации GOLD, научный комитет в отчете‑2019 предлагает последовательный и раздельный подход к менеджменту ХОЗЛ: начальная терапия основывается на ABCD-оценке, а последующая – на мониторинге состояния пациента и результатах фармакотерапии. Кроме того, в обновленном отчете вводится оценка количества эозинофилов периферической крови в качестве биомаркера эффективности ингаляционных кортикостероидов (ИКС) для предотвращения обострений.
Следует отметить, что рекомендации комитетов GOLD относительно использования любых препаратов основаны на лучших доказательствах из научных публикаций, а не на директивах регулирующих органов. В свою очередь, комитеты не дают рекомендаций относительно методов лечения, не одобренных хотя бы одним крупным регулирующим органом.
Основные изменения, внесенные в GOLD‑2019
В целом отчет GOLD‑2019 представляет собой пересмотр версии 2017 года, в который добавлены ключевые рецензируемые научные публикации за период с января 2017 по июль 2018 года.
Глава 1. Определение и обзор проблемы
Выявлены новые факторы, способствующие развитию ХОЗЛ в крупных популяциях.
Страница 11. В странах с низким социально-экономическим уровнем развития для приготовления пищи и обогрева традиционно используется органическое топливо (древесина, навоз животных, растительные остатки, уголь, другая биомасса), продукты горения которого способствуют сильному загрязнению воздуха в плохо вентилируемых помещениях. У женщин, постоянно занимающихся домашних хозяйством, воздействие продуктов горения биомассы является фактором высокого риска развития ХОЗЛ (Sana A. et al., 2018). Учитывая тот факт, что почти 3 млрд человек во всем мире используют биомассу и уголь в качестве основного источника энергии для бытовых нужд, риск развития у них ХОЗЛ очень велик.
Страница 12. Низкий социально-экономический статус в целом ассоциируется с повышенным риском ХОЗЛ; между бедностью и формированием ограничения воздушного потока установлена четкая взаимосвязь (Townend J. et al., 2017).
Страница 13. Систематический обзор 11 исследований, проведенный J.J. Bigna и соавт. (2018), продемонстрировал повышенный риск развития ХОЗЛ у пациентов с ВИЧ-инфекцией (95% ДИ 1,05-1,25).
Глава 2. Первичная оценка и диагностика
Несмотря на то что ХОЗЛ широко распространено во всем мире, в рутинной клинической практике все еще необходимы эффективные методы раннего выявления заболевания на уровне первичного звена медицинской помощи. У пациентов с недиагностированным ХОЗЛ симптомы, связанные с ограничением воздушного потока, обычно отсутствуют до тех пор, пока не разовьется значительное нарушение легочной функции. При этом обычные методы врачебного осмотра у бессимптомных пациентов имеют низкую чувствительность и специфичность. Скрининговая спирометрия, несмотря на свою неинвазивность и доступность, не может использоваться в качестве единственного диагностического теста в силу недостаточной специфичности и неоднозначности результатов, полученных в общей популяции.
Страница 29. Облегчить клиницистам выявление новых случаев ХОЗЛ может применение комплексной оценки рисков (шкала рисков), основанной на обычных данных электронных медицинских карт первичного звена (Haroon et al. 2017).
Страница 30. Ранее R.E. Jordan и соавт. (2016) установили, что в учреждениях первичного звена медицинской помощи эффективным способом выявления недиагностированных случаев данного заболевания является систематическая активная рассылка скрининговых анкет (целевое выявление пациентов с ХОЗЛ).
Глава 3. Фармакотерапия, профилактика обострений, поддерживающая терапия
Глава содержит общие данные о стратегиях ведения ХОЗЛ в отношении контроля симптомов и предупреждения обострений фармакологическими и нефармакологическими методами, основанными на доказательствах их эффективности и безопасности.
Страница 48. Систематический обзор с включением 12 рандомизированных исследований применения инъекционных поливалентных пневмококковых вакцин для защиты от внебольничной пневмонии пациентов с ХОЗЛ показал снижение вероятности обострений этого заболевания. Полученные данные были недостаточными для сравнения различных типов пневмококковых вакцин (Walters et al., 2017).
Комбинированные бронхолитики. Комбинации бронхолитических препаратов с различными механизмом и длительностью действия могут в большей степени усиливать бронходилатацию с меньшим риском развития побочных эффектов, чем увеличение дозы бронхолитика при монотерапии. Уровни доказательств эффективности применения комбинаций бронхолитиков представлены в таблице 1 (адаптированная таблица 3.4 главы 3).
Страница 53. В исследовании F.G. Martinez и соавт. (2017) было показано, что у пациентов с большей исходной симптоматической нагрузкой использование комбинации ДДАХП/ДДБА имело наибольший эффект в сравнении с плацебо и терапией отдельными компонентами комбинации. Также было показано, что снижение дозы комбинации ДДБА/ДДАХП и кратность приема 2 раза в день снижает симптомы и улучшает состояние пациентов с ХОЗЛ. Полученные результаты были подтверждены в различных популяциях Азии и Европы (Bai C. et al., 2017).
Страница 54. Большинство исследований, посвященных изучению комбинаций препаратов ДДБА/ДДАХП, проводились в группах пациентов с нечастыми обострениями. Исследование Wedzicha и соавт. (2013) продемонстрировало, что для предотвращения обострений комбинация бронхолитиков длительного действия более эффективна, чем монотерапия этими препаратами. Затем еще одно крупное исследование показало, что применение комбинации ДДБА/ДДАХП не настолько снижало частоту обострений, как это ожидалось по сравнению с монотерапией ДДАХП (Calverley et al., 2018). В свою очередь, исследование Wedzicha и соавт. (2014) продемонстрировало, что комбинация ДДБА/ДДАХП уменьшала обострения в большей степени, чем комбинация ИКС/ДДБА.
Другое недавнее исследование в популяции пациентов с высокой частотой обострений (≥2 обострения и/или ≥1 госпитализация в течение предыдущего года) показало, что при более высоких уровнях эозинофилии комбинация ИКС/ДДБА эффективнее по сравнению с комбинацией ДДБА/ДДАХП (Lipson et al., 2018). У пациентов с ХОЗЛ средней тяжести монотерапия флутиказона фуроатом или его комбинацией с вилантеролом ассоциировалась с более медленным снижением ОФВ1 (в среднем на 9 мл/ч) по сравнению с плацебо или монотерапией вилантеролом (Calverley et al., 2018).
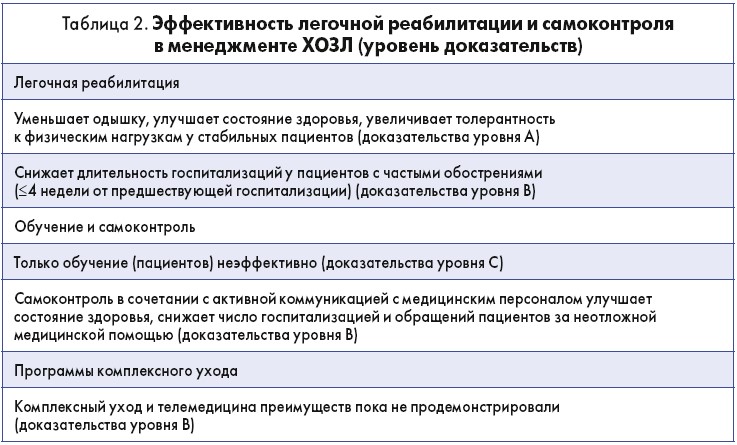
Обновлен раздел по легочной реабилитации и самоконтролю
Страница 63. Преимущества легочной реабилитации для пациентов с ХОЗЛ представлены в таблице 2 (адаптированная таблица 3.8 главы 3).
Недостаточная информированность пациентов и медперсонала ограничивает количество людей, которые могли бы воспользоваться преимуществами легочной реабилитации. Проблемой также является стимулирование пациентов к длительному повышению физической активности. Наряду с персонифицированным подходом снижение малоподвижного образа жизни и повышение двигательной активности у пациентов с умеренным и тяжелым течением ХОЗЛ показали многообещающие результаты (Coultas D.B. et al., 2018). Основным препятствием к достижению высоких результатов легочной реабилитации является то, что ее доступность ограничена географическим фактором, логистикой, культурными особенностями и финансовыми возможностями пациентов в разных странах. Одним из вариантов решения этих проблем могут быть различные дистанционные программы, если их частота и интенсивность эквивалентны программам, используемым в условиях стационара (Bourne S. et al., 2017).
Добавлен новый раздел о возможности использования оценки количества эозинофилов крови в качестве биомаркера эффективности ИКС
Страница 56. В ряде недавних исследований было показано, что уровень эозинофилии периферической крови может служить предиктором эффективности ИКС, используемых в качестве дополнительной терапии к базисному лечению бронхолитиками, для предотвращения обострений (Lipson D.A. et al., 2018; Bafadhel M. et al., 2018; Vestbo J. et al.,2017). Между количеством эозинофилов периферической крови и эффективностью ИКС существует прямая корреляция: возрастание эффекта ИКС при увеличении концентрации эозинофилов крови. Полученные в ходе исследования М. Bafadhel и соавт. (2018) данные показывают, что при концентрации эозинофилов периферической крови ≤100 клеток/мкл ИКС практически не оказывают эффекта, поэтому данное значение можно использовать как пороговое для выявления пациентов с низкой результативностью лечения этими препаратами.
Концентрация эозинофилов периферической крови ≥300 кл/мкл коррелирует с наибольшей эффективностью ИКС. Таким образом, подсчет количества эозинофилов периферической крови может служить биомаркером для оценки результативности применения ИКС, что (в сочетании с оценкой клинической ситуации) позволит принять решение относительно их использования в качестве дополнительной терапии или профилактики обострений ХОЗЛ. При этом механизм усиления ответа на ИКС при возрастании эозинофилии у пациентов с ХОЗЛ все еще остается невыясненным. Также пока нет достаточных данных относительно рутинного использования указанного биомаркера для индивидуального прогнозирования риска будущих обострений у пациентов.
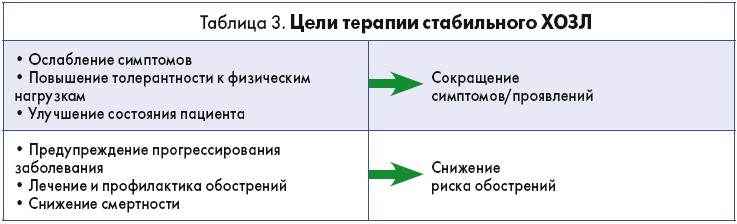
Глава 4. Менеджмент стабильного ХОЗЛ
Цели терапии ХОЗЛ со стабильным течением представлены в таблице 3.
Пересмотрены алгоритмы стартовой и поддерживающей фармакотерапии с учетом данных последних рандомизированных клинических исследований (РКИ), а также рекомендации GOLD по лечению групп A, B, C и D; также обновлены рекомендации относительно последующей фармакотерапии, в которой подчеркивается необходимость регулярной оценки, пересмотра и корректировки.
Страница 87. После установления диагноза ХОЗЛ эффективная терапия должна базироваться на индивидуальном подходе к оценке состояния пациента, целью которого является уменьшение текущих симптомов, а также снижение рисков обострений (алгоритмы персонифицированного подхода в соответствии с инструментом оценки ABCD подробно рассмотрены в главе 2).
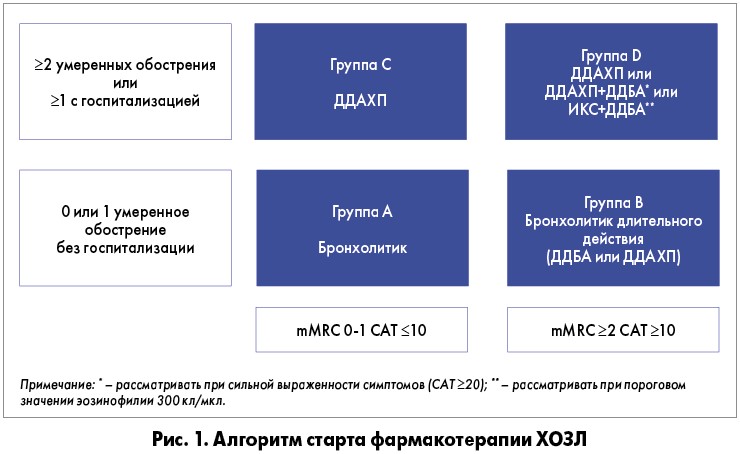
Страница 92. Модель инициации фармакотерапии ХОЗЛ в соответствии с инструментом индивидуальной оценки симптомов и риска обострений ABCD показана на рисунке 1 (адаптированный рис. 4.1 главы 4).
Страница 88. Текущий мониторинг состояния пациента также должен включать в себя оценку воздействия факторов риска, прогрессирования заболевания, эффективности фармакотерапии, возможное развитие побочных эффектов, истории обострений и сопутствующей патологии.
Страница 92. После начала лечения необходима повторная оценка соответствия состояния пациента целям фармакотерапии, выявления любых препятствий в их достижении и коррекции в случае необходимости.
Страница 93. Для последующей фармакотерапии предусмотрен отдельный алгоритм, по-прежнему основанный на оценке симптомов и истории обострений у пациента, при этом рекомендации не зависят от принадлежности к группе GOLD, установленной при диагностике ХОЗЛ (рис. 2).
Данный алгоритм предлагает стратегии эскалации/деэскалации терапии, базирующиеся на эффективности и безопасности. При эскалации в случае отсутствия клинической пользы и/или возникновения побочных эффектов терапия должна быть пересмотрена в сторону деэскалации.
Другие группы препаратов, использующихся при фармакотерапии ХОЗЛ, подробно рассмотрены в главах 3 и 4. Раздел нефармакологических методов лечения и раздел по интервенционной бронхоскопии и хирургии также обновлены и пересмотрены.
Глава 5. Менеджмент обострений
Страница 117. У некоторых пациентов при обострениях возможно применение небулизированного будесонида, который обеспечивает преимущества, аналогичные внутривенному введению метилпреднизолона, при этом выбор варианта терапии может зависеть от объема финансирования местных систем здравоохранения (Ding et al., 2016). Интенсивная комбинированная терапия ИКС/КДБА в течение 10 дней после начала острых респираторных инфекций ассоциируется с уменьшением обострений, особенно у пациентов с тяжелым течением ХОЗЛ (Stolz et al., 2018). В недавнем РКИ было показано, что в амбулаторных условиях добавление доксициклина к пероральному кортикостероиду не удлиняло время наступления следующего обострения (van Velzen et al., 2017).
Страница 119. В ходе небольшого пилотного РКИ (n=29) сообщалось, что оксигенотерапия в течение 6 нед через носовую канюлю с высоким давлением снижала гиперкапнию и улучшала качество жизни пациентов со стабильным течением ХОЗЛ и гиперкапнией (Nagata et al., 2018).
Страница 120. В случае улучшения состояния пациента и возможности самостоятельного дыхания в течение хотя бы 4 ч неинвазивную вентиляцию легких можно сразу же отменить без необходимости постепенного «отлучения» (Sellares et al., 2017).
Страница 121. Недавнее РКИ продемонстрировало, что телемониторинг не влияет на частоту обострений и госпитализаций у пациентов с ХОЗЛ (Walker et al., 2018).
Ключевые положения рекомендаций GOLD‑2019 по диагностике и лечению ХОЗЛ
Заподозрить ХОЗЛ и провести спирометрию необходимо в тех случаях, когда любой из нижеприведенных признаков присутствует у пациента ≥40 лет. Каждый из этих признаков сам по себе не является индикатором ХОЗЛ, однако их сочетание у пациента повышает вероятность диагноза этого заболевания:
- Одышка (стойкая, постоянно прогрессирует; усиливается во время физических нагрузок).
- Хронический кашель (может быть прерывистым, непродуктивным; рецидивирующий обструктивный синдром).
- Продуктивность кашля (любая продуктивность мокроты может свидетельствовать в пользу ХОЗЛ).
- Рецидивирующие инфекции нижних дыхательных путей.
- Анамнез факторов риска: генетические; врожденные аномалии/патология развития; курение (в том числе при помощи таких популярных устройств, как кальян и т.п.); воздействие бытового дыма (приготовление пищи, отопление жилья); промышленные поллютанты (производственная пыль, газы, испарения, другие химические вещества).
- Анамнез жизни / семейный анамнез ХОЗЛ (в том числе низкий вес пациента при рождении, наличие рецидивирующих респираторных инфекций в раннем детстве и т.п.).
Оценка ХОЗЛ
Целями оценки ХОЗЛ является определение степени тяжести ограничения воздушного потока, его влияния на состояние пациента и риск развития будущих неблагоприятных событий (обострения, госпитализация, смерть) и выбор адекватного варианта терапии. Для этого необходимо детально рассмотреть следующие аспекты заболевания у конкретного пациента:
- наличие и тяжесть отклонений спирометрии;
- текущий характер и масштабы выраженности симптомов;
- история умеренных и тяжелых обострений, вероятность их повторения в будущем;
- наличие сопутствующих заболеваний.
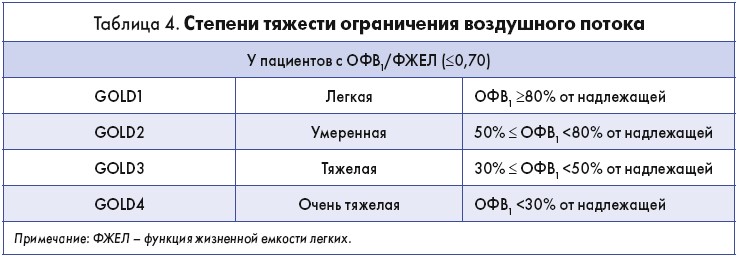
Классификация степени тяжести ограничения воздушного потока, основанная на постбронхолитическом ОФВ1, представлена в таблице 4.
Оценку состояния пациента, одышки, выраженности симптомов и риска развития обострений проводят при помощи простых опросников (mMRC и тест САТ).
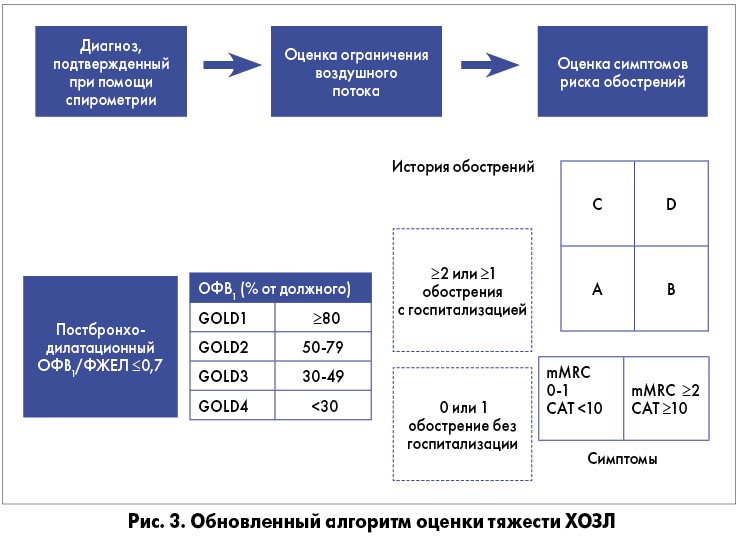
Комплексная оценка ХОЗЛ у отдельного пациента сочетает в себе оценку симптомов, степень тяжести ограничения воздушного потока и уровня спирометрических отклонений и/или риск развития обострений. Основные принципы оценки тяжести ХОЗЛ при помощи инструмента ABCD представлены на рисунке 3.
Фармакотерапия стабильного ХОЗЛ
Общие ключевые моменты:
- Фармакотерапия уменьшает симптомы, риск и тяжесть обострений, улучшает состояние здоровья и толерантность к физическим нагрузкам у пациентов с ХОЗЛ.
- Классы препаратов для лечения ХОЗЛ подробно описаны в главе 3. Выбор препаратов того или иного класса зависит от их доступности, предпочтений пациента и его ответа на терапию.
- Большинство препаратов применяется в виде ингаляторов, поэтому правильность выполнения техники ингаляции очень важна. Ключевые моменты применения ингаляционных и других препаратов для терапии ХОЗЛ приведены в таблицах 4.4-4.7 главы 4.
Для немедленного облегчения симптомов пациентам всех групп вначале могут применяться КДБА.
Группа А. Всем пациентам рекомендованы бронхолитики в зависимости от их влияния на одышку; это могут быть бронхолитики короткого и длительного действия. Подобное лечение можно продолжать, если отмечается положительное влияние на симптомы.
Группа В. При инициации терапии следует выбрать бронхолитик длительного действия. Ингаляционные бронхолитики длительного действия эффективнее, чем бронхолитики короткого действия, принимаемые по требованию. Для пациентов с тяжелой одышкой можно рассмотреть стартовую терапию двумя бронхолитиками. У пациентов указанной группы существует высокая вероятность коморбидных заболеваний, которые могут влиять на течение ХОЗЛ, что требует дополнительных обследований.
Группа С. Начальная терапия предполагает использование одного бронходилататора длительного действия. В сравнительных исследованиях было показано, что в отношении профилактики обострений ДДБА менее эффективны, чем ДДАХП (см. главу 3), поэтому для группы С рекомендовано начинать фармакотерапию с применения ДДАХП.
Группа D. Как правило, в качестве средства стартовой терапии применяют ДДАХП, которые эффективны как при одышке, так и при обострениях (см. главу 3).
Для пациентов с более тяжелым течением ХОЗЛ (САТ ≥20), особенно при наличии сильной одышки и/или ограничения физической активности, в качестве стартовой терапии можно рассматривать комбинацию ДДБА/ДДАХП. Эта рекомендация базируется на РКИ, в которых сообщения пациентов о результатах лечения являются первичной конечной точкой, а комбинации ДДБА/ДДАХП показали превосходные результаты по сравнению с монотерапией (см. главу 3).
К сожалению, формат данной статьи не позволяет представить все положения обновленного документа. Более детально с рекомендациями GOLD‑2019 можно ознакомиться в открытом доступе на официальном сайте Глобальной инициативы по хроническому обструктивному заболеванию легких: https://goldcopd.org/wp-content/uploads/2018/11/GOLD‑2019-v1.7-FINAL‑14Nov2018-WMS.pdf
Адаптированный перевод с англ. Наталии Поздняковой
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 1 (46), лютий 2019 р.