7 травня, 2019
Реферативний огляд рекомендацій 2018 року з клінічної практики в Канаді для профілактики та лікування цукрового діабету
Визначення та діагностичні критерії
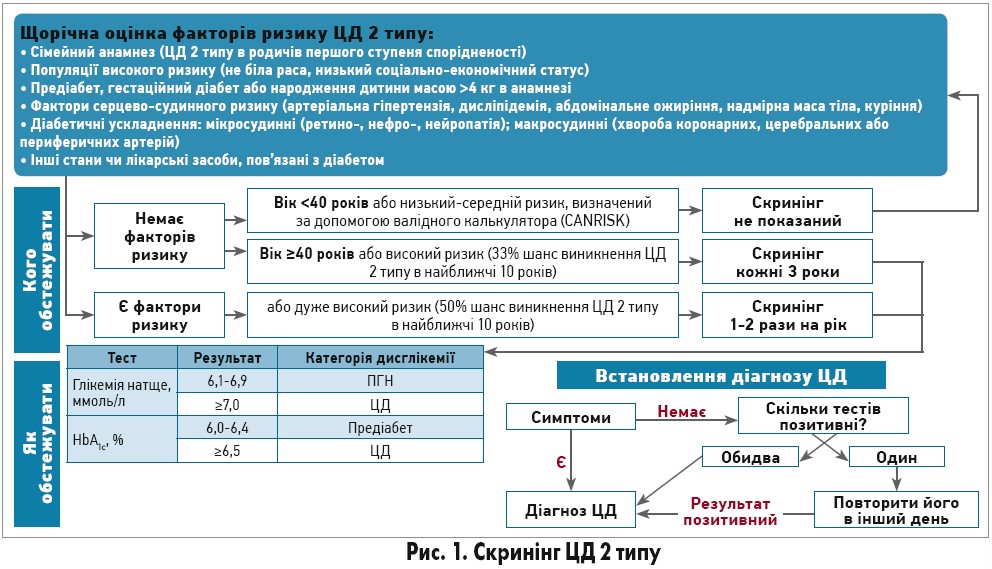
Цукровий діабет (ЦД) – це гетерогенний метаболічний розлад, який характеризується хронічною гіперглікемією внаслідок порушення секреції, дефектної дії інсуліну чи їх поєднання. Діабетична гіперглікемія зумовлює специфічні довгострокові мікросудинні ускладнення з боку очей, нирок і нервів та підвищує ризик серцево-судинних захворювань (ССЗ). Діагноз встановлюється за будь-яким із критеріїв (табл. 1), оскільки всі вони пов’язані з мікроангіопатіями, насамперед із ретинопатією. За відсутності симптомів гіперглікемії одноразове виявлення результату лабораторного тесту в діабетичному діапазоні потребує його повторення (рис. 2); якщо підвищена випадкова глікемія, то для встановлення діагнозу ЦД потрібно визначити глікемію натще чи глікований гемоглобін (HbА1с).
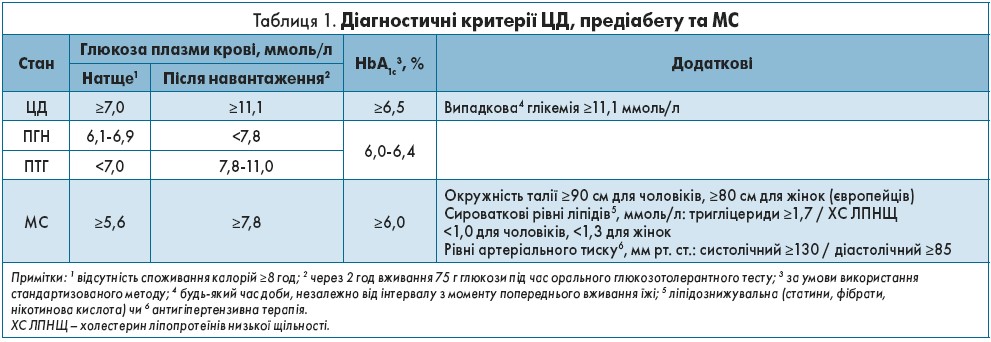
Предіабет пов’язаний із високим ризиком виникнення ЦД та його ускладнень і включає такі стани: порушення глікемії натще (ПГН), порушення толерантності до глюкози (ПТГ), показники HbA1c в межах 6,0-6,4% (табл. 1).
Метаболічний синдром (МС) – поширене багатокомпонентне порушення, що включає різноманітні поєднання предіабету чи діабету з абдомінальним ожирінням, артеріальною гіпертензією, дисліпідемією й істотно підвищує ризик ССЗ. Встановлення діагнозу потребує наявності ≥3 критеріїв (табл. 1). За відсутності ЦД 2 типу в осіб із МС істотно підвищений ризик його виникнення. Пацієнти з МС потребують агресивнішої терапії та контролю факторів ризику для уникнення ССЗ і зниження смертності.
Класифікація
Більшість випадків діабету відносять до 1 чи 2 типу, хоча іноді їх важко класифікувати. Окремо виділяють гестаційний діабет і рідкісні форми, пов’язані з генетичними мутаціями, хворобами підшлункової залози, лікарськими впливами тощо.
Моногенний ЦД – рідкісний сімейний розлад з аутосомно-домінантним успадкуванням, спричинений генетичними дефектами функції β-клітин, що переважає в молодих людей (<25 років) і не залежить від інсуліну. Треба диференціювати різні форми ЦД, хоча іноді це проблематично, оскільки клініко-діагностичні критерії неспецифічні. При атипових проявах доцільно проводити додаткове тестування, якщо конкретизація діагнозу вплине на тактику ведення пацієнта. Важливою моногенною формою є діабет новонароджених, який зазвичай проявляється у віці ≤6 міс, клінічно не відрізняється від ЦД 1 типу, але піддається терапії препаратами сульфонілсечовини. Тому генетичне тестування показане всім дітям цієї категорії, а також хворим із діагнозом ЦД 1 типу без ожиріння, котрі почали хворіти з періоду новонародженості чи мають обтяжений спадковий анамнез щодо ЦД у кількох поколіннях.
Скринінг
Оскільки можливість запобігти чи відтермінувати початок ЦД 1 типу не доведена, рутинний скринінг цієї хвороби не проводиться. Скринінг ЦД 2 типу показано на рисунку 1. У зв’язку з високим ризиком особливої уваги заслуговують такі прояви інсулінорезистентності: предіабет, зниження рівня ХС ліпопротеїнів високої щільності та/або гіпертригліцеридемія, артеріальна гіпертензія, абдомінальне ожиріння, надмірна маса тіла, acanthosis nigricans, синдром полікістозних яєчників, гіперурикемія/подагра, неалкогольний стеатогепатит. Ризик ЦД перевищує загальнопопуляційний рівень у таких категорій пацієнтів: а) з біполярними розладами, депресією, шизофренією – втричі; б) ВІЛ‑інфіковані, особливо за умови застосування високоактивної антиретровірусної терапії – в 1,5-4 рази; в) з обструктивним апное уві сні – коефіцієнт ризику 1,43.
Первинна профілактика
Оскільки безпечна й ефективна профілактика ЦД 1 типу поки що не визначена, будь-які превентивні заходи не мають виходити за рамки офіційних протоколів.
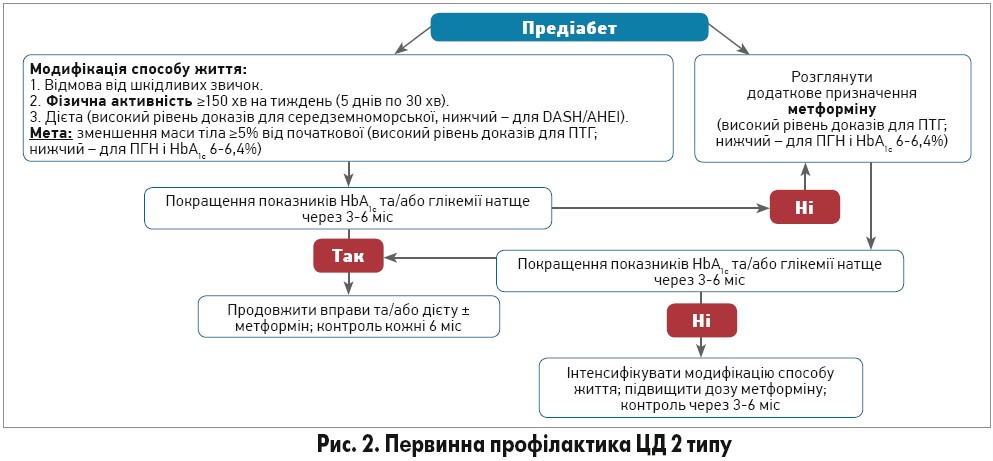
Інтенсивна та структурована модифікація способу життя (рис. 2), яка супроводжується втратою ≥5% початкової маси тіла, знижує ризик трансформації предіабету в ЦД 2 типу на 60%. За умови раннього початку ефект може тривати >20 років. Пацієнтам із високим ризиком рекомендовано такі варіанти дієти: середземноморська, DASH, AHEI. Метформін знижує ризик ЦД на ≈30%, причому позитивний ефект зберігається навіть через 10 років після припинення терапії. Первинна профілактика ЦД 2 типу суттєво знижує частоту ССЗ, ниркової недостатності, сліпоти й передчасної смерті (від усіх причин – на 6,2%, від ССЗ – на 9%).
Цілі та моніторинг глікемічного контролю
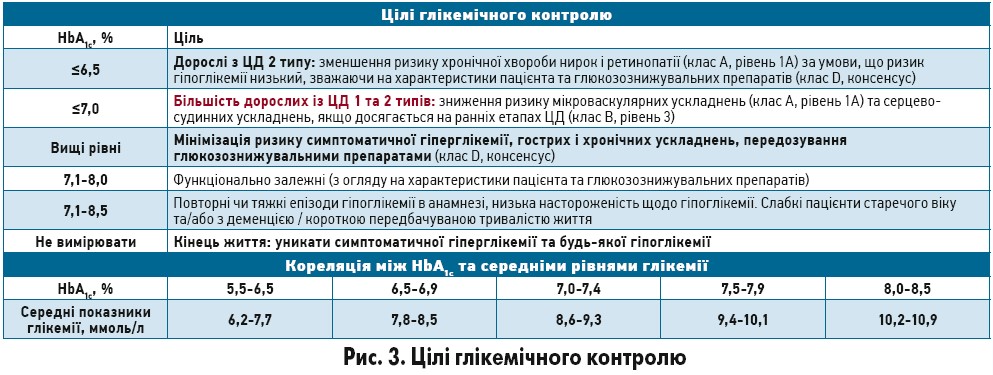
Оптимальний глікемічний контроль – це фундаментальний принцип ведення ЦД. Із ризиком ускладнень пов’язані як глікемія натще, так і постпрандіальна, тому найкращим критерієм оцінки вважається HbА1с. Цільові рівні глікемії (ЦРГ) бажано індивідуалізувати, зважаючи на загальний стан пацієнта, функціональну залежність і ймовірну тривалість життя (рис. 3). Зниження рівнів HbА1с ≤7,0% потребує досягнення таких рівнів глікемії: натще чи препрандіальна – 4,0-7,0 ммоль/л; 2-годинна постпрандіальна – 5,0-10,0 ммоль/л. Якщо за таких рівнів глікемії цільове значення HbA1c не досягнуто, можна розглядати подальше зниження глікемії натще до 4,0-5,5 ммоль/л, постпрандіальної – до 5,0-8,0 ммоль/л за умови низького ризику розвитку гіпоглікемії.
Рівень HbA1c відображає тривале глікемічне навантаження (8-12 тиж), тому є ідеальним критерієм оцінки ефективності антигіперглікемічної терапії (АГТ). Для контролю досягнення чи підтримки ЦРГ рекомендовано визначати HbА1с кожні 3 міс, а за певних обставин (значні зміни АГТ, вагітність) – частіше. Після досягнення ЦРГ у стабільні періоди лікування та здорового способу життя контроль HbА1с можна здійснювати двічі на рік.
Самоконтроль рівнів глікемії (СРГ), блискавичний/тривалий моніторинг глюкози (БМГ/ТМГ) використовують як допоміжні методи оцінки ефекту АГТ, а також для виявлення й запобігання гіпоглікемії. Ці показники включені до структурованої навчально-терапевтичної програми покращення якості глікемічного контролю.
Пацієнти, котрі використовують інсулін >1 раз на добу, обов’язково мають здійснювати СРГ щонайменше 3 рази на добу з визначенням пре- та постпрандіальних показників. Хворим на ЦД 2 типу, що використовують інсулін 1 раз на добу в комбінації з іншою АГТ, рекомендовано здійснювати СРГ хоча б 1 раз на добу в різні періоди часу. Якщо пацієнт не використовує інсулін, частота СРГ визначається індивідуально залежно від класів АГТ, глікемічного контролю та ризику гіпоглікемії. За відсутності адекватного глікемічного контролю треба обов’язково розпочати СРГ (пре- та постпрандіальної) й навчити пацієнта чи опікуна, як змінювати спосіб життя й АГТ залежно від отриманих результатів. Після досягнення ЦРГ та при застосуванні АГТ, що не пов’язана з ризиком гіпоглікемії, СРГ здійснюють рідше. Частоту визначень рекомендовано збільшувати ситуативно, коли цього потребують обставини. Точність показників глюкометра потрібно перевіряти, порівнюючи показник глікемії натще з лабораторним показником з того самого зразка крові принаймні раз на рік, а також тоді, коли рівні HbA1c не відповідають показникам глюкометра (рис. 3).
Проведення ТМГ рекомендовано для досягнення адекватного глікемічного контролю та зменшення тривалості гіпоглікемії у хворих на ЦД 1 типу, особливо якщо вони використовують тривалі підшкірні інфузії інсуліну (ТПІІ), а БМГ – для зменшення тривалості епізодів гіпоглікемії.
Хворим на ЦД 1 типу потрібно провести інструктаж із визначення кетонів у крові та сечі; тест виконують у таких випадках: періоди гострих захворювань, які супроводжуються гіперглікемією; препрандіальна глікемія >14,0 ммоль/л; наявність симптомів діабетичного кетоацидозу (див. нижче); краще визначати кетони в крові, а не в сечі, оскільки це дає можливість раніше виявити кетоз і швидше оцінити відповідь на терапію.
Антиглікемічна терапія в дорослих
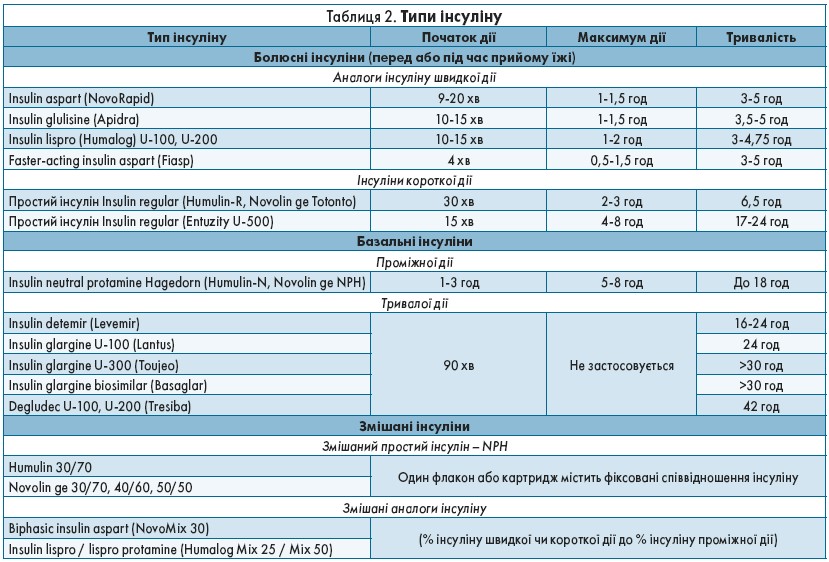
У разі ЦД 1 типу застосовують різні типи інсуліну (табл. 2). Для досягнення ЦРГ використовують ТПІІ чи базально-болюсну ін’єкційну терапію (ББІТ).
Замість простого інсуліну рекомендовано використовувати аналоги інсуліну короткої дії для покращення HbA1c та мінімізації ризику гіпоглікемій (вищий рівень доказів для ТПІІ з lispro й aspart, нижчий – для ТПІІ з glulisine), а також для досягнення постпрандіальних ЦРГ. Пацієнтам, які використовують ТПІІ + ТМГ і мають епізоди нічної гіпоглікемії, можна рекомендувати помпи з підсиленим сенсором.
При використанні ББІТ замість змішаного простого інсуліну (NPH) рекомендовано застосовувати аналоги інсуліну тривалої дії для зниження ризику гіпоглікемії (вищий рівень доказів для detemir, glargine U‑100, нижчий – для degludec, glargine U‑300); у разі схильності до нічної гіпоглікемії краще призначати degludec. Пацієнтам, які не досягають ЦРГ, для покращення показників HbА1с можна призначити ТПІІ. Поєднання ТПІІ з ТМГ або СРГ покращує якість життя, прихильність до терапії та має сприятливі наслідки для здоров’я. Пацієнтам, які використовують ТПІІ, треба періодично проводити обстеження для визначення доречності продовження ТПІІ.
Усіх пацієнтів та опікунів треба проінформувати про ризик і шляхи запобігання гіпоглікемії, визначити й обговорити фактори ризику тяжкої гіпоглікемії. У пацієнтів, які не знають про гіпоглікемії, для зниження ризику можна використовувати такі нефармакологічні стратегії: стандартизовану освітню програму, спрямовану на суворе уникнення гіпоглікемії при збереженні загального глікемічного контролю; частіше проведення СРГ, у тому числі в нічний час; ТМГ із високочутливим сенсором при використанні ТПІІ; менш жорсткі ЦРГ до 3 міс.
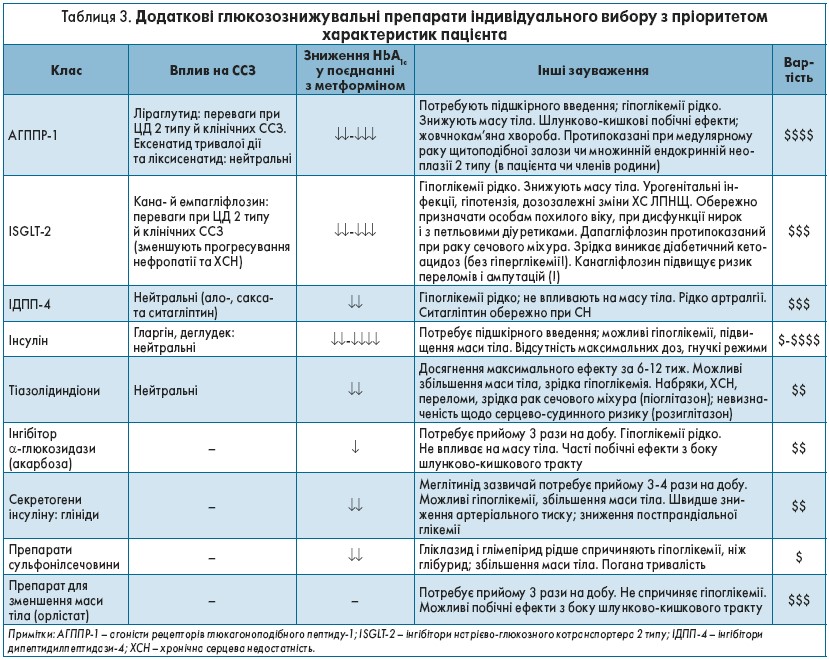
У разі ЦД 2 типу застосовують різні класи глюкозознижувальних препаратів (табл. 3), за потреби – інсулін.
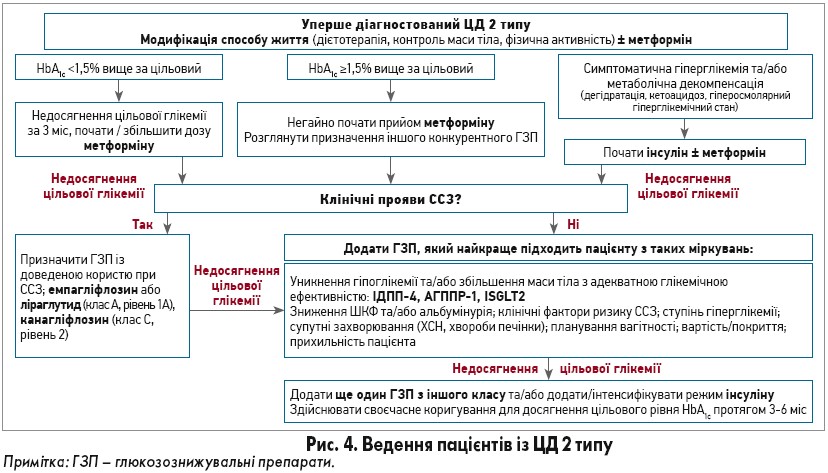
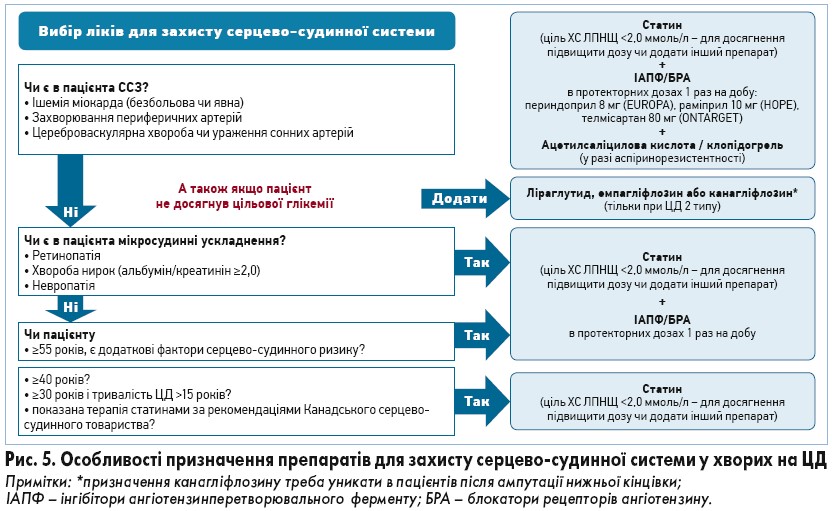
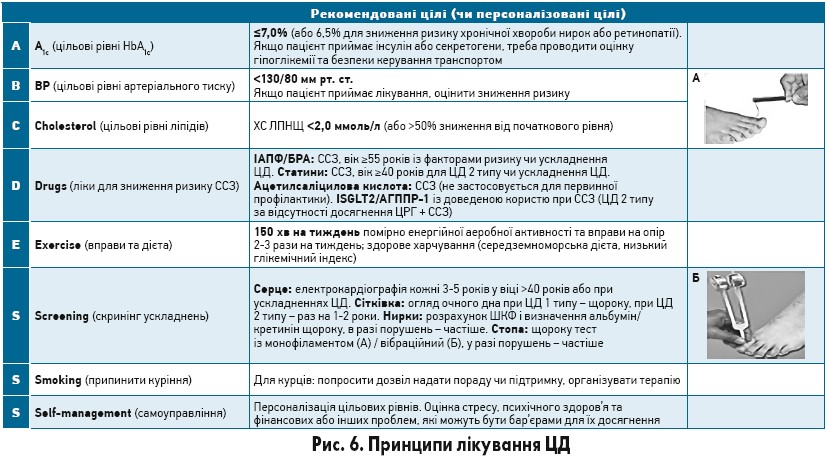
Алгоритм ведення пацієнта з уперше виявленим ЦД 2 типу підсумовано на рисунку 4. У хворих на ЦД часто виникає нефропатія (діабетична/гіпертензивна), котра спричиняє зниження швидкості клубочкової фільтрації (ШКФ) і хронічну хворобу нирок, на що слід зважати в разі призначення АГТ. Важливо також призначати препарати для захисту серцево-судинної системи (рис. 5). Основні принципи лікування ЦД підсумовано на рисунку 6.
Гострі ускладнення ЦД та їх ведення в дорослих
Гіпоглікемія визначається за такими критеріями: 1) поява автономних (тремор, серцебиття, пітливість, тривога, голод, нудота, парестезії, затерпання) та нейроглікопенічних симптомів (слабкість, сонливість, запаморочення, порушення концентрації, мови, зору та притомності); 2) низька концентрація глюкози в крові (<4,0 ммоль/л для людей, які приймають інсулін і секретогени); 3) покращення симптомів після призначення вуглеводів. Тяжкість гіпоглікемії визначається за клінічними проявами. Це найчастіше ускладнення при ЦД 1 типу, дещо рідше виникає в інсулінозалежних хворих на ЦД 2 типу чи в тих, які лікуються секретогенами.
При легкій-середній гіпоглікемії призначають 15 г вуглеводів перорально, краще у вигляді глюкози чи сахарози в таблетках, розчинах (вода, апельсиновий сік) або глюкозному гелі; якщо через 15 хв рівень глікемії <4,0 ммоль/л – терапію повторюють. При тяжкій гіпоглікемії в дорослих зі збереженою свідомістю застосовують 20 г вуглеводів у вигляді таблеток глюкози чи їх еквівалентів; якщо через 15 хв рівень глікемії <4,0 ммоль/л – уживають 15 г глюкози. Якщо пацієнт непритомний без доступу до вени, вводять 1 мг глюкагону підшкірно чи внутрішньом’язово; якщо є доступ до вени – 10-25 г глюкози струминно (20-50 мл 50% розчину декстрози); особи, що надають допомогу, мають якнайшвидше викликати швидку допомогу.
Після ліквідації гіпоглікемії пацієнт має дотримуватися звичного режиму харчування, щоб запобігти рецидиву. Якщо їжа недоступна >1 год, необхідно перекусити (15 г вуглеводів і джерело білка). Особи, котрі наглядають за хворими на діабет із високим ризиком тяжкої гіпоглікемії, мають навчитися вводити глюкагон.
Гіперглікемічні порушення. Діабетичний кетоацидоз (ДКА) та гіперосмолярний гіперглікемічний стан (ГГС) – невідкладні стани у хворих на ЦД, які мають багато спільних ознак і потребують госпіталізації у відділення інтенсивної терапії. При ДКА основним порушенням є кетоацидоз, у разі ГГС – гіперосмолярність і суттєве зменшення об’єму позаклітинної рідини.
За умови підозри на ДКА (симптоми, глікемія >14,0 ммоль/л, ЦД 1 типу) треба виміряти β-гідроксибутират у капілярній крові в амбулаторних умовах або в стаціонарі; значення >1,5 ммоль/л потребує подальшого обстеження на ДКА. Відсутність кетонів у сечі не виключає ДКА. У разі появи симптомів ДКА в пацієнтів, які лікуються ISGLT2, треба провести ретельне тестування навіть за умови, що рівні глікемії не дуже високі.
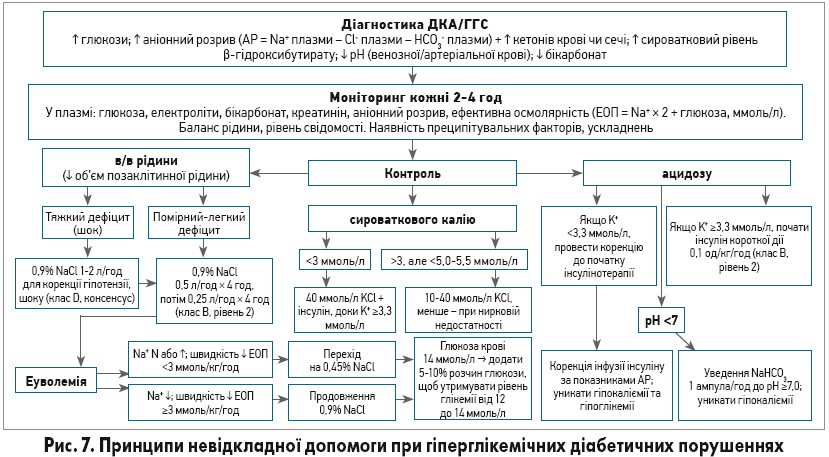
Лікування ДКА/ГГС передбачає: введення рідини, корекцію гіпокаліємії, введення інсуліну, уникнення швидкого зниження осмолярності та пошук причин виникнення. Введення рідини (0,9% NaCl) пацієнтам із ДКА чітко дозоване (рис. 7), тоді як при ГГС швидкість інфузії рекомендують визначати індивідуально. Початкову швидкість інфузії інсуліну (0,1 од/кг/год) треба підтримувати до зникнення кетозу, критерієм якого є нормалізація аніонного розриву; коли рівень глікемії зменшиться до 14,0 ммоль/л, в інфузійну суміш потрібно додати глюкозу для уникнення гіпоглікемії.
Підготувала Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 7 (452), квітень 2019 р