23 липня, 2019
Персоналізована антиангінальна терапія: роль ранолазину
 Чинні міжнародні та вітчизняні рекомендації визначають оптимальну медикаментозну терапію стабільної ішемічної хвороби серця (ІХС) як поєднання антиангінальних засобів (≥1) та препаратів для запобігання кардіоваскулярним (КВ) ускладненням. Така терапія передбачає призначення:
Чинні міжнародні та вітчизняні рекомендації визначають оптимальну медикаментозну терапію стабільної ішемічної хвороби серця (ІХС) як поєднання антиангінальних засобів (≥1) та препаратів для запобігання кардіоваскулярним (КВ) ускладненням. Така терапія передбачає призначення:
- швидкодіючих нітратів для купірування і ситуативної профілактики стенокардії;
- антиангінальних препаратів (1-ї та 2-ї лінії) – для попередження нападів та покращення якості життя;
- антитромбоцитарних — ацетилсаліцилової кислоти та гіполіпідемічних засобів (статинів) – для покращення прогнозу пацієнтів.
Наявність супутніх артеріальної гіпертензії (АГ), серцевої недостатності (СН), цукрового діабету (ЦД) чи хронічного захворювання нирок є показанням для призначення інгібіторів ангіотензинперетворюючого ферменту, вони також є прогноз-модифікуючими складовими лікування [1].
Разом із тим призначення антиангінальної терапії конкретному хворому нерідко є складною задачею для практикуючого лікаря. Наприклад, за даними Австралійського реєстру CADENCE, у 48% пацієнтів, які нібито «оптимально контролювали» симптоматику, залишалися напади стенокардії (>1 на тиждень), а 37% із них відзначали больові епізоди майже щодня. У цьому дослідженні брали участь переважно типові пацієнти з амбулаторного прийому кардіолога; хворі похилого віку (у середньому 71 рік); майже кожен другий – після черезшкірного коронарного втручання (ЧКВ) [2].
Важливе питання стосується реальної оцінки клінічних проявів ІХС з боку спеціалістів-медиків. Так, результати обсерваційного дослідження APPEAR (Angina Prevalence and Provider Evaluation of Angina Relief) засвідчили, що наявність стенокардії лікарі часто недооцінюють. Це стосується приблизно 40% пацієнтів, більшості з яких до початку спостереження встигли виконати реваскуляризацію міокарда (57%) [3]. Загалом, за даними клінічних випробувань, існуючих реєстрів та метааналізів, приблизно у третини хворих зберігаються напади стенокардії незважаючи на проведення реваскуляризації міокарда. У 25% пацієнтів повернення ангінального болю спостерігається приблизно через 5 років після ЧКВ [4]. Серед осіб із супутнім ЦД більше половини скаржаться на відновлення нападів уже до кінця першого року після ендоваскулярних чи хірургічних втручань. За нашими даними, клінічні (больовий синдром) чи електрокардіографічні (ЕКГ) (депресія сегмента ST під час навантажувальних проб) ознаки ішемії міокарда виявлялись у 9% пацієнтів у разі повної і у 14% – неповної реваскуляризації міокарда через місяць після стентування. Через рік відповідні показники становили 11% у випадках із повною реваскуляризацією міокарда та 14% – неповною.
Тобто ендоваскулярні та хірургічні методи реваскуляризації – ЧКВ чи аорто-коронарне шунтування (АКШ) – не завжди гарантують пацієнтам зі стабільною ІХС повну ліквідацію клінічної симптоматики. У нещодавно завершеному дослідженні BRIDGE (StaBle Angina: PeRceptIon of NeeDs, Quality of Life and ManaGemEnt of Patients) хворі, які пройшли ЧКВ за порадою лікарів, відзначали повторну появу симптомів протягом року [5]. Подібні результати були отримані у першому, плацебо-контрольованому за даними ЧКВ, дослідженні ORBITA (Objective Randomized Blinded Investigation with optimal medical Therapy of Angioplasty in stable angina), яке продемонструвало відсутність переваг ендоваскулярного втручання перед медикаментозним лікуванням щодо симптоматики стенокардії та підвищення толерантності до фізичних навантажень [6]. Міжнародні експерти пов’язують подібні факти з тим, що не у всіх випадках за допомогою стентування можна досягти повної анатомічної реваскуляризації міокарда, а отже, пацієнти і надалі потребують фармакотерапії [7].
Традиційна трійка препаратів 1-го ряду – β-адреноблокатори (ББ), блокатори кальцієвих каналів (БКК), швидкодіючі нітрати – характеризується беззаперечною антиангінальною ефективністю. Ці медикаменти доступні для більшості пацієнтів і в усьому світі мають прийнятну аптечну ціну. Проте, незважаючи на великий історичний та практичний досвід використання, усі вони не вивчалися системно у форматі сучасної доказової медицини, що періодично спричиняє серйозні дискусії про їхній особливий «першорядний» статус для хворого на стабільну ІХС. Виключенням можуть бути хіба що швидкодіючі нітрати, які не мають альтернативи для симптоматичного купірування ангінальних нападів. Деякі препарати (зокрема, ранолазин), які сьогодні належать до 2-го ряду, мають більшу і набагато сучаснішу науково-доказову базу щодо лікування стенокардії. Разом із тим для всіх, без винятку, існуючих антиангінальних засобів – як 1-го так і 2-го ряду, немає переконливих доказів щодо впливу на прогноз захворювання і можливості запобігання КВ-ускладненням.
Багатьом пацієнтам для контролю клінічних симптомів доводиться призначати комбіноване лікування двома та більше препаратами. Доказова база стосовно комбінованої антиангінальної терапії містить ще менше даних, існуючі рекомендації не дають чітких інструкцій щодо вибору оптимальних поєднань різних класів медикаментів. Як результат — не завжди враховуються патофізіологія захворювання конкретного пацієнта, взаємодія відповідних засобів, вплив супутньої патології тощо.
Певні складнощі у зв’язку з недостатньою ефективністю стандартної терапії виникають у пацієнтів з особливими формами стенокардії. Наприклад, при вазоспастичній стенокардії ББ протипоказані, а ефективні дози БКК значно перевищують звичайні та потребують відповідального спостереження з боку лікарів після їхнього призначення. Традиційна терапія часто не забезпечує адекватного контролю симптомів при мікроваскулярній стенокардії. Разом із тим ця форма, за даними деяких авторів, зустрічається приблизно в 40% випадків стабільної стенокардії, переважно у жінок на тлі інтактних або малозмінених коронарних артерій (КА). Рефрактерна стенокардія визначається як хронічний стан, спричинений клінічно підтвердженою рекурентною ішемією міокарда (за наявності ураження КА), який не піддається адекватному контролю незважаючи на поєднання медикаментозної терапії, ангіопластики (ЧКВ) чи АКШ. При цьому, за наявними даними, прогноз таких хворих мало відрізняється від популяційного щодо стабільної ІХС. Тому, як зазначив Ranil dе Silva на Європейському конгресі кардіологів (2015), зусилля стосовно лікування рефрактерної стенокардії варто спрямувати на усунення клінічної симптоматики та поліпшення якості життя пацієнтів. Проте нині для цієї форми стенокардії немає чітко визначених стандартів лікування. Наявні немедикаментозні заходи (enhanced external counterpulsation – підсилена зовнішня контрапульсація; transcutaneous electrical nervestimulation – черезшкірна електрична нейростимуляція; spinal cord stimulation – стимуляція спинного мозку) використовувались в одиничних невеликих дослідженнях, а отже, їхня терапевтична ефективність потребує додаткового вивчення і підтвердження. Міжнародні експерти рекомендують не відмовлятись у таких хворих від підбору ефективного медикаментозного лікування і, за показаннями, – від повторних реваскуляризаційних процедур.
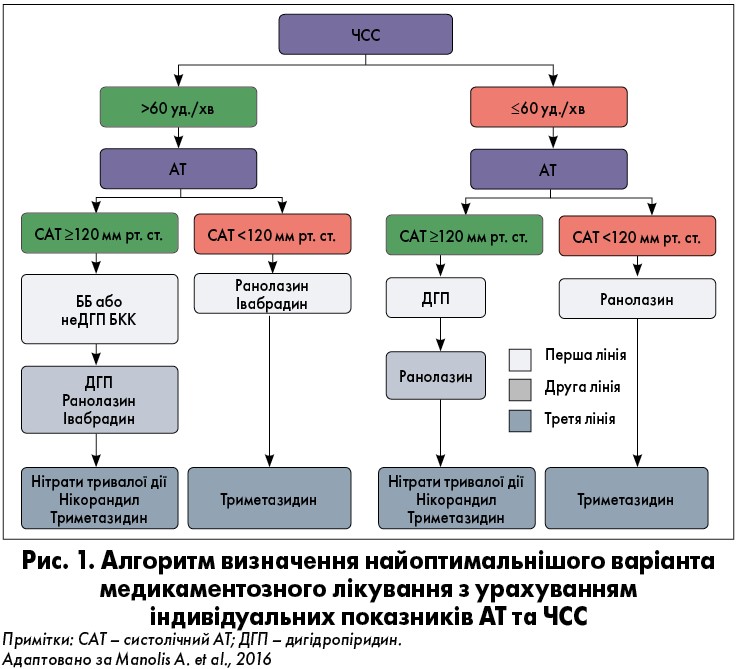
Актуальність питання щодо персоналізації лікування стабільної стенокардії навіть спонукала експертів-кардіологів розробити новий підхід, що полягає у визначенні найоптимальнішого варіанта медикаментозної терапії для кожного пацієнта з урахуванням індивідуальних потреб та особливостей, патофізіологічних механізмів захворювання, показників артеріального тиску (АТ) та частоти серцевих скорочень (ЧСС), незалежно від ряду, до якого належить обраний антиангінальний препарат (рис. 1) [7].
З огляду на запропонований підхід, у деяких складних клінічних випадках першочерговим вибором для лікування стенокардії може стати препарат ранолазин. Він є першим представником блокаторів пізніх натрієвих каналів. Цей лікарський засіб був запатентований ще 1986 р., але спочатку використовувався у невеликих дозах (по 90, 180, 360 мг/добу), які виявилися недостатньо дієвими для профілактики стенокардії. Після визначення сучасних терапевтичних дозувань із 2006 р. ранолазин схвалений для клінічного використання у США, а з 2008 р. – у Європі. За даними 2018 р., ранолазин увійшов у топ‑10 серцево-судинних препаратів, що найбільше продавалися у світі. Він затверджений для терапії стабільної стенокардії Управлінням із контролю за якістю харчових продуктів та препаратів США (FDA), для симптоматичного лікування пацієнтів із хронічною стабільною стенокардією, резистентною стосовно іншої терапії, Європейським агентством із лікарських засобів (ЕМА). Рекомендовані нині дози ранолазину становлять 500 чи 1000 мг двічі на день, лікарська форма – з уповільненим вивільненням.
Фармакологічні характеристики, механізм дії ранолазину
Точний механізм дії ранолазину до кінця не визначений, проте відомо, що він сприяє окисненню глюкози, стимулюючи анаеробний метаболізм в умовах ішемії. Завдяки цьому механізму спочатку препарат відносили до метаболічних засобів, що модулюють енергетичний обмін в ішемізованих кардіоміоцитах за рахунок активації процесів окиснення глюкози. Пізніше було показано, що він дозозалежно пригнічує пізній потік іонів натрію у клітини міокарда, знижує їхню внутрішньоклітинну концентрацію і, відповідно, запобігає надлишковому натрій-залежному накопиченню іонів кальцію та пов’язаним із ним негативним наслідкам для міокарда [9, 10]. Вважається, що саме цей механізм під час ішемії зменшує внутрішньоклітинний іонний дисбаланс і забезпечує оптимальне діастолічне розслаблення міокарда. Зменшення напруження у період діастоли сприяє покращенню перфузії міокарда, включно з ішемізованими зонами, що, ймовірно, забезпечує антиангінальний/антиішемічний ефект препарату. Є клінічні свідчення позитивного впливу ранолазину на ендотеліальну функцію пацієнтів зі стабільною ІХС. Так, призначення препарату в дозі 2000 мг/добу сприяло збільшенню ендотеліальної вазодилатації під час проби з реактивною гіперемією на плечовій артерії [11]. Використання ранолазину асоціювалось із меншими значеннями маркерів запалення, показниками С-реактивного білка і симетричного диметиларгініну.
Препарат здатний дозозалежно подовжувати інтервал QT, що потребує відповідного лікарського контролю. Зазначені зміни ЕКГ були найбільшими у хворих з печінковою недостатністю. Крім того, на тлі прийому препарату в деяких випадках спостерігалися зниження амплітуди та двогорбість зубця Т. Вважається, що цей вплив зумовлений блокадою не тільки пізнього натрієвого потоку (скорочує шлуночковий потенціал дії), але й швидкого ректифікаційного калієвого току (подовжує шлуночковий потенціал дії).
Після перорального прийому ранолазину в формі пролонгованої дії максимальна концентрація препарату реєструється у плазмі крові через 2-6 годин. Вживання їжі не впливає на швидкість і повноту всмоктування засобу. Період напіввиведення ранолазину після перорального прийому становить приблизно 7 годин. Препарат майже повністю метаболізується за допомогою печінкових цитохромів (переважно CYP 3А4, меншою мірою CYP 2D6) з утворенням великої кількості метаболітів, з яких до 70% елімінуються нирковим шляхом, близько 25% – через шлунково-кишковий тракт. Слід зауважити, що ранолазин є достатньо потужним інгібітором глікопротеїну-Р і слабким інгібітором CYP 3А4, CYP 2D6 та CYP 2В6, що слід враховувати, призначаючи його разом з іншими лікарськими засобами. Фармакокінетика ранолазину не залежить від статі та віку хворих. У пацієнтів із низькою вагою, застійною СН, середньої тяжкості / тяжкою нирковою та печінковою недостатністю концентрація препарату підвищується, що вимагає певної обережності щодо його застосування.
Антиангінальна ефективність ранолазину
Систематичний огляд рандомізованих клінічних досліджень (РКД), дані цілого ряду невеликих робіт і кокранівський метааналіз показали, що ранолазин у дозах 1000-2000 мг/добу ефективно полегшує симптоми стабільної стенокардії, підвищує толерантність до фізичних навантажень, зменшує прояви безбольової ішемії міокарда. Антиангінальна ефективність ранолазину є аналогічною дії інших лікарських засобів, рекомендованих при стенокардії [10]. Препарат суттєво не впливає на основні гемодинамічні показники, АТ і ЧСС, а також внутрішньосерцеву провідність і скоротливу функцію міокарда. Зазначені особливості дозволяють використовувати його у широкого загалу пацієнтів за наявності гіпотензії, брадикардії, при порушеннях серцевого ритму та провідності. Препарат також можна призначати хворим із супутньою патологією, зокрема хронічним обструктивним захворюванням легень тощо. У чинних рекомендаціях з лікування стабільної коронарної хвороби Європейського товариства кардіологів (ESC, 2013) та Американської асоціації серця (AHA, 2012) ранолазин визначений як антиангінальний засіб ІІа класу.
У рандомізованих дослідженнях (MARISA, ERICA, CARISA) доведено антиангінальну ефективність ранолазину у хворих на ІХС, яку оцінювали за збільшенням толерантності до фізичних навантажень, зменшенням кількості нападів стенокардії та потреби у нітрогліцерині (НГ). Призначення препарату було безпечним. Побічні реакції включали запаморочення, закреп, нудоту, а також потенційну можливість подовження коригованого інтервалу QT. У дослідженні MARISA (Monotherapy Assessment of Ranolazine in Stable Angina) за участю 191 хворого зі стенокардією напруження вивчали ефективність трьох доз препарату: 500, 1000 та 1500 мг двічі на день. Усі дози ранолазину виявились ефективнішими, ніж плацебо щодо зниження частоти нападів стенокардії та збільшення тривалості дозованого фізичного навантаження (ДФН) у середньому на 94, 103 та 116 секунд відповідно (р<0,005) [12]. У РКД ERICA (Efficacy of Ranolazine in Chronic Angina) було включено 565 пацієнтів із підтвердженою ІХС, що мали не менше трьох нападів стенокардії щотижня незважаючи на прийом максимальної дози амлодипіну (10 мг). Приєднання до терапії ранолазину по 1000 мг два рази на день протягом шести тижнів супроводжувалося достовірним зниженням частоти ангінальних нападів порівняно з лікуванням амлодипіном + плацебо (2,88 проти 3,31 епізоду на тиждень відповідно; р=0,028). До 2,03 таблетки скоротилася потреба у НГ проти 2,68 – на монотерапії амлодипіном; р=0,014 [13]. У дослідженні CARISA (Combination Assessment of Ranolazine in Stable Angina) пацієнти були рандомізовані у три паралельні групи. Первинна мета полягала у порівнянні впливу додаткового призначення ранолазину (по 750 чи 1000 мг двічі на день) на показник тривалості ДФН під час проби на тредмілі проти плацебо. Всі учасники (n=823) до початку дослідження мали персистуючі симптоми тяжкої стабільної стенокардії зі середньою частотою 4,5 нападу на тиждень незважаючи на застосування терапевтичних доз атенололу, амлодипіну чи дилтіазему. Ранолазин підвищував толерантність до навантаження, подовжуючи тривалість тесту в середньому на 115,6 с проти 91,7 с у групі плацебо; р=0,01 незалежно від супутньої терапії [14].
R. Venkataraman et al. [15] вивчали вплив ранолазину на міокардіальну перфузію за даними однофотонної емісійної комп’ютерної томографії. Хворим на ІХС із дефектами перфузії під час виконання тесту на тредмілі (n=20) протягом чотирьох тижнів призначали терапію ранолазином у дозі 1000 мг двічі на день на додаток до базових антиангінальних засобів. Як результат, на тлі лікування ранолазином спостерігалося подовження тривалості навантаження у середньому на 32 c (р=0,017); зменшення частоти нападів стенокардії у 15 із 20 хворих (75%) та покращення перфузії міокарда у 14 (70%).
Ранолазин виявився ефективним антиішемічним засобом у пацієнтів із гострим коронарним синдромом (ГКС) (нестабільною стенокардією / інфарктом міокарда [ІМ] без підйому сегмента ST) у РКД MERLIN-TIMI 36 (Metabolic Efficiency with Ranolazine for Less Ischemia in Myocardial Infarction 36). Учасники були рандомізовані у співвідношенні 1:1 у групи ранолазину (n=3279) чи плацебо (n=3281). Пацієнти отримували ранолазин (спочатку внутрішньовенно, потім по 2000 мг на добу у два прийоми) або плацебо на додаток до стандартної терапії (аспірин – 95%, ББ – 89%, статини – 78%). Термін спостереження становив близько року. Первинна кінцева точка (смертність від КВ-причин, ІМ та рецидивуюча ішемія міокарда) не відрізнялась у групах ранолазину і плацебо (21,8 та 23,5%, відносний ризик [ВР] 0,92). Не було відмінностей і за показниками КВ-смертності та ІМ. Достовірно нижчою на тлі призначення ранолазину була частота епізодів рецидивуючої ішемії міокарда (13,9 проти 16,1% у групі плацебо, р=0,03). Аналіз додаткових кінцевих точок також підтвердив антиангінальну ефективність препарату. Різниця у 23% на користь ранолазину стосувалася ризику погіршення перебігу захворювання, що визначався як ЕКГ-зміни, які потребували госпіталізації або термінової реваскуляризації міокарда, а також збільшення функціонального класу (ФК) стенокардії. Вірогідність призначення додаткового антиангінального засобу за умови використання ранолазину також була меншою на 19%. Автори дослідження зауважили, що хоча препарат і не мав вірогідного прогностичного впливу, все ж підтвердив свою потужну антиангінальну та антиішемічну дію у пацієнтів з особливо тяжкими проявами захворювання [16].
Деякі міжнародні експерти наголошують, що ранолазин є дієвою та безпечною складовою комбінованої антиангінальної терапії стабільної ІХС, особливо за необхідності «агресивного» лікування тяжкої стенокардії. P. Stone звернув увагу на той факт, що терапевтичний ефект препарату виявився тим вищим, чим більшими були прояви «гемодинамічного і міокардіального стресу», з відповідною клінічною картиною захворювання [17]. Наприклад, у РКД MERLIN максимальний ефект, включно з покращенням прогностичного показника, первинної кінцевої точки, спостерігався у хворих з ГКС та підвищеними значеннями натрійуретичного пептиду. У дослідженнях ЕRІСА та MARISA найкращі результати лікування відзначали у пацієнтів, які попередньо мали найбільше нападів стенокардії та найвиразніші прояви ішемії міокарда, індукованої ДФН. Відомо, що патологічні чинники (гемодинамічні та метаболічні), задіяні під час ішемії, здатні активувати й підтримувати відкритими пізні натрієві канали. Автор припускає, що у зв’язку з цим патогенетичним підґрунтям антиангінального/антиішемічного ефекту ранолазину може бути реалізація його основного механізму – блокади пізнього натрієвого потоку.
Рефрактерна стенокардія
Ціла серія робіт засвідчила ефективність ранолазину у хворих з рефрактерною стенокардією. R. Garberich et al. протягом року спостерігали за такими пацієнтами (n=141), оцінюючи ФК стенокардії, прийом медикаментів, потребу у стаціонарному лікуванні та реваскуляризації, частоту ІМ та смертність [18]. Учасники дослідження – переважно чоловіки (75%), середній вік – 64,7 року. З урахуванням недостатньої ефективності попередньої антиангінальної терапії ранолазин призначали як додатковий засіб у рекомендованих терапевтичних дозах. До кінця терміну спостереження препарат продовжували приймали 65,3% хворих, переважна більшість (90,7%) використовували дозування 500 мг двічі на день. Відмова від лікування була пов’язана з побічними реакціями у 15% випадків (n=21), проведенням реваскуляризації міокарда — у 5% (n=7), вартістю препарату – у 4% (n=5), неефективністю – у 5% (n=8), вартістю і неефективністю – у 3% (n=4), смертю – у 1,5% (n=2), з невідомими причинами – у 1,5% (n=2). При цьому відсоток хворих, у яких клінічний стан суттєво покращився (зменшення ФК стенокардії більше ніж на 2 пункти), був вірогідно вищим за умови постійного прийому ранолазину (51,8 проти 23,1% на тлі відміни препарату; р=0,003).
Показовим є невелике обсерваційне дослідження за участю хворих (n=25) із тяжкою стенокардією на рівні ІІІ-IV ФК, більшість – після коронарної реваскуляризації. Усі пацієнти постійно приймали у середньому по 3,6 антиангінального засобу [19]. Ранолазин додавали як 4-й чи 5-й препарат у зв’язку з недостатньою ефективністю попередньої терапії. Термін спостереження після призначення ранолазину становив два роки. Для порівняння використовували дані за дворічний період до початку терапії. У більшості учасників (68%) використання досліджуваного препарату супроводжувалося зменшенням кількості та тяжкості симптомів стенокардії. Важливим результатом випробування можна вважати той факт, що прийом ранолазину супроводжувався удвічі меншою потребою (-54,5%) у госпіталізації пацієнтів.
Ще в одному дослідженні (Texas Southwestern Medical Center, Даллас, США) за участю пацієнтів (n=18) з рефрактерною стенокардією традиційна антиангінальна терапія з використанням >2 лікарських засобів (ББ, БКК та нітрати пролонгованої дії) не забезпечувала адекватного контролю клінічної симптоматики [20]. Пацієнти свідчили про поганий стан та низьку якість життя у зв’язку з частими тяжкими нападами стенокардії (в середньому 14 разів на тиждень) та необхідністю приймати НГ (у середньому 10 разів на тиждень). Призначення ранолазину розпочинали зі стартової дози 500 мг двічі на добу, з наступним її підвищенням до 1000 мг двічі на добу через два тижні. Терапія виявилась ефективною. У групі ранолазину кількість нападів стенокардії зменшилася з 14 до 0,7 на тиждень, а потреба у НГ скоротилася до нуля. У 8 із 18 хворих (близько 44%) напади стенокардії зникли взагалі. Тільки троє пацієнтів не відреагували на лікування (у них дозу ранолазину з різних причин не підвищували). Автори дослідження зробили висновок щодо ефективності приєднання ранолазину до терапії хворих із тяжкою стенокардією після реваскуляризації міокарда, рефрактерною до стандартних антиангінальних засобів.
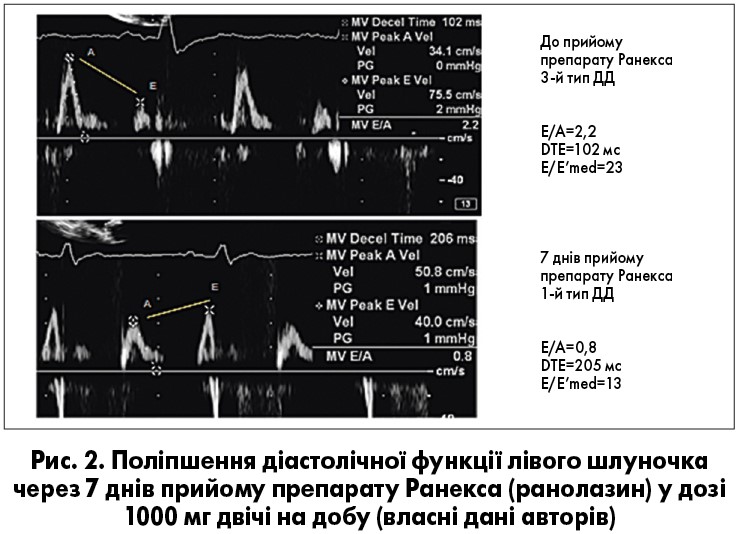
Ми маємо власний досвід ефективного лікування тяжкої рефрактерної стенокардії з використанням ранолазину на додаток до традиційних препаратів (ББ, дигідропіридиновий БКК, аспірин, клопідогрель, статини, НГ). Пацієнт, чоловік віком 68 років, до призначення ранолазину скаржився на ангінальний біль при незначних фізичних навантаженнях, приймав НГ – до 10 таблеток щодня. В анамнезі – перенесені ІМ (2010, 2014), неодноразові ЧКВ (балонна ангіопластика – 1999, 2002, 2010; 7 DES у правій КА – 2002, 2004, 2007, 2014). Супутні захворювання – ЦД 2-го типу, АГ, облітеруючий атеросклероз судин нижніх кінцівок. Призначення ранолазину в дозі 1000 мг двічі на день через сім днів сприяло суттєвому покращенню клінічного стану і збільшенню тривалості ДФН на тредмілі на 56 с. За даними ехокардіографії (рис. 2), відзначали покращення діастолічної функції лівого шлуночка (ЛШ). Препарат був рекомендований для подальшого постійного прийому [21].
Мікроваскулярна стенокардія
За результатами серії пілотних досліджень ранолазин виглядає перспективним засобом для лікування мікросудинної стенокардії. S. Tagliamonte et al. (2014) спостерігали зростання резерву коронарного кровотоку (РКК) під впливом ранолазину (1000 мг/добу) у 58 пацієнтів зі стенокардією, дефектами перфузії міокарда, але без обструктивних уражень КА. РКК, важливий показник стану мікроваскулярного русла, визначали як співвідношення максимальної швидкості діастолічного коронарного кровотоку, індукованої дипіридамолом, до швидкості у стані спокою за даними трансторакальної доплерографії передньої низхідної гілки лівої КА. Після восьми тижнів лікування РКК суттєво зріс при використанні ранолазину і не змінився у групі плацебо. Визначення динаміки РКК на тлі прийому ранолазину було метою ще одного пілотного дослідження з подвійним сліпим плацебо-контролем у пацієнтів із мікроваскулярною стенокардією. Як метод обстеження використовували позитронно-емісійну томографію. Для стимуляції максимального коронарного кровотоку використовували аденозин. Учасниками дослідження були хворі (n=31) зі стенокардією без обструктивних уражень КА і коронарної кальцифікації. Термін спостереження становив один місяць. Ранолазин титрували, починаючи із 500 мг двічі на день протягом тижня, а надалі по 1000 мг двічі на день. Як результат – прийом ранолазину порівняно із плацебо асоціювався зі статистично вірогідним зростанням РКК (р=0,005) [22].
P. Mehta et al. вивчали ранолазин (по 500-1000 мг двічі на день) у рандомізованому подвійному сліпому плацебо-контрольованому випробуванні за участю 142 жінок зі стенокардією напруження, але без обструктивного ураження КА [23]. Термін спостереження становив два тижні. Результати не досягли вірогідності (можливо через короткий термін спостереження). Проте у підгрупі з порушеннями коронарного резерву до початку лікування було відзначено ефективність ранолазину. E. Rayner-Hartley et al. оцінювали ефективність ранолазину в 31 хворого на тяжку рефрактерну мікроваскулярну стенокардію, 27 учасників – жінки, середній вік – 57 років [24]. Тяжкість клінічних симптомів визначали за допомогою Сіетлівського опитувальника при стенокардії (Seatle Angina Questionnaire) і показниками щодо якості життя пацієнтів із використанням відповідних анкет і шкал. Терапія ранолазином протягом шести тижнів значно покращила клінічний статус хворих. Один із найпоказовіших результатів дослідження полягав у тому, що після лікування пацієнти майже утричі рідше зверталися по допомогу до медичних закладів (35,5 проти 93,5% до початку терапії; р<0,01). Аналогічні результати (зменшення клінічних проявів мікроваскулярної стенокардії та поліпшення якості життя) після 6-тижневої терапії ранолазином (n=65) отримали також S. Saha et al. (2017).
Ранолазин для лікування вторинної стенокардії
A. Amin та B. Kim описали два клінічних випадки щодо ефективності ранолазину в жінки (31 рік) та чоловіка (49 років) з гіпертрофічною кардіоміопатією (ГКМП) і клінічною симптоматикою стенокардії. Автори пояснювали терапевтичну дію препарату блокуючим впливом на пізній натрієвий потік, що приводить до зниження діастолічного напруження гіпертрофованої стінки ЛШ і, відповідно, покращує коронарну перфузію, попереджаючи появу ішемії міокарда. В обох випадках були виключені обструктивні ураження КА та діагностовано ГКМП зі значними порушеннями відтоку з ЛШ. Обидва пацієнти мали симптоми вторинної стенокардії. Стандартне лікування з використанням ББ (метопрололу) не давало достатнього ефекту. Призначення ранолазину у дозі 1000 мг двічі на день супроводжувалося суттєвим зменшенням кількості больових нападів в обох випадках [25].
Застосування ранолазину в пацієнтів із супутнім ЦД
Призначення ранолазину видається чи не найбільш раціональним вибором антиангінальної терапії для пацієнтів зі стенокардією та супутнім ЦД 2-го типу – одним із найважливіших факторів КВ-ризику, що у декілька разів підвищує частоту розвитку ІХС та її прогресування. Ураження КА у таких пацієнтів, як правило, мають більш виразний та поширений характер, що зумовлює тяжкість клінічної симптоматики і гірші результати стандартного антиангінального лікування.
Ранолазин знижував рівні глікованого гемоглобіну (HbA1c) у пацієнтів із ЦД 2-го типу, поліпшував контроль глікемії у хворих на ІХС та супутній ЦД і зменшував ймовірність гіперглікемії за наявності ризику розвитку ЦД. Наприклад, у дослідженні CARISA, залежно від дози, ранолазин сприяв зниженню HbA1c на 0,48-0,7%, що асоціювалось з суттєвим зменшенням частоти нападів стенокардії та потреби у НГ [14]. У випробуванні MERLIN-TIMI 36 під впливом препарату показник HbA1c статистично вірогідно снижувався на 0,6%. Більше пацієнтів із ЦД досягли його цільових значень (<7%): 59% у групі ранолазину проти 49% – плацебо (р=0,001). Паралельно спостерігалось зменшення частоти епізодів рекурентної міокардіальної ішемії. Покращення глікемічного контролю не супроводжувалося зростанням ризику гіпоглікемії [26].
TERISA (Type 2 Diabetes Evaluation of Ranolazine in Subjects With Chronic Stable Angina) було першим проспективним масштабним рандомізованим плацебо-контрольованим дослідженням, мета якого полягала у вивченні антиангінальної ефективності ранолазину у пацієнтів із ЦД 2-го типу (n=949). Препарат значно зменшував кількість нападів стенокардії порівняно з плацебо: з 6,7 до 3,8 на тиждень (у контрольній групі – 4,3; р=0,008). Терапевтична дія спостерігалась від самого початку лікування і, за даними ретроспективного аналізу, була за усіма показниками максимальною у хворих із найвищими значеннями HbA1c >8% [27]. У субдослідженні RIVER-PCI (Rranolazine for Incomplete Vessel Revascularisation Post-Percutaneous Coronary Intervention) за участю 854 пацієнтів із ЦД терапія ранолазином суттєво впливала на зниження HbA1c. Крім того, серед учасників РКД, які отримували ранолазин, було менше нових випадків ЦД порівняно із групою плацебо [28].
Ефективність та безпечність ранолазину вивчали у подвійному сліпому плацебо-контрольованому дослідженні за участю пацієнтів із ЦД 2-го типу з неадекватним глікемічним контролем за рахунок тільки модифікації способу життя. Термін спостереження становив 24 тижні. Прийом ранолазину супроводжувався вірогідним впливом на HbA1c, зокрема щодо кількості хворих, які досягли цільового рівня <7,0% (41,2 проти 25,6% у групі плацебо відповідно; р=0,0004). Крім того, значно покращувались показники глікемічного контролю, зокрема вмісту глюкози натщесерце і 2-годинної постпрандіальної глюкози [29].
Точний механізм гіпоглікемічної дії ранолазину невідомий. Одна з гіпотез пов’язує його з антиангінальним ефектом, підвищенням толерантності до фізичних навантажень і збільшенням утилізації глюкози периферичними м’язами. Експериментальні дані свідчать, що препарат може збільшувати секрецію інсуліну, стимульовану глюкозою, ймовірно, за рахунок впливу на іонні натрієві канали β-клітин підшлункової залози. Крім того, в експериментальних роботах було показано, що гіперглікемія активує пізній натрієвий потік і, відповідно, збільшує внутрішньоклітинну концентрацію натрію, з усіма негативними наслідками щодо ішемії міокарда. Не виключено, що у пацієнтів із поєднанням стенокардії і ЦД використання ранолазину (блокатора пізніх натрієвих каналів) забезпечує одночасний вплив на суттєві патофізіологічні чинники обох захворювань і може розглядатись як раціональна патогенетична терапія.
Антиаритмічний ефект ранолазину
Важлива характеристика ранолазину стосується його антиаритмічної дії. Механізм такого ефекту, ймовірно, зумовлений як блокуючим впливом на пізній натрієвий потік, так і модуляцією активності інших іонних каналів. Не виключено, що нормалізація серцевого ритму пов’язана з антиішемічною дією препарату. Крім того, ранолазин має властивості слабкого інгібітору кальцієвих каналів L-типу.
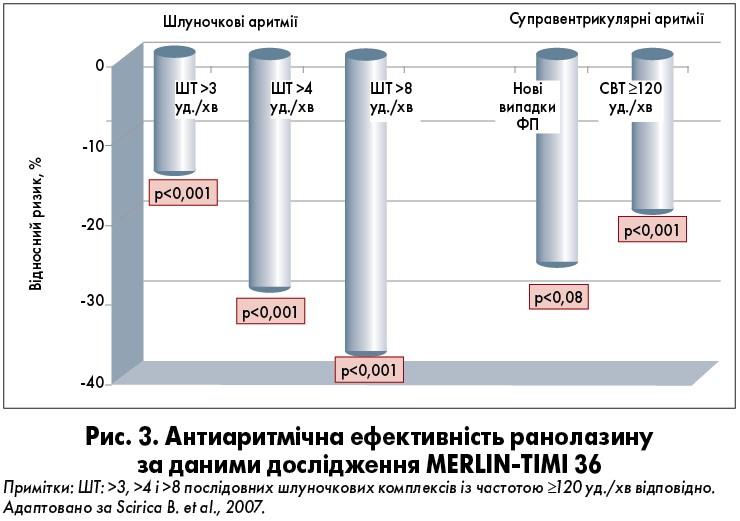
Антиаритмічний вплив ранолазину на вентрикулярні й суправентрикулярні порушення ритму був зареєстрований у РКД MERLIN-TIMI 36 (рис. 3) [30]. За даними холтерівського моніторування ЕКГ, антиаритмічна дія препарату спостерігалася від самого початку лікування, протягом першого тижня після госпіталізації хворих. Терапія ранолазином супроводжувалася зменшенням числа учасників, у яких реєстрували епізоди шлуночкової тахікардії (ШТ) більше 8 комплексів (5,3 проти 8,3% у контрольній групі; р<0,001); суправентрикулярної тахікардії (44,7 проти 55,0% відповідно; р<0,001). У пацієнтів, які приймали ранолазин, рідше порівняно із групою контролю зустрічалися паузи тривалістю більше ніж 3 с (3,1 проти 4,3%; р=0,01). При цьому між групами ранолазину і плацебо не було різниці за частотою проаритмогенних реакцій (виникнення поліморфної шлуночкової тахікардії, випадків раптової смерті).
G. Bazoukis et al. проаналізували існуючі дані щодо антиаритмічної дії ранолазину у хворих із шлуночковими порушеннями ритму [31]. Аналіз включав 14 робіт (3 рандомізованих дослідження, 2 – обсерваційних, 8 описів одиничних клінічних випадків і 1 – серію випадків). Отриманий результат засвідчив позитивний терапевтичний вплив препарату в різних клінічних ситуаціях за наявності ШТ/фібриляції, екстрасистолії. Антиаритмічну дію ранолазину щодо зменшення кількості епізодів ШТ порівняно із плацебо було підтверджено у РКД RAID (Ranolazine Implantable Cardioverter-Defibrillator Trial). У плацебо-контрольованому дослідженні RYPPLE (Ranolazine for the Treatment of sYmPtoms of PaLpitations in patiEnts With Ischemic Heart Disease) препарат виявився ефективним стосовно складних вентрикулярних порушень ритму.
Показовий клінічний випадок описали P. Margos et al. [32]. У 75-річного пацієнта з АГ, гіпертензивним серцем і систолічною СН ІІ ФК за класифікацією Нью-Йоркської асоціації кардіологів (NYHA) (фракція викиду ЛШ 40%) спостерігались тяжкі вентрикулярні порушення серцевого ритму. Хворий мав імплантований кардіовертер-дефібрилятор. Протягом попередніх трьох років у нього було зафіксовано 2871 епізод шлуночкових аритмій і 109 – дефібриляцій для відновлення синусового ритму. Серед препаратів, які він приймав, були аміодарон і мексилетин; обидва засоби відмінили у зв’язку з побічними реакціями. Перед призначенням ранолазину антиаритмічна терапія включала карведилол (12,5 мг тричі на день) і флекаїнід (100 мг двічі на день), без достатнього ефекту. Приєднання ранолазину дозволило повністю позбавити хворого порушень серцевого ритму. Препарат титрували до кінцевої дози 750 мг два рази на день. Термін спостереження становив сім місяців, протягом яких не було зафіксовано жодного випадку вентрикулярної тахікардії чи фібриляції. Автори роботи відзначили ефективність ранолазину, зважаючи на тяжкість клінічного стану пацієнта і наявність аритмій, загрозливих для життя.
Ціла низка різних за масштабом досліджень свідчить про можливість використання ранолазину для запобігання фібриляції передсердь (ФП) і навіть для відновлення синусового ритму при виникненні пароксизму. За даними субаналізу MERLIN-TIMI 36, у пацієнтів із ГКС на тлі терапії ранолазином відзначали тенденцію до зниження частоти ФП вже протягом першого тижня після госпіталізації. Відповідні показники становили 2,4% за умови стандартного лікування проти 1,7% у групі ранолазину (ВР 0,74 проти плацебо; 95% довірчий інтервал 0,52-1,05; р=0,08). Протягом річного спостереження ефект препарату зберігався і набував статистичної вірогідності, включно із загальною частотою пароксизмів ФП і пов’язаних із ними симптомів (ВР 0,71; р=0,01). Проаритмогенні реакції не спостерігались [30].
Метааналіз Ch. Trivedi et al. [33] стосовно хворих, які перенесли АКШ, засвідчив, що периопераційне призначення ранолазину в терапевтичних дозах (n=259) проти стандартної терапії (n=369) супроводжувалося зниженням ризику післяопераційної ФП на 54% (р<0,001). Позитивні результати щодо ефективності ранолазину були отримані у ретроспективному дослідженні R. Miles et al. за участю 393 пацієнтів після АКШ [34]. У ньому порівнювали ефективність ранолазину (1500-2000 мг/добу) й аміодарону (400 мг/добу) стосовно запобігання ФП протягом 14 днів післяопераційного періоду. ФП виникла у 26,5% випадків у групі аміодарону та у 17,5% – ранолазину (р=0,035). Подібні результати спостерігались у пацієнтів, які перенесли кардіологічні операції, – АКШ, корекцію клапанних вад чи комбіновані хірургічні втручання. Більшість хворих периопераційно приймали ББ. Додаткове використання ранолазину у частини з них супроводжувалося значним скороченням кількості пароксизмів ФП порівняно з контрольною групою (10,1 проти 41,9%; р<0,0001). У дослідження G. Tagarakis et al. були залучені 102 пацієнти, яким провели АКШ [35]. Протягом трьох днів до операції та після неї половині учасників призначали ранолазин у невисокій дозі (375 мг двічі на добу), інші отримували стандартну терапію. Частота виникнення ФП у післяопераційний період у групі ранолазину була утричі нижчою порівняно з контролем (8,8 проти 30,8% відповідно; р<0,001).
У кількох роботах вивчали можливість застосування ранолазину для відновлення синусового ритму при появі пароксизмів ФП. У невеликому проспективному рандомізованому пілотному дослідженні оцінювали роль ранолазину при медикаментозній кардіоверсії у хворих із ФП, що виникла нещодавно (<48 годин) [36]. Пацієнти були розподілені на дві групи. В одній застосовували комбіноване лікування: внутрішньовенно (в/в) аміодарон + одноразово перорально 1500 мг ранолазину під час рандомізації (n=25). Друга отримувала тільки аміодарон в/в. Відновлення синусового ритму відбулось у 88% хворих у групі комбінованої терапії проти 65% – аміодарону; р=0,056. На користь лікування ранолазином відрізнялися й терміни відновлення синусового ритму – 9,8±4,1 проти 14,6±5,3 годин відповідно; р=0,002. D. Murdock et al. [37] використовували одноразовий прийом 2000 мг ранолазину з метою кардіоверсії у 18 хворих під час пароксизмів ФП; 17 із них мали кардіологічну патологію. Після застосування ранолазину у 72% пацієнтів протягом шести годин відновився синусовий ритм. У жодному разі не спостерігались проаритмогенні ефекти чи серйозні побічні реакції. Автори дослідження припускають, що після додаткового вивчення високі дози ранолазину можуть стати новою «таблеткою у кишені» для відновлення синусового ритму при ФП у хворих з кардіологічною патологією.
У дослідженні RAFFAELLO (The Ranolazine in Atrial Fibrillation Following an Electrical Cardioversion) оцінювали безпечність та ефективність ранолазину щодо утримання синусового ритму після успішної електричної кардіоверсії. Через дві години після процедури пацієнти (n=241) отримували плацебо чи ранолазин у дозах 375-750 мг двічі на день. Рецидиви ФП були зареєстровані у 56,4% хворих у групі плацебо, подібний результат спостерігався при застосуванні низьких доз ранолазину, тоді як призначення 1500 мг/добу супроводжувалося зменшенням цього показника до 39,7%, хоча різниця і не була статистично вірогідною [38].
Згідно з результатами дослідження HARMONY (A Study to Evaluate the Effect of Ranolazine and Dronedarone When Given Alone and in Combinationin Patients with Paroxysmal Atrial Fibrillation), комбінація ранолазину (750 мг два рази на день) і низьких доз дронедарону (150 чи 225 мг двічі на день) забезпечувала суттєве зменшення частоти пароксизмів ФП (на 45%) порівняно з плацебо. Термін спостереження становив 12 тижнів, учасники РКД – хворі з пароксизмальною формою ФП. Монотерапія як ранолазином, так і дронедароном не була достатньо ефективною [39].
У рандомізованому перехресному подвійному сліпому дослідженні RYPPLE у пацієнтів зі стабільною ІХС / стенокардією та скаргами на серцебиття вивчали ефективність ранолазину щодо кількості нападів стенокардії, тривалості фізичного навантаження (на тредмілі) та порушень серцевого ритму (48-годинний ЕКГ-моніторинг) [40]. Після місячного лікування у групі ранолазину достовірно (p<0,008) зменшилася кількість пацієнтів із вентрикулярними (p<0,045) та суправентрикулярними аритміями (p<0,01). Порівняно з плацебо (p<0,001) знизилася частота нападів стенокардії – з 20 до 5 на місяць, а також зросла тривалість фізичного навантаження до появи депресії сегмента ST (p<0,001).
Висновки
Ранолазин є безпечним та ефективним антиангінальним/антиішемічним засобом для лікування пацієнтів із різними формами ІХС, включно зі стабільною, нестабільною, рефрактерною та мікроваскулярною стенокардією. Слід відзначити важливість позитивних результатів, отриманих у клінічних дослідженнях із використанням ранолазину, для терапії тяжкої рефрактерної та мікроваскулярної форм стенокардії, оскільки останні погано контролюються традиційними лікарськими засобами і становлять серйозну проблему для практикуючих кардіологів і терапевтів. Перспективним видається наступне вивчення ранолазину як препарату для лікування ІХС у поєднанні з ЦД 2-го типу, враховуючи можливість контролювати симптоми стенокардії та глікемію за допомогою одного засобу. Важливою характеристикою ранолазину є його універсальна антиаритмічна дія щодо ФП, вентрикулярних та суправентрикулярних порушень серцевого ритму.
Таким чином, ранолазин може забезпечити персоналізований вибір терапії у багатьох складних клінічних випадках з урахуванням форми стенокардії, особливостей перебігу захворювання, параметрів гемодинаміки, наявності аритмій та супутньої патології.
Література
- ESC guidelines on the management of stable coronary artery disease // European Heart Journal. – 2013. – 34. – Р. 2949-3003.
- Beltrame J., Weekes A., Morgan C. et al. The prevalence of weekly angina among patients with chronic stable angina in primary care practices: the coronary artery disease in general practice (CADENCE) Study // Arch Intern Med. – 2009. – 169. – Р. 1491-1499.
- Arnold S., Grodzinsky A., Gosch K. et al. Predictors of physician under-recognition of angina in outpatients with stable coronary disease // Circ Cardiovasc Qual Outcomes. – 2016. – 9. – Р. 554-559.
- Berger P. Ranolazine and other antianginal therapies in era of the drug-eluting stent // JAMA. – 2004. – Р. 291.
- Ambrosio G., Collins P., Dechend R. et al. Stable Angina: PeRception of NeeDs, Quality of Life and ManaGemEnt of Patients (BRIDGE Study) — A Multinational European Physician Survey, 2018. DOI:10.1177/0003319718796313.
- Al-Lamee R., Thompson D., Dehbi H. et al. Percutaneous coronary investigation in stable angina (ORBITA): a double-blind, randomized controlled trial // Lancet. – 2018. – 391. – Р. 31-40.
- Manolis A., Poulimenos L., Ambrosio G. et al. Medical treatment of stable angina: A tailored therapeutic approach // International J of Cardiology. – 2016. – 220. – Р. 445-453.
- https://www.igeahub.com/2018/05/04/best-selling-drugs‑2018.
- Hasenfuss G., Maier L. Mechanism of action of the new anti-ischemic drug ranolazine // Clin Res Cardiol. – 2008. – 97. – Р. 222-226.
- Rayner-Hartley E., Sedlak T. Ranolazine: a contemporary review // J Am Heart Assoc. – 2016. – 5. – e003196.
- Deshmukh S., Patel R., Pinassi E. et al. Ranolazine improves endothelial function in patients with stable coronary artery disease // Coron Artery Dis. – 2009. – 20 (5). – Р. 343-347.
- Chaitman B.R., Skettino S.L., Parker J. et al. for the MARISA Investigators. Anti-ischemic effects and long-term survival during ranolazine monotherapy in patients with chronic severe angina // J Am Coll Cardiol. – 2004. – 43. – Р. 1375-1382.
- Stone P., Gratsiansky N., Blokhin A. et al. Antianginal efficacy of ranolazine when added to treatment with amlodipine: The ERICA (Efficacy of Ranolazine in Chronic Angina) trial // J Am Coll Cardiol. – 2006. – 48. – Р. 566-575.
- Chaitman B., Pepine C., Parker J. et al. Combination Assessment of Ranolazine in Stable Angina (CARISA) Investigators. Effects of ranolazine with atenolol, amlodipine, or diltiazem on exercise tolerance and angina frequency in patients with severe chronic angina: a randomized controlled trial // JAMA. – 2004. – 291. – Р. 309-316.
- Venkataraman R. et al. // JACC Cardiovasc Imaging. – 2009. – 2. – Р. 1301-1309.
- Morrow D., Scirica B., Karwatowska-Prokopczuk E., Skene A., McCabe C., Braunwald E. Evaluation of a novel anti-ischemic agent in acute coronary syndromes: design and rationale for the Metabolic Efficiency with Ranolazine for Less Ischemia in Non-ST-elevation acute coronary syndromes (MERLIN)-TIMI 36 trial // Am Heart J. – 2006. – 151. – 1186.e1-1186.e9.
- Stone P. Ranolazine in diabetics with stable ischemic heart disease // J Am Coll Cardiol. – 2017. – 69. – Р. 2314-2316.
- Garberich R., Lips A., Bennett N. et al. Effectiveness of ranolazine in patients with refractory angina // JACC. – 2014. – 63 (12). – A1535.
- Khalid Khan et al. Ranolazine in the management of chronic stable angina // Br J Cardiol. – 2011. – 18. – Р. 179.
- Shane Greene R. et al. Ranolazine for the treatment of refractory angina in a veterans population // Cardiovasc Revasc Med. – 2012. – 13 (2). – 141.e1-141.e5.
- Лутай М. И., Голикова И. П. Рефрактерная стенокардия: пути преодоления. Клинический случай эффективного применения ранолазина // Здоров’я України. – 2016. – № 3. – С. 2-4.
- Safdar B., D’Onotio G., Dzlura J. et al. Ranolazine and Microvascular Angina by PET in the Emergency Department: Results from a Pilot Randomized Controlled Trial // Clin Therapeutics. – 2017. – 39 (1). – Р. 55-63.
- Mehta P., Goykhman P., Thompson L. et al. Ranolazine improves angina in women with evidence of myocardial ischemia but no obstructive coronary artery disease //JACC Cardiovasc Imaging. – 2011. – 4. – Р. 514-522.
- Rayner-Hartley E., Parvand M., Humphries K. et al. Ranolazine for Symptomatic Management of Microvascular Angina // Am J Ther. – 2018; doi10.1097/MJT00000000000779.
- Amin A., Kim B. Ranolazine for Angina in Hypertrophic Cardiomyopathy, 2018; doi/jrg/10 1155/2018/5142572.
- Morrow D., Scirica B., Chaitman B .et al. Evaluation of the glycometabolic effects of ranolazine in patients with and without diabetes mellitus in the MERLIN-TIMI 36 randomized controlled trial // Circulation. – 2009. – 119. – Р. 2032-2033.
- Arnold S., McGuire D., Spertus J. et al. Effectiveness of ranolazine in patients with type 2 diabetes mellitus and chronic stable angina according to baseline hemoglobin A1c // Am Heart J. – 2014. – 168. – Р. 457-465 e2.
- Weisz G., Genereux P., Iniguez A. et al. Ranolazine in patients with incomplete revascularization after percutaneous coronary intervention RIVER-PCI: multicenter, randomized, double-blind, placebo-controlled trial // Lancet. – 2016. – 387. – Р. 136-145.
- Eckel R., Henry P., Yue A. et al. Effect of ranolazine monotherapy on glycemic control in subjects with type 2 diabetes // Diabetes Care. – 2015. – 38. – Р. 1189-1196.
- Scirica B., Morrow D., Hod H. et al. Effect of ranolazine an antianginal agent with novel electrophysiological properties on the incidence of arrhythmias in patients with non ST-segment elevation acute coronary syndrome (from MERLIN-TIMI 36 the randomized controlled trial) // Circulation. – 2007. – 116. – Р. 1647-1652.
- Bazoukis G., Tse G., Letsas K. et al. Impact of ranolazine on ventricular arrhythmias. A systematic review // J of Arrhythmia. – 2018. – 34. – Р. 124-128.
- Margos P., Margos N., Mokadem N. et al. Ranolazine: safe and effective in patient with hypertensive cardiomyopathy and multiple episodes of electrical storm // Clinical Case Reports. – 2017. – 5 (7). – Р. 1170-1175; Doi:10. 1002/ccr3.1019.
- Trivedi Ch., Blasé L., Mohanty S. et al. Ranolazine: a novel anti-ischemic drug in prevention post-operative AF in patients undergoing coronary artery bypasses grafting: meta-analysis // Circulation. – 2015. – 132. – A17401.
- Miles R., Passman R., Murdock D. Comparison of effectiveness and safety of ranolazine versus amiodarone for prevention atrial fibrillation after coronary artery bypass grafting // Am J Cardiol. – 2011. – 108. – Р. 673-676.
- Tagarakis G., Aidonidis I., Daskalopoulou S. et al. Effect of ranolazinedrug in prevention postoperative atrial fibrillation in patients undergoing coronary revascularization surgery // Curr Vasc Pharmacol. – 2013. – 11. – Р. 988-991.
- Fragakis N., Koskinas K., Katritsis D. et al. Comparison of effectiveness of ranolazine plus amiodarone versus amiodarone alone for conversion of recent-onset atrial fibrillation // Am J Cаdiol. – 2012. – 110. – Р. 673-677.
- Murdock D., Kersten M., Kaliebe J. et al. The use of oral ranolazine to convert new or paroxysmal atrial fibrillation: a review of experience with implication for possible «pill in the pocket» approach to atrial fibrillation // Indian Pacing Electrophysiol J. – 2009. – 9. – Р. 260-267.
- Saad M., Mahmoud A., Elgendy I., Conti R. Ranolazine in cardiac arrhythmia // Clin Cardiol. – 2016. – 39. – Р. 170-178.
- Kowey P. The effect of the combination of ranolazine and low dose dronedarone on atrial fibrillation burden in patients with paroxysmal atrial fibrillation (HARMONY trial) // Heart Rhythm Society. – 2014. – A I.B03-05.
- Pelliccia F. et al. Ranolazine reduces symptoms of palpitations and documented arrhythmias in patients with ischemic heart disease — The RYPPLE randomized cross-over trial // IJC Metabolic and Endocrine, 2015. DOI: 10.1016/j.ijcme.2015.05.016.
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (63) травень 2019 р.