24 липня, 2019
Рекомендації щодо ведення пацієнтів із серцевою недостатністю зі зниженою фракцією викиду лівого шлуночка
Серцева недостатність зі зниженою фракцією викиду лівого шлуночка (СН ЗФВ ЛШ) – клінічний синдром, причинами якого зазвичай є ішемічна хвороба серця (ІХС), часто внаслідок інфаркту міокарда (ІМ), неконтрольована артеріальна гіпертензія (АГ), клапанні вади та кардіоміопатії. Цей стан супроводжується низкою типових симптомів: задишкою, набряками, підвищеною стомлюваністю тощо. Основною метою лікування таких хворих є поліпшення клінічного стану, функціонування та якості життя, запобігання госпіталізаціям і зниження смертності. До вашої уваги представлено огляд рекомендацій щодо ведення пацієнтів із цим захворюванням, розроблених фахівцями Національної служби охорони здоров’я Великої Британії (NHS, 2019).
Для всіх пацієнтів із СН ЗФВ ЛШ (<40%) слід розглядати застосування інгібіторів ангіотензинперетворювального ферменту (іАПФ) та β-блокаторів. Призначати слід спочатку один лікарський засіб, і щойно стан хворого стабілізується при терапії першим препаратом (зазвичай іАПФ), доцільно додати другий. Метою є досягнення цільової дози іАПФ та β-блокатора, за неможливості використовують максимальну стерпну дозу.
Особам із СН ЗФВ ЛШ, у яких, незважаючи на оптимальну терапію, симптоми не зникають, слід призначати антагоніст мінералокортикоїдних рецепторів (АМР) спіронолактон як лікарський засіб першої лінії. Жоден пацієнт не повинен отримувати три препарати, які блокують ренін-ангіотензин-альдостеронову систему (РААС), оскільки це зазвичай призводить до розвитку гіперкаліємії та порушення функції нирок. Безпеку й ефективність поєднання іАПФ, блокаторів рецепторів ангіотензину II (БРА) і АМР не визначено, тому їхнє одночасне використання не рекомендоване.
Моніторинг функції нирок має дуже важливу роль у веденні осіб із СН. Його потрібно проводити кожні шість місяців у стабільних пацієнтів і частіше, якщо відбуваються зміни у фармакотерапії та/або різке порушення стану хворого. При хронічній нирковій недостатності через підвищений ризик гіперкаліємії необхідний ретельний моніторинг відповіді на титрування дози медикаментів. Якщо розрахункова швидкість клубочкової фільтрації (рШКФ) <45 мл/хв/1,73 м2, доцільно розглянути призначення нижчих доз та/або повільніше титрування дози іАПФ чи БРА, АМР і дигоксину.
Тест на N-термінальний фрагмент натрійуретичного пептиду B-типу (NT-proBNP) використовується для скринінгу пацієнтів (без ІМ) перед направленням на ехокардіографію (ЕхоКГ) за підозри на СН. У ситуації, коли дані ЕхоКГ дають підставу припустити розвиток СН, необхідно виконати електрокардіографічне дослідження (ЕКГ), якщо його ще не було проведено, щоб визначити основну причину СН.
Сакубітрил/валсартан – варіант лікування, який застосовують згідно з рекомендаціями NICE (2016). Пацієнтам, які розпочинають терапію, слід припинити прийом іАПФ або БРА принаймні за 36 годин до її початку. Якщо стан хворого погіршується з нез’ясованої причини, проте був стабільним упродовж років при оптимальній фармакотерапії, необхідно звернутися до спеціаліста.
Ключові рекомендації
Клінічні дослідження та діагностика
У пацієнтів із підозрою на хронічну СН (ХСН) слід виконати низку основних тестів. Вибір досліджень відрізняється залежно від проявів симптомів, але зазвичай вони повинні включати:
- тест на NT-proBNP;
- ЕКГ;
- рентгенографічне обстеження грудної клітки;
- аналіз крові: функція нирок (електроліти, креатинін, рШКФ), розгорнутий загальний аналіз крові, дослідження функції щитоподібної залози, функціональні печінкові проби, вміст глікозильованого гемоглобіну (HBA1С), ліпідів;
- загальний аналіз сечі;
- визначення максимальної швидкості видиху (пікфлоуметрія) або спірометрія;
- трансторакальну ЕхоКГ для виключення серйозної патології клапанів, оцінки систолічної функції ЛШ і виявлення внутрішньосерцевих шунтів.
Дані заходи стосуються лише пацієнтів із підтвердженим діагнозом СН.
Моніторинг
Усі пацієнти із СН мають високий ризик ураження нирок і гіперкаліємії, що є наслідком поширених захворювань (наприклад, цукровий діабет), медикаментозного лікування або самої СН. Моніторинг функції нирок дуже важливий при веденні таких пацієнтів. Так, оцінювання функції нирок необхідне при зміні медикаментозного лікування або різкому порушенні стану хворого. Терапія СН, особливо за використання комбінації іАПФ та АМР, пов’язана з гострим зниженням функції нирок та ризиком гіперкаліємії. Якщо стан пацієнта є клінічно стабільним за сталих доз препаратів, слід перевіряти функцію нирок кожні шість місяців. У разі інтеркурентних патологій, особливо за діареї та блювання, хворі мають проконсультуватися з лікарем загальної практики і призупинити використання іАПФ та АМР (зазвичай на 48 годин), перш ніж буде виконано аналіз крові або до поліпшення стану й можливості прийому рідини перорально.
Моніторинг (як мінімум протягом шести місяців для стабільних пацієнтів) повинен включати:
- клінічну оцінку функціональних можливостей, гідратації, серцевого ритму, когнітивного та аліментарного статусу;
- огляд лікарських засобів, зокрема потреби у змінах, наприклад припинення прийому блокаторів кальцієвих каналів (БКК) із негативним інотропним ефектом, як-то верапаміл, дилтіазем, а також ймовірних побічних реакцій;
- визначення вмісту сечовини та електролітів у сироватці крові, визначення рШКФ;
- огляд та консультацію кардіолога у пацієнтів, які не відповідають на лікування.
Виписка пацієнта
Пацієнтів із СН, як правило, слід виписувати зі стаціонара лише тоді, коли їхній клінічний стан є стабільним, а план ведення оптимізований. Команда первинної медико-санітарної допомоги, хворий і доглядач мають бути ознайомлені з планом лікування.
Підтримка пацієнтів та доглядачів
Ведення осіб із СН слід розглядати як спільну відповідальність пацієнта і медпрацівника. Якщо необхідно, доцільно звернутися по допомогу до медичної сестри, що спеціалізується на догляді пацієнтів із СН.
На рисунку 1 представлено алгоритм клінічних досліджень для діагностування СН.
Слід зважати, що ожиріння, африканське або афро-карибське сімейне походження, прийом діуретиків, іАПФ, β-блокаторів, антиретровірусних засобів або АМР можуть знизити рівень натрійуретичних пептидів у сироватці крові. Тому варто припинити прийом даних препаратів за три дні до тестування або продовжити лікування і провести ЕхоКГ.
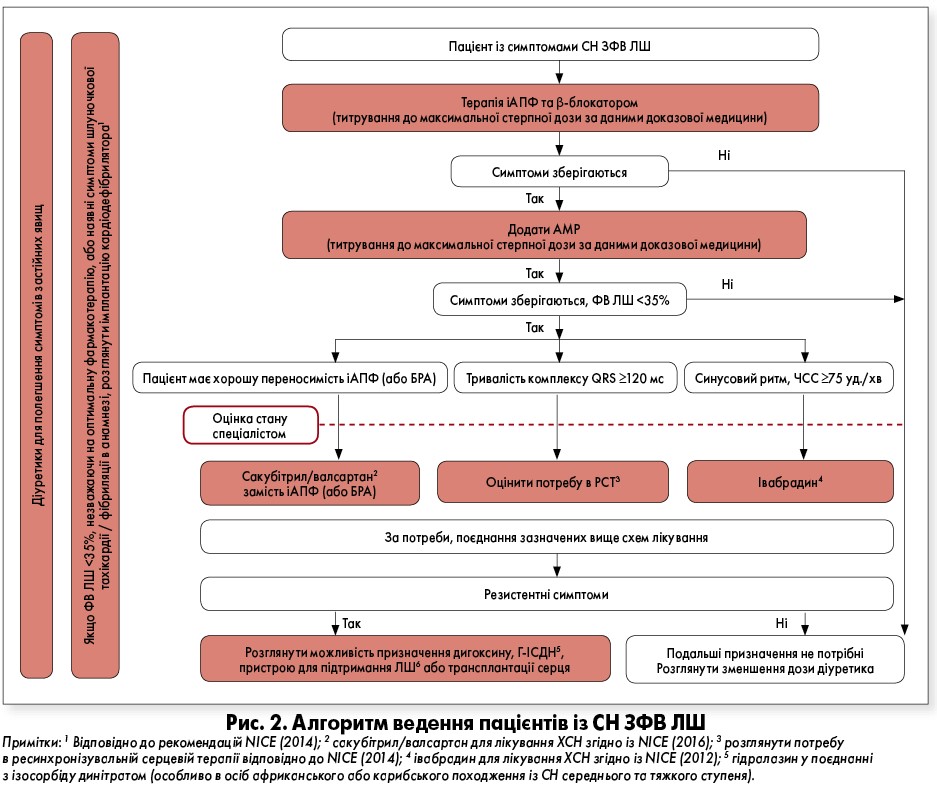
На рисунку 2 представлено алгоритм ведення пацієнтів із СН ЗФВ ЛШ.
Фармакотерапія
Всім пацієнтам із СН ЗФВ ЛШ слід рекомендувати терапію іАПФ та β-блокаторами, схваленими для застосування при СН (навіть якщо симптоми не проявляються при використанні діуретика та іАПФ), але призначати препарати бажано послідовно. Зазвичай (але не обов’язково) спочатку застосовують іАПФ, але певні клінічні причини можуть зумовлювати призначення β-блокатора (наприклад, за необхідності додаткового антиангінального лікування).
На початку та упродовж терапії необхідний ретельний моніторинг. При хронічній нирковій недостатності через підвищений ризик гіперкаліємії потрібен контроль відповіді на титрування доз лікарських засобів. Якщо рШКФ <45 мл/хв/1,73 м2, слід розглянути призначення препаратів у нижчих дозах та/або повільніше титрування дози іАПФ або БРА, АМР і дигоксину.
Діуретики
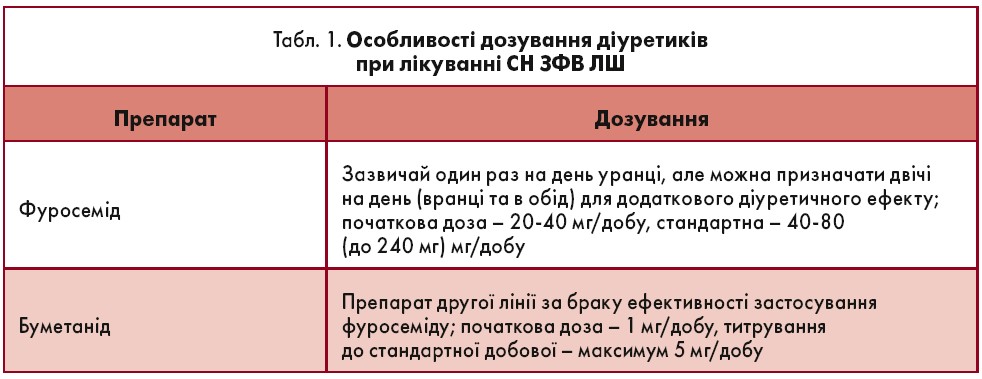
Рутинне застосування діуретиків необхідне для полегшення застійних симптомів і запобігання затримці рідини у пацієнтів із СН. За потреби слід проводити висхідне/низхідне титрування перед початком використання подальших схем терапії при СН. Оптимальною вважається найнижча доза, ефективна для полегшення симптомів / застійних явищ. У таблиці 1 представлено особливості дозування діуретиків.
Важливо перевіряти функцію нирок і вміст електролітів у сироватці крові через 1‑2 тижні від початку лікування і після кожного титрування дози; за досягнення стабільного стану – один раз на шість місяців.
У разі розвитку резистентності до терапії діуретиками (після призначення та оцінки спеціалістом) тіазидні та тіазидоподібні (метолазон) можна додавати до петльових для потужного синергічного діуретичного ефекту в пацієнтів, які не відповідають адекватно на збільшення дози петльових діуретиків. Комбіновану терапію має розпочинати й контролювати фахівець, а на етапі первинної медичної допомоги хворому зі стабілізованим клінічним та нирковим статусом надається постійний догляд.
Таке лікування може бути ефективним і дозволяє уникнути потреби у госпіталізації, але пов’язане з певним ризиком.
Інгібітори ангіотензинперетворювального ферменту
Терапію іАПФ слід починати у відповідних низьких дозах і здійснювати висхідне титрування на коротких інтервалах часу (наприклад, кожні два тижні) до досягнення максимальної стерпної або цільової дози. У таблиці 2 наведено початкові та цільові дози іАПФ.
Біохімічний аналіз крові (вміст сечовини, креатиніну й електролітів) слід проводити при ініціації лікування, через 1‑2 тижні від початку і через 1‑2 тижні після кожного збільшення дози. Моніторинг артеріального тиску (АТ) необхідний до і після кожного підвищення дози (NICE, 2018). Після досягнення стабільної дози слід повторити біохімічний аналіз крові для оцінки стану нирок через місяць, а потім продовжити відстежувати вміст сечовини й електролітів та побічні ефекти принаймні кожні шість місяців. Необхідність частішого спостереження залежить від клінічного стану, режиму лікування або супутніх захворювань.
Підвищення вмісту сечовини, креатиніну та калію може спостерігатися після початку терапії іАПФ. Досягнення концентрації креатиніну до такої, що на 50% більша від базової, або 266 мкмоль/л (залежно від того, що є меншим), прийнятне; нормальним є також підвищення рівня калію до <5,5 ммоль/л. Якщо збільшення концентрації креатиніну або калію є значнішим від зазначеного вище і зберігається, незважаючи на коригування доз супутніх лікарських засобів, наприклад припинення прийому нестероїдних протизапальних препаратів (НПЗП), препаратів калію або таких, що утримують калій (тріамтерен, амілорид, спіронолактон/еплеренон), а також за відсутності ознак застою крові, доцільно знизити дозу діуретика. Дозу іАПФ слід зменшити вдвічі, а вміст сечовини, креатиніну й електролітів – повторно перевіряти протягом 1‑2 тижнів.
У разі якщо рівень калію зростає до ≥5,5 ммоль/л або вміст креатиніну збільшується більш ніж на 100% чи перевищує 310 мкмоль/л, прийом іАПФ слід припинити. Концентрацію сечовини, креатиніну й електролітів крові слід регулярно і послідовно контролювати, доки рівні калію та креатиніну не стабілізуються.
Блокатори рецепторів ангіотензину II
БРА можуть бути альтернативою іАПФ для пацієнтів із непереносимістю останніх (наприклад, через кашель). Якщо необхідно призначити БРА, препаратом вибору є кандесартан. Слід контролювати біохімічні показники функціонування нирок, побічні ефекти та АТ згідно з наведеними вище рекомендаціями щодо іАПФ. У таблиці 3 представлені початкові та стабільні дози БРА.
Комбіноване застосування лікарських засобів, що блокують РААС. Хоча Агентство з контролю за лікарськими засобами і виробами медичного призначення Великої Британії (MHRA, 2014) не рекомендує сумісне застосування препаратів із двох класів блокаторів РААС (включно з іАПФ, БРА та аліскіреном), у деяких пацієнтів із СН може виникнути потреба в терапії комбінацією іАПФ і БРА.
Є докази на користь того, що переваги такого поєднання можуть переважати ризики (гіперкаліємія, гіпотензія, порушення функції нирок) для певної групи осіб із СН, яким не підходять інші види лікування.
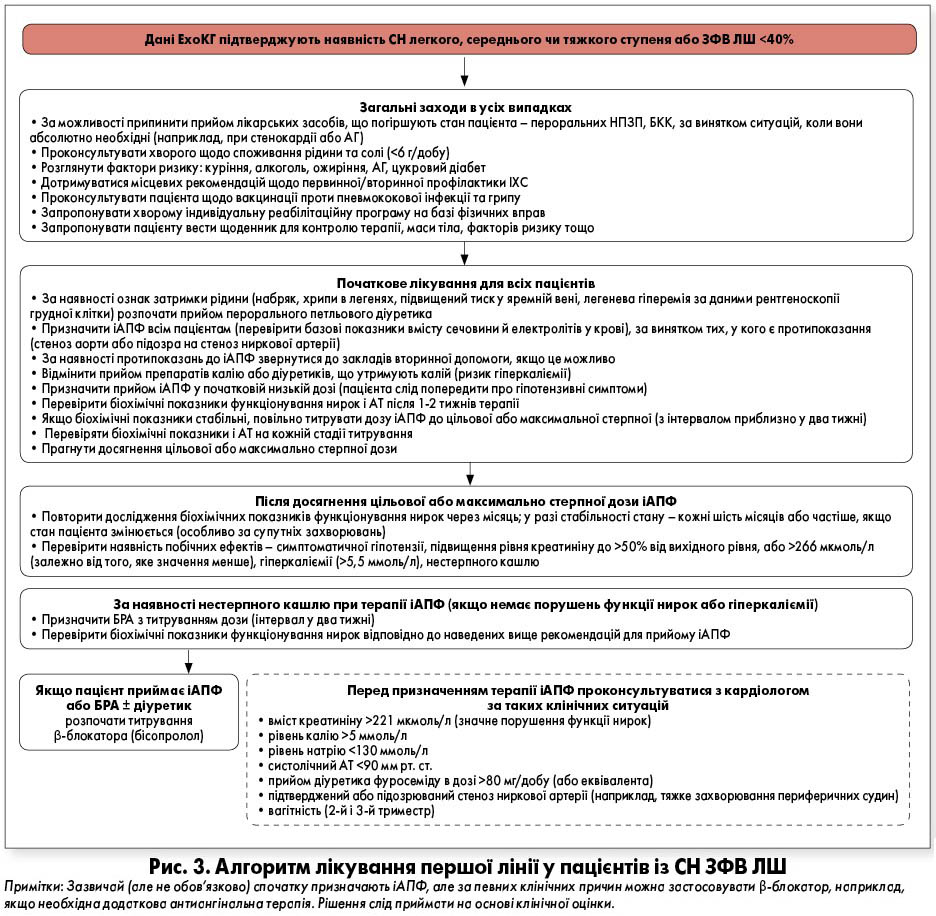
Блокатор РААС кандесартан схвалений як засіб додаткової до іАПФ терапії в осіб із симптоматичною СН, для яких така комбінація є необхідною. Використання потрійної комбінації іАПФ, β-блокатора та БРА можна розглянути для пацієнтів зі стійкими симптомами; призначає її лише кардіолог. Застосування комбінації іАПФ + БРА + АМР не рекомендоване. На рисунку 3 представлено алгоритм лікування першої лінії пацієнтів із СН ЗФВ ЛШ.
Бета-блокатори
Бета-блокатори, схвалені для застосування при СН, слід призначати пацієнтам із симптоматичною СН ЗФВ ЛШ після діуретика та, зазвичай, іАПФ (навіть за безсимптомного перебігу при терапії діуретиками та іАПФ). Терапію β-блокатором при СН варто розпочинати за принципом «start low, go slow» (починати з низьких доз і повільно їх підвищувати), з оцінкою частоти серцевих скорочень (ЧСС), АТ та клінічного стану після кожного титрування. Пацієнтам із СН, що розвинулася внаслідок систолічної дисфункції ЛШ, та які вже приймають β-блокатор через супутнє захворювання (наприклад, стенокардія, АГ), потрібно продовжувати терапію даним препаратом. Крім того, слід оцінювати ЧСС і клінічний стан (симптоми, особливо ознаки застійних явищ, масу тіла) після початку прийому та при кожному титруванні дози, визначати АТ до і після збільшення дози. У таблиці 4 представлено початкові та цільові дози β-блокаторів.
За наявності низької ЧСС (<50 уд./хв) і якщо симптоми стають тяжчими, потрібно розглянути застосування дигоксину, аміодарону, дилтіазему і верапамілу (останні два, як правило, протипоказані при СН). Також слід вдвічі зменшити дозу β-блокатора, а за серйозного погіршення стану – припинити прийом (така ситуація рідкісна) і переглянути необхідність терапії іншими препаратами. Альтернативним варіантом лікування після консультації кардіолога є івабрадин (NICE, 2012). Крім того, для виключення блокади важливо оцінити дані ЕКГ.
Терапія бісопрололом у пацієнтів із СН
Призначати бісопролол доцільно за таких умов:
- пацієнт страждає на стабільну ХСН протягом останніх шести тижнів та отримує переважно незмінну базову терапію останні два тижні;
- хворий повинен зазвичай отримувати іАПФ в оптимальній дозі (або БРА, якщо має непереносимість іАПФ);
- пацієнт не повинен мати жодних абсолютних протипоказань до застосування бісопрололу, як-от:
- гостра СН або епізоди декомпенсованої СН, що потребують внутрішньовенної інотропної терапії;
- кардіогенний шок;
- атріовентрикулярна блокада другого або третього ступеня (без кардіостимулятора);
- синдром тахі-брадикардії;
- синоатріальна блокада;
- симптоматична/тяжка брадикардія при <60 уд./хв до початку терапії;
- симптоматична/тяжка гіпотензія (систолічний АТ <90 мм рт. ст.);
- тяжка бронхіальна астма;
- пізні стадії оклюзійної хвороби периферичних артерій і синдрому Рейно;
- нелікована феохромоцитома;
- метаболічний ацидоз.
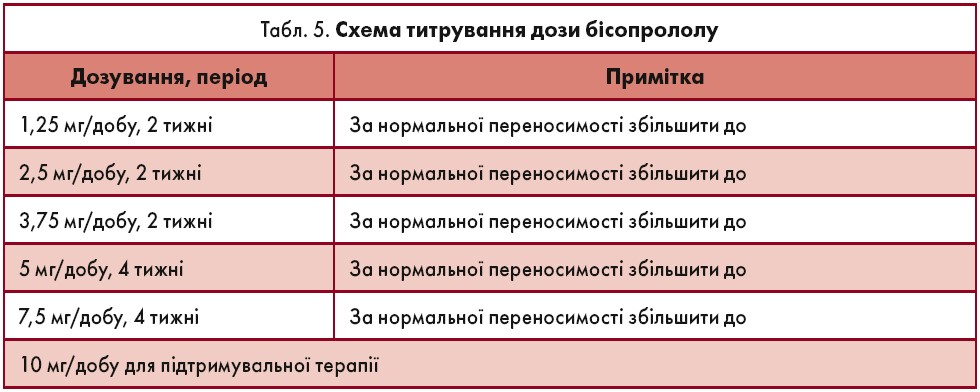
Деякі з наведених протипоказань можуть бути відносними, наприклад, NICE рекомендує призначати селективний β-блокатор хворим на ХОЗЛ без зворотного розвитку. У таблиці 5 наведено схему титрування дози бісопрололу.
В інструкції для застосування препарату зазначено, що після початку лікування та збільшення дози рекомендовано спостерігати за станом пацієнтів протягом чотирьох годин (АТ, ЧСС, ознаки погіршення СН). На місцевому рівні це не вважається за необхідне, і повернення додому під нагляд відповідальної попередженої дорослої особи буде більш ніж достатньо.
Зміна дози при переході від однієї стадії титрування до наступної має бути мінімальною на цих інтервалах, навіть якщо це займає більше часу. Побічні явища можуть перешкоджати пацієнтам у досягненні максимальної рекомендованої дози, але приймати бісопролол принаймні в будь-якій дозі краще, ніж не приймати зовсім.
Якщо пацієнт скаржиться на посилення задишки, слід тимчасово припинити титрування та залишити дозу бісопрололу незмінною. Проте варто збільшити дозу діуретика та спостерігати за станом хворого ще протягом двох тижнів. Якщо прояви задишки зменшилися до попереднього рівня, титрування доцільно відновити. За необхідності дозу сечогінного засобу можна зменшити. Альтернативною стратегією при задишці є тимчасове зниження дози бісопрололу і подовження інтервалів між наступними підвищеннями, якщо її прояви при цьому зменшуються.
Не слід надалі збільшувати дозу бісопрололу без консультації кардіолога, якщо пульс (або верхівковий поштовх при фібриляції передсердь) знижується до рівня <50 уд./хв та/або систолічний АТ становить <90 мм рт. ст. Також не рекомендується різко припиняти лікування бісопрололом, оскільки ймовірне тимчасове погіршення проявів СН. У пацієнтів з ІХС раптова відміна β-блокатора може призвести до нападу стенокардії або ІМ. Якщо необхідно припинити прийом, дозу слід поступово зменшувати, розділяючи її навпіл щотижня.
Показаннями для припинення терапії бісопрололом є:
- тяжка симптоматична гіпотензія;
- гострий набряк легенів;
- кардіогенний шок;
- тяжка симптоматична брадикардія;
- атріовентрикулярна блокада 2-го або 3-го ступеня.
Антагоністи мінералокортикоїдних рецепторів
Пацієнтам із СН ЗФВ ЛШ, у яких залишаються симптоми незважаючи на оптимальну терапію, слід призначати спіронолактон у дозі від 12,5 або 25 мг/добу через день до 25‑50 мг/добу. Цільова доза залежить від симптомів і стабільності біохімічних показників. Якщо спіронолактон не підходить (зазвичай чоловікам <50 років через ризик гінекомастії), можна застосовувати еплеренон (початкова доза – 25 мг/добу з титруванням до цільової 50 мг/добу, зазвичай упродовж чотирьох тижнів). Пацієнти із СН, які приймають спіронолактон, повинні контролювати рівень калію та креатиніну в крові з метою виявлення ознак гіперкаліємії та/або погіршення функції нирок. За значної гіперкаліємії дозу спіронолактону слід зменшити вдвічі і перевірити біохімічні показники. Не рекомендовано призначати одночасно іАПФ + БРА + АМР.
Практичні рекомендації щодо призначення препаратів
- Переносимість препаратів із прогностичною перевагою, особливо іАПФ, погіршується за зменшення волемії через надмірний діурез. Часто необхідно знизити дозу діуретика, щоб «звільнити місце» для іАПФ, β-блокатора і АМР (альдостерону).
- При СН систолічний АТ 90 мм рт. ст. часто нормально переноситься. Немає необхідності знижувати дози препаратів, якщо пацієнт не скаржиться на пов’язані з цим симптоми. Якщо є потреба у зменшенні доз, спочатку слід розглянути можливість зниження дози діуретика.
- Якщо гіпотонія є проблемою, слід відмінити препарати, які знижують АТ, але не впливають на лікування СН, наприклад БКК, α-блокатори.
- Потрібно відміняти БКК із негативним інотропним ефектом (дилтіазем, верапаміл), якщо це можливо, оскільки вони асоційовані зі зменшенням виживаності. Дигідропіридини тривалої дії (амлодипін, фелодипін) мають нейтральний вплив на смертність при СН.
- Варто прагнути до досягнення цільових доз іАПФ і β-блокатора, але дотримуватися принципу «дещо краще, ніж зовсім нічого, а потроху обох – краще, ніж багато одного з них і нічого іншого».
- Кашель є частим симптомом при СН. У деяких пацієнтів його викликають іАПФ. Ефект іАПФ щодо виживаності значніший, ніж у БРА. Не слід відміняти іАПФ, поки немає абсолютної впевненості, що саме цей препарат викликає кашель.
- іАПФ не протипоказані при нирковій недостатності. Вони не рекомендовані, якщо наявність реноваскулярного захворювання призводить до зниження функції нирок (збільшення вмісту креатиніну >50%) з початком терапії іАПФ. Слід перевірити вміст сечовини й електролітів у крові через тиждень після початку прийому іАПФ. За вже наявної ниркової недостатності важливо перевіряти ці показники раніше й частіше. Варто бути уважними щодо розвитку гіперкаліємії (>5,5 ммоль/л).
- Бета-блокатори зазвичай добре переносяться при ХОЗЛ. За СН і ХОЗЛ періодично наявні хрипи у легенях. Не слід відміняти прийом β-блокатора, якщо немає абсолютної впевненості, що саме він викликає бронхоспазм.
- Титрування дози іАПФ часто може відбуватися швидше, ніж рекомендовано. Дозу β-блокатора завжди слід збільшувати повільно. Іноді необхідно залишати її на одному рівні набагато довше, ніж протягом запропонованих двох тижнів перед збільшенням дози. Інколи полегшення симптомів при терапії β-блокатором є негайним, а іноді необхідно переконувати пацієнта, що можливе тимчасове погіршення стану, перш ніж самопочуття поліпшиться.
Підготувала Наталія Купко
Повний текст документа читайте на сайті www.nhs.uk
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (63) травень 2019 р.