25 квітня, 2016
Конгрес Американської асоціації з вивчення захворювань печінки (AASLD): останні досягнення сучасної гепатології

13-17 листопада 2015 р. у м. Сан-Франциско (США) відбувся щорічний конгрес Американської асоціації з вивчення захворювань печінки (AASLD Liver meeting). Це визначна подія як для науковців, так і для практичних лікарів. Більш ніж 9500 фахівців охорони здоров’я зі Сполучених Штатів Америки і всього світу зібралися разом, щоб обмінятися інформацією про останні досягнення у вивченні захворювань печінки, обговорити результати лікування та поспілкуватися з колегами. В рамках роботи конгресу проводились курси післядипломної освіти, симпозіуми, лекції, майстер-класи, сателітні симпозіуми.
Курс післядипломної освіти, розроблений для клініцистів, охоплював широкий спектр проблем лікування пацієнтів із захворюваннями печінки. Велика увага приділялась новітнім підходам до лікування, особливо таким, як персоналізована цільова медицина. Детально розглядалися питання управління в системі охорони здоров’я, пов’язані з проблемами покращення якості лікування пацієнтів, зниження витрат ресурсів, а також полегшення доступу до сучасного медичного обслуговування.
На розгляд учасників конгресу була представлена рекордна кількість абстрактів – 3191. Після ретельного розгляду експерти відібрали з них певну кількість для представлення на конгресі у формі усної або стендової доповіді з можливістю ставити запитання авторам/доповідачам. Кожного дня демонструвалося більш ніж 500 постерів з таких тем: метаболічні захворювання печінки, фундаментальні та клінічні дослідження фіброзу печінки, вірусні гепатити В та С (вірусологічні, імунологічні, патогенетичні аспекти).
В рамках конгресу проводились цікаві сателітні симпозіуми, зокрема, присвячені досягненням у діагностиці й лікуванні неалкогольного стеатогепатиту (НАСГ) та новітнім підходам до проблеми неалкогольного стеатогепатиту у дитячому віці.
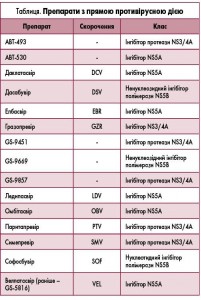
Значна увага приділялась питанням лікування вірусних гепатитів. За чверть століття, що минули з моменту відкриття вірусу гепатиту С (HCV), медицина досягла величезних успіхів у лікуванні цієї інфекції: позитивні результати спостерігаються більш ніж у 90% випадків. На першому засіданні післядипломного курсу конгресу AASLD, присвяченому питанню лікування вірусного гепатиту С (ВГС), доктор медицини, доктор філософії Jean-Michel Pawlotsky (Франція) розглянув чотири доступних наразі групи препаратів з прямою противірусною дією (ПППВД) та їх використання в потрійних схемах без інтерферону (IFN-free). Деякі з цих препаратів вже доступні для використання у широкій клінічній практиці, інші – ще перебувають на стадії клінічних випробувань (табл.). Вчений ще раз нагадав міжнародні рекомендації про недоцільність застосовування схем лікування з інтерфероном як першої лінії терапії. «Незважаючи на високу вартість, схеми, що не містять інтерферон, є найкращими варіантами терапії завдяки їх високій вірусологічній ефективності, простоті використання і переносимості», – відзначив доктор Pawlotsky.
В сучасних схемах лікування ВГС виділяють такі групи противірусних препаратів:
- Інгібітори NS3/4A протеази (першого покоління: телапревір, боцепревір; другого покоління: симепревір, паритапревір, асунапревір та ваніпревір) – переривають життєвий цикл вірусу.
- Інгібітори NS5A (першого покоління: даклатасвір, ледипасвір, омбітасвір; другого покоління: елбасвір, велпатасвір) – дезорганізують комплекс реплікації, а також здатні блокувати збір і вихід вірусних частинок.
- Ненуклеозидні інгібітори (дасабувір) – непрямо блокують реплікацію РНК.
- Нуклеотидні аналоги (софосбувір) – призводять до обриву ланцюга після включення у знов синтезовану РНК вірусу.
З препаратів цих чотирьох груп сьогодні складаються три поточні стратегії лікування ВГС. Доктор Pawlotsky зазначив, що він не прогнозує появу нових методів лікування.
Перша стратегія як основу лікування використовує аналог нуклеотиду з високим бар’єром до резистентності у поєднанні з одним з препаратів, якій має низький бар’єр резистентності, або інгібітор протеази NS3/4A (паритапревір), або NS5A інгібітор (даклатасвір).
Другий варіант вибору поєднує в собі три препарати з низькими бар’єрами резистентності: інгібітор протеази NS3/4A, інгібітор NS5A та ненуклеозидний інгібітор для підвищення бар’єру резистентності в групі в цілому. Прикладом даної схеми лікування є комбінація паритапревіру, омбітасвіру і дасабувіру.
Третя стратегія включає використання одного з препаратів другої генерації, який має покращений бар’єр резистентності, у поєднанні з іншим лікарським засобом. Одна з таких комбінацій – інгібітор протеази другої генерації гразопревір у поєднанні з інгібітором NS5A другого покоління елбасвіром – повинна бути схвалена в найближчі місяці, зазначив доктор Pawlotsky.
Згідно з рекомендаціями AASLD, Американського товариства інфекційних захворювань (Infectious Diseases Society of America, IDSA) та Європейської асоціації з вивчення печінки (EASL), усі хворі з хронічною HCV-інфекцією повинні отримувати лікування. Але на практиці через велику кількість пацієнтів з HCV-інфекцією і високу вартість лікування не всі пацієнти зможуть отримати до нього доступ в найближчі рік-два. «Забезпечення лікуванням є великим питанням, – сказав доктор Pawlotsky. – Більшість з нас є вихідцями з країн, де медицина доступна, а вартість препаратів відшкодовується, але це можливо не повсюди. Це захворювання вражає 150 мільйонів людей у всьому світі, і ми повинні всіма засобами забезпечити доступ до сучасного лікування для всіх інфікованих осіб у світі. Кожен має право на лікування».
Доповідачі симпозіуму, присвяченого НСV-інфекції, основну увагу приділили найбільш складним популяціям пацієнтів з HCV-інфекцією та запропонували новітні підходи до їх ведення та лікування. Доктор медицини Hugo E. Vargas (FAASLD) ознайомив учасників симпозіуму з оновленими даними керівництва AASLD-IDSA щодо лікування HCV-інфекції.
Доктор медицини Paul Y. Kwo під час своєї презентації «Оптимізація стійкої вірусологічної відповіді (СВВ) у хворих, яких важко лікувати» зосередився на тій невеликій групі населення, яка залишається проблемною для лікування, особливо на тих пацієнтах, які проходять лікування методом діалізу, а також хворих з декомпенсованим цирозом печінки і тих, які перенесли трансплантацію печінки.
Доктор Paul Y. Kwo навів зведені дані про дослідження пацієнтів з термінальною стадією ниркової недостатності при лікуванні ВГС з використанням схеми лікування, запропонованої компаніями Merck і Abbvie, а також дані щодо використання схем на основі софосбувіру.
У своїй презентації доктор David L.Wyles зробив огляд всіх наявних сьогодні даних щодо резистентності та розкрив їх значення для прийняття рішення про лікування. Це особливо актуально для пацієнтів, які мають рецидив інфекції, або для тих, у кого лікування ПППВД виявилось невдалим. Доповідач окремо проаналізував кожну схему лікування видів HCV-інфекції, асоційованих з резистентністю, з використанням інгібіторів протеази NS3/4A, NS5A та NS5B.
Характеризуючи досягнені за останні роки успіхи в терапії вірусних гепатитів, доктор Ramon Bataller з Університету Північної Кароліни наголосив, що «з появою високоефективних препаратів для лікування вірусного гепатиту пріоритетом сучасної гепатології стає жирова хвороба печінки. Лікування ВГC сьогодні відбувається відносно легко, хоча і є досить дорогим: хворий приймає таблетки, які вбивають вірус. У лікуванні ж неалкогольної жирової хвороби печінки (НАЖХП) і алкогольної жирової хвороби печінки (AЖХП) не все так просто, тому що вони зумовлені особливостями способу життя людини. І, на жаль, переконати таких хворих змінити цей спосіб життя досить складно».
Професор Arun Sanyal, співорганізатор симпозіуму та координатор спеціальної групи з вивчення стеатозу печінки і стеатогепатиту, в своїй вступній промові «Лікування причини: зміни в способі життя при АЖХП та НАЖХП» підкреслив, що кожний пацієнт бажає отримати препарат (пігулку) від кожної проблеми, але розвитку ЖХП багато в чому сприяє спосіб життя людини. Ми повинні змінити парадигму лікування від повністю медичного підходу до поєднання медичних втручань і немедикаментозних змін у житті пацієнта. Зміна способу життя відіграє ключову роль у лікуванні ЖХП печінки, яка у своєму розвитку має виражений поведінковий компонент, але, як правило, гепатологи намагаються лікувати тільки метаболічну складову цього захворювання. Реальність така, що пацієнтам з АЖХП або НАЖХП для довгострокового відновлення необхідні істотні зміни способу життя. Не існує специфічних медикаментів, схвалених саме для лікування ЖХП.
Доктор Bataller доповів про те, що найперспективнішим новим препаратом для лікування НАЖХП є обетихолева кислота, яка ефективно блокує секрецію жовчних кислот, але і стимулює гіперліпідемію, зокрема підвищує рівень холестерину ліпопротеїнів низької щільності (ЛПНЩ). Препарат може поліпшити перебіг НАЖХП в короткостроковій перспективі, але збільшує ризик розвитку серцево-судинних захворювань в подальшому. Він також може викликати значний свербіж.
Без змін способу життя та усунення етіологічного фактора медикаментозна терапія АЖХП також малоефективна. Найбільше дослідження STOPAH по вивченню лікування АЖХП виявило, що стандартні схеми терапії із застосуванням кортикостероїдів або пентоксифіліну не є ефективними в довгостроковій перспективі. Навпаки, зміна способу життя при НАЖХП і АЖХП є ефективною стратегією немедикаментозного лікування і покращення довгострокових наслідків.
Вчені досліджували сироваткові рівні двох розчинних форм позаклітинного цитокератину 18 (M30-антигену і M65-антигену) для диференціювання НАСГ від простого стеатозу. Рівні M30-антигену і M65-антигену в сироватці крові можуть мати клінічне значення для виявлення пацієнтів з НАСГ. Подальші дослідження фрагментів цитокератину 18 є обов’язковими для більш точної оцінки ролі цих aпоптонекротичних біомаркерів у патофізіології НАЖХП.
На конгресі значна увага приділялась фундаментальним дослідженням. В рамках симпозіуму з проблем аутофагії в печінці виступив професор Jiandie D. Lin з доповіддю «Печінкова аутофагія: циркадне регулювання та її роль у розвитку НАЖХП». Його лабораторія займається вивченням ритмічної природи аутофагії в печінці та її впливу на перебіг НЖХП на експериментальних групах мишей. Симпозіум дозволив по-новому подивитися на роль аутофагії у підтримці гомеостазу печінки при НАСГ. Аутофагія – це процес утилізації клітинних органел і макромолекул, який супроводжує життєдіяльність нормальної клітини в звичайних умовах. Однак за певних умов, аутофагія може призводити до клітинної загибелі. Нові дані свідчать про те, що інгібування аутофагії відбувається в добовому ритмі, що регулюється як печінковим «біологічним годинником», так і сигналами навколишнього середовища, такими як світло і харчова поведінка. Пригнічення цього добового ритму і інгібування аутофагії також може відігравати важливу роль у прогресуванні від стеатозу до фіброзу при НАЖХП.
«Поведінка майже всіх живих організмів на нашій планеті підпорядковується добовому ритму аж до тканинного рівня і глибше, – підкреслив професор Jiandie D. Lin. – Зрозуміло, що діяльність жирової тканини, м’язів і печінки дуже ритмічна. Ми знаємо, що аутофагія є важливою складовою нормального функціонування клітин, особливо при відповіді на голод, який так само, як і голодування, залежить від добового ритму. Однак раніше ми не знали, чи є ритмічний цикл у самої аутофагії, тепер ми знаємо, що він існує».
Дослідження останніх декількох років істотно покращили розуміння аутофагії як з фізіологічної, так і з патофізіологічної точки зору. Метаболізм глюкози та ліпідів, зміни в органелах (таких як мітохондрії і ендоплазматичний ретикулум), видалення білкових агрегатів, пошкодження клітин і виживання, фіброз і клітинна трансформація – всі ці процеси відбуваються опосередковано (щонайменше частково) за рахунок аутофагії. Існують чіткі добові ритми зміни рівня метаболітів, гормональної секреції, експресії генів і метаболічного потоку, що, як відомо, контролюються «біологічним годинником», зазначив професор Jiandie D. Lin. Про добовий ритм аутофагічних вакуолей в тканині печінки відомо з початку 1980-х років. Нові дані показують, що активація аутофагії в печінці теж має аналогічний добовий патерн, досягаючи максимального рівня у другій половині дня і знижуючись в нічний час. Експресія гена аутофагії у ритмі показує ті ж сильні добові закономірності, хоча час максимального прояву може відрізнятися. Ulk1, наприклад, має піки в середині дня, Bnip3 – у вечірні години, Atg4c – вранці. «Біологічний годинник» потрібен для цієї ритмічної індукції аутофагії: діючи через C/EBPb, він допомагає підтримувати рівні поживних речовини і енергію гомеостазу, а також зміни протеома і органел та тимчасове відокремлення метаболізму.
«Руйнування цілого «біологічного годинника» при виключенні FIP200 (family interacting protein) погіршує процес аутофагії, – констатував доктор Lin. – Ми виявили, що в умовах голодування FIP200 був перерозподілений з цитоплазми в ізольовану мембрану. У FIP200-дефіцитних клітин індукція аутофагії різними засобами була скасована. Пригнічення аутофагії пов’язано з двома різноплановими змінами. Одним з його наслідків є зниження поглинання тригліцеридів у гепатоцитах. Інгібування протеїну FIP200, вочевидь, захищає печінку мишей від стеатозу. Якщо ці миші не могли накопичувати зайвий жир в печінці, пошкодження печінки у них збільшувалося внаслідок фіброзу. Різке гальмування аутофагії на моделі НАЖХП у мишей посилює пошкодження печінки. Це свідчить про те, що інгібування аутофагії може бути тим фактором, який сприяє переходу від стеатозу до запалення і фіброзу при НАСГ».
Значну увагу на конгресі викликали лекціїї провідних гепатологів у форматі майстер-класів. Так, доктор медичних наук, професор Guadalupe Garcia-Tsao (FAASLD) на майстер-класі «Зміна перебігу цирозу» проаналізувала перебіг цирозу на різних прогностичних етапах. Вона описала поліпшення перебігу хвороби на тлі сучасного лікування, яке стало можливим в результаті збільшення обсягу знань про патофізіологічні механізми, задіяні у розвитку різних ускладнень цирозу.
Доктор Roger Davis на майстер-класі «Прогресування стеатозу печінки сигнальним шляхом JNK» надав сучасне розуміння ролі JNK (с-Jun N-термінальна кіназа) у розвитку жирової дистрофії печінки. Професор підкреслив, що більш глибоке розуміння значення шляху JNK покращує терапевтичне уявлення про механізми ЖХП. JNK належить до сімейства мітоген-активованої протеїнкінази і реагує на стрес та інші стимули, такі як цитокіни, ультрафіолетове опромінення, тепловий і осмотичний шок.
 О.М. Бака (перша зліва) і Е.Г. Манжалій (четверта зліва) з Крісом Дагмором (Chris Dugmore),
О.М. Бака (перша зліва) і Е.Г. Манжалій (четверта зліва) з Крісом Дагмором (Chris Dugmore),директором з контролю цілісності інформації AASLD
ЖХП є кінцевим результатом задіяння регуляторних шляхів, які активуються екологічними стресами, що можуть включати як високий вміст жиру, так і споживання алкоголю. У процесі розвитку стеатозу печінки беруть участь декілька сигнальних шляхів, але все більш доказів вказує саме на JNK або опосередкований JNK-сигнальний шлях як на важливий регулятор і активатор розвитку цього патологічного стану.
«JNK була асоційована з низкою захворювань, що супроводжуються метаболічним стресом, зумовленим високим вмістом жирів в раціоні або високим рівнем цукру в крові, – пояснив професор молекулярної медицини Roger Davis (Медичний інститут Говарда Хьюза і Артура Сміта). – Вона безпосередньо залучена в розвиток жирової дистрофії печінки і в більш широкому сенсі – в розвиток серцево-судинних захворювань і діабету». Зазначимо, що поняття «стрес-пов’язаних сигнальних шляхів» не є новим для гепатології. Давно визнано, що стеатоз печінки є фізіологічною реакцією на екологічні стреси і особливості раціону. Дослідники давно припускали, що стрес-специфічні регуляторні шляхи так чи інакше залучені в розвиток клінічно значущої ЖХП. «Початкове захоплення викликало зростаюче розуміння шляху JNK як корисної мішені для дії лікарських препаратів. Я думаю, що ще більш привабливою потенційною терапевтичною ціллю є деякі з механізмів, які регулює JNK», – зазначив Roger Davis.
У той час як печінка складається переважно з гепатоцитів, в ній також є значні популяції імунних клітин та клітин інших типів. «Одним з важливих питань є питання про те, коли активація конкретного шляху стає метаболічно значущою», – сказав доктор Davis. – Щоб відповісти на це запитання, ви повинні знати весь цей шлях і те, що відбувається на кожному його етапі. Тепер ми в змозі описати механізми, за допомогою яких функціонує JNK, що вона робить в імунних клітинах і в клітинах печінки і як це впливає на відкладення ліпідів».
Велику зацікавленість учасників конгресу викликала нова магнітно-резонансна (МР) методика – LiverMultiScan, яка була представлена вченими з Оксфордського університету в рамках виставки медичного обладнання. Вона виводить діагностику захворювань печінки на новий рівень. У зв’язку з глобальною епідемією стеатогепатиту (алкогольного і неалкогольного) і високою захворюваністю на вірусні гепатити (близько 450 мільйонів людей) є нагальна необхідність у точному, швидкому та простому діагностичному тесті для визначення типу і ступеня ураження печінки. Новий метод оцінки стану печінки за допомогою багатопараметричного МР-зображення і спектроскопії надає докладну неінвазивну характеристику великій вибірці паренхіми печінки і може швидко і безпечно кількісно визначати ступінь фіброзу, стеатозу та вміст заліза при високому рівні чутливості і специфічності методу.
Дана МР-методика об’єктивно оцінює біологічні ознаки фіброзу, стеатозу і гемосидерозу печінки, які є невід’ємними компонентами характеристики тканини печінки при біопсії. Оцінка фіброзу печінки за допомогою цієї методики особливо цінна тим, що надає можливість диференціювати тканину з будь-яким ступенем фіброзу від нормальної, а також тканину з вираженим фіброзом від тканини з незначним або помірним фіброзом у невибраній популяції пацієнтів. Слід зазначити, що сучасні альтернативні методи неінвазивної оцінки фіброзу, такі як еластографія печінки (на основі УЗД або МРТ), були протестовані тільки на попередньо обраній обмеженій за кількістю популяції пацієнтів з ожирінням та асцитом. Сироваткові маркери фіброзу печінки чутливі, але неспецифічні і не були протестовані в загальній популяції з наявністю співіснуючого фіброзу в інших органах. На відміну від методів діагностики на основі акустики (таких як еластографія) спосіб відображення Т1 не залежить від ступеня ожиріння або наявності асциту; він має здатність демонструвати, які саме ділянки печінки страждають. Багатопараметрична МР-технологія включає відображення T1 для візуалізації фіброзу/запалення, відображення Т2 для визначення кількості заліза і протонну магнітно-резонансну спектроскопію (1Н-MRS) для визначення кількості жиру в печінці. Зображення Т1 – це МР-методика, яка дозволяє оцінити тканину in vivo. Вміст ліпідів у печінці може бути встановлений кількісно. T1 – це швидкий і по-справжньому неінвазивний тест, який не вимагає внутрішньовенної ін’єкції жодної контрастної речовини.
Проведені дослідження показали хорошу кореляцію даних Т1 з результатами гістологічного дослідження, які були отримані при біопсії печінки у пацієнтів з хворобою печінки змішаної етіології. Як істинно кількісна ця неінвазивна методика оцінки стану тканини печінки може застосовуватись для безпечного довгострокового аналізу та прогнозування прогресування і регресії захворювання і/або відповіді на терапію без необхідності проведення повторної біопсії, що раніше було неможливо. Завдяки цій методиці відкривається багато перспектив для досліджень і клінічного застосування нових стратегій лікування печінки та метаболічних порушень, наприклад, можливість кількісно оцінювати ступінь пошкодження печінки при АЖХП і НАЖХП у динаміці.
Ця методика також надає можливість оцінити регіонарні відмінності по всій печінці, що особливо цікаво при неоднорідності фіброзу, що відзначається при таких захворюваннях, як первинний склерозуючий холангіт і первинний біліарний цироз печінки. Планується проведення багатоцентрового дослідження для оцінки значення цього методу, а також для визначення, чи дійсно МР-оцінка фіброзу печінки за допомогою Т1-зображення здатна прогнозувати розвиток захворювання. Результати цього дослідження визначать, чи зможе використання багатопараметричної МР-оцінки печінки замінити в кінцевому результаті біопсію печінки з метою встановлення стадії фіброзу, ступеня стеатозу і гемосидерозу.