30 жовтня, 2019
Реферативний огляд європейських настанов 2019 року щодо ведення діабету, предіабету та серцево-судинних захворювань
Цьогоріч Європейським товариством кардіологів (ESC) спільно з Європейською асоціацією з вивчення діабету (EASD) опубліковано нові настанови з ведення діабету, предіабету та серцево-судинних захворювань (Cosentino F. et al., 2019).
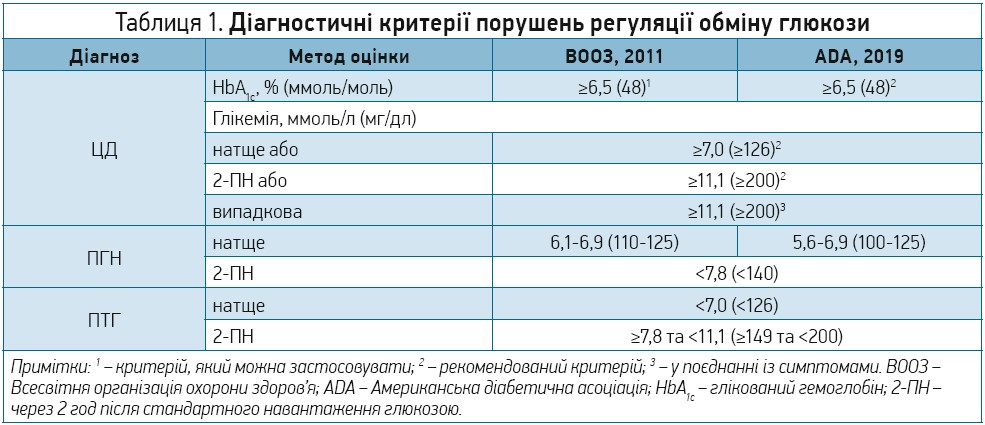
До порушень регуляції обміну глюкози належать цукровий діабет (ЦД) та предіабетичні стани – порушення глікемії натще (ПГН) і порушення толерантності до глюкози (ПТГ). Їх діагностичні критерії підсумовано в таблиці 1.
Поширеність ЦД та предіабету серед пацієнтів із серцево-судинними захворюваннями (ССЗ) особливо висока. Після проведення орального глюкозотолерантного тесту (ОГТТ) у 2/3 учасників дослідження GAMI з інфарктом міокарда (ІМ) уперше діагностовано діабет або предіабет. Інші масштабні дослідження продемонстрували, що ОГТТ дає змогу виявити більшу кількість порушень обміну глюкози, ніж глікемія натще чи HbА1с. Отже, для діагностики ПТГ рекомендовано ОГТТ, а для скринінгу ЦД – визначення HbА1с та глікемії натще, якщо цього недостатньо – ОГТТ (клас рекомендації І, рівень доказів А). Для мінімізації хибнопозитивних результатів у пацієнтів із гострим коронарним синдромом (ГКС) ОГТТ треба проводити не раніше ніж через 4-5 днів після появи симптомів.
Стратифікація серцево-судинного ризику в пацієнтів із діабетом і предіабетом
Метааналіз 102 проспективних досліджень продемонстрував, що ЦД удвічі підвищує ризик ішемічної хвороби серця (ІХС), ішемічного інсульту та смерті від них, незалежно від інших факторів ризику. На відміну від здорових жінок фертильного віку, хворі на діабет не захищені від передчасного виникнення ССЗ. Тому шкали ризику, розроблені для загальної популяції, можуть застосовуватися лише в осіб із предіабетом, а критерії визначення ризику у хворих на ЦД підсумовано в таблиці 2.
За відсутності клінічних проявів хворим на ЦД рекомендовано визначення мікроальбуміну в сечі для ідентифікації осіб із ризиком виникнення дисфункції нирок і високого ризику ССЗ (І, В) та запис стандартної електрокардіограми (ЕКГ) усім пацієнтам з артеріальною гіпертензією (АГ) або підозрою на ССЗ (І, С). Модифікаторами ризику в асимптомних хворих на ЦД із помірним-високим ризиком можуть вважатися бляшки в сонних або стегнових артеріях, виявлені методом ультрасонографії – УСГ (ІІа, В), комп’ютерної томографії (КТ) або магнітно-резонансної томографії (МРТ), а також індекс коронарного кальцію методом КТ або гомілково-плечовий індекс – ГПІ (ІІb, В). Для скринінгу ССЗ у безсимптомних пацієнтів можна застосувати КТ-ангіографію чи функціональні методи візуалізації, як-от радіонуклідна оцінка міокардіальної перфузії, стресові МРТ серця чи ехокардіографія (ІІb, В). Визначення товщини комплексу інтима-медіа сонних артерій (ІІІ, А) та рівня циркулюючих біомаркерів (ІІІ, В) як скринінгові тести не рекомендовано.
Профілактика ССЗ у хворих на діабет і предіабет
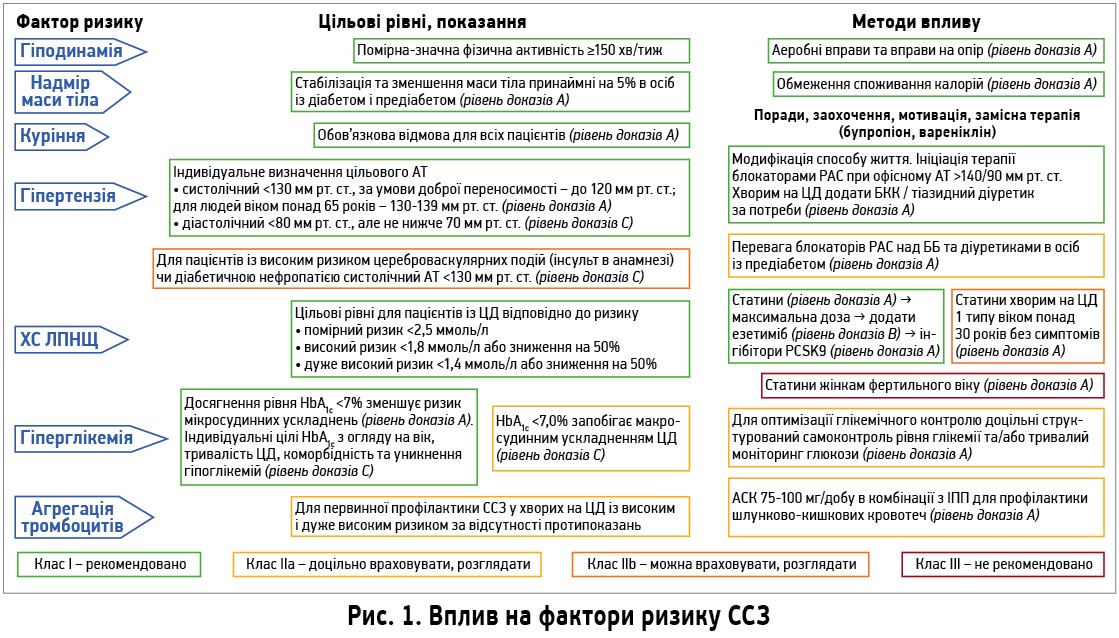
Ключовим методом профілактики як ЦД, так і ССЗ є модифікація способу життя (I, A). Пацієнтам із діабетом і предіабетом рекомендовано зниження надлишкової маси тіла принаймні на 5% шляхом зменшення споживання калорій (I, A). Для зниження частоти великих серцево-судинних ускладнень і нормалізації артеріального тиску (АТ) рекомендовано середземноморську дієту з додаванням оливкової олії та/або горіхів (IIa, B). Натомість добавки, що містять вітаміни та мікроелементи, не знижують ризик ЦД або ССЗ (III, B). Усім пацієнтам з АГ рекомендовано включати до раціону овочі, фрукти й нежирні молочні продукти, але обмежити споживання алкоголю та натрію <100 ммоль/добу (І, А). Фізична активність сповільнює трансформацію предіабету в діабет, покращує глікемічний контроль і знижує ризик ССЗ. Аеробні вправи та динамічні вправи на опір покращують чутливість до інсуліну, контроль глікемії, знижують рівні ліпідів крові й АТ на 7/5 мм рт. ст. Отже, фізичну активність помірної чи значної інтенсивності ≥150 хв/тиж рекомендовано як для запобігання ЦД, так і для його контролю, за винятком пацієнтів із тяжкою коморбідністю або обмеженою очікуваною тривалістю життя (I, A). Пацієнтам, які ведуть сидячий спосіб життя, показані періоди фізичної активності тривалістю ≥10 хв, що еквівалентно 1000 кроків. Активне й пасивне куріння підвищує ризик ЦД, ССЗ і передчасної смерті. Тому всім пацієнтам рекомендовано відмовитися від куріння (I, A).
Поширеність АГ у хворих на діабет перевищує 60%. Оптимальний контроль АТ зменшує ризик мікро- та макросудинних ускладнень і смертності. Настанови 2019 року пропонують індивідуальне визначення цільових рівнів АТ (рис. 2). Докази твердо підтримують пріоритетність призначення блокаторів ренін-ангіотензинової системи (РАС), насамперед інгібіторів ангіотензинперетворювального ферменту (ІАПФ), а за умови їх поганої переносимості – блокаторів рецепторів ангіотензину (БРА), особливо в пацієнтів з альбумінурією чи гіпертрофією лівого шлуночка (ЛШ). Комбінація ІАПФ + БРА не показана. Оскільки більшість пацієнтів потребують комбінованої антигіпертензивної терапії (АГТ), хворим на діабет рекомендовано поєднання блокатора РАС із блокатором кальцієвих каналів (БКК) або тіазидним (тіазидоподібним) діуретиком. Використання фіксованих комбінацій покращує прихильність до лікування. Пацієнтів на комбінованій АГТ потрібно заохочувати до самоконтролю АТ. Для корекції АГТ доцільно проводити добовий моніторинг АТ (ІІа, С). В осіб із предіабетом препаратами вибору є блокатори РАС через менший ризик виникнення діабету порівняно з бета-блокаторами (ББ) та діуретиками. З-поміж усіх ББ лише небіволол не порушує чутливості до інсуліну в пацієнтів із метаболічним синдромом.
За результатами метааналізу, що включав 18 686 хворих на ЦД обох типів, зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) на 1 ммоль/л під впливом статинів асоціюється зі зниженням загальної смертності на 9%, великих серцево-судинних подій – на 21%. Сприятливий вплив на прогноз у поєднанні з невеликим відсотком небажаних ефектів робить статини класом вибору у хворих на ЦД. Інтенсивність терапії визначається профілем ризику (рис. 2). Ще більшого зниження ХС ЛПНЩ можна досягти, призначаючи езетиміб у комбінації зі статинами. Пацієнтам із дуже високим ризиком і стійким підвищенням ХС ЛПНЩ, незважаючи на застосування максимально переносимої дози статину в комбінації з езетимібом, або пацієнтам, які не толерують до статинів, рекомендовано призначати інгібітор пропротеїнової конвертази субтилізин-кексинового типу 9 (PCSK9). У частини хворих на ЦД спостерігається зниження ХС ЛПВЩ, підвищення тригліцеридів крові та збагачених ними ліпопротеїнів (хіломікрони, ремнанти ліпопротеїнів дуже низької щільності) та переважання малих щільних часточок ЛПНЩ на тлі нормального рівня ХС ЛПНЩ. У цих випадках рекомендовано модифікацію способу життя з акцентом на зниження маси тіла, обмеження споживання швидко засвоюваних вуглеводів і алкоголю та призначення фібратів (ІІа, В).
З-поміж усіх показників глікемічного контролю з факторами ризику ССЗ найбільше корелює рівень HbA1c. Досягнення цільового рівня HbA1c <7% сприяє зниженню ризику мікро- та макросудинних ускладнень. Менш жорсткі цільові рівні (<8% або ≤9%) можна розглядати в пацієнтів похилого віку з тривалим анамнезом діабету й обмеженою очікуваною тривалістю життя, тяжкими ССЗ або іншими коморбідними станами. Украй важливо уникати гіпоглікемій, які суттєво погіршують прогноз, підвищуючи ризик ішемії міокарда, аритмій і смерті.
Що стосується застосування ацетилсаліцилової кислоти (АСК) для первинної профілактики, то вона не показана пацієнтам із помірним ризиком, але може призначатись особам із високим і дуже високим ризиком у комбінації з інгібітором протонної помпи (ІПП) для зменшення ризику кровотечі. Сучасні концепції впливу на фактори ризику ССЗ підсумовано на рисунку 1. Максимальну ефективність забезпечує багатофаторний підхід: одночасне досягнення цільових рівнів систолічного АТ, ХС ЛПНЩ та HbA1c знижує ризик серцево-судинних ускладнень на 75%.
Ведення ІХС
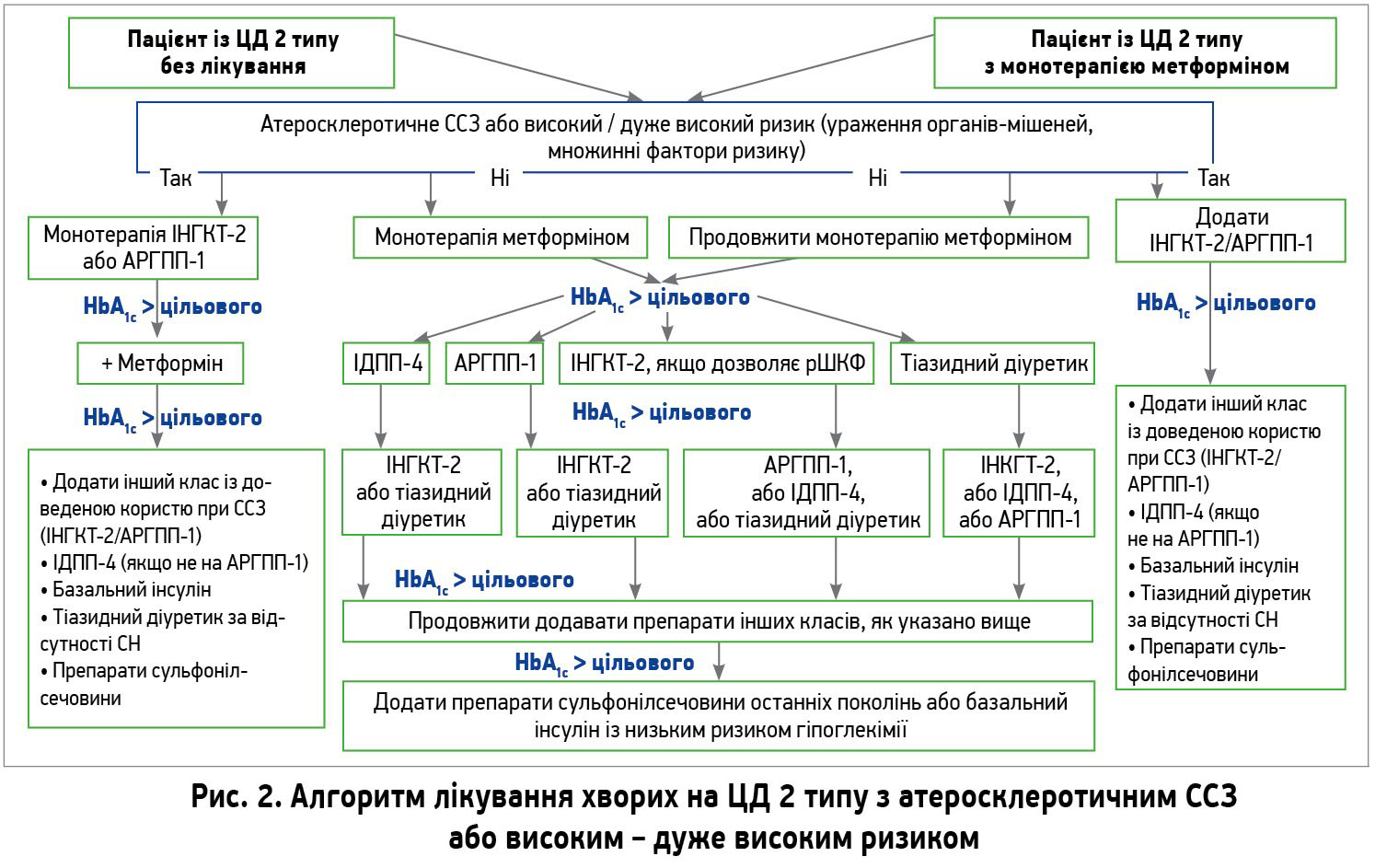
У пацієнтів із гострим і хронічним коронарними синдромом часто діагностують діабет або предіабет, що значно погіршує прогноз. Тому всі пацієнти з ІХС потребують систематичної оцінки глікемічного статусу для вчасного виявлення й корекції вказаних порушень. Інтенсивний контроль глікемії має сприятливіший вплив на перебіг ССЗ за умови ранньої ініціації. Лікарські засоби для контролю глікемії можна класифікувати на п’ять класів: інсуліносенситайзери – метформін, піоглітазон; інсулінопровайдери – інсулін, препарати сульфонілсечовини та меглітиніди; інкретинова терапія – інгібітори дипептидилпептидази‑4 (ІДПП‑4) й агоністи рецептора глюкагоноподібного пептиду‑1 (АРГПП‑1); інгібітори зворотного захоплення глюкози в нирках – інгібітори натрій-глюкозного котранспортера 2 типу (ІНГКТ‑2); інгібітори абсорбції глюкози в кишечнику – акарбоза. Вперше отримано докази про переваги ІНГКТ‑2 та АРГПП‑1 у хворих на ЦД 2 типу із ССЗ або високим – дуже високим ризиком, що змінило парадигми лікування й дало змогу створити алгоритм гіпоглікемічної терапії (рис. 2).
Отож для зменшення ризику серцево-судинних подій пацієнтам цієї категорії рекомендовано ІНГКТ‑2 емпагліфлозин, канагліфлозин, дапагліфлозин або АРГПП‑1 ліраглутид, семаглутид, дулаглутид (І, А), а для зменшення ризику смерті – емпагліфлозин і ліраглутид (І, В). Бігуанід метформін має розглядатися в пацієнтів із ЦД 2 типу без ССЗ із помірним ризиком (ІІа, С). Призначення інсуліну доцільне в пацієнтів із ГКС і гіперглікемією >10 ммоль/л до досягнення цільових рівнів відповідно до коморбідності (ІІа, С). Пацієнтам із серцевою недостатністю (СН) не рекомендовано тіазолідиндіони (ІІІ, А) й ІДПП‑4 саксагліптин (ІІІ, В).
Для зниження ризику серцево-судинних подій хворим на ІХС із ЦД показані ІАПФ або БРА, статини й АСК у дозі
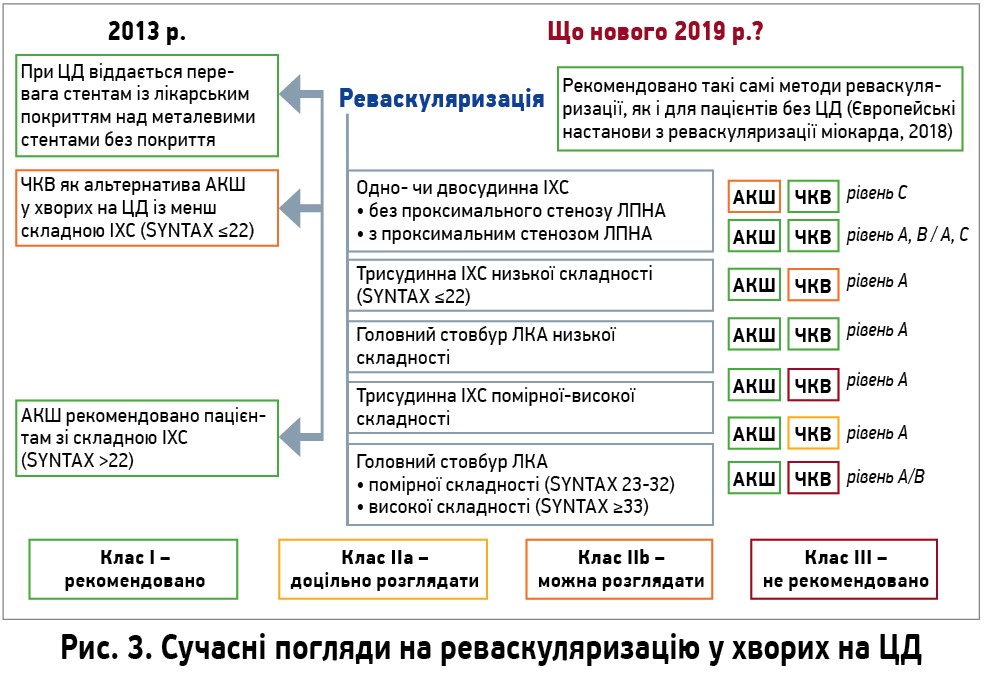
Реваскуляризація
У хворих на ЦД сучасні настанови рекомендують застосовувати ті самі методи реваскуляризації, що й у пацієнтів без ЦД (І, А). В осіб, які приймають метформін, рекомендовано перевірити функцію нирок безпосередньо перед ангіографією або ЧКВ, а в разі її погіршення – відмінити метформін (І, С). Принципи вибору методу реваскуляризації підсумовано на рисунку 3. За відсутності неконтрольованих ішемічних симптомів, великих ділянок ішемії чи значних уражень головного стовбура лівої коронарної артерії (ЛКА) чи проксимального стенозу лівої передньої низхідної артерії (ЛПНА) найкращим методом лікування хворих на ЦД із хронічним коронарним синдромом вважається оптимальна медикаментозна терапія (ІІа, В).
Ведення пацієнтів із СН
Пацієнти з діабетом і предіабетом мають підвищений ризик СН усіх фенотипів (рис. 4). Діастолічна дисфункція часто трапляється як при ЦД, так і в осіб із предіабетом, а її тяжкість корелює з інсулінорезистентністю та ступенем дисрегуляції глюкози. З іншого боку, СН підвищує ризик розвитку ЦД. Поєднання СН із діабетом підвищує ризик госпіталізації та смертності від СН, а також ризик загальної смертності.
Медикаментозна й апаратна терапія (ресинхронізаційна з або без імплантації кардіовертера-дефібрилятора – ІКД) однаково ефективна в усіх пацієнтів, незалежно від наявності ЦД (рис. 4). З огляду на те що у хворих на діабет частіше виникають гіперкаліємія та дисфункція нирок, рекомендовано коригувати дози деяких лікарських засобів, зокрема блокаторів РАС. Хворим на ЦД із багатосудинним ураженням коронарних артерій і СН зі зниженою фракцією викиду (ФВ) ЛШ рекомендовано АКШ (І, В).
Що стосується терапії ЦД, то за умови СН препаратами вибору є ІНГКТ‑2 емпагліфлозин, канагліфлозин або дапагліфлозин, оскільки вони сприяють зниженню ризику госпіталізації (І, А). Пацієнтам із рШКФ >30 мл/хв/1,73 м2 можна призначати метформін (ІІа, С). Інсулін (ІІb, С), АРГПП‑1 ліксисенатид, ліраглутид, семаглутид і дулаглутид (ІІb, A), а також ІДПП‑4 ситагліптин і лінагліптин мають нейтральний вплив на ризик СН і можуть призначатися (ІІb, В). Натомість ІДПП‑4 саксагліптин і тіазолідиндіони (піоглітазон, розиглітазон) пацієнтам із СН не рекомендовано через погіршення перебігу та підвищений ризик госпіталізації (ІІІ, А/В).
Ведення аритмій
У хворих на ЦД часто виникає фібриляція передсердь (ФП), що суттєво підвищує захворюваність і смертність. Отож усім пацієнтам віком понад 65 років рекомендовано скринінг ФП методом пальпації пульсу чи носіння пристроїв із подальшим підтвердженням на ЕКГ (IIa, C). Усім пацієнтам із ФП показані антикоагулянти. За відсутності протипоказань хворим на ЦД віком понад 65 років та оцінкою ≥2 за шкалою CHA2DS2-VASc показані НОАК, яким віддається перевага перед антагоністами вітаміну К (I, A). Якщо оцінка за шкалою CHA2DS2-VASc <2 або вік пацієнта менш як 65 років, питання про призначення оральних антикоагулянтів треба вирішувати індивідуально (IIa, C). Призначаючи антитромботичну терапію таким пацієнтам, треба оцінювати ризик кровотеч за шкалою HAS-BLED (IIa, C).
Пацієнти з ЦД мають також підвищений ризик раптової серцевої смерті (РСС), насамперед жінки. Через те у хворих на діабет із СН потрібно регулярно вимірювати тривалість QRS та ФВ ЛШ із метою визначення потреби в ресинхронізації міокарда з або без ІКД. Показаннями до ІКД у хворих на діабет є: 1) симптоматична СН (II-III класу за NYHА) з ФВ ЛШ ≤35% після 3 міс оптимальної фармакотерапії за умови, що очікувана тривалість життя становить хоча б 1 рік із добрим функціональним статусом; 2) документована фібриляція шлуночків або гемодинамічно нестабільна шлуночкова тахікардія за відсутності оборотних причин або терміну до 48 год після гострого ІМ (I, A). Для запобігання РСС у хворих на діабет із СН із ФВ ЛШ <40% після гострого ІМ рекомендовано ББ (I, A). Хворим на діабет із перенесеним ІМ або СН доцільно проводити скринінг факторів ризику РСС, особливо вимірювання ФВ ЛШ (IIa, C). Пацієнтам із частою шлуночковою екстрасистолією треба провести обстеження для виключення структурного захворювання серця (IIa, C).
Атеросклеротичне ураження периферичних артерій
Частим ускладненням ЦД є хвороба артерій нижніх кінцівок (ХАНК), поширеність якої збільшується пропорційно до тривалості ЦД та наявності інших факторів ризику. На будь-якій стадії ХАНК поєднання з діабетом асоціюється з гіршим прогнозом. Хворі на ЦД мають також вищий ризик хронічної ішемії, що загрожує втратою кінцівки (ХІЗВК) як першого прояву ХАНК, що зумовлює важливість щорічного скринінгу шляхом клінічної оцінки чи вимірюванням ГПІ для ранньої діагностики (І, С). Діагностичним для ХАНК є значення ГПІ <0,90 незалежно від симптомів. За наявності симптомів показане подальше обстеження, включно з дуплексною УСГ (І, С). У разі підвищеного ГПІ >1,40 показані інші неінвазивні тести, як-от індекс «великий палець – плече» чи дуплексна УСГ (І, С). Дуплексна УСГ є візуалізаційним методом першого вибору для оцінки анатомії та гемодинамічного статусу артерій нижніх кінцівок (І, С). КТ- або МРТ-ангіографія показані, коли планується реваскуляризація (І, С). Якщо в пацієнта є симптоми переміжної кульгавості з нормальними показниками ГПІ, треба провести тредміл-тест із визначенням ГПІ після навантаження (ІІа, С). У хворих на діабет із ХІЗВК та ураженнями нижче коліна перед реваскуляризацією треба розглядати проведення ангіографії з оцінкою кровообігу в стопі (ІІа, С). Усім хворим на ЦД рекомендовано навчання щодо догляду за стопами, особливо в разі ХАНК, навіть за відсутності симптомів. Рання діагностика втрати тканин і/або інфекції та скерування до мультидисциплінарної команди (діабетолог, судинний хірург) є дуже важливими для врятування кінцівок (І, С).
Ведення пацієнтів і показання до різних терапевтичних стратегій у хворих на ЦД не відрізняються від таких у інших пацієнтів, однак опції до реваскуляризації можуть бути гіршими у зв’язку з більш дифузним і дистальним ураженням. Хворим на ЦД із симптоматичною ХАНК рекомендовано антитромбоцитарну терапію (І, А). Оскільки ці пацієнти належать до групи дуже високого ризику, рекомендовано досягнути цільового рівня ХС ЛПНЩ <1,4 ммоль/л (<55 мг/дл) або хоча би на 50% від вихідного рівня (І, В). Пацієнтам із ХІЗВК рекомендовано оцінювати ризик ампутації, використовуючи шкалу WIfI (рана, ішемія, інфекція стопи) (І, В). У разі ХІЗВК реваскуляризація показана за будь-яких умов, якщо це сприятиме порятунку кінцівки (I, C). Для покращення клінічних наслідків у хворих на діабет із ХІЗВК необхідний оптимальний глікемічний контроль (IIa, C). У хворих на ЦД із хронічними симптомами ХАНК за відсутності високого ризику кровотечі слід розглядати комбінацію низької дози ривароксабану (2,5 мг 2 р/добу) з АСК у дозі 100 мг 1 р/добу (IIa, B).
Хронічна хвороба нирок
Асоціюється з високою поширеністю ССЗ, унаслідок чого цей стан віднесено до групи найвищого ризику. Як скринінговий тест хворим на ЦД рекомендовано щорічний підрахунок рШКФ і визначення відношення альбумін/креатинін у сечі (I, A). Оптимізація контролю глікемії та АТ із досягненням цільових рівнів HbA1c (<7,0%, або <53 ммоль/моль) уповільнює зниження функції нирок і запобігає мікросудинним ускладненням (I, A). Рекомендовано індивідуалізоване лікування хворих на діабет з АГ із досягненням цільового рівня АТ (рис. 1). Препаратами вибору для контролю АТ у пацієнтів з альбумінурією, протеїнурією чи гіпертрофією ЛШ є ІАПФ або БРА, оскільки зниження альбумінурії асоціюється з ренопротекторним ефектом (I, A). Нещодавно отримано докази того, що ІНГКТ‑2 емплагліфлозин, канагліфлозин, дапагліфлозин (I, B) та АРГПП‑1 ліраглутид і семаглутид (IIa, B) забезпечують ренопротекторний ефект і мають призначатися за умови рШКФ у діапазоні від 30 до 90 мл/хв/1,73 м2.
Підготувала Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 19 (464), жовтень 2019 р.