19 лютого, 2020
Анатомія стресового нетримання сечі у жінок
 Нетримання сечі зустрічається у кожної 3‑4-ї жінки після 40 років, і деякі автори називають цю патологію «соціальним раком» [37, 65, 67]. Ризик бути прооперованою з приводу нетримання сечі та випадання тазових органів у віці до 80 років мають 11,1% жіночого населення [70]. Саме з приводу стресового нетримання сечі у разі відсутності ефекту від консервативної терапії застосовують хірургічні реконструктивно-пластичні операції.
Нетримання сечі зустрічається у кожної 3‑4-ї жінки після 40 років, і деякі автори називають цю патологію «соціальним раком» [37, 65, 67]. Ризик бути прооперованою з приводу нетримання сечі та випадання тазових органів у віці до 80 років мають 11,1% жіночого населення [70]. Саме з приводу стресового нетримання сечі у разі відсутності ефекту від консервативної терапії застосовують хірургічні реконструктивно-пластичні операції.
Чітке знання анатомії нижніх сечових шляхів жінки, розуміння механізму утримання сечі та патофізіології її нетримання необхідне будь-якому спеціалісту (урологу, акушеру-гінекологу, фізіотерапевту, невропатологу), який займається діагностикою та лікуванням нетримання сечі у жінок. Із всіх видів нетримання сечі частка стресового нетримання складає 50‑75% [2, 5, 6, 12, 15, 16, 19, 20, 24, 31‑34, 45, 53, 64, 65, 67, 81, 85]. На жаль, в україномовних підручниках з урології, гінекології, анатомії, топографічної анатомії та оперативної хірургії питання анатомії, фізіології та патофізіології сфінктерного апарату уретри у жінок, а також механізму утримання сечі зовсім не висвітлені. А тому оперуючому урологу чи гінекологу складно вибрати необхідий вид хірургічного втручання для конкретної хворої зі стресовим нетриманням сечі, адже сьогодні існує понад 200 методик хірургічного лікування цієї патології.
Анатомічні особливості сфінктерного апарату сечового міхура та уретри у жінок
Сечовий міхур (СМ) та сечівник відносять до нижніх сечовивідних (сечових) шляхів. Анатомічно вони тісно пов’язані між собою та утворюють єдину функціональну систему, яка забезпечує резервуарну (накопичення та утримання сечі), евакуаторну (виділення сечі) та вентильну (перешкоджання зворотному руху сечі у сечоводи) функції [1, 4, 8, 12, 17, 18, 25, 28, 37, 43, 44, 64, 65, 85]. Стресове нетримання сечі – захворювання, яке є порушенням накопичувальної функції СМ.
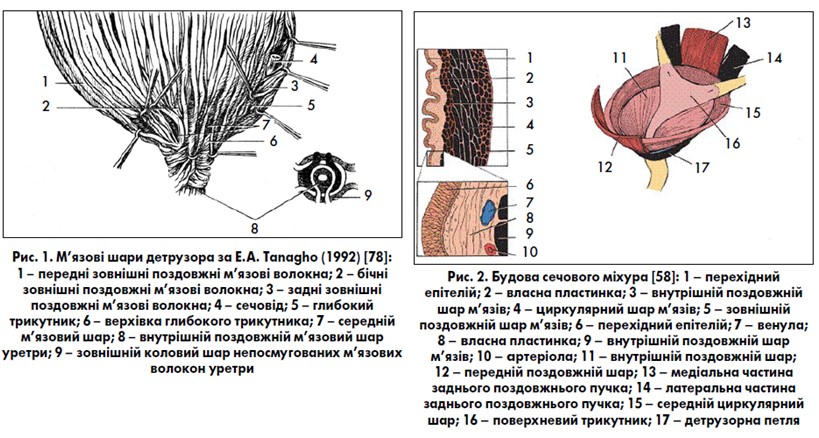
Сечовий міхур – непарний порожнистий м’язовий орган, об’єм якого у нормі становить 250‑500 мл. Стінка СМ складається зі слизової оболонки, підслизової основи, м’язової та серозної оболонок. М’язова оболонка представлена трьома шарами непосмугованих м’язів: зовнішнім і внутрішнім поздовжніми та середнім циркулярним (коловим). Особливість анатомічної структури м’яза, що виштовхує сечу (детрузора), полягає у тому, що в ділянці верхівки, тіла та дна він являє собою єдину систему взаємопов’язаних, поздовжньо та спірально орієнтованих м’язових пучків, які лише в ділянці шийки СМ концентруються у чітко диференційовані шари з утворенням окремих, але взаємопов’язаних, специфічних у функціональному відношенні м’язових структур. У ділянці шийки СМ м’язові волокна набувають вигляду кілець, що переплітаються.
Другою особливістю непосмугованих м’язів СМ є те, що в процесі еволюції вони потрапили під вольовий контроль. Внутрішній поздовжній шар СМ має радіальний вигляд, у ділянці шийки пучки концентруються навколо поздовжньої осі, після проходження шийки формують внутрішній поздовжній м’язовий шар уретри, який простягається по всій її довжині аж до зовнішнього отвору. Пучки середнього колового шару закінчуються в ділянці шийки СМ, не продовжуючись на сечівнику. Кількість циркулярно орієнтованих пучків (до 2 см шириною) значно виражена в ділянці передніх та бічних відділів шийки СМ, ззаду вони зливаються із глибоким сечоміхуровим трикутником. Цю структуру вперше описав R. Heiss (1915) [60, 61]. J. Hutch (1971) [62] середній коловий м’язовий шар у ділянці шийки СМ із глибоким сечоміхуровим трикутником назвав «кільцем основи сечового міхура» (рис. 1, 2). Це утворення є найменш розтяжною частиною СМ і перекриває отвір у шийці у фазу його наповнення. При акті сечовипускання кільце основи лійкоподібно витягується та відкриває внутрішній отвір уретри. Зовнішній поздовжній шар найбільш виражений на передній та задній поверхнях СМ, формує шар радіально розташованих м’язових пучків навколо внутрішнього отвору уретри, які при зливанні утворюють петлі. Задня група пучків зовнішнього м’язового шару довша та більш виражена, формує кільцеподібну передню детрузорну петлю. М’язові пучки зовнішнього поздовжнього шару переходять на проксимальну частину сечівника і утворюють коловий (напівколовий, оскільки покриває лише передню та бічні поверхні) м’язовий шар уретри, розташований над внутрішнім поздовжнім шаром. Частина передніх пучків зовнішнього м’язового шару у жінок прикріплюється до лобково-уретральної зв’язки і сприяє відкриттю шийки СМ під час сечовипускання (деякі анатоми називають цю частину зв’язки лобково-міхуровим м’язом). Міхуровий відділ сечовода має довжину близько 1,5 см, його поділяють на дві частини: інтрамуральний сегмент, повністю оточений стінкою СМ, та підслизовий (близько 0,8 см), що знаходиться безпосередньо під слизовим шаром СМ. М’язові волокна сечовода входять в основу СМ і змішуються з його м’язами в межах сечоміхурового трикутника Льєто.
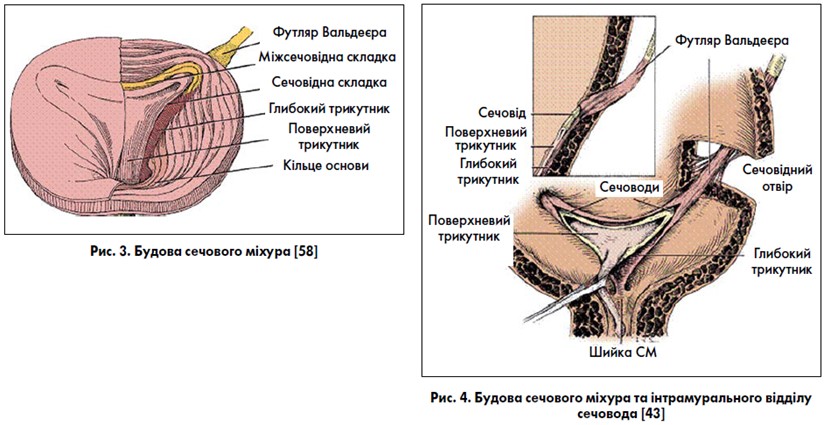
Дистальні 3‑4 см сечовода, як і його інтрамуральний відділ, оточені фіброзно-м’язовим футляром Вальдеєра, який додатково фіксує сечовід до детрузора. Сечоміхуровий трикутник має поверхневі та глибокі шари (рис. 3, 4). Поздовжні волокна інтрамурального відділу сечовода розходяться біля вічка останнього й утворюють поверхневий шар сечоміхурового трикутника, далі продовжуючися по середній лінії задньої стінки уретри аж до її зовнішнього отвору. Волокна поверхневого трикутника утворюють потовщення: між сечовідними отворами – складку Мерсьє, між сечовідним отвором та внутрішнім отвором уретри – м’яз Bell. Поверхневий трикутник знаходиться у СМ над його середнім коловим м’язовим шаром. Всі волокна футлярів Вальдеєра обох сечоводів простягаються до основи СМ та утворюють глибокий шар сечоміхурового трикутника, який найкраще виражений у ділянці міжсечовидної складки Мерсьє. Таким чином, обидва шари сечоміхурового трикутника зв’язані з нижніми відділами сечоводів, а сечоводи не закінчуються вічками, а продовжуються в основі СМ у вигляді пласких структур (сечоводи змінюють трубчасту форму на форму листка). Функція м’язових утворень трикутника полягає у запобіганні зворотному потраплянню (рефлюксу) сечі у сечоводи та в координаційній діяльності внутрішнього отвору уретри (шийки СМ).
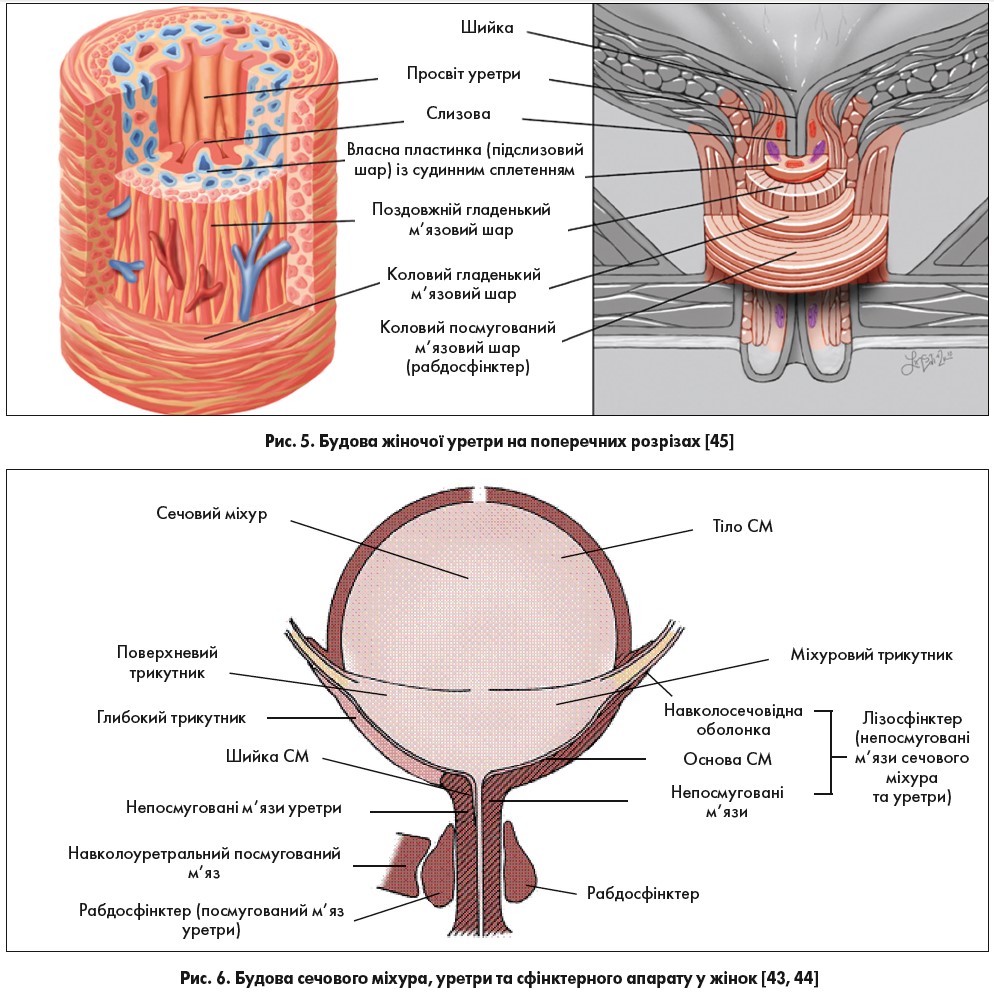
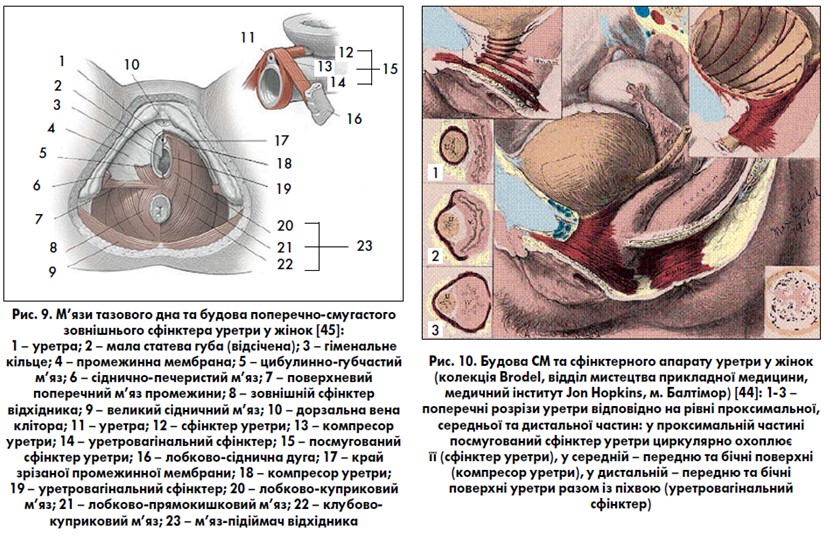
Уретра (сечівник) у жінок нагадує форму циліндра завдовжки 3,5‑4 см, який починається внутрішнім отвором у ділянці шийки СМ і закінчується зовнішнім отвором у присінку піхви на 2 см нижче клітора. Діаметр уретри – близько 6 мм. Стінка жіночої уретри складається із слизової оболонки, підслизового та м’язового шарів [7]. Підслизовий шар уретри представлений пухкою сполучною тканиною зі значною кількістю еластичних та колагенових волокон, що дає можливість їй легко розширятись до 9 мм при проведенні інструментів. Підслизовий шар також пронизаний тонкими непосмугованими м’язовими пучками та судинним артеріовенозним комплексом, який утворює губчасту тканину й заповнює простір між слизовою та іншими шарами стінки уретри у вигляді «надувної подушки», сприяє герметичному закриттю уретри та утриманню сечі. Деякі автори називають його «слизовим» сфінктером, він знаходиться під гормональним контролем і за недостатньої кількості естрогенів (у період менопаузи) атрофується. М’язова оболонка сечівника складається із двох непосмугованих м’язових шарів: внутрішнього поздовжнього та середнього колового (рис. 5). М’язові шари є продовженням непосмугованих м’язових шарів СМ. Внутрішній поздовжній м’язовий шар СМ після проходження шийки формує внутрішній поздовжній м’язовий шар уретри. М’язові пучки зовнішнього поздовжнього шару СМ переходять на проксимальну частину сечівника й утворюють коловий м’язовий шар, розташований над внутрішнім поздовжнім шаром. Таким чином, усі описані непосмуговані м’язові структури уретри (переважно за рахунок її проксимального відділу), а також м’язові структури шийки СМ (передня та задня петлі, тригональне кільце) являють собою внутрішній сфінктер уретри (внутрішній сфінктерний механізм) (рис. 6). Цей сфінктер не анатомічний, а фізіологічний [64]. Непосмуговану мускулатуру уретри разом із шийкою СМ називають також лізосфінктером [43, 44]. Скорочення поздовжнього непосмугованого м’язового шару СМ призводить до розширення просвіту уретри, що сприяє акту сечовипускання; розслаблення – до подовження, що сприяє утриманню сечі у СМ. Для нормальної роботи сфінктерного апарату уретри та СМ велике значення має збереження іннервації цих органів [12, 13, 20, 33, 48, 54, 81, 85].
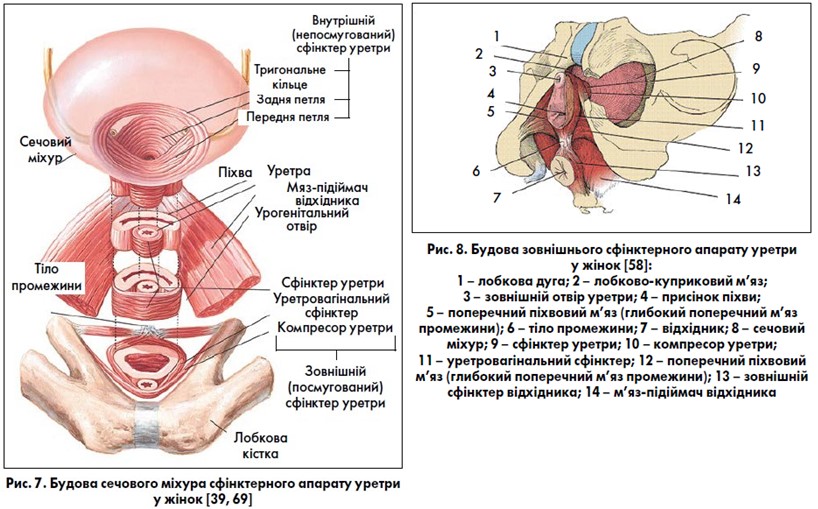
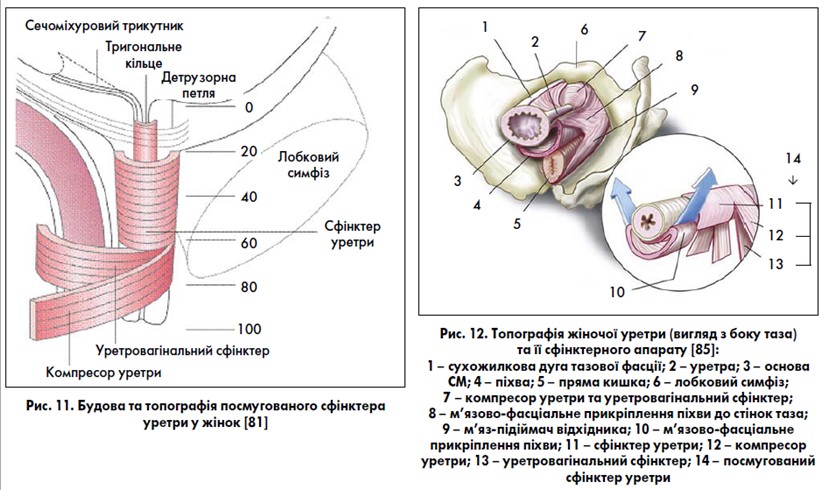
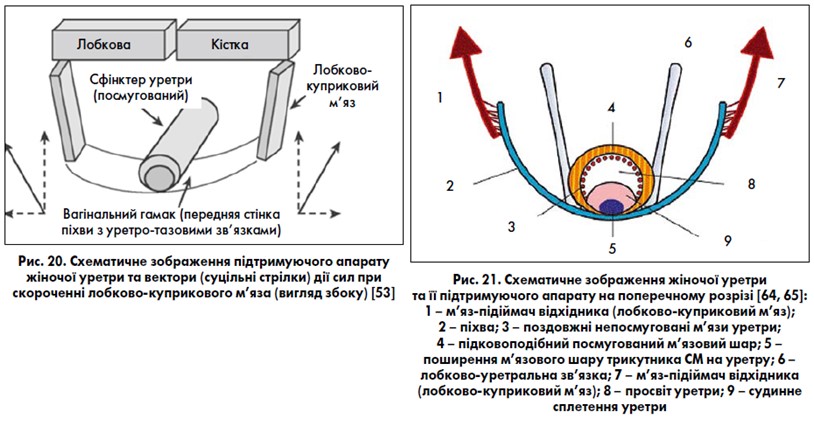
Зовнішній сфінктер уретри представлений посмугованими м’язами, які ембріологічно поріднені з мускулатурою тазового дна, але анатомічно відрізняються. У стінці уретри поверх колового непосмугованого м’язового шару розташований посмугований шар м’язів – сфінктер уретри. Його також називають рабдосфінктером (рис. 6) [43, 44]. За даними E. A. Tanagho (1992) [78], він знаходиться в ділянці середньої третини уретри, є більш чи менш повним кільцем навколо неї, за винятком її задньої поверхні. Сфінктер уретри є частиною зовнішнього сфінктера уретри, інші дві частини зовнішнього сфінктера уретри розташовані поза її стінкою. Сучасними дослідженнями [38, 39, 56, 58, 59, 69, 79, 82, 85] встановлено, що зовнішній сфінктер у різних місцях уретри має різну будову (рис. 7‑10). У проксимальній третині він повністю охоплює її у вигляді кільця (цю частину зовнішнього сфінктера уретри називають сфінктером уретри) і знаходиться зовні непосмугованого колового шару уретри. У середній третині уретри пучки зовнішнього сфінктера охоплюють лише її передню стінку й переходять на бічні стінки піхви. При скороченні волокон сфінктера цієї ділянки передня стінка уретри притискається до передньої стінки піхви, тому цю частину сфінктера називають ще компресором уретри. Дистальна частина зовнішнього сфінктера уретри охоплює передню та бічні стінки уретри разом із піхвою, цю частину сфінктера називають уретровагінальним сфінктером. У лікуванні стресового нетримання сечі для посилення тонусу зовнішнього сфінктера уретри і м’язів тазового дна успішно використовують вправи за Кегелем та інтравагінальну (ректальну) електростимуляцію. Утриманню сечі у жінок також сприяє цибулинно-губчастий м’яз (m. bulbospongiosus), який діє як сфінктер навколо присінка піхви. Топографія уретри у жінок та парауретральних структур представлена на рис. 11, 12. Підтримуюча зв’язка клітора (її також називають передньою уретральною зв’язкою) та лобково-уретральна (задня уретральна) зв’язка формують петлю, яка підвішує уретру до лобкових кісток (рис. 13, 14).
Таким чином, функція внутрішнього сфінктера уретри та шийки СМ (внутрішнього сфінктерного механізму уретри) забезпечується структурами, які розташовані у стінці нижніх сечових шляхів: непосмугованими петльовими м’язами детрузора основи СМ та сечоміхурового трикутника; непосмугованими поздовжнім, коловим та посмугованим коловим м’язами проксимального відділу уретри; слизовою оболонкою та підслизовим судинним сплетенням уретри; сполучною тканиною уретри. Ці анатомічні утворення визначають пасивний (за відсутності фізичного напруження та підвищення внутрішньочеревного тиску) внутрішньоуретральний опір, або резистентність уретри. До структур, розташованих поза стінкою нижніх сечових шляхів, які забезпечують активне (при фізичному напруженні та підвищенні внутрішньочеревного тиску) утримання сечі, відносять: посмугований сфінктер сечостатевої діафрагми (уретровагінальний сфінктер, компресор уретри), м’яз-підіймач відхідника (m. levator ani) та тазову фасцію. Активному утриманню сечі в СМ сприяє також посмугований коловий м’яз проксимального відділу уретри (сфінктер уретри), розташований у її стінці. Одні автори [43, 73] вважають, що посмугований сфінктер уретри складається виключно із волокон, що повільно скорочуються, інші [78] – як із тих, що повільно скорочуються, так і з тих, що швидко скорочуються (подібно м’язам тазового дна). Повільні волокна при скороченні мають низьку амплітуду, але можуть підтримувати скорочення тривалий час. Швидкі волокна мають високу амплітуду скорочення, але підтримують його короткий період часу. Повільні волокна складають 35% всієї маси зовнішнього посмугованого сфінктера уретри, швидкі – 65%. Перші необхідні для підтримання постійного тонусу, другі – для негайного скорочення, яке виникає у випадку підвищення внутрішньочеревного тиску. У спокою внутрішньоуретральний опір (резистентність уретри) на третину зумовлений тонусом посмугованого сфінктера уретри, на третину – непосмугованих м’язів уретри та на третину – слизовим і підслизовим шарами уретри [43, 73, 78].
М’язово-фасціальний апарат підтримки уретри та сечового міхура
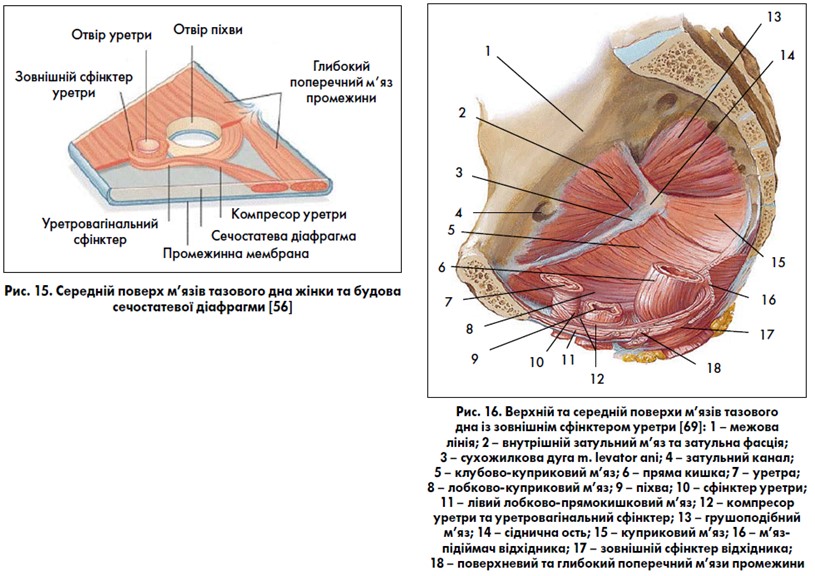
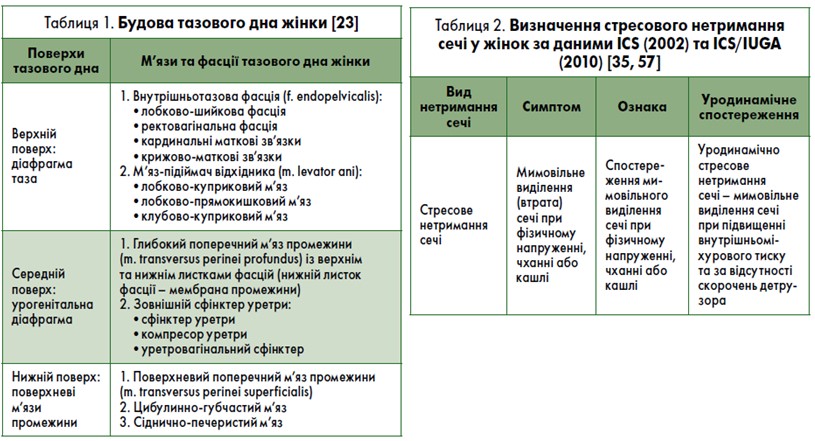
Для нормального функціонування акту сечовипускання та утримання сечі велике значення має взаємоспіввідношення нижніх сечових шляхів жінки та м’язово-фасціальних структур таза, особливо підтримка шийки СМ та проксимального відділу уретри. Тазове дно є основною опорою для органів черевної порожнини та малого таза, що забезпечує їх фізіологічне положення, створює опір внутрішньочеревному тиску та бере участь в утриманні сечі. Фасція – фіброзно-м’язова тканина, яка підвішує чи укріплює органи, а також зв’язує їх із м’язами. Виражені потовщення фасцій можуть мати назву зв’язок [22, 34]. Фасції укріплюють та підтримують стінки органів, а зв’язки – підвішують ці органи. Крім цього зв’язки грають роль опори для прикладання м’язових сил. М’язові зусилля розтягують органи, тим самим підтримуючи їхню форму та натяг. Зв’язки таза жінки мають свої особливості: вони є умовно виділеними відділами фасцій (в основному – внутрішньотазової фасції); фасції містять значну кількість м’язових елементів, що дає можливість їм скорочуватися й створювати тонус тазового дна. Порушення або ушкодження м’язово-фасціальних утворень тазового дна жінки (під час пологів, хірургічних операцій на тазових органах) призводить до пролапсу тазових органів та порушення їхньої функції. Більш детальна анатомія тазового дна жінки представлена в [1, 8, 12, 14, 21, 24, 39, 40, 46, 47, 49‑53, 56, 58, 79, 82], а також у табл. 1 та на рис. 9, 15‑17.
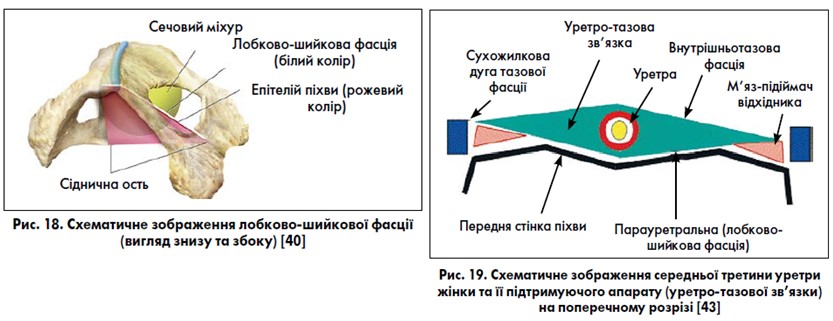
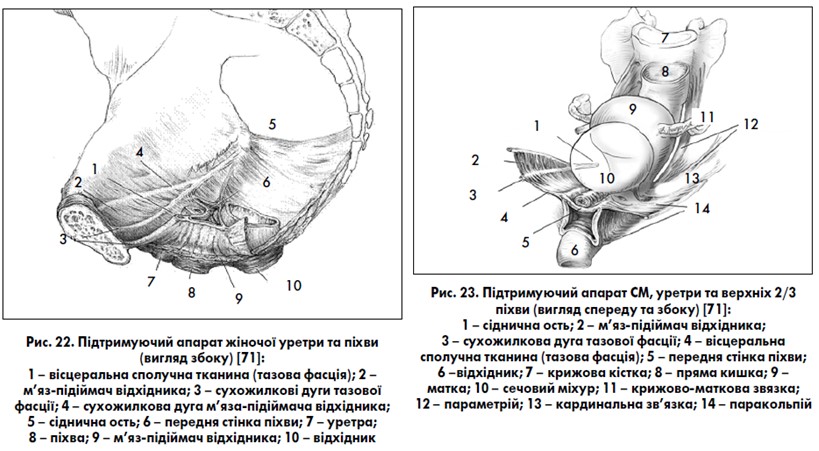
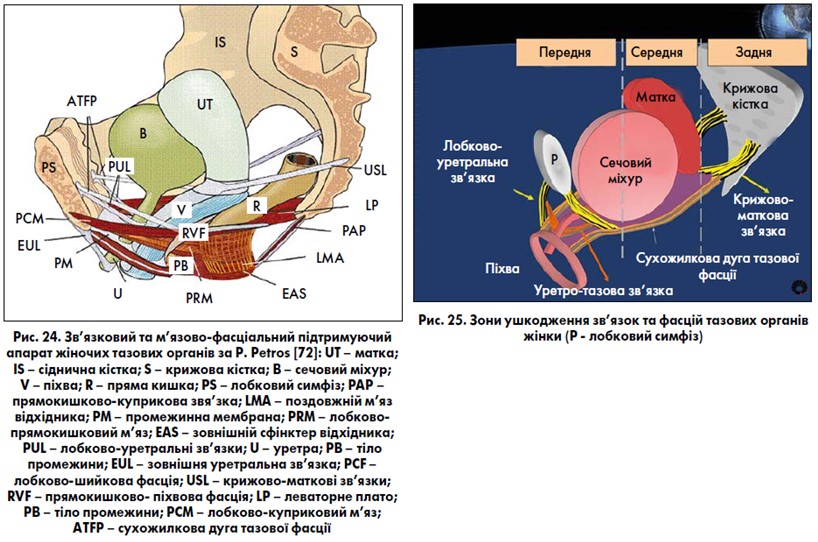
Між парієтальною очеревиною та мязом – підіймачем відхідника розташовується фіброзно-м’язoва тканина – тазова (внутрішньотазова) фасція. Вона починається від бічних стінок таза й оточує тазові органи, фіксує та стабілізує їх положення (рис. 18‑24). Тазова фасція нагадує гамак, що натягнутий між передньою, задньою та бічними стінками малого таза й охоплює своєю центральною частиною шийку матки, сечоміхуровий трикутник та уретру. У тазовій фасції виділяють кардинальні, крижово-маткові зв’язки, лобково-шийкову та прямокишково-піхвову фасції (рис. 17). Частина тазової фасції, яка проходить донизу по передній стінці піхви, називається лобково-шийковою фасцією (рис. 18). Остання приєднується до передньої поверхні шийки матки. У верхній частині піхви лобково-шийкова фасція приєднується до волокон кардинально-матково-крижового зв’язкового комплексу. Уздовж піхви лобково-шийкова фасція утворює волокна – бічні зв’язки, які з’єднують піхву із стінками таза впродовж сухожилкової дуги тазової фасції Лінія прикріплення лобково-шийкової фасції до сухожилкової дуги тазової фасції утворює передні латеральні борозни піхви (рис. 22, 23). Дистальніше лобково-шийкова фасція проходить під лобковим симфізом і зливається з мембраною промежини. Частину тазової фасції, яка проходить по задній стінці піхви, називають прямокишково-піхвовою фасцією (ректовагінальною перегородкою), або фасцією Денонвільє. У промежині прямокишково-піхвова фасція зливається із мембраною промежини. Лінія прикріплення піхви до ректовагінальної перегородки утворює задні латеральні борозни піхви.
За рахунок ущільнення ділянок тазової фасції (лобково-шийкової фасції), а також м’язових волокон тазового дна виділяють (частіше в урологічній літературі): лобково-уретральні зв’язки, які з’єднують внутрішню поверхню лобкового симфізу та середню частину уретри; уретро-тазові зв’язки, які з’єднують уретру із сухожилковою дугою тазової фасції (рис. 19). Ці зв’язки у комплексі із м’язово-фасціальними утвореннями тазового дна забезпечують нормальне анатомічне положення уретри та основи СМ в порожнині таза, уретро-везикальний кут та пасивне утримання сечі при підвищенні внутрішньочеревного тиску. Скорочення m. levator ani збільшує натяг цих зв’язок, створює опір внутрішньочеревному тиску, забезпечує притиснення уретри до передньої стінки піхви та утримання сечі (рис. 20, 21). Наступне ущільнення лобково-шийкової фасції – міхурово-тазова зв’язка, яка прикріплює основу СМ до сухожилкової дуги тазової фасції, при цьому підтримуючи СМ, передню стінку піхви та матку. Пошкодження (розриви) лобково-шийкової фасції призводять до утворення пролапсів уретри та СМ – уретроцеле, уретроцистоцеле, цистоцеле. Ушкодження прямокишково-піхвової фасції ведуть до утворення пролапсу прямої кишки – ректоцеле. Більш детальна інформація про м’язово-фасціальну підтримку органів таза жінки за J. L. DeLancy та види пролапсів представлена у спеціальній літературі [8, 9, 12, 46, 47, 71, 75, 79, 83‑85].
Незважаючи на наявність такої м’язово-фасціальної підтримки уретри та СМ, сучасні дослідження взаємоспіввідношень між уретрою та тазовим дном виявили, що лише в дистальній частині уретра знаходиться у фіксованому стані (за допомогою сечостатевої діафрагми та нижньої частини посмугованого сфінктера уретри), верхні 2/3 уретри є рухомими. Сполучна тканина фасцій та зв’язок таза залежить від гормонального статусу жінки, особливо під час вагітності та пологів, а також у період старіння організму. P. Petros (2007, 2015) [22, 72] виділяє три зони ушкодження підтримуючих зв’язок, фасцій тазових органів і тазового дна жінки (рис. 25): 1) передня – простягається від зовнішнього отвору уретри до шийки СМ (включає лобково-уретральні зв’язки, субуретральний гамак та зовнішню уретральну зв’язку); 2) середня – простягається від шийки СМ до шийки матки чи купола піхви після гістеректомії (включає лобково-шийкову фасцію, сухожилкову дугу тазової фасції, кардинальні зв’язки та парацервікальне фіброзне кільце); 3) задня – простягається від шийки матки (купола піхви після гістеректомії) до тіла промежини (включає крижово-маткові зв’язки, прямокишково-піхвову фасцію та тіло промежини). Порушення фасцій та зв’язок першої зони проявляється клінічно стресовим нетриманням сечі, другої – різними видами цистоцеле, третьої – ентероцеле, пролапсом матки або купола піхви (у разі перенесеної гістеректомії), ректоцеле.
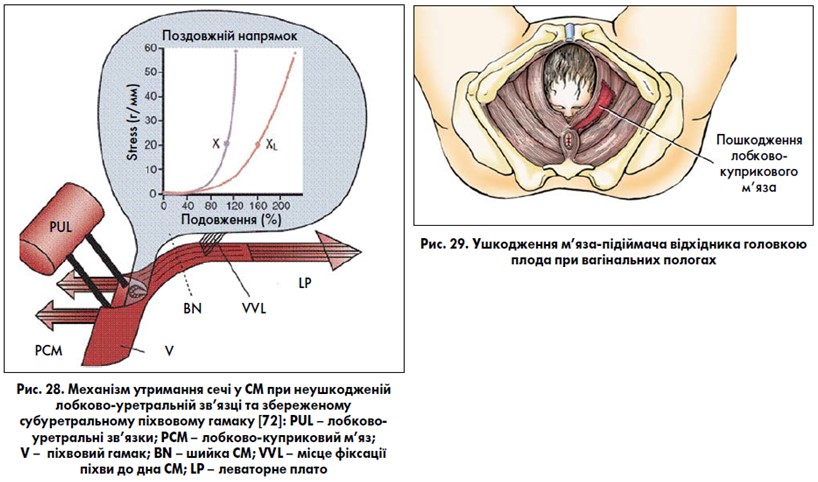
Існують дві антагоністичні сили при роботі непосмугованих м’язових волокон шийки СМ. Скорочуюча система включає: 1) волокна середнього м’язового шару детрузора навколо шийки, які відтягують її краніально; 2) петлі м’язів детрузора навколо шийки, які звужують її просвіт. Ці циркулярні волокна створюють задній уретро-везикальний кут. Дилатаційна система шийки СМ представлена передніми та задніми поздовжніми м’язовими пучками зовнішнього шару детрузора (див. рис. 2). При сечовипусканні скорочення цих м’язових волокон призводить до опущення та відкриття шийки СМ, яка набуває лійкоподібної форми (рис. 26). Відкриттю шийки сприяють скорочення внутрішніх поздовжніх волокон трикутника СМ та уретри по всій її довжині, а також релаксація м’язових компонентів лобково-уретральної зв’язки (деякі автори цю частину лобково-уретральної зв’язки називають лобково-міхуровим м’язом) [46, 82]. Роль посмугованого зовнішнього сфінктера уретри в пасивному утриманні сечі обмежена. Посмугований сфінктер спрацьовує при невідкладному позиві до сечовипускання, при переміщенні тіла із горизонтального положення у вертикальне, при фізичному навантажені, а також у процесі зупинки акту сечовипускання. Рефлекс скорочення посмугованого сфінктера спрацьовує раніше, ніж відбувається зміна тиску в СМ. У процесі зупинки сечовипускання м’язи компресора уретри та уретровагінального сфінктера стискають уретру в середній частині та разом із m. bulbospongiosus тягнуть донизу й каудально дистальний відділ уретри; лобково-куприковий м’яз (частина m. levator ani) та лобково-міхуровий м’яз тягнуть проксимальний відділ уретри догори й краніально. При цьому виникає ефект стискання та подовження уретри з одночасним підняттям шийки СМ на ±3 см (рис. 27). P. E. Petros (2007) [72] в утриманні сечі велике значення приділяє лобково-уретральним зв’язкам, які створюють «коліно» (вигин) утетри при дії протилежних сил – лобково-куприкового м’яза та леваторного плато (м’язово-зв’язкове утворення, яке складається із клубово-куприкового м’яза та прямокишково-куприкової зв’язки) (рис. 28). Подовження та вигин уретри дозволяє докласти значно менших сил (за рахунок внутрішнього та зовнішнього сфінктерних механізмів уретри) для її стиснення. Ш. Раз (2019) [27] порівнює уретру із садовим шлангом виходячи із фізичних законів: стиснути шланг та перервати струмінь води у ньому значно легше, коли під ним твердий ґрунт (мається на увазі субуретральний піхвовий гамак), а шланг має вигин (вигин уретри). Даний постулат підтримують більшість урологів та гінекологів [15, 53, 85].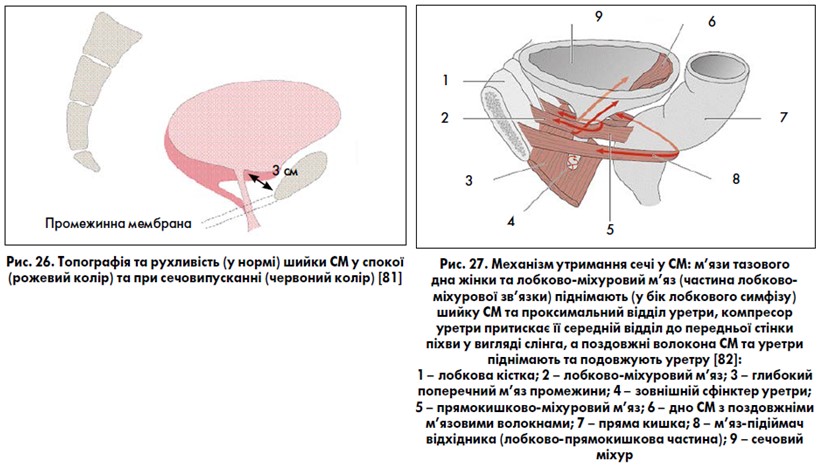
Нетримання сечі може бути міхуровим та уретральним (сфінктерним). Міхурове нетримання зумовлене гіперактивністю СМ (детрузора), поганою розтяжністю та податливістю його стінок, а також нездатністю детрузора до скорочення (нетримання сечі від переповнення СМ – парадоксальне нетримання сечі, або парадоксальна ішурія). При міхуровому нетриманні сечі підвищений внутрішньоміхуровий тиск перевищує нормальний внутрішньоуретральний. Уретральне стресове нетримання сечі називають сфінктерним, і воно пов’язане із нездатністю сфінктерного апарату уретри утримувати її в закритому стані під час фізичного напруження, кашлю, чхання та за інших станів, які ведуть до підвищення внутрішньочеревного тиску (під стресом розуміють підвищення внутрішньочеревного тиску, а не психологічний стан). Раніше (за часів СРСР) стресовим називали нетримання сечі при напруженні. У 2002 році Міжнародне товариство з вивчення утримання сечі (ICS), а згодом (2010) сумісно із Міжнародною урогінекологічною асоціацією (ІUGА) опублікувало оновлену термінологію та класифікацію дисфукцій нижніх сечовивідних шляхів та пролапсу жіночих тазових органів [35, 57]. Визначення стресового нетримання сечі у жінок представлено в табл. 2.
J. G. Blaivas та співавт. (1998) [41] виділяють такі основні фізіологічні уретральні фактори утримання сечі у СМ:
- змикання стінок уретри за рахунок багатоваскуляризованого слизового та підслизового шарів уретри;
- стиснення уретри за рахунок еластичності її тканин (наявність в уретрі колагену, еластину створює структуральну підтримку її тканин), наявності непосмугованих та посмугованих м’язів уретри;
- збережена м’язово-фасціальна підтримка уретри та СМ;
- збережений функціональний та невральний контроль уретри.
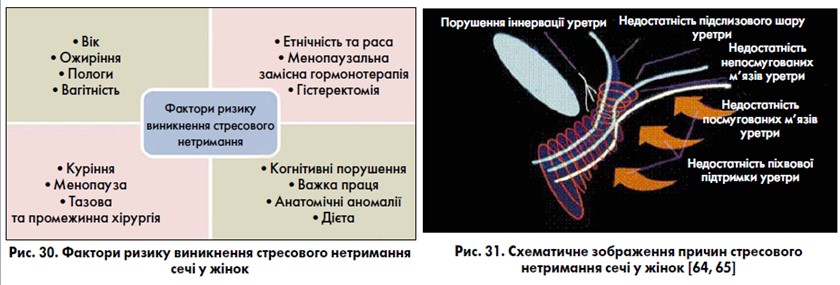
Стресове нетримання сечі буває двох видів: 1) анатомічним (гіпермобільність уретри) – у результаті ослаблення м’язово-фасціальної підтримки проксимального відділу уретри та шийки СМ виникає зміщення (опущення) міхурово-уретрального сегмента, втрата ним інтраабдомінальної позиції, що проявляється порушенням функції (нетриманням сечі) за стресових ситуацій; 2) недостатність функції сфінктерів уретри через пренесені раніше операції в ділянці шийки СМ та уретри, травми (пологової), опромінення, неврологічні розлади, а також недостатність естрогенів в організмі жінки в післяменопаузі. Необхідно пам’ятати про можливе поєднання цих двох видів нетримання, а також про те, що 10% жінок похилого віку мають первинну (ідеопатичну) недостатність функції сфінктерів уретри [41]. Основним етіологічним фактором розвитку стресового нетримання сечі є травматичні пологи із розтягненням, розривом та порушенням іннервації сфінктерного апарату уретри та підтримуючого м’язово-фасціально-зв’язкового апарату тазового дна (рис. 29).
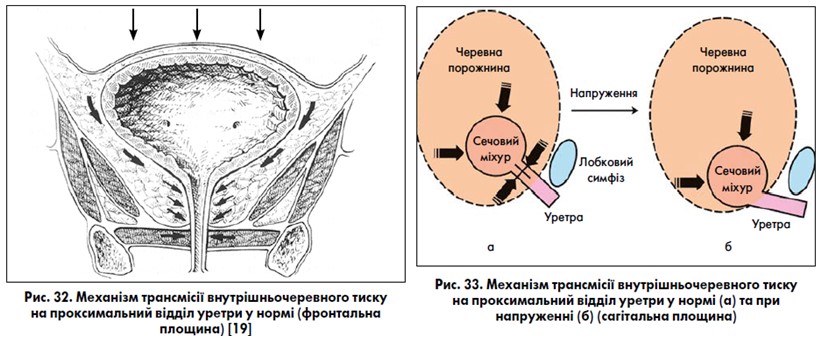
У патофізіології стресового нетримання сечі велике значення приділяється також сполучній тканині нижніх сечових шляхів, а також зв’язкам та фасціям. Найважливішими елементами сполучної тканини є колаген та еластин, структура яких змінюється під час вагітності, пологів та у процесі старіння. У результаті цього зв’язки та фасції можуть слабшати, розтягуватися, розриватися, що негативно позначається на функції нижніх сечових шляхів та утримання сечі [22, 72]. Порушення іннервації уретри та атрофія її багатоваскуляризованого підслизового шару («слизового сфінктера») у післяменопаузі є також важливими причинами виникнення стресового нетримання сечі у жінок. На рис. 30 представлені основні фактори ризику стресового нетримання сечі у жінок, серед яких найбільш вивченими та доведеними є вік, ожиріння, вагітність та пологи [2, 31, 36, 53, 65, 85].
На рис. 31 представлені основні патогенетичні чинники стресового нетримання сечі у жінок Міжнародної консультації (наради) із нетримання сечі (ІСІ, 2013, 2017).
Патофізіологія стресового нетримання сечі у жінок
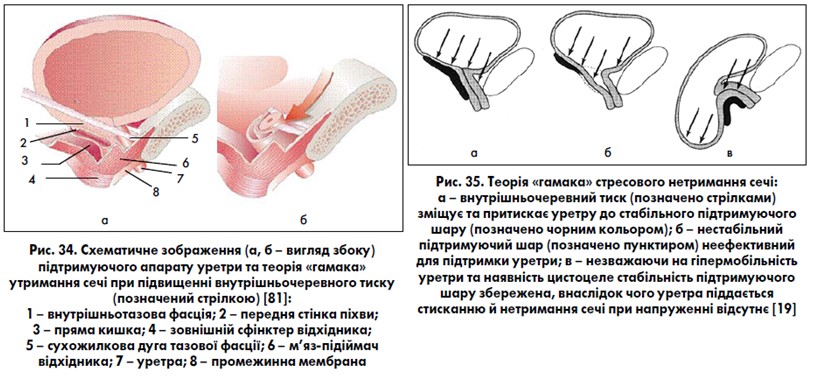
Теорія манометричного тиску в закритій порожнині (Enhorning G. E., 1961) [15, 19, 23, 24, 31, 32, 85] базується на уродинамічних поглядах: СМ та проксимальний відділ уретри знаходяться в черевній порожнині, що закрита знизу тазовим дном, і в нормі будь-яке підвищення внутрішньочеревного тиску передається на ці ділянки рівномірно (рис. 32, 33). При стресовому нетриманні сечі через ослаблення м’язово-фасціальних підтримуючих структур шийка СМ та проксимальний відділ уретри опускаються нижче рівня діафрагми таза, виходять із манометричної порожнини, на відміну від СМ. При цьому виникає нерівномірна передача внутрішньочеревного тиску: він передається на СМ і не передається на шийку СМ та проксимальний відділ уретри. Внутрішньоуретральний тиск стає меншим за суму внутрішньоміхурового та внутрішньочеревного тисків – виникає нетримання сечі.
Ця теорія набула популярності після впровадження операцій із підвішуванням піхви у високому залобковому положенні (залобкових кольпопексій та кольпосуспензій за Marshall-Marchetti-Krantz та Burch) у 50‑60-х роках минулого століття. На жаль, вона не роз’яснює, чому не у всіх жінок із опущенням шийки СМ та проксимального відділу уретри виникає стресове нетримання сечі. Крім того, проведені експерименти довели, що згідно з фізико-математичними розрахунками тиск із черевної порожнини не може передаватися на просвіт уретри. Уродинамічні дослідження також виявили, що тиск в уретрі при кашлі перевищує тиск у СМ ще до початку передачі внутрішньочеревного тиску, а практика показала, що лише одна передня кольпорафія без підняття та фіксації шийки СМ у високій залобковій позиції може бути успішною в лікуванні стресового нетримання сечі. Перед виконанням операцій із підвішуванням піхви хірург повинен визначити функціональний стан сфінктерного апарату уретри за допомогою уродинамічних досліджень, і в разі його порушення підвішуюча операція не показана, натомість пацієнтці потрібно виконати встановлення субуретрального слінга.
Теорія «гамака» (De Lancey J. O.L., 1994) [15, 19, 23, 24, 31, 32, 85]. Прибічники теорії вважають, що уретра лежить у гамакоподібному утворенні, сформованому тазовою фасцією та передньою стінкою піхви (рис. 34, 35). Стабільність цього «гамака» зумовлена тим, що латерально він прикріплений до внутрішніх країв m. levator ani за допомогою сухожилкової дуги тазової фасції. При підвищенні внутрішньочеревного тиску виникає сила, направлена вниз на вентральну (передню) поверхню уретри, що притискає її до «гамака». Від цілісності та стабільності цього шару залежить утримання уретри в порожнині таза та ефективність затульного механізму шийки СМ і проксимального відділу уретри.
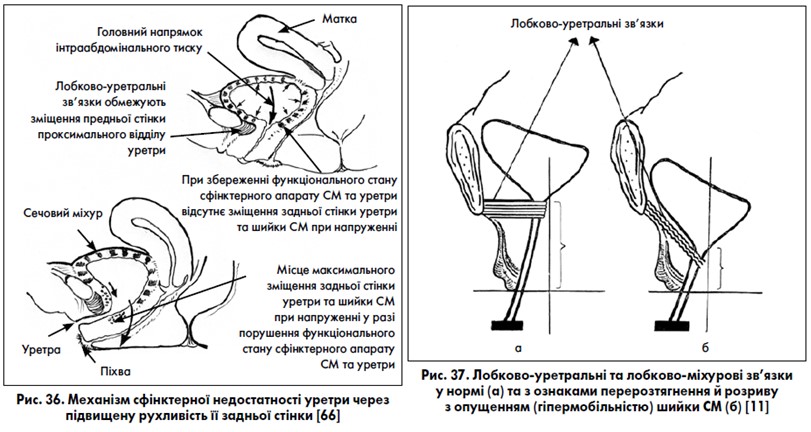
Теорія підвищеної рухливості задньої стінки уретри та шийки СМ. Деякі автори [66] пропонують такий механізм розвитку сфінктерної недостатності уретри та шийки СМ, який виникає внаслідок уретральної гіпермобільності (рис. 36). Вони вважають, що проксимальний відділ уретри та шийка СМ (їхні передні поверхні) міцно втримуються лобково-уретральними та лобково-міхуровими зв’язками. У хворих із гіпермобільністю уретри та ослабленням її задньої підтримки під час підвищення внутрішньочеревного тиску задня стінка уретри опускається значно більше, ніж передня. Це призводить до відкриття (провисання) проксимального відділу уретри та шийки СМ. Якщо сфінктерний апарат уретри та шийки СМ не ушкоджений, то він запобігає провисанню й відкриттю зазначених структур. Із виснаженням або ушкодженням сфінктерного апарату цих органів виникає стресове нетримання сечі. Уретроскопія із виявленням розширення шийки СМ та проксимального відділу уретри була й залишається одним із методів діагностики стресового нетримання сечі у жінок. Саме тому слінгові операції раніше були зосереджені на встановленні субуретральної петлі під проксимальним відділом уретри.
Теорія перерозтягнення та розриву лобково-уретральних та лобково-міхурових зв’язок. Х. Кремлинг (1985) [11], P. Petros (2007) [72] вважають, що причиною стресового нетримання сечі, крім ослаблення підтримуючих уретру та шийку СМ м’язово-фасціальних структур, є перерозтягнення та розрив лобково-уретральних та лобково-міхурових зв’язок, що призводить до опущення міхурово-уретрального сегмента, порушення передачі внутрішньочеревного тиску на уретру та виникнення стресового нетримання сечі (рис. 37). Сучасні ультразвукові та магнітно-резонансні дослідження підтверджують наявність перерозтягнення та розриву лобково-уретральних зв’язок.
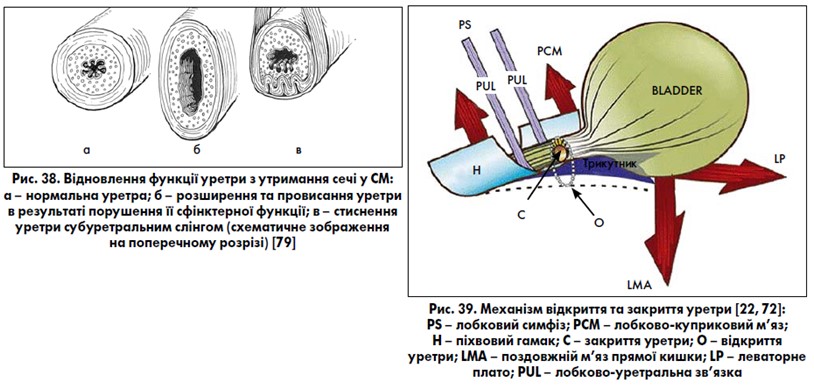
Теорія сфінктерної недостатності уретри. Теорії порушення сфінктерної функції уретри в етіології стресового нетримання сечі у жінок підтримується як урологами, так і гінекологами протягом останніх 100 років. Із впровадженням у практичну урогінекологію методів визначення функціонального стану уретри у жінок ця теорія є однією з основних. Було виявлено, що сфінктерна недостатність уретри виникає не лише після операцій на передній стінці піхви та органах тазового дна, травматичних пологів, попередніх антистресових операцій, опромінення органів таза, при гормональній недостатності у післяменопаузі, порушенні іннервації тазових органів, але може бути і вродженою та спадковою. Сфінктерна недостатність уретри зустрічається у жінок як із гіпермобільністю уретри, так і без неї. Порушення сфінктерної функції уретри вимагає виконання слінгової операції (у гінекологічній літературі – уретропексії) для стиснення уретри [18] (рис. 38).
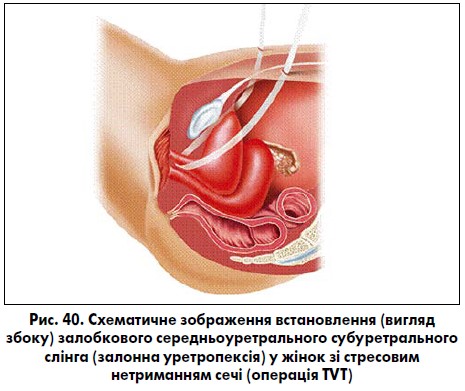
Інтегральна теорія виникнення стресового нетримання сечі у жінок, запропонована P. Petros та U. Ulmsten (1990, 1994) [22, 72], розглядає нормальну функцію тазового дна жінки як збалансовану та взаємопов’язану систему, що складається з м’язів, сполучної тканини та нервів. Сполучна тканина при цьому є найбільш уразливим компонентом системи. Згідно з цією теорією, закриття та відкриття уретри відбувається завдяки скороченню або розслабленню лобково-куприкового м’яза (PCM) (рис. 39). Уретра міцно фіксується лобково-уретральною зв’язкою (PUL) та передніми частинами лобково-куприкового м’яза, що дозволяє м’язам, які виконують тягу назад (LMA – поздовжній м’яз прямої кишки; LP – леваторне плато – м’язово-зв’язкове утворення, яке складається із клубово-куприкового м’яза та прямокишково-куприкової зв’язки), витягувати уретру та закривати її проксимальну частину (позначено літерою «с» – «closure», або закриття). Розслаблення лобково-куприкового м’яза дозволяє леваторному плато та поздовжньому м’язу прямої кишки відкрити просвіт уретри (позначено літерою «о» – «opening», або відкриття) під час сечовипускання (передня стінка піхви позначена пунктирною лінією). Порушення лобково-уретральної зв’язки, субуретрального піхвового гамака та зовнішньої уретральної зв’язки призводить до стресового нетримання сечі. P. Petros та U. Ulmsten запропонували залобковий синтетичний субуретральний пубо-вагінальний слінг (операція TVT, при якій синтетична поліпропіленова стрічка встановлюється під уретрою через розріз передньої стінки піхви без натягу) під середньою частиною уретри (де найбільший внутрішньоуретральний тиск) для заміщення втраченої функції лобково-уретральних зв’язок та лікування стресового нетримання сечі у жінок (рис. 40).
 Через високий ризик ушкодження СМ, судин, нервів, кишечника, затримки сечі у післяопераційному періоді та виходячи з положень інтегральної теорії Е. Delorm у 2001 р. запропонував встановлювати середньоуретральний слінг через затульний отвір (операція ТОТ).
Через високий ризик ушкодження СМ, судин, нервів, кишечника, затримки сечі у післяопераційному періоді та виходячи з положень інтегральної теорії Е. Delorm у 2001 р. запропонував встановлювати середньоуретральний слінг через затульний отвір (операція ТОТ).
Г. А. Савицкий та співавт. (2011) [29, 30] зазначають, що механізм утримання сечі у жінок при напруженні є складною та багатофакторною системою, де кожний елемент робить свій внесок у її успішне функціонування. Подальші наукові дослідження механізму утримання сечі та патофізіології стресового нетримання сечі у жінок, можливо, допоможуть практичним лікарям успішно лікувати таке поширене жіноче захворювання, адже сьогодні ані консервативне, ані хірургічне лікування не гарантує жінці 100-відсоткового успіху в одужанні.
Література
- Акушерство та гінекологія: у 4 т.: національний підручник / За ред. акад. НАМН України проф. В. М. Запорожана. – Т. 4: оперативна гінекологія. – К.: ВСВ «Медицина», 2014. – 696 с.
- Александров В. П., Куренков А. В., Николаева Е. В. Стрессовое недержание мочи у женщин. – С.‑ Петербург: Издательский дом СПб МАПО, 2006. – 94 с.
- Баггиш М. С., Каррам М. М. Атлас анатомии таза и гинекологической хирургии: Пер. с англ., 2-е изд. – Лондон: Elsevier Ltd., 2009. – 1180 с.
- Гаджиева З. К. Нарушения мочеиспускания: Руководство для врачей. – М.: ГЭОТАР-Медиа, 2010. – 176 с.
- Гаджиева З. К., Газимиев М. А., Касян Г. Р. Недержание мочи у женщин // Урология. – 2016. – № 2 (прил. 2). – С. 20‑37.
- Горовий В. І. Сучасні підходи до діагностики та лікування нетримання сечі у жінок. Деякі аспекти класифікації та лікуваня стресового нетримання сечі у жінок // Урологія. – 2012. – Т. 16, № 1 (60). – С. 21‑33.
- Горовий В. І. Захворювання уретри у жінок // Медичні аспекти здоров’я жінки. – 2015. – № 7 (93). – С. 42‑47.
- Запорожан В. М. Оперативна гінекологія. – Одеса: Одеський державний медичний університет, 2006. – С. 293‑315.
- Запорожан В. Н., Процепко О. О. Оперативное лечение урогенитального пролапса влагалищным доступом. – Одесса: Одесский медуниверситет, 2010. – 160 с.
- Илюхин Ю. А., Переверзев А. С., Щукин Д. В. и др. Урогинекологический атлас. – Белгород, 2001. – 272 с.
- Кан Д. В. Руководство по акушерской и гинекологической урологии, 2-е изд. – М.: Медицина, 1986. – 488 с.
- Клінічна анатомія сечостатевих органів / За ред. В. І. Горового, В. О. Шапринського, Б. Ф. Мазорчука. – Вінниця: Твори, 2016. – 640 с.
- Крупин В. Н., Белова А. Н. Нейроурология: Руководство для врачей. – М.: Антидор, 2005. – 464 с.
- Куликовский В. Ф., Олейник Н. В. Тазовый пролапс у женщин: Руководство для врачей. – М.: ГЭОТАР-Медиа, 2008. – 256 с.
- Недержание мочи у женщин: Методические рекомендации, 4-е изд. / О. Б. Лоран и др. – Москва, 2017. – 72 с.
- Нeймарк А. И., Раздорская М. В. Недержание мочи у женщин. – М.: ГЭОТАР-Медиа, 2013. – 128 с.
- Оперативна хірургія та топографічна анатомія: підручник / За ред. М. П. Ковальського. – К.: ВСВ «Медицина», 2010. – 504 с.
- Оперативная гинекология / В. И. Краснопольский, С. Н. Буянова, Н. А. Щукина, А. А. Попов. – 2-е изд., перераб. – М.: МЕДпресс-информ, 2013. – 320 с.
- Переверзев А. С. Клиническая урогинекология. – Харьков: Факт, 2000. – 360 с.
- Переверзев А. С., Козлюк В. А. Симптомы нижних мочевых путей. – Харьков: Факт, 2009. – 431 с.
- Перинеология: Болезни женской промежности в акушерско-гинекологических, сексологических, проктологических аспектах / Под ред. В. Е. Радзинского. – М.: ООО «Медицинское информационное агентство», 2006. – 336 с.
- Петрос П. Женское тазовое дно. Функции, дисфункции и их лечение в соответствии с интегральной теорией: пер. с англ. / Под ред. Д. Д. Шкарупы. – М.: МЕДпресс-информ, 2016. – 400 с.
- Петров С. Б., Куренков А. В., Шкарупа Д. Д., Карнаухов И. В. Механизм удержания мочи у женщин и предпосылки клинической эффективности синтетического среднеуретрального слинга // Журнал акушерства женских болезней. – 2009. – Т. LVIII, вып. 3. – С. 86‑94.
- Практична урогінекологія: курс лекцій / За ред. В. І. Горового. – Вінниця: Вінницька обласна друкарня, 2015. – 728 с.
- Пушкарь Д. Ю., Касян Г. Р. Функциональная урология и уродинамика. – М.: ГЭОТАР-Медиа, 2013. – 376 с.
- Пушкарь Д. Ю., Касян Г. Р. Ошибки и осложнения в урогинекологии. – М.: ГЭОТАР-Медиа, 2017. – 384 с.
- Раз Ш. Атлас реконструктивной хирургии влагалища: пер. с англ. / Под ред. В. Е. Радзинского. – М.: ГЭОТАР-Медиа, 2019. – 312 с.
- Савицкий Г. А., Савицкий А. Г. Уродинамические аспекты недержания мочи при напряжении у женщин. – С.‑ Петербург: Синтез Бук, 2008. – 240 с.
- Савицкий Г. А., Беженарь В. Ф., Савицкий А. Г. и др. Физиология и патология механизма удержания мочи у женщин: теоретические и практические аспекты // Эксперементальная и клиническая урология. – 2011. – № 1. – С. 26‑32.
- Савицкий Г. А., Беженарь В. Ф., Савицкий А. Г. и др. Физиология и патология механизма удержания мочи у женщин: теоретические и практические аспекты (ч. 2) // Эксперементальная и клиническая урология. – 2011. – № 4. – С. 16‑22.
- Стресове нетримання сечі у жінок / В. І. Горовий, В. П. Головенко, О. О. Процепко та ін. – Вінниця: РВВ ВАТ «Віноблдрукарня», 2003. – 304 c.
- Сучасні принци діагностики та лікування нетримання сечі у жінок без пролапсу тазових органів: Метод. рекомендації / В. І. Горовий, Б. Ф. Мазорчук, Г. В. Чайка та ін. – Вінниця: Вінницька обласна друкарня, 2014. – 148 с.
- Урогинекологическая гинекология: Практическое руководство для врачей // Под ред. Ю. В. Цвелева, С. Б. Петрова. – С.‑ Петербург: ООО «Издательство Фолиант», 2006. – 272 c.
- Херт Г. Оперативная урогинекология: пер. с англ. / Под ред. Н. А. Лопаткина, О. И. Аполихина. – М: ГЭОТАР-Медиа, 2003. – 276 c.
- Abrams P., Cardozo L., Fall M. et al. The standardization of terminology of lower urinary tract function: report from the standardization sub-committee of the International Continence Society // Neurourology and Urоdynamics. – 2002. – Vol. 21. – P. 167‑178.
- Abrams P. Artibani W. Understanding stress urinary incontinence. – Belgium: Ismar Healthcare, 2004. – 96 p.
- Аoki Y., Brown H. W., Brubaker L. et al. Urinary incontinence in women // Nat. Rev. Dis. Primes. – 2018. – Doi: 10.1038.
- Atlas of human anatomy / M. Schuenke, E. Schulter, U. Schumacher. – Stuttgunt, New York: Thieme, 2010. – 386 p.
- Atlas of human anatomy / Frank H. Netter. – 5th ed. – Saunders Elsevier, 2011. – 618 р.
- Baggish M. S., Karram M. M. Atlas of pelvic anatomy and gynecologic surgery. – 3rd ed. – Elsevier Saunders, 2011. – P. 1007‑1126.
- Blaivas J. G., Romauzi L. J., Heritz D. M. Urinary incontinence: pathophysiology, evaluation, treatment, overview and nonsurgical management // Campbell’s Urology / Walsh P. C. et al. – 7th ed. – Vol. 1. – Philadelphia: W. B. Sаunders, 1998. – P. 1007‑1043.
- Bratila E., Vladareanu S., Berceanu C. et al. The anatomy of urinary continence in women // Ginecologie. – 2015. – № 10. – Р. 45‑57.
- Campbell-Walsh Urology / L. R. Kavoussi et al. – 10th ed. – Elsevier Saunders, 2012. – 3754 p.
- Campbell-Walsh Urology / A. J. Wein et al. – 11th ed. – Philadelphia: Elsevier, 2016. – 4904 p.
- Comprehensive gynecology / G. M. Lentz et.al. – 6th ed. – Philadelphia: Elsevier Mosby, 2012. – 922 p.
- DeLancy J.O.L. Anatomy // Clinical urogynaecology / S. L. Stanton, A. K. Monga. – 2nd ed. – London: Churchill Livingstone, 2000. – P. 3‑18.
- DeLancy J., Gosling J., Creed K. et al. Gross anatomy and cell biology of the lower urinary tract // Incontinence / P. Abrams et al. – 2nd ed. – Paris: Health Publication Ltd., 2002. – P. 19‑82.
- De Groat W., Graffiths D., Yoshimura N. Neural control of the Lower urinary tract // Compr. Physiol. – 2015. – Vol. 5. – P. 327‑396.
- Female pelvic medicine and reconstructive pelvic surgery / H. P. Drutz et al. – Springer, 2003. – P. 25‑36.
- Female genital prolapse and urinary incontinence / V. Gomel, B. van Herendael. – Informa Healthcare, 2008.
- Female urology, urogynecology, and voiding disfunction / S. P. Vasavada et al. – New York: Marcel, 2005. – 950 p.
- Female urology. A practical clinical guide / H. B. Goldman, S. P. Vasavada – Humana Press Inc., 2007. – 434 p.
- Female urology / S. Raz, L. V. Rodriguez. – 3rd ed. – Elsevier Saunders, 2008. – 1038 p.
- Fowler C., Griffiths D., de Groat W. C. The neural control of micturation // Nat. Rev. Neurosci. – 2008. – Vol. 9. – P. 433‑466.
- Gosling J. A., Dixon J. S., Critchley H. O.D., Thomson S. A. Acomparative study of human external sphincter and periurethral levator ani muscles // J. Urol. – 1981. – Vol. 53. – P. 35‑41.
- Gray’s Anatomy. The anatomical basis of clinical practice / S. Standring et al. – 40th ed. – Churchill Livingstone Elsevier, 2008. – 2672 p.
- Haylen B. T., Ridder D., Freeman R. M. et al. An International Urogynecological Association (IUGA) / International Continence Society (ICS) join report on the tetminology for female pelvic floor dysfunction // Neurourology and Urodynamics. – 2010. – Vol. 29. – P. 4‑20.
- Hinman’s atlas of urosurgical anatomy / MacLennan G.T. – 2nd ed. – Elsevier Saunders, 2012. – 360 p.
- Hinata N., Murakami G. The urethral rhabdosphincter, levator ani muscle, and perineal membrane: a review // BioMed. Research International. – 2014. – 18 p.
- Hutch J. A. A new theory of the anatomy of the internal urinary sphincter and the phisiology of micturition. IV. The urinary sphincteric mechanism // J. Urol. – 1967. – Vol. 97. – P. 705‑712.
- Hutch J. A. A new theory of the anatomy of the internal urinary sphincter and the phylology of micturition. II. The base plate // J. Urol. – 1966. – Vol. 96. – P. 182‑188.
- Hutch J. A. The internal urinary sphincter: double-loop system // J. Urol. – 1971. – Vol. 105. – P. 375‑383.
- Hutch J. A., Rambo O. N. A new theory of the anatomy of the internal urinary sphincter and phisiology of micturition. III. Anatomy of the urethra // J. Urol. – 1967. – Vol. 97. – P. 696‑704.
- Incontinence / P. Abrams et al. – 5th ed. – ICUD – EAU, 2013. – 1982 р.
- Incontinence / P. Abrams et al. – 6th ed. – ICS – ICUD, 2017. – 2336 p.
- Koelbl H., Mostwin J., Boiteux J. P. et al. Pathophisiology // Incontinence / P. Abrams, L. Cardoso, S. Khoury, A. Wein editors. – 2nd ed. – Plymouth: Plymbridge Distributors Ltd., 2002. – P. 203‑241.
- Lukacz E. S., Santiago-Lastra Y., Albo M. E., Brubaker L. Urinary incontinence in women. A review // JAMA. – 2017. – Vol. 318. – P. 1592‑1604.
- McGuire E. J. Pathophysiology of stress urinary incontinence // Reviews in Urology. – 2004. – Vol. 6. – P. 11‑17.
- Netter F. H. Atlas of human anatomy. – 7th ed. – Summit, New Jersey: CIBA-GEIGY Corporation, 1994. – P. 337‑377.
- Olsen A. L., Smith V. J., Bergstrom J. O. et al. Epidemiology of surgically managed pelvic organ prolapse and urinary incontinence // Obstet. Gynecol. – 1997. – Vol. 89. – P. 501‑506.
- Pelvic floor dysfunction: a multidicciplinary approach / G. W. Davila et al. – Springer – Verlag London Limited, 2006. – P. 70‑93.
- Petros P. The female pelvic floor. Function, dysfunction and management to the integral theory. – 2nd ed. – Springer Medizin Verlag Heidelberg, 2007. – 260 p.
- Raz S., Slothers L., Chopra A. Vaginal reconstructive surgery for incontinence and prolaps // Campbell’s Urology / P. C. Walsh et al. – 7th ed. – Vol. 1. – Philadelphia: W. B. Saunders, 1998. – P. 1059‑1094.
- Stanton S. L., Monga A. K. Clinical urogynaecology. – 2nd ed. – Churchill Livigstone, 2000. – 742 р.
- Surgical management of pelvic organ prolapsed / M. Karram, S. F. Maher. – Elsevier Saunders: Philadelphia, 2013. – 186 p.
- Tanagho E. A., Pugh R. C. The anatomy and function of the ureterovesical function // Br. J. Urol. – 1965. – Vol. 35. – P. 151‑155.
- Tanagho E. A., Smith D. R. Mechanism of urinary continence / Embriologic, anatomic and pathologic considerations // J. Urol. – 1968. – Vol. 100. – P. 640‑646.
- Tanagho E. A. Anatomy of the lower urinary tract // Campbell’s Urology / P. C. Walsh et al. – 6th ed. – Vol. 1. – Philadelphia: W. B. Saunders, 1992. – P. 40‑69.
- Te Linde’s operative gynecology / J. A. Rock, H. W. Jones – 10th ed. – Philadelphia: Walters Klumer, Lippincott Williams & Wilkins, 2008. – 1470 p.
- Therapeutic Management of incontinence and pelvic pain / J. Haslam, J. Laycock. – 2nd ed. – Springer, 2008. – 302 p.
- Textbook of female urology and urogynaecology / L. Cardozo, D. Staskin. – 2nd ed. – Informa Healthcare. – 2006. – 1384 p.
- Thieme Atlas of Anatomy / M. Schuenke et al. – Thieme: Stuttgart. – New York, 2010. – 370 p.
- Vaginal surgery for incontinence and prolapse / P.E. Zimmern et al. – Springer – Verlag London Limited, 2006. – 304 p.
- Vaginal surgery for the urologist / V.W. Nitti et al. – Elsevier Saunders, 2012. – 190 p.
- Urogynecology and reconstructive pelvic surgery / M.D. Walters, M.M. Karram. – 3rd ed. – Philadelphia: Mosby Elsevier, 2007. – 600 р.
- Uroginecologia in primare care / P.J. Culligan, R.P. Goldberg. – Springer – Verlag London, 2007. – 166 p.
- Williams obstetrics / F.G. Cunningham et al. – 24th ed. – New York: Mc Graw – Hill Education, 2014. – 1358 p.