22 травня, 2020
Дослідження НОРЕ: зміна парадигми лікування артеріальної гіпертензії
На сьогодні проведено чимало рандомізованих клінічних досліджень (РКД) ефективності препаратів, зокрема для лікування та профілактики серцево-судинних захворювань (ССЗ). Більшість із них мають більшу чи меншу наукову вагу, відкривають для лікарів-практиків грані та нюанси клінічного процесу. Та є випробування, що змінюють терапевтичну парадигму й розуміння причинно-наслідкових зв’язків перебігу захворювання. До таких можна долучити дослідження HOPE (2000), що вперше було опубліковане 20 років тому та досі не втрачає своєї актуальності, в якому вивчали ефективність інгібітора ангіотензинперетворювального ферменту (іАПФ) раміприлу в осіб із високим серцево-судинним (СС) ризиком. Чому ж дана тема й досі на топових позиціях, а результати роботи цитують на профільних конференціях та використовують у сучасних настановах авторитетних наукових товариств?
За даними ВООЗ (2014), ССЗ є однією із провідних причин смерті у світі: колосальна частка у 30% від загальної летальності припадає саме на цю групу захворювань. Артеріальна гіпертензія (АГ) – один із найвагоміших факторів ризику ССЗ. Поширеність АГ теж вражає – 40% населення страждають на цю недугу (Figueiredo et al., 2009). Проте досі лише 34% хворих на АГ вдається контролювати рівень артеріального тиску (АТ). Слід зазначити, що даний показник суттєво гірший у країнах із низьким рівнем розвитку (Chobanian et al., 2003). В Україні статистика щодо поширеності АГ серед хворих на ССЗ теж маловтішна – майже половина (46,8%) пацієнтів цієї когорти мають підвищений АТ (Долженко та співавт., 2018).
З іншого боку, зниження АТ може попереджати прогресування і виникнення СС-ускладнень. Так, у метааналізі C. Thomopoulos et al. (2014) було показано, що зниження систолічного АТ (САТ) на 10 мм рт. ст. і діастолічного (ДАТ) – на 5 мм рт. ст. скорочує ризик виникнення ішемічної хвороби серця (ІХС) на 16%, інсульту – на 33%. За досягнення цільових показників АТ можна попередити коронарні події на >20%, інсульту – ще на 35%.
Відповідно до рекомендацій щодо терапії АГ Європейського товариства кардіологів / Європейського товариства гіпертензії (ESC/ESH, 2018), серед антигіпертензивних препаратів іАПФ є засобами першої лінії та показали ефективне зниження АТ і відсутність поширених побічних явищ у РКД (І, А). Крім того, у минулорічних настановах ESC із лікування хронічного коронарного синдрому з’явилися положення щодо доцільності застосування іАПФ при серцевій недостатності (СН), АГ, цукровому діабеті (ЦД). Призначення цих препаратів слід розглядати в осіб з ІХС при високому СС-ризику.
Раміприл – представник іАПФ, чиї фармакологічні властивості вигідно відрізняються порівняно з іншими лікарськими засобами даного класу. Під час проходження через печінку раміприл відносно швидко гідролізується в активний метаболіт раміприлат. Завдяки виразній ліпофільності, що визначає здатність препарату розчинятися в жирах, раміприл входить до трійки лідерів серед усіх іАПФ разом із периндоприлом і беназеприлом (Brown, Vaughan, 1998). Саме тому він легко проникає у тканини і, відповідно, має високу здатність зв’язувати тканинний АПФ (Unger et al., 1996). Відомо, що активація саме тканинної ренін-ангіотензинової системи відіграє провідну роль у формуванні ураження органів-мішеней, як-то судини, міокард, нирки (Kwakernaak et al., 2017).
Своєю чергою пригнічення АПФ під впливом його інгібіторів реалізується у два етапи: спершу відбувається швидке зв’язування активного препарату із зазначеним ферментом, після чого дане з’єднання трансформується у стабільний ізомерний комплекс, швидкість дисоціації якого і визначає тривалість дії іАПФ у тканинах. Константа дисоціації ізомерного комплексу раміприлат-АПФ є дуже низькою, оскільки період його напіврозпаду становить 640 хв, тоді як комплексів, наприклад, каптоприл-АПФ і еналаприлат-АПФ – 29 та 105 хв відповідно. Саме тому період напіввиведення раміприлу в дозах 5‑10 мг досягає 17 год, а 80% раміприлату зберігається в організмі через 24 год.
Слід зауважити, що раміприл (раміприлат) характеризується швидким настанням піку пригнічення АПФ (1‑2 год), що можна порівняти з таким для каптоприлу (1 год), і перевершує даний показник для еналаприлу (3‑4 год). Раміприл та його метаболіти мають збалансований (60% – із сечею, 40% – через кишечник) подвійний шлях виведення. Необхідність коригувати дозу препарату в бік зменшення виникає за порушення функції нирок (кліренс креатиніну <50 мл/хв) (Bunning, 1987; Воронков, 2018).
Як зазначалося вище, у дослідженні НОРЕ було доведено високу ефективність раміприлу та його вплив на суттєве покращення прогнозу тяжкого ССЗ при тривалому застосуванні (Sleight et al., 2000). У РКД, що проводилося на базі 267 медцентрів у 19 країнах, взяли участь 9297 осіб із ознаками ІХС, інсультом в анамнезі або атеросклеротичним ураженням периферичних судин. Середній вік хворих склав 65,9 року, серед них було 26,7% жінок. У 89,6% пацієнтів були ознаки коронарного атеросклерозу, 38,3% страждали на ЦД. Усім учасникам, окрім базової терапії, призначали раміприл по 10 мг/добу, вітамін Е або плацебо.
Первинною кінцевою точкою було визначено комбінацію інфаркту міокарда (ІМ), інсульту або смерті через СС-причини. При цьому кожен із випадків аналізували окремо. Вторинними кінцевими точками були смерть від будь-яких причин, випадки реваскуляризації міокарда, нестабільної стенокардії та СН (для обох включно з госпіталізацією), зупинки серця, а також нові випадки ЦД і його ускладнення. Встановлено, що у хворих із високим ризиком СС-ускладнень тривале застосування іАПФ раміприлу приводило до зменшення вірогідності їхнього розвитку за первинною кінцевою точкою на 22% (рис. 1). Крім того, по кожному проаналізованому показнику (смерть від СС-причин, ІМ, інсульт) було продемонстровано позитивну дію препарату: зниження ризику вказаних подій порівняно із плацебо склало 26, 20 і 32% відповідно (р<0,001). Імовірність летальних наслідків через усі причини при лікуванні раміприлом знизилася на 26%.
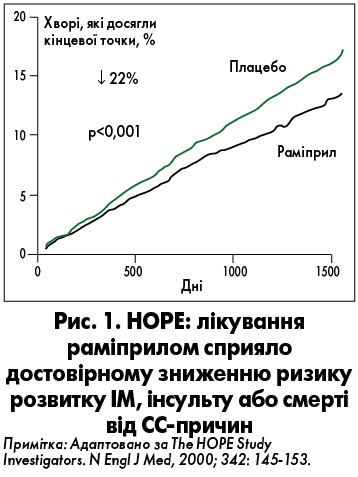
Варто зазначити, що іАПФ раміприл в осіб із високим ризиком СС-подій викликав достовірне зниження потреби в реваскуляризації міокарда (на 15%, p=0,002), частоти випадків зупинки серця (на 38%, р=0,02), прогресування стенокардії (на 11%, р=0,004), розвитку СН (на 23%, p<0,001), але не госпіталізацій із приводу даного стану (на 12%, p=0,25), а також нових випадків ЦД (на 34%, p<0,001) і ускладнень, пов’язаних із ним (на 16%, p=0,03). Цікаво, що сприятливий вплив раміприлу щодо розвитку ІМ, інсульту або СС-смерті був порівнянний у підгрупах пацієнтів з/без ЦД, чоловіків і жінок, що страждали і не страждали на ССЗ, АГ, ІХС, віком молодше і старше 65 років, які перенесли і не перенесли ІМ. Ефект лікування не залежав від супутньої терапії (аспірин та інші антитромбоцитарні засоби, β-блокатори, гіполіпідемічні й антигіпертензивні препарати).
Основними причинами припинення терапії у хворих із високим ризиком, що отримували раміприл, стали кашель (7,3% проти 1,8% у контрольній групі), гіпотонія або запаморочення (1,9% проти 1,5% у контрольній групі). Своєю чергою плацебо частіше відміняли через неконтрольовану АГ (3,9% проти 2,3% у групі раміприлу). Значимим є той факт, що частка пацієнтів, які продовжували приймати раміприл по 10 мг/добу, через один рік склала 82,9%, через 2, 3 і 4 роки – 74,6, 70,9 та 62,4% відповідно, а наприкінці дослідження – 65%. Це свідчить про високий комплаєнс із боку хворих.
Із метою вивчити, чи зберігається досягнутий ефект раміприлу, дослідники вирішили продовжити спостереження за хворими, що взяли участь у випробуванні НОРЕ. До РКД тривалістю 2,6 року, що отримало назву НОРЕ-ТОО, увйшли 4528 пацієнтів (72% у групі раміприлу та 68% – плацебо) (Bosch et al., 2005). Хворі із групи плацебо були переведені на лікування раміприлом, решта продовжили терапію.
На тлі продовження терапії раміприлом сумарний ризик виникнення первинної комбінованої кінцевої точки (ІМ, інсульт, СС-смерть) додатково знизився на 17%. Цікаво, що в когорті хворих, які від початку були рандомізовані до групи раміприлу, виявляли додаткове зменшення вірогідності розвитку ІМ на 19% порівняно із пацієнтами, які у дослідженні НОРЕ отримували плацебо, реваскуляризації – на 16%, ЦД – на 34%. Частота інсульту на тлі застосування раміприлу знизилася на 21%, СС-смерті – на 14%. Тобто чим раніше розпочати ефективне лікування та що триваліше його продовжувати, тим кращого результату можна очікувати у майбутньому.
Частина хворих (n=3654), які були включені у дослідження, мали ЦД 2-го типу та мікроальбумінурію. Аналіз даних пацієнтів, оприлюднений під назвою MICRO-HOPE, показав не лише зниження за первинною кінцевою точкою (на 25%) (рис. 2), але й нефропротекторний ефект раміприлу (Gerstein et al., 2001). Так, лікування раміприлом протягом більше як чотири роки сприяло достовірному зниженню розвитку протеїнуричної стадії діабетичної нефропатії на 24% незалежно від антигіпертензивної активності препарату.
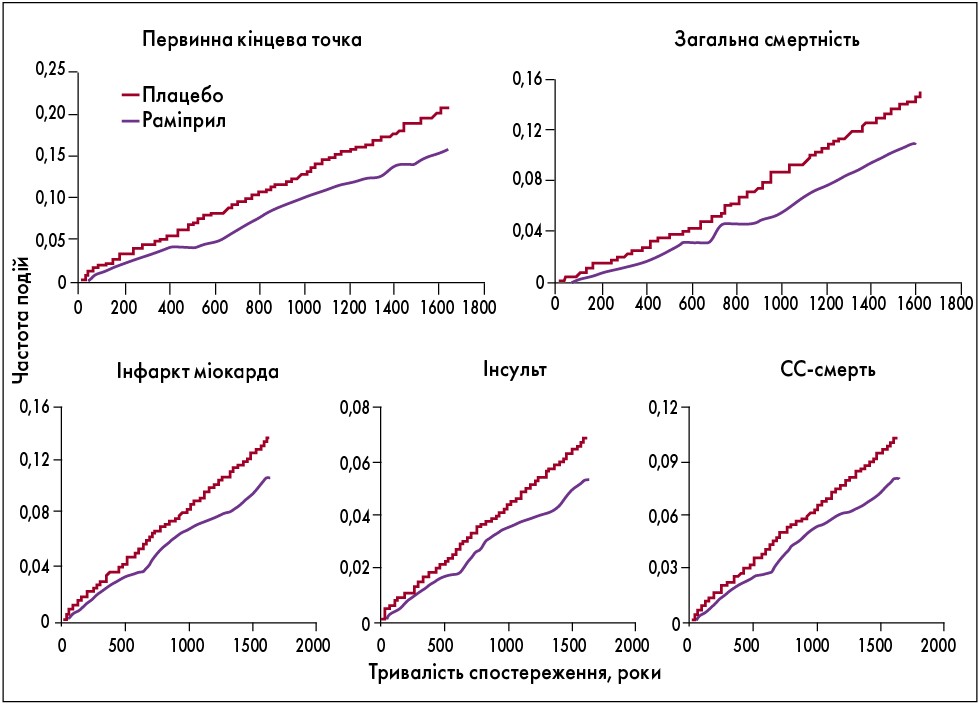 Рис. 2. Частота несприятливих подій у динаміці спостереження за пацієнтами у дослідженні MICRO-HOPE: ранній прояв захисного ефекту раміприлу, що наростав у міру продовження лікування
Рис. 2. Частота несприятливих подій у динаміці спостереження за пацієнтами у дослідженні MICRO-HOPE: ранній прояв захисного ефекту раміприлу, що наростав у міру продовження лікування
Таким чином, результати дослідження НОРЕ принципово змінили сучасну клінічну практику. Крім того, раміприл має найширший спектр показань (згідно з інструкціями до медичного застосування препаратів) та найвищу прихильність у пацієнтів серед усіх іАПФ (Manicia et al., 2011).
Підготувала Наталія Нечипорук
SAUA.RAH.20.04.0306
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (69) 2020 р.


