25 травня, 2020
Ротація режимів антибіотикотерапії як один із напрямків подолання резистентності бактерій
 Головними чинниками, які призводять до збільшення антимікробної резистентності бактерій, є недостатній контроль інфекцій та некоректне застосування антибіотиків. Оскільки ці чинники добре відомі, слід впроваджувати у практику спеціальні стратегії використання антибіотиків, щоб запобігти зростанню антибіотикорезистентності. Складові стратегії включають: обмеження нераціонального застосування антибіотиків, призначення комбінованої та циклічної антибіотикотерапії (АБТ) відповідними курсами й режимами. На результат циклічної програми впливають багато чинників: вибір антибіотиків для проведення курсу лікування, черговість їх застосування. Оптимальна тривалість кожного курсу лікування часто залишається невизначеною, і її слід коригувати відповідно до конкретних умов.
Головними чинниками, які призводять до збільшення антимікробної резистентності бактерій, є недостатній контроль інфекцій та некоректне застосування антибіотиків. Оскільки ці чинники добре відомі, слід впроваджувати у практику спеціальні стратегії використання антибіотиків, щоб запобігти зростанню антибіотикорезистентності. Складові стратегії включають: обмеження нераціонального застосування антибіотиків, призначення комбінованої та циклічної антибіотикотерапії (АБТ) відповідними курсами й режимами. На результат циклічної програми впливають багато чинників: вибір антибіотиків для проведення курсу лікування, черговість їх застосування. Оптимальна тривалість кожного курсу лікування часто залишається невизначеною, і її слід коригувати відповідно до конкретних умов.
Ключові слова: антибіотики, антибіотикорезистентність, ротація, циклічність і змішування антибіотикотерапії.
Частота інфекцій, спричинених антибіотикорезистентними бактеріями, зростає в усьому світі з кожним днем, що, як наслідок, підвищує витрати на охорону здоров’я, захворюваність і смертність. Існує безліч причин, які пояснюють цю тенденцію: зростання частоти захворювань із тяжким перебігом у госпіталізованих пацієнтів, збільшення частоти застосування інвазивних процедур, наявність імуноскомпрометованих пацієнтів у суспільстві і в стаціонарах. Однак головним чинником постійного збільшення стійкості бактерій до антибіотиків є нераціональне застосування антимікробних препаратів, й особливо антибіотиків широкого спектра дії. Першим кроком до запобігання зростанню частоти резистентності є ефективна політика контролю над інфекціями та поліпшення чіткості рекомендацій стосовно антимікробної терапії.
Незважаючи на те що політика контролю над інфекціями не може цілком забезпечити ефективну профілактику резистентності, вона необхідна для зниження розповсюдження антибіотикорезистентних штамів. Миття рук – найбільш важливий засіб запобігання інфекціям, а внаслідок зниження контамінації медичних приладів, які використовуються для маніпуляцій, зменшується вірогідність перенесення потенційно вірулентних та резистентних штамів від людини до людини. Оптимізація контролю над інфекціями шляхом недорогих освітніх процедур сприяє зниженню частоти так званих вентилятор-асоційованих пневмоній і катетерних інфекцій. Постійний контроль над інфекціями дозволяє запобігти горизонтальному механізму передачі резистентних штамів завдяки ранній ідентифікації та належній ізоляції, оскільки колонізація може передувати поширенню інфекцій, спричинених резистентними бактеріями.
Іншим важливим компонентом профілактики появи резистентних патогенів є чітке дотримання рекомендацій стосовно антибіотикотерапії (АБТ). Доведено, що приблизно у 50% випадків застосування антибіотиків є нераціональним. Надмірне й некоректне використання антимікробних засобів призводить до значного селективного тиску, що сприяє виникненню антибіотикорезистентних патогенів. Програми рекомендацій і довідники з АБТ передбачають оптимізацію вибору, селекції, дозування й тривалості АБТ із метою профілактики та лікування інфекцій. Така оптимізація часто можлива щодо окремих пацієнтів, проте впровадження її у практику на рівні популяції значно ускладнене.
Що являє собою принцип ротації антибіотиків?
Застосування виключно одного класу антибіотиків при лікуванні окремої популяції, незважаючи на оптимальні підходи до лікування, може призводити до селекції резистентних мікроорганізмів у цій популяції. Метод чергування, або ротації, антибіотиків всередині або між класами знижує селективний тиск й порушує механізми формування резистентності у мікроорганізмів до певного антибіотика, що вважають дієвим методом вирішення зазначеної проблеми. Хоча циклічне застосування антибіотиків виглядає перспективним напрямом подолання резистентності, оптимальний його метод залишається не визначеним до кінця, і, перш ніж запровадити програму такої ротації, слід врахувати низку чинників [9].
Метод ротації антибактеріальних препаратів полягає у тимчасовому вилученні із застосування у клініці/лікарні/регіоні засобу з низькою бактеріологічною ефективністю та заміні його антибіотиком із бактеріальною ефективністю не нижче 80%. За сучасними даними, найдостовірнішими є клінічні дані стосовно потенційної користі ротації саме аміноглікозидів. Багато досліджень із циклічного використання цієї групи антибіотиків було проведено на початку 1980-х років внаслідок зростання резистентності серед грампозитивних патогенів, спричинених плазмідо-активованими аміноглікозидо-модифікуючими ферментами. Цей механізм резистентності виявився специфічним для гентаміцину та тобраміцину [4].
На думку М. Бассетті (2015), створюється враження, що ми йдемо по тупиковій колії. Бактерії підлаштовуються під АБТ швидше, ніж з’являються нові лікарські засоби даної групи. Чи не простіше повсюдно виводити на деякий час (півроку або рік) певний антибіотик? Чи можна очікувати, що за цей час чутливість мікробів до даного антибіотика підвищиться? Подібну ротацію антибіотиків уже випробували, але очікуваних результатів вона не дала. Ми продовжуємо той шлях, яким ішли останні 70 років. Мабуть, це хибна дорога. Ми створюємо нові антибіотики, механізм дії яких такий же, як у старих. Потрібні ліки з новим механізмом дії. Можливо, це будуть не антибіотики, а мінерали або щось іще. Також необхідно раціонально застосовувати наявні антибіотики, за допомогою біомаркерів проводити підбір дози, моніторинг тощо. Потрібно призначати антибіотики з різним механізмом дії з урахуванням особливостей хворого. На жаль, концепція їх раціонального застосування в багатьох лікарнях існує лише на папері, а не на практиці [2].
Оскільки переважне застосування одного класу антибіотиків протягом тривалого часу може призводити до селекції резистентних мікроорганізмів, в якості одного із заходів для обмеження поширення резистентних штамів серед госпітальних пацієнтів запропонована циклічна зміна, або ротація, антибактеріальних препаратів, які мають схожий спектр антимікробної дії. Після тимчасового обмеження застосування деяких класів антибіотиків або їхніх окремих представників можна очікувати підвищення чутливості мікрофлори до них, що дозволило б успішно застосовувати їх у подальшому.
Ефективність ротації антимікробних препаратів в якості одного із заходів для стримування антибіотикорезистентності активно дискутується. Незважаючи на велику кількість публікацій, присвячених цьому питанню, до теперішнього часу не вироблено загальної методики застосування циклічної зміни режимів емпіричної АБТ. Зокрема, немає чітких рекомендацій щодо оптимальної тривалості циклів, необхідної кількості режимів ротації, як і немає єдиної думки стосовно заміни антимікробних препаратів однієї фармакологічної групи [3].
Механізми антибіотикорезистентності – мутація хромосом, що спричиняє зміну структур-мішеней для антибіотиків, позахромосомні генетичні елементи (R-плазміди), які здатні до хімічної модифікації антибіотиків або зменшення проникності мембран, ферменти, що руйнують хіміопрепарати, посилення синтезу природних метаболітів, що пригнічують дію антибіотика. Існують три глобальні механізми, за допомогою яких бактерія набуває фенотип, резистентний до антимікробних препаратів: пошкодження мішені для антимікробних засобів, руйнування антимікробного засобу, запобігання надходженню антимікробного засобу до мішені.
Учені із Данії запропонували метод боротьби з антибіотикорезистентністю бактерій, який базується на вивченні того, як стійкість мікроорганізмів до одних речовин впливає на чутливість до інших. Суть методу полягає в тому, щоб використовувати для боротьби з бактеріями кілька антибіотиків різних груп, які періодично замінювали у ході лікування. Подібний підхід відомий іще з 1950-х років, однак новий метод має принципову відмінність – він заснований на вивченні взаємного впливу між різними механізмами резистентності [1].
Причини антибіотикорезистентності – тривале застосування традиційних препаратів, тривале перебування хворого у стаціонарі, нераціональні дози й режими лікування. У лікарнях висока частота застосування антибіотиків призводить до зростання рівнів резистентності; у той же час хворі, які знаходяться на стаціонарному лікуванні перебувають у групі ризику стосовно нозокоміальних інфекцій. Тому виникає необхідність пошуку нових стратегій лікування, які обмежують стійкість патогенів без шкоди для лікування пацієнтів. У глобальному масштабі у 8% випадків перебування пацієнтів у стаціонарі спостерігається розвиток внутрішньолікарняних інфекцій. За оцінками, 70% із них спричинені мультирезистентними штамами, стійкими до багатьох антибактеріальних препаратів. Порівняно з інфекціями, спричиненими чутливими бактеріями, ті, що спричинені резистентними штамами, часто підвищують смертність, захворюваність та витрати на лікування. В окремих стаціонарах застосовується кілька підходів для боротьби з резистентністю. Стратегії, на яких зосереджена більшість клінічних і теоретичних досліджень, – це ротація, тобто заплановані зміни домінуючого антибіотика в цілому відділенні або лікарні, і змішування, тобто випадковий розподіл пацієнтів для призначення різних антибіотиків [5, 6].
Принцип використання ротації антибіотиків базується на припущенні, що стійкі бактерії завжди менш конкурентоспроможні, ніж звичайні. Тобто, якщо в середовищі є мікроорганізми, стійкі й чутливі до антибіотика «А», то у разі відміни препарату «А» стійкі завжди програють у конкуренції зі звичайними. Вважалося, що за призначення антибіотика «В», який має інший механізм дії, це правило також актуальне. Проте існують і протилежні думки, оскільки феномен резистентності до одних речовин може впливати на чутливість до інших, причому як в один, так і в інший бік. Наприклад, розвиток стійкості за рахунок появи у бактерій спеціальних молекулярних насосів, які «викачують» антибіотик із клітини, може зробити останню більш чутливою до речовин, які ці насоси вивести не можуть. Проте, якщо ці насоси все-таки тропні до альтернативного антибіотика, то клітина, навпаки, стає «колатерально стійкою». Тому пропонується використовувати подвійну, потрійну антибіотикотерапію або інші послідовності (метод змішування), за яких резистентність до одного препарату підвищує чутливість до іншого. Тоді, якщо при застосуванні препарату «А» з’являться стійкі бактерії, то при одночасному застосуванні антибіотика «B» вони будуть конкурентно витіснені звичайною флорою, і тільки потім останні зможуть виробити стійкість до «В» [4].
При розробці стратегії оптимального призначення антибіотиків у стаціонарних хворих слід враховувати можливість їх застосування за межами лікарняних закладів. Це питання включає сільськогосподарське застосування і практику застосування антибактеріальних препаратів у суспільстві (малоконтрольоване амбулаторне лікування або самолікування). Сільськогосподарське застосування антибіотиків стало наслідком появи ванкоміцин-резистентних ентерококів у Європі та хінолон-резистентних штамів Campylobacter у США. Практика частого призначення антибіотиків продемонструвала свій вплив на стійкість звичайних бактеріальних патогенів. Стаціонари проявили себе як резервуар антибіотикорезистентних штамів. Усі наведені вище чинники мають прийматися в розрахунок при розробці оптимальної стратегії використання антибіотиків, спрямованої на запобігання формуванню резистентності [9].
Ротація антибіотиків – це концепція мінімізації стійкості до них шляхом зміни алгоритмів використання препаратів першого ряду. При тимчасовому призначенні препарату іншого класу знижується селективний тиск, що сприяє зниженню резистентності. Проте теоретичне й експериментальне обґрунтування не завжди знаходить своє відображення на практиці. Існують три основні чинники, які гальмують відновлення чутливості популяції збудників до антибіотиків [12]:
1. Перші резистентні штами зазвичай менш стійкі, проте вони можуть набути компенсаторних мутацій, які роблять притаманні їм рівні чутливості подібними до рівня звичайних чутливих штамів. Так було з метицилін-резистентним золотистим стафілококом (Methicillin-resistant Staphylococcus aureus, MRSA) – перші резистентні штами верифікувалися в малій кількості у стаціонарах, оскільки вони могли конкурувати лише в умовах підвищеного застосування антибіотиків. У подальшому ці штами стали більш сильними та «врятувалися» від лікарняного середовища, перетворившись на штами основної спільноти (госпітальної мікрофлори), які створюють сьогодні одну з основних проблем антибіотикорезистентності.
2. Багато генів резистентності переносяться на генетичні касети разом із іншими генами резистентності. Якщо штам містить гени резистентності як до пеніциліну, так і до тетрацикліну, то перехід від одного антибіотика до іншого не дає ефекту – рівень резистентності до пеніциліну не знизиться.
3. Після того як ген резистентності з’явиться в популяції, він ніколи не знищиться повністю і буде швидко реплікуватися за частотою, якщо будуть відновлені вибіркові умови. Однак у циклічних режимах застосування антибіотиків є певна цінність, що може знизити рівень резистентності приблизно на 25% [12].
Починаючи з 1980-х років концепція циклічного застосування антибіотиків у пацієнтів із бактеріальними інфекціями розглядалася як потенційна стратегія зниження рівня стійкості до антибіотиків лікарняної мікрофлори. Ідея стратегії полягає в тому, що відмова від використання одного антибактеріального препарату на користь іншого знизить селективний тиск та збереже ефективність препарату. Ротація антибіотиків передбачає використання певного препарату для терапії першої лінії у всіх пацієнтів протягом певного періоду з подальшою заміною цього антибіотика препаратом іншого класу, але аналогічним за спектром дії, протягом такого ж періоду, із подальшим повторенням циклу. Допускається застосування більше двох різних антибіотиків, які можуть бути частиною цієї ротації. Інша стратегія зменшення ризику розвитку резистентності до антибактеріальних препаратів, яка називається змішуванням антибіотиків, має менш структурований підхід, і кожний наступний пацієнт у палаті отримує альтернативний клас антибіотиків [14].
Циклічність, або ротація, є запланованою заміною класу антибіотиків/конкретного препарату на інший клас/препарат, який демонструє порівнянний спектр активності. Заміну слід проводити після фіксованого інтервалу й їх може бути будь-яка кількість, проте цикл має бути повторений, із повторним введенням вихідного класу/препарату [7]. Циклічність (ротація) не повинні ототожнюватися із запланованими змінами або обмеженнями режимів АБТ без повторення процесу (звичайне явище серед дослідників). Тривалість кожного циклу ґрунтується на шаблонах локальної сприйнятливості або на заданому періоді часу. Хоча деякі дослідники здійснюють заміну одного аміноглікозиду (гентаміцин) на інший (амікацин), ця практика загрожує труднощами, оскільки препарати, що належать до одного класу, зазвичай сприяють однаковим механізмам резистентності. З іншого боку, антибіотик, що належить до одного класу, може сприяти феномену резистентності до препаратів, що належать до одного або декількох не пов’язаних між собою класів, у результаті генетичної зв’язки детермінантів резистентності, що кодують стійкість штамів бактерій до декількох класів антибіотиків [7].
Принцип ротації полягає в тому, що, чим частіше призначають антибіотик, тим більша ймовірність розвитку резистентності до нього. Таким чином, вилучення класу антибіотиків протягом заздалегідь визначеного періоду обмежуватиме селективний тиск з боку патогенів (а отже, виникнення резистентності), тим самим дозволяючи стабілізувати резистентність до вилученого препарату або навіть знизити її протягом періоду обмеження. Це дозволить застосувати його знову у більш пізньому терміні. Результат буде залежати від ситуації, яка існувала до здійснення ротації. Наприклад, якщо показники стійкості до певного антибіотика стабільні, до введення ротації, збільшення (або зменшення) частоти призначення цього препарату призведе до поступового збільшення (або зменшення) частоти резистентності до нього. Проте, якщо рівень резистентності до препаратів першого ряду збільшувався до впровадження ротації, зменшення використання антибіотика може не призвести до негайного зниження частоти резистентності. Не менш важливою метою ротації є уникнення появи значних популяцій організмів, стійких до замінника, тому тривалість кожного циклу має бути достатньо короткою, щоб забезпечити зазначений ефект [7].
Результати клінічних досліджень із впровадження різних стратегій ротації антибіотиків
Дослідники із США довели, що ротація антибіотиків у педіатричному відділенні реанімації й інтенсивної терапії (ВРІТ) може бути ефективною стратегією, спрямованою на зниження частоти антибіотикорезистентності збудників нозокоміальних інфекцій [11]. Moss et al. (2002) провели обсерваційне пілотне дослідження, у ході якого вивчався вплив стратегії ротації антибіотиків на частоту колонізації та розвитку внутрішньолікарняних інфекцій, спричинених резистентними нозокоміальними штамами мікроорганізмів у госпіталізованих дітей, а також на фенотип антибіотикорезистентності збудників. Були досліджені три режими АБТ: монотерапія іміпенемом/циластатином, монотерапія піперациліном/тазобактамом і призначення комбінації цефалоспорину 4-го або 3-го покоління з антисиньогнійною активністю (цефепіму або цефтазидиму) із кліндаміцином. Кожний із режимів призначення АБТ використовували протягом 3 міс, проводячи циклічну зміну препаратів після закінчення цього терміну. Загальний період спостереження склав 18 міс. За час проведення дослідження не було виявлено появи резистентних штамів із новими, що не зустрічалися раніше, фенотипами антибіотикорезистентності. Результати регресивного аналізу довели, що частота інфікування госпіталізованих у ВРІТ дітей антибіотикорезистентними нозокоміальними штамами бактерій знизилася з 29,3% на початку дослідження до 23,9% на момент його завершення. Порівняно з іншими ВРІТ, де не проводилася ротація антибіотиків, частота резистентних нозокоміальних інфекцій знизилася за час проведення дослідження до 27%. Встановлено, що стратегія систематичної ротації антибіотиків не призводить до виникнення нових фенотипів резистентності. Таким чином, циклічна ротація режимів АБТ у ВРІТ є ефективним методом запобігання поширенню антибіотикорезистентності у збудників нозокоміальних інфекцій [11].
D. Gruson et al. (2003) провели проспективне дослідження з оцінювання довгострокового впливу ротації антибіотиків на частоту виникнення вентилятор-асоційованої пневмонії (ВАП), спричиненої грамнегативними збудниками, і чутливості даних патогенів до проведеної АБТ. Було обстежено 2856 хворих, які отримували штучну вентиляцію легень. Дослідження проводили згідно з протоколом, який визначив порядок застосування антибіотиків як при їх початковому(емпіричному) призначенні, так і при застосуванні відповідно до даних мікробіологічного дослідження харкотиння. Протокол передбачав щомісячну зміну антибіотиків, які відносяться до класів β-лактамів і аміноглікозидів. Правильність використання препаратів перевіряли щомісяця. При призначенні антибіотиків не допускали застосування кращих препаратів з якоїсь однієї групи. Автори довели, що за семирічний період спостережень було отримано достовірне зменшення частоти виникнення ранніх варіантів ВАП. Цей показник на різних етапах дослідження становив у хронологічній послідовності: 13, 9 і 5,9% (р=0,02 при порівнянні етапів 3 і 1). Проте потенційно антибіотикорезистентні штами грамнегативних бактерій залишалися чутливими до більшості β-лактамів, особливо до піперациліну/тазобактаму і цефепіму. Отже, періодична зміна антибіотика у відділенні реанімації може сприяти зниженню ризику розвитку ВАП й істотно підвищити чутливість до лікування потенційно антибіотикорезистентних штамів грамнегативних бактерій, що є домінуючими збудниками пізніх форм ВАП. Запропонований протокол здатний приносити позитивні результати навіть по закінченні 5 років. Автори дослідження пропонують не оригінальний, але цілком раціональний підхід до зниження ризику розвитку резистентності до антибіотиків, і подібні протоколи цілком можуть бути реалізовані в будь-якому відділенні без істотних економічних та організаційних витрат [13].
В.Г. Краснов у дисертаційній роботі дослідив ротацію режимів емпіричної антимікробної терапії. Препарат для наступного етапу ротації вибирали з урахуванням даних мікробіологічного моніторингу. В якості препарату для емпіричної АБТ використовували в І періоді цефтазидим, у II періоді – цефепім як монотерапію (4 г на добу), у ІІІ періоді антимікробним препаратом вибору став цефоперазон/сульбактам у дозі 8 г на добу. ІV період дослідження включав комбінацію цефтазидиму (6 г на добу) та амікацину (1 г на добу). У разі неефективності стартової емпіричної терапії переходили до лікування карбапенемами (меропенем або іміпенем/циластатин); у вкрай тяжких пацієнтів (оцінка за шкалою APACHE II >15 балів) карбапенеми призначали на етапі емпіричної терапії. Дослідженням було доведено, що чутливість грамнегативної госпітальної флори до високоефективних препаратів може зберігатися досить тривалий час, незважаючи на їх широке застосування. Всі чотири режими емпіричної антимікробної терапії у рамках ротаційної програми продемонстрували досить високу клінічну ефективність без достовірних відмінностей. Найбільшу клінічну й мікробіологічну ефективність (82 і 89% відповідно) у хворих із нозокоміальною інфекцією продемонстрував цефоперазон/сульбактам. Дослідники наводять дані про можливість обмеження поширення стійких клонів грамнегативних бактерій шляхом проведення регулярної ротації емпіричних режимів антимікробної терапії у ВРІТ, однак суттєвої елімінації стійких штамів при коротких 6-місячних циклах ротації не відзначено. Ймовірно, поліпшення епідеміологічної ситуації у ВРІТ можливе або за більшої тривалості періодів ротації, або за одночасного використання інших підходів до контролю та елімінації стійких штамів мікроорганізмів [3].
Метою дослідження P.J. van Duijn et al. (2018), яке проводилося у стаціонарах кількох країн Європи, стало встановлення, чи буде циклічне використання антибіотиків порівняно зі стратегією змішування (заміна антибіотика на препарат іншого класу у кожного наступного пацієнта) сприяти зниженню поширення резистентних грамнегативних збудників у ВРІТ. Для реалізації поставленої мети було проведено кластер-рандомізоване перехресне дослідження, у ході якого кожне ВРІТ випадковим чином розподілялося на використання однієї із трьох груп антибіотиків (III або IV покоління цефалоспоринів, піперацилін/тазобактам або карбапенеми) як пріоритетне для емпіричного лікування за 6-тижневий період (циклічне використання) або на послідовну зміну кожного препарату, який отримує для лікування кожний наступний пацієнт (змішування). Комп’ютерна рандомізація, включаючи тип лікування і послідовність ротації антибіотиків, виконувалася централізовано. Циклічне використання, або змішування, впроваджувалося у стаціонарі протягом 9 міс, а потім після періоду санації починалося використання альтернативної стратегії. Дослідники визначили стійкі грамнегативні бактерії як мікроорганізми сімейства Enterobacteriaceae, які продукують β-лактамази розширеного спектра (БЛРС) або стійкі до піперациліну/тазобактаму та карбапенемів Acinetobacter spp. і Pseudomonas aeruginosa. Первинним оцінюваним параметром була середня специфічна для відділення щомісячна поширеність стійких грамнегативних патогенів із дихальних шляхів і в мазках із періанальної ділянки з урахуванням корекцій інших потенційних чинників. Усього у проекті брали участь 8 стаціонарів у Бельгії, Франції, Німеччині, Португалії та Словенії. Протягом зазначеного періоду до дослідження було залучено 4069 пацієнтів за принципом циклічного застосування антибіотиків і 4707 осіб – за принципом змішування. Результати мікробіологічного скринінгу показали, що середня поширеність антибіотикорезистентних грамнегативних бактерій становила 23% під час циклічного застосування (168 із 745 пацієнтів) та 22% під час змішування (184 із 853 пацієнтів).
Автори дослідження стверджують, що стратегії лікування досягли наміченої мети – змінити використання трьох антибіотиків, не змінюючи об’єму використаних препаратів у часі. Крім того, були помітні відмінності впливу трьох антибіотиків у двох застосованих підходах. Під час ротації частка застосування невідповідних препаратів зменшилася наполовину, тоді як використання цих трьох антибіотиків залишалося стабільним у ході методики змішування. Але відмінності в експозиції не вплинули на загальну поширеність резистентності до антибіотиків у стаціонарах. Автори зазначили, що у восьми відділеннях 9-місячні періоди циклічної заміни та змішування антибіотиків не змінили загальної поширеності стійких грамнегативних бактерій. Отже, структурована політика ротації призначення антибактеріальних препаратів стосовно грамнегативних бактерій не може розглядатися як засіб для зниження стійкості до антибіотиків у стаціонарі.
Незважаючи на отримані результати, провідний дослідник van Duijn засвідчив, що багато питань щодо ротації антибіотиків залишаються без відповіді. Можливо, інші стратегії ротації, з яких вони перевірили лише дві, потребують додаткового вивчення для з’ясування, яка саме модель підходить найкраще для кожного конкретного відділення. Зрештою, зменшення загального об’єму антибіотиків, які застосовуються у стаціонарах, залишається найкращою стратегією зниження селективного тиску та контролю за появою антибіотикорезистентних бактерій. Цього краще досягти за допомогою вдосконаленої діагностики й визначення, яким пацієнтам потрібні антибіотики, а яким – ні, зменшення терміну застосування антибіотиків за допомогою відповідних біомаркерів [14].
Зростання резистентності бактерій поруч із дефіцитом нових антибіотиків широкого спектра дії підкреслює актуальність оптимізації використання наявних лікарських засобів. Теоретичні та клінічні дослідження містять різні висновки, які стосуються корисності циклічної терапії першої лінії. P. Abel et al. (2014) виконали метааналіз патоген-специфічних клінічних досліджень, які порівнюють принцип ротації зі стандартною практикою. Було проаналізовано результати 46 клінічних досліджень стосовно впливу ротації на внутрішньолікарняні інфекції. Автори використовували теоретичні моделі, які відображають різні інфекції та лікарняні заклади для порівняння циклічності з випадковим призначенням різних лікарських засобів (змішування). Вони навели реалістичне припущення, що терапія змінюється при неефективному лікуванні першою лінією, яку назвали «регульованим циклом/змішуванням». У відповідності до попередніх теоретичних досліджень встановили, що за суворих режимів ротація спричинила негативний вплив. Проте за регульованих режимів зникають поодинокі випадки резистентності. Теоретична модель свідчить про те, що «регульована ротація» є особливо корисною для запобігання мультирезистентності. Незважаючи на те що модель передбачає тривалість періодів ротації до одного місяця, очікується, що надто тривалі періоди циклу є шкідливими [8].
Практичні аспекти ротації антибіотиків у стаціонарі
Даними метааналізу доведено, що ротація є корисною для зменшення загального рівня захворюваності на госпітальні інфекції та частоту появи резистентних збудників, особливо за низьких базових рівнів резистентності. У випадку якщо встановлені проблеми з резистентністю не піддаються контролю відповідними заходами, необхідно розглянути питання поліпшення рекомендацій щодо застосування антибіотиків. Зокрема, має бути розглянута відповідна циклічна програма (табл. 1).
Після верифікації наведених чинників здійснюється вибір антибіотиків для циклів, тривалість кожного циклу і порядок, в якому будуть застосовуватися вибрані препарати. Якщо антибіотик корелює з істотною резистентністю у звичайних клінічних ізолятах, краще обмежити його застосування, наскільки це є можливим, з метою зменшення селективного тиску. Наприклад, можуть призначатися карбапенем і фторхінолон після призначення цефалоспорину 3-го (Цефтум) і 4-го покоління (Квадроцеф). Менш доречним заходом буде застосування антипсевдомонадних пеніцилінів, які подібно до цефалоспоринів індукують механізми резистентності.
Тривалість циклів не має бути дуже великою, але вона повинна бути достатньою, щоб не спричинити плутанину серед практикуючих лікарів. Чинник, який слід брати до уваги, – це можливість поширення інформації про антибіотик, який застосовується у визначеній фазі циклу, кількість лікарів, які беруть участь у лікувальному процесі. В яких умовах буде застосовуватися ротація – в закритому чи відкритому підрозділі? Яким буде рівень залучення фармацевтів? Слід визначити, чи дозволяється деескалація і коли можлива деескалація стосовно інших антибіотиків.
Деескалація – це емпірична АБТ препаратами широкого спектра, який охоплює всі ймовірні збудники конкретної інфекції (табл. 2). Перший етап деескалаційної терапії – призначення антибіотиків широкого спектра. Другий етап – призначення антибіотиків вузького спектра після отримання даних про виділений збудник та його чутливість до антибактеріального препарату. Це дозволяє уникнути необґрунтовано тривалої АБТ, розвитку антибіотикорезистентності, високої летальності, яка асоціюється із неадекватною АБТ. Ескалація – перехід від менш до більш ефективних антибіотиків. Такий підхід може спричинити генералізацію інфекції та значно погіршити стан хворого. Шляхи посилення антибіотикочутливості наведено в табл. 2.
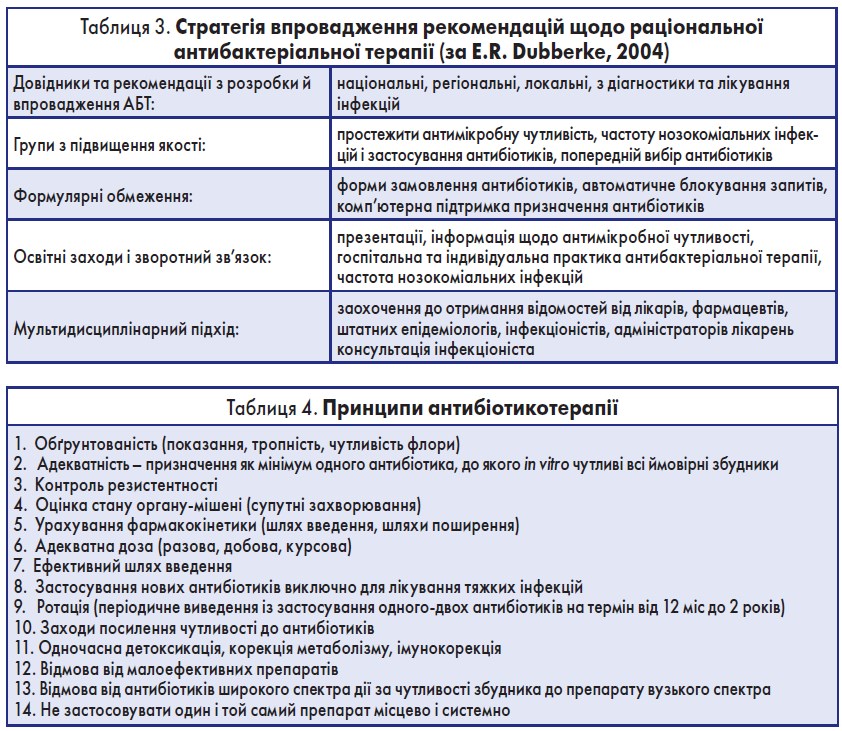
У проведених дослідженнях застосовували цикли тривалістю від 1 до 4 міс, що дозволило підтримувати рівновагу, хоча оптимальна тривалість циклу остаточно не встановлена. Після визначення чутливості й верифікації механізмів розвитку резистентності, вибору АБТ, послідовності циклів та їх тривалості особа, яка залучена до дослідження, повинна переконатися в імплементації програми. Загалом, методи імплементації циклічних програм ідентичні принципам і рекомендаціям стосовно АБТ, але існує певна особливість – це обмеження на застосування антибіотиків, яке змінюється залежно від циклу (табл. 3-5). Зазначимо, що обов’язковою умовою є зворотний зв’язок із лікарями для отримання інформації про те, який антибіотик застосовується в даній фазі циклу [9, 10].
У разі виникнення нового захворювання слід застосовувати інший антибіотик, відмінний від того, що використовувався раніше, навіть якщо останній довів свою високу ефективність. Вдруге його можна застосувати не раніше ніж через 3-5 міс. Така концепція АБТ має назву «пацієнт-специфічна ротація антибіотика».
Але перед клініцистами залишається низка питань стосовно принципу ротації антибіотиків.
- Коли її слід здійснювати в лікарні або в окремих відділеннях? З одного боку, через високі витрати, пов’язані зі зміною антибіотика, можна стверджувати, що цю процедуру не слід вводити там, де немає серйозної проблеми резистентності. З іншого боку, вплив циклічної зміни антибіотика може бути максимізований внаслідок уведення його до того, як така проблема виникне, запобігаючи появі та поширенню детермінант резистентності.
- У яких підрозділах лікарні необхідно запровадити принцип ротації антибіотиків? Підрозділи спеціалізованої допомоги, такі як ВРІТ, піддаються циклічній заміні антибіотиків через високу частоту серйозних інфекцій, які є причиною більш частого призначення антибактеріальних препаратів, що призводить до підвищеного ризику появи бактеріальних патогенів, стійких до лікарських засобів.
- Чи можна повернутись до призначення антибіотиків, які були виведені з лікувального алгоритму через високі або зростаючі показники стійкості до них, не сричиняючи повторну появу резистентних штамів?
- На яких параметрах ґрунтується принцип заміни антибіотиків: на інтервалі часу, на стані пацієнта або виді інфекційного захворювання?
- Які пацієнти мають бути введені у протокол ротації?
- Які оптимальні еквівалентні агенти/схеми лікування має містити кожен цикл?
- Яка оптимальна тривалість кожного циклу?
- Якщо цикли занадто короткі, зміни частоти резистентності не можуть бути виявлені. Наприклад, у дослідженні, проведеному Bradley et al., зниження частоти колонізації глікопептид-резистентних ентерококів було найбільш помітним у другій половині другої фази протоколу ротації. З іншого боку, занадто велика тривалість може бути пов’язана із високим ризиком виникнення стійких штамів під час циклу.
- Чи має тривалість кожного циклу бути однаковою? (Чи розвивається стійкість до різних антибіотиків з однаковою швидкістю?)
- Які заходи слід контролювати (показники резистентності, клінічний результат, у т. ч. показники смертності, тривалості перебування пацієнта у стаціонарі, економічної ефективності)?
- Якою має бути антимікробна резистентність стосовно антибіотиків?
- Як слід відрізняти лікарняні штами від ізолятів, набутих у позагоспітальних умовах?
- Чи слід контролювати використання антибіотиків і показники резистентності до них, крім тих, які знаходяться в циклічному режимі?
Отже, концепція ротації (циклічної заміни) класу антибіотиків у стаціонарі була запропонована як одна з можливих стратегій, спрямованих на зниження поширеності антибіотикорезистентності. Вона полягає в тому, що певний клас антибіотиків або окремий препарат перестає використовуватися у стаціонарі протягом встановленого періоду часу, після чого знову вводиться у схеми терапії. Такий підхід дозволяє сповільнити розвиток резистентності у бактерій до антибіотиків, що піддаються циклічній зміні.
Щоквартальна ротація антибіотиків, які входять у схеми емпіричної терапії, може бути ефективним способом зниження захворюваності та летальності, пов’язаної із хірургічними інфекціями, спричиненими антибіотикорезистентними штамами мікроорганізмів. Згідно з даними досліджень, застосування ротації антибіотиків призводило до значного зниження частоти інфекцій, спричинених резистентними штамами як грампозитивних, так і грамнегативних мікроорганізмів. Летальність, пов’язана із цими інфекціями, також знижувалася в пацієнтів, які отримували антибіотики, що входили до схеми ротації [5, 6].
Вибір антимікробних препаратів, які використовуються у схемах ротації, ґрунтується на щомісячних локальних даних про найбільш поширені збудники інфекцій та їхню чутливість до антибіотиків. Використання ротації антибіотиків є найефективнішим, коли вона застосовується протягом обмеженого часу у відділеннях із відносно стабільною мікрофлорою, таких як ВРІТ. Однак цей підхід вимагає проведення адекватного мікробіологічного моніторингу, пов’язаного з монотонним селективним тиском одного препарату і можливим розвитком резистентності до інших класів препаратів за рахунок передачі генів, що забезпечують стійкість. Нарешті, збільшення доступності різних класів антибіотиків, можливо, є більш ефективною стратегією зниження ризику розвитку резистентності, ніж ротація антибіотиків.
Висновки
Першим кроком до зниження ризику появи та розповсюдження антибіотикорезистентних бактерій є оптимізація політики контролю над інфекціями і формування адекватної політики стосовно АБТ. У випадку якщо не буде розроблена оптимальна тактика застосування антибіотиків, навряд чи можна буде досягти стабілізації та зниження рівня резистентності. До методів покращення застосування антибіотиків належать: розробка рекомендацій, освітніх програм для лікарів, моніторинг та зворотний зв’язок, комп’ютеризація призначень антибіотиків, пряме введення інформації від фармацевтів та експертів з інфекційних захворювань.
Призначення антибіотиків у відповідності до зазначених підходів допоможе стримати антибіотикорезистентніcть шляхом обмеження застосування, комбінованої терапії та циклічної зміни цих препаратів. Чинники, які впливають на антибіотикорезистентність, дуже складні й потребують подальшого вивчення. Необхідно встановити, яким чином формуються механізми резистентності при різних стратегіях застосування антибіотиків.
Відносно ротації антибіотиків слід зазначити, що не відомо, якою має бути їх кількість протягом циклу, а також тривалість кожного циклу. Це, ймовірно, слід визначати на місцевому рівні, в окремій популяції пацієнтів, залежно від мікроорганізму-мішені та механізмів формування резистентності. Таким чином, успіх від циклічного застосування антибіотиків може бути пов’язаний із розвитком антибактеріальної гетерогенності в поєднанні із належним підходом до застосування антибіотиків.
Циклічне застосування антибіотиків може бути перспективним напрямом для підтримки антибактеріальної гетерогенності та оптимізації менеджменту в даній галузі. Наведені підходи є багатообіцяючими стосовно контролю над ендемічною резистентністю нозокоміальних грамнегативних бактерій.
Література
- Андрух В.С., Андрух В.Н., Слободян М.В. Антибіотики і антибіотикорезистентність: проблеми і шляхи вирішення // Дитячий лікар. –2017;5-6 (56-57). – C.33-35.
- Бассетти М. Бактериальный пейзаж в отделении реанимации // Медицинская газета. – 2018, № 31. http://www.mgzt.ru/31-ot‑8-avgusta‑2018-g/bakterialnyi-peizazh-v-otdelenii-reanimatsii.
- Краснов В.Г. Ротация режимов антимикробной терапии в отделении реанимации / Автореф. дис. канд. мед. наук. – М., 2010. – 24 с. http://medical-diss.com/medicina/rotatsiya-rezhimov-antimikrobnoy-terapii-v-otdelenii-reanimatsii#ixzz5tpCNToOI.
- Пасєчніков С.П., Нашеда С.В., Шило В.М. Раціональна емпірична антибіотикотерапія гострих інфекцій сечостатевої системи в урологічному стаціонарі // Медицинские аспекты здоровья мужчины. – 2016, № 3 (22). – C. 5-9.
- Antibiotic Cycling and Antibiotic Mixing: Which One Best Mitigates Antibiotic Resistance?/ R.E. Beardmore, R. Pen-a-Miller, F. Gori [et al.] // Mol. Biol. Evol. – 2017;34(4):802-817 doi:10.1093/molbev/msw292.
- Antibiotic Rotation and Development of Gram-Negative Antibiotic Resistance/H.J. van Loon, M.R. Vriens, A.C. Fluit [et al.] // Am. J Respir. Crit. Care Med. –2005;171:480-487. doi: 10.1164/rccm.200401-070OC.
- Brown E.M, Nathwani D. Antibiotic cycling or rotation: a systematic review of the evidence of efficacy // J Antimicrob. Chemother. – 2005;55:6-9. doi:10.1093/jac/dkh482.
- Cycling Empirical Antibiotic Therapy in Hospitals: Meta-Analysis and Models / W.P. Abel, R. Kouyos, S. Abel [et al.] // PLoS Pathog. – 2014;10(6): e1004225. doi:10.1371/journal.ppat.1004225.
- Dubberke E.R. Fraser V.J. Cycling and Other Strategies to Slow and Reverse Antibiotic Resistance // St Louis Infect. Med. – 2004;21(11):544-556. http://www.medscape.com/ viewarticle/494369.
- Masterton R.G. Antibiotic cycling: more than it might seem? // J Antimicrob. Chemother. – 2004.DOI: 10.1093/jac/dkh506.
- Pilot study of antibiotic cycling in a pediatric intensive care unit / W.J. Moss, M.C. Beers, E. Johnson [et al.] // Crit. Care Med. – 2002;30(8):1877-82.
- Smith D.(2015) What is antibiotic rotation? // https://www.quora.com/What-is-antibiotic-rotation/answer/Drew-Smith‑48.
- Strategy of Antibiotic Rotation: Long-Term Effect on Incidence and Susceptibilities of Gram-negative Bacilli Responsible for Ventilator-Associated Pneumonia / D. Gruson, G. Hilbert, F. Vargas [et al.] // Crit Care Med. – 2003;31(7):1908-1914.
- The effects of antibiotic cycling and mixing on antibiotic resistance in intensive care units: a cluster-randomised crossover trial/P.J.van Duijn, W. Verbrugghe, P.G. Jorens [et al.] // Lancet Infect. Dis. – 2018;18(4):401-409. doi: 10.1016/S1473-3099(18)30056-2.
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 1 (39), 2020 р.