26 липня, 2020
Діабетична ретинопатія: мультидисциплінарний підхід до діагностики та лікування
 Сьогодні є всі підстави вважати цукровий діабет (ЦД) епідемією, адже він поширений у всіх верствах населення всіх країн світу з різним рівнем доходів. ЦД – небезпечна хвороба ще й з погляду тяжких ускладнень, які вона спричинює. Одним із таких серйозних наслідків є діабетична ретинопатія (ДР) – ключова причина порушень зору в осіб середнього віку. Утраті зору внаслідок ДР можна запобігти шляхом застосування мультидисциплінарного підходу суспільної охорони здоров’я широкого рівня до діагностики та лікування. Це, зокрема, розробка програм скринінгу ДР, своєчасне направлення пацієнтів до медичних закладів і спеціалізованих центрів для консультації з досвідченими фахівцями з проблем зору, призначення економічно доступних і водночас ефективних лікарських засобів для терапії загрозливих зору рівнів ДР.
Сьогодні є всі підстави вважати цукровий діабет (ЦД) епідемією, адже він поширений у всіх верствах населення всіх країн світу з різним рівнем доходів. ЦД – небезпечна хвороба ще й з погляду тяжких ускладнень, які вона спричинює. Одним із таких серйозних наслідків є діабетична ретинопатія (ДР) – ключова причина порушень зору в осіб середнього віку. Утраті зору внаслідок ДР можна запобігти шляхом застосування мультидисциплінарного підходу суспільної охорони здоров’я широкого рівня до діагностики та лікування. Це, зокрема, розробка програм скринінгу ДР, своєчасне направлення пацієнтів до медичних закладів і спеціалізованих центрів для консультації з досвідченими фахівцями з проблем зору, призначення економічно доступних і водночас ефективних лікарських засобів для терапії загрозливих зору рівнів ДР.
У лютому, у ході чергового засідання науково-освітнього проекту «Школа ендокринолога», було висвітлено вітчизняну статистику захворюваності: офіційно зареєстровано майже 1,3 млн пацієнтів із ЦД. У 2017 р. було виявлено майже 104 тис нових випадків захворювання.
За даними Центру медичної статистики (ЦМС) Міністерства охорони здоров’я (МОЗ) України, приріст показника поширеності ЦД за 2003-2013 рр. становив 55,1%, показник первинної захворюваності (виявлення) ЦД за 2004-2013 рр. зріс на 59,2%. На 1 січня 2016 року, знову ж таки за інформацією ЦМС МОЗ України, зареєстровано 1 223 604 хворих на ЦД (без урахування даних з АР Крим та окупованих територій Донецької та Луганської областей).
В уніфікованому клінічному протоколі з менеджменту ЦД сказано, що, за даними ЦМС МОЗ України, на початок 2011 року зареєстровано 1 813 000 пацієнтів із ЦД, з яких майже 90-95% – пацієнти із ЦД 2 типу. Проте осіб із недіагностованою патологією насправді в 3-4 рази більше кількості виявлених хворих. Щодо загальносвітової статистики, то в 2017 р. приблизно 451 млн дорослої популяції в усьому світі страждали на діабет, і, за прогнозами ВООЗ, до 2045 року ця цифра зросте до 693 млн. Увесь драматизм ситуації полягає в тому, що зростає також і кількість летальних випадків, більшість яких зумовлена мікро- та макросудинними ускладненнями діабету.
До діабетичних мікросудинних ускладнень, зумовлених пошкодженням дрібних кровоносних судин, належать ДР, діабетична хвороба нирок і діабетична нейропатія.
Діабетична ретинопатія
ДР є специфічним мікросудинним ускладненням ЦД. Вона залишається провідною причиною втрати зору в працездатного дорослого населення. Повідомляється, що в пацієнтів із тяжким рівнем ДР спостерігається зниження якості життя та погіршення фізичного, емоційного й соціального благополуччя; до того ж на цю когорту пацієнтів витрачається більше ресурсів системи охорони здоров’я. Епідеміологічні дослідження та клінічні випробування продемонстрували, що оптимальний контроль рівня глюкози в крові, артеріального тиску (АТ) та ліпідів крові може знизити ризик розвитку ретинопатії та уповільнити її прогресування. Своєчасне лікування за допомогою лазера, фотокоагуляція, внутрішньоочне введення інгібітора фактора росту ендотелію судин (vascular endothelial growth factor, VEGF) здатні запобігти втраті зору за умови розвитку тяжкої форми ретинопатії, особливо при діабетичному макулярному набряку (ДМН). Оскільки на ранніх стадіях ретинопатії можуть бути відсутні будь-які симптоми, необхідно регулярно проводити обстеження осіб із діабетом. Епідеміологічні дослідження показали, що приблизно в 1 особи з 3 осіб із ЦД є ДР, а в 1 з 10 – проліферативна ДР (ПДР) або ДМН. З огляду на ці співвідношення, можна припустити, що від 100 до 120 млн осіб страждають на ДР і, можливо, від 20 до 30 млн хворих мають ПДР або ДМН. Викликає неабияку стурбованість і той факт, що під час обстеження у 20% пацієнтів ДР виявляють одночасно з встановленням діагнозу ЦД і що більшість обстежених не знає про ризик виникнення в них ДР та інших ускладнень.
ДР розвивається при тривалому перебігу ЦД і асоційована з поганим контролем рівнів цукру в крові, АТ і ліпідів крові. Серед пацієнтів із ЦД 2 типу вікової когорти >30 років із перебігом захворювання <5 років 40% тих, хто приймає інсулін, і 24% тих, хто його не приймає, мають проліферативну ретинопатію. При встановленій тривалості діабету до 19 років частота ДР збільшується до 84 і 53% відповідно.
Глікемічний контроль
Це головний модифікуючий фактор ризику. З моменту виявлення ДР тривалість діабету в плані прогнозу прогресування ретинопатії стає менш важливим фактором ризику, ніж глікемічний контроль. У ході основних досліджень із цього питання продемонстровано, що жорсткий глікемічний контроль зменшує частоту й прогресування ДР. Меншою мірою ретельний контроль АТ, особливо у хворих на ЦД і гіпертонію, також знижує ризик і прогресування ДР і, що не менше важливо, серцево-судинних ускладнень.
Загальні факти про ДР
- ДР – це пошкодження кровоносних судин у сітківці, яке виникає внаслідок прогресування діабету.
- ДР – основна причина втрати зору в Україні.
- Симптоми включають помутніння зору, утруднення бачення кольорів, спливаючі пятна і навіть повну сліпоту.
- Хворі на діабет мають перевіряти свій зір принаймні 1 раз на рік, щоб виключити ДР.
- Деякі операції на сітківці можуть полегшити симптоми, але контроль діабету і ранніх симптомів є найбільш ефективними способами запобігання ДР.
За останні два десятиріччя відбулися важливі зміни в діагностиці та класифікації діабету та інших порушень обміну глюкози. Це й широке застосування оптичної когерентної томографії для оцінки товщини сітківки і внутрішньоретинальної патології, і широкоформатна фотографія очного дна для виявлення клінічно мовчазних мікросудинних уражень. Сьогодні лікування ДМН здійснюється шляхом інтравітреального введення інгібітора VEGF, ті ж самі ліки тепер використовуються для терапії ПДР. Більш ефективні препарати й удосконалення пристроїв самодіагностики також поліпшили здатність пацієнтів оптимізувати метаболічний контроль.
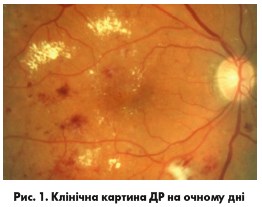 ДР – високоспецифічне нейросудинне ускладнення діабету 1 і 2 типу, поширеність якого корелює як з тривалістю діабету, так і з рівнем контролю глікемії. В основі розвитку ДР лежить ураження судин сітківки з подальшими змінами на очному дні у вигляді мікроаневризм, крововиливів, твердих і м’яких ексудативних вогнищ, появи новоутворених судин, відшарування сітківки й розвитку вторинної глаукоми (рис. 1).
ДР – високоспецифічне нейросудинне ускладнення діабету 1 і 2 типу, поширеність якого корелює як з тривалістю діабету, так і з рівнем контролю глікемії. В основі розвитку ДР лежить ураження судин сітківки з подальшими змінами на очному дні у вигляді мікроаневризм, крововиливів, твердих і м’яких ексудативних вогнищ, появи новоутворених судин, відшарування сітківки й розвитку вторинної глаукоми (рис. 1).
Точний механізм виникнення ретинопатії при діабеті залишається незрозумілим, проте для пояснення типового перебігу та історії хвороби було запропоновано кілька теорій:
- Вплив соматотропного гормону. Схоже, гормон росту відіграє певну роль у розвитку та прогресуванні ДР. Виявлено, що ДР є зворотною в жінок, які мали післяпологовий геморагічний некроз гіпофіза (синдром Шейхана). Це призвело до суперечливої практики абляції гіпофіза для лікування або профілактики ДР у 1950-х роках та виявлення ефективності лазерного лікування. Слід зазначити, що про ДР повідомлялося також у пацієнтів із гіпопітуїтаризмом.
- Тромбоцити і в’язкість крові. Різноманітність гематологічних порушень при діабеті, такі як посилення агрегації еритроцитів і зниження їх деформації, збільшення агрегації тромбоцитів та адгезія, зумовлюють погіршення кровообігу, пошкодження ендотелію та осередкової оклюзії капілярів. Це призводить до ішемії сітківки, а далі – до розвитку ДР.
- Альдоредуктаза та вазопроліферативні фактори. ЦД викликає аномальний метаболізм глюкози внаслідок зниження рівня або активності інсуліну. Вважається, що підвищений рівень глюкози в крові структурно-фізіологічно впливає на капіляри сітківки, що спричинює їх функціональну та анатомічну некомпетентність. Постійне підвищення рівня глюкози в крові перетворює надлишок глюкози в шлях альдози-редуктази в певних тканинах, який перетворює цукор в алкоголь (наприклад, глюкозу в сорбіт, галактозу в дульцитол). Інтрамуральний перицит капілярів сітківки впливає на цей підвищений рівень сорбіту, і з часом втрачається первинна функція сітківки – авторегуляція її капілярів. Це призводить до слабкості та можливої сакулярної перетинки стінок капілярів. Такі мікроаневризми є найбільш ранніми виявленими ознаками ретинопатії. Наслідком підвищеної проникності цих судин є виток рідини та білкового матеріалу, що клінічно проявляється потовщенням (активація вазопроліферативних факторів) сітківки та ексудатом. Якщо набряк і ексудація залучають макулу, може спостерігатися зниження центрального зору.
- Макулярний набряк. Це найчастіша причина втрати зору в пацієнтів із непроліферативною ДР (НПДР). Є теорія, згідно з якою макулярний набряк розвивається внаслідок підвищеного рівня діацилгліцерину, зумовленого маневровим надлишком глюкози. Вважається, що це активує протеїнкіназу С, що, своєю чергою, впливає на динаміку крові сітківки, особливо на проникність і потік, а це призводить до витоку рідини та потовщення сітківки.
- Гіпоксія. У міру прогресування захворювання відбувається можливе закриття капілярів сітківки, що веде до гіпоксії. Інфаркт шару нервових волокон призводить до утворення плям, із супутнім застоєм в аксоплазматичному потоці. Більш обширна гіпоксія сітківки запускає компенсаторні механізми в оці, аби забезпечити тканинам достатню кількість кисню. Аномалії венозного калібру, такі як венозне згинання, петлі та розширення, означають посилення гіпоксії і майже завжди спостерігаються на межі ділянок капілярної неперфузії.
- Неоваскуляризація. Подальше збільшення ішемії сітківки викликає вироблення вазопроліферативних факторів, які стимулюють утворення нових судин. Позаклітинний матрикс розщеплюється спочатку протеазами, а нові судини, що виникають головним чином із венул сітківки, проникають у внутрішню обмежувальну мембрану та утворюють капілярну сітку між внутрішньою поверхнею сітківки та задньою гіалоїдною поверхнею. У пацієнтів із ПДР нічна переривчаста гіпоксія/реоксигенація,через порушення дихання уві сні може бути фактором ризику неоваскуляризації райдужної оболонки та/або кута. Неоваскуляризація найчастіше спостерігається на межі перфузованої та неперфузованої сітківки та виникає вздовж судинних аркад та на голівці зорового нерва. Нові судини прориваються і розростаються вздовж поверхні сітківки. Вони крихкі і дуже проникні, тому легко руйнуються, що призводить до крововиливу в склоподібну порожнину або передретинальний простір [4].
Об’єднаний метааналіз 35 досліджень, який проводився в усьому світі з 1980 по 2010 рік, виявив, що глобальна поширеність ДР і ПДР у пацієнтів із ЦД складає 35,4% і 7,5% відповідно. У країнах із високим доходом ДР є найбільш частою причиною нових випадків сліпоти в дорослих у віці 20-74 роки. Глаукома, катаракта та інші порушення зору спостерігаються раніше й частіше у хворих на діабет.
Крім тривалості діабету є й інші фактори, що підвищують ризик розвитку ретинопатії або асоційовані з нею: це хронічна гіперглікемія, нефропатія, гіпертонія та дисліпідемія. Як показали результати великих проспективних рандомізованих досліджень, інтенсивне лікування діабету з метою досягнення нормоглікемії здатне запобігти початку й прогресуванню ДР і/або затримати ці процеси.
Зазначено, що зниження АТ зменшує прогресування ретинопатії в пацієнтів із ЦД 2 типу, хоча прагнення за будь-яку ціну досягти систолічного АТ (САТ) <120 мм рт. ст. не дає додаткової вигоди проти САТ <140 мм рт. ст. У пацієнтів із дисліпідемією прогресування ретинопатії може сповільнюватися додаванням фенофібрату, особливо при дуже легкій НПДР на початку дослідження. Кілька випадків і контрольоване проспективне дослідження демонструють, що вагітність у жінок із діабетом 1 типу може посилювати ретинопатію і загрожувати ризиком зниження зору, особливо при низькому глікемічному контролі.
Рекомендації
Оптимізуйте глікемічний контроль для зменшення ризику або сповільнення прогресування ДР. Оптимізуйте АТ і контроль рівня ліпідів у сироватці, щоб знизити ризик або сповільнити прогресування ДР.
У цілому ретинопатія починається з легких непроліферативних порушень, що характеризуються збільшенням числа мікроаневризм, які можуть розростатися та стоншуватись. Зі збільшенням ступеня тяжкості спостерігається підвищення проникності та оклюзії судин, а також прогресування від помірної і тяжкої НПДР до ПДР, що характеризується зростанням нових кровоносних судин на сітківці і задньої поверхні склоподібного тіла. Визначення стадій ДР представлено в таблиці 1.
Є декілька механізмів «запуску» втрати зору через ДР. По-перше, центральний зір може погіршуватися внаслідок набряку жовтої плями через підвищену проникність судин і/або неперфузію капілярів. По-друге, проліферація нових кровоносних судин при ПДР і скорочення супутньої фіброзної тканини можуть деформувати сітківку і призвести до її тракційного відшарування і, як слідство, до значної й часто незворотної втрати зору. По-третє, нові кровоносні судини можуть кровоточити, що спричиняє подальше ускладнення – преретинальні або склоподібні крововиливи. Ці клінічно очевидні судинні зміни супроводжуються пошкодженням нейронів сітківки, що є остаточним загальним шляхом втрати зору.
У декількох епідеміологічних дослідженнях описані показники прогресування ДР. Когорта з найтривалішим періодом спостереження – Вісконсінське епідеміологічне дослідження ДР (WESDR), в якому повідомлялося про 25-річне прогресування ДР у пацієнтів із діабетом 1 типу. WESDR почав набір у 1979 р., коли можливості глікемії, кров’яного тиску і ліпідного контролю були помітно обмежені, якщо порівняти з доступними сьогодні варіантами. Фактори ризику, виявлені під час WESDR – більш тривалий перебіг діабету, підвищені гіперглікемія, кров’яний тиск і дисліпідемія, – залишаються актуальними, тоді як показники прогресування в більш пізніх дослідженнях можуть помітно відрізнятися. Наприклад, дані WESDR передбачили приблизно 40% частоту прогресування протягом 4 років для дослідження «Дія з контролю серцево-судинного ризику при діабеті (ACCORD)», але фактична частота прогресування в пацієнтів із діабетом 2 типу на момент завершення дослідження склала всього 10%. У таблиці 2 представлені відношення шансів (ВШ), пов’язаних із найбільш послідовно асоційованими факторами ризику ретинопатії в дослідженнях, проведених у сучасних умовах контролю глюкози, ліпідів і АТ [1].
У ході WESDR було виявлено зв’язок між початком ретинопатії та тривалістю діабету. Встановлено, що прогресування захворювання є функцією базової ретинопатії. Більш виражена форма останньої призводила до більшої частоти прогресування ретинопатії до такої форми, яка вже загрожувала втратою зору. У пацієнтів із ЦД 2 типу на світлинах, на яких не було виявлено ретинопатії, спостерігалося на 54% менше прогресування ПДР протягом 10 років порівняно з пацієнтами із вираженою НПДР на початковому рівні [47].
При тривалому перебігу діабету гіперглікемія була найбільш послідовно пов’язаним фактором ризику розвитку ретинопатії. Численні клінічні випробування підтверджують асоціацію поганого контролю рівня глюкози та ретинопатії. Дослідження контролю за діабетом та ускладненнями (DCCT), рандомізоване клінічне дослідження інтенсивного глікемічного контролю порівняно зі звичайним глікемічним контролем у хворих на діабет 1 типу, продемонструвало, що інтенсивна терапія знизила розвиток або прогресування ДР на 34-76% [50]. Крім того, DCCT виявило остаточну залежність між гіперглікемією та діабетичними мікросудинними ускладненнями, зокрема ретинопатією [18]. Чим раніше починали інтенсивну терапію, тим більшого ефекту досягали. Інтенсивна терапія мала значущий сприятливий вплив на весь діапазон ретинопатії. Зниження HbA1c на 10%, наприклад з 10 до 9% або з 8 до 7,2%, знижує ризик прогресування ретинопатії на 43% [52].
Проспективне дослідження ЦД у Великій Британії (United Kingdom Prospective Diabetes Study – UKPDS) пацієнтів, яким нещодавно діагностували діабет 2 типу, остаточно довело, що покращений контроль рівня глюкози в крові знижує ризик розвитку ретинопатії та нефропатії та, можливо, нейропатії [8]. Загальний показник мікросудинних ускладнень зменшився на 25% у хворих, які отримували інтенсивне лікування, порівняно зі звичайною терапією. Епідеміологічний аналіз даних UKPDS показав пряму кореляцію між ризиком виникнення мікросудинних ускладнень та контролем глікемії, тобто кожне зниження процентного пункту HbA1c (наприклад, з 9% до 8%) було асоційоване зі зниженням ризику мікросудинних ускладнень на 35%.
Нещодавно завершене дослідження ефективності медикаментозної терапії ACCORD (n=2556; тривало протягом 4 років) виявило, що інтенсивний контроль глікемії знижує ризик прогресування ДР у пацієнтів із ЦД 2 типу тривалістю 10 років [9].
Результати дослідження діабетичних мікросудинних ускладнень DCCT, UKPDS та ACCORD демонструють, що хоча інтенсивна терапія не запобігає ретинопатії повністю, вона знижує ризик розвитку та прогресування ДР. Клінічно ми спостерігаємо більш високу ймовірність збереження зору та зменшення потреби в лікуванні. Крім того, усі ці дослідження продемонстрували, що через 3 роки після закінчення початкового клінічного випробування ефект інтенсивного контролю глікемії зберігався, незважаючи на те що обидві групи лікування мали однаковий рівень HbA1c. Насправді через 25 років після припинення дії DCCT частота очної хірургії була знижена в тих, кому був призначений інтенсивний глікемічний контроль [19]. У DCCT з різними інтервалами корисні ефекти інтенсивного контролю глікемії зберігалися, але з часом зменшувалися. Цей стійкий сприятливий ефект поза клінічним випробуванням спостерігався в пацієнтів із діабетом 1 та 2 типу.
Контроль АТ також вивчався в кількох спостережних та клінічних випробуваннях, у тому числі в UKPDS, в якому було зазначено 37% зниження мікросудинних порушень, наприклад ДР і, зокрема, ДМН, при зниженні САТ із середнього значення 154 мм рт. ст. до 144 мм рт. ст. [20]. Однак більш недавнє дослідження ретинопатії ACCORD не виявило ані шкідливого, ані сприятливого ефекту при порівнянні САТ 120 мм рт. ст. та 140 мм рт. ст. в аналогічній групі пацієнтів [9].
За результатами кількох інших досліджень припустили, що дисліпідемія може грати роль у прогресуванні ДР, оскільки пов’язана з твердим ексудатом сітківки та втратою зору. Для зниження рівня тригліцеридів у сироватці крові було проведено 2 випробування фенофібрату [9, 21]. Хоча фенофібрат не впливає на серцево-судинний ризик, обидва дослідження показали його вплив на прогресування ДР. Дослідження фенофібрату при діабеті (FIELD) виявило корисні ефекти фенофібрату (200 мг щодня) порівняно з плацебо для зменшення потреби в лазерній фотокоагуляції (ЛФ) [21]. Піддослідження учасників FIELD зі світлинами очного дна показали сприятливий вплив згідно з даними шкали дослідження раннього лікування ДР (ETDRS, the Early Treatment Diabetic Retinopathy Study scale), особливо в пацієнтів із ретинопатією на початковому етапі та на етапі макулярного набряку. Дослідження ACCORD, в якому порівнювали фенофібрат 160 мг щодня із симвастатином против плацебо з симвастатином, виявило, що ризик прогресування ДР зменшився на третину. Ефект був особливо значущим у пацієнтів із вже наявною ДР. Ефект фенофібрату не був очевидним після припинення прийому препарату в клінічному випробуванні ACCORD.
 Результати згаданих двох великих рандомізованих випробувань, досліджень ACCORD Eye та FIELD дають підстави припустити, що фенофібрат може бути потенційною терапією у хворих на ДР. Слід зазначити, що ці результати не являли собою висновки підгрупового аналізу, а корисні ефекти були підкріплені двома великими рандомізованими контрольованими клінічними випробуваннями. Через відсутність доказів сприятливого впливу на серцево-судинні захворювання медики неохоче призначають фенофібрат пацієнтам із ДР. Але на сьогодні є достатньо даних, які дають можливість у рамках співпраці між офтальмологами та сімейним лікарем розглянути таке лікування у хворих на ДР [2, 3].
Результати згаданих двох великих рандомізованих випробувань, досліджень ACCORD Eye та FIELD дають підстави припустити, що фенофібрат може бути потенційною терапією у хворих на ДР. Слід зазначити, що ці результати не являли собою висновки підгрупового аналізу, а корисні ефекти були підкріплені двома великими рандомізованими контрольованими клінічними випробуваннями. Через відсутність доказів сприятливого впливу на серцево-судинні захворювання медики неохоче призначають фенофібрат пацієнтам із ДР. Але на сьогодні є достатньо даних, які дають можливість у рамках співпраці між офтальмологами та сімейним лікарем розглянути таке лікування у хворих на ДР [2, 3].
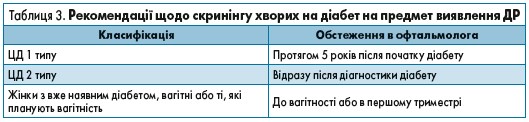
Стратегії скринінгу залежать від частоти появи та прогресування ДР та від факторів ризику, які змінюють ці показники. Короткий зміст рекомендацій щодо скринінгу наведено в таблиці 3.
Щодо виникнення ДР, то ретинопатія, яка загрожує втратою зору, рідко виникає у хворих на ЦД 1 типу в перші 3-5 років захворювання або до статевого дозрівання [22, 23]. Оскільки ретинопатія розвивається через 5 років після того, як розвинулася гіперглікемія, дорослі пацієнти з діабетом 1 типу мають пройти первинний розширений та всебічний очний огляд в офтальмолога протягом 5 років після встановлення діагнозу діабету.
У 1/5 частини хворих на ЦД 2 типу спостерігається ретинопатія на момент першої діагностики діабету [24, 25]. Таким пацієнтам після встановлення діагнозу також необхідно пройти той самий комплексний очний огляд в офтальмолога.
Рекомендації
- Доросла популяція хворих на ЦД 1 типу має пройти первинний розширений та всебічний огляд в офтальмолога протягом 5 років після початку діабету (рівень доказовості В).
- Пацієнти з ЦД 2 типу мають пройти первинний розширений та всебічний огляд в офтальмолога на момент встановлення діагнозу (рівень доказовості В).
- Якщо під час одного або декількох щорічних очних оглядів не виявлено доказів ретинопатії, обстеження проводять кожні 2 роки.
- Якщо виявлений будь-який рівень ДР, наступні розширені обстеження сітківки пацієнтів із ЦД 1 або 2 типу мають повторюватися щонайменше щороку.
- Якщо ретинопатія прогресує або загрожує зору, обстеження необхідно проводити частіше (рівень доказовості В).
- Жінкам із уже наявним діабетом 1 або 2 типу, які планують вагітність або завагітніли, слід проконсультуватися щодо ризику розвитку та/або прогресування ДР (рівень доказовості В).
- Обстеження очей має проводитися до вагітності або в першому триместрі в жінок із наявним ЦД 1 або 2 типу; у подальшому цю когорту пацієнтів необхідно контролювати кожен триместр та протягом року після пологів,
- як зазначено за ступенем ретинопатії (рівень доказовості В).
- Хоча світлина із зображенням сітківки може бути інструментом скринінгу на предмет виявлення ретинопатії, вона не є заміною комплексного очного огляду, який доцільно проводити принаймні спочатку та через деякий час,
- як рекомендує лікар-офтальмолог (рівень доказовості Е).
Подальші обстеження зазвичай проходять щороку ті пацієнти з діабетом 1 або 2 типу, в яких ретинопатія мінімальна або повністю відсутня. У хворих на ЦД 1 та 2 типу, в яких ретинопатія мінімальна або повністю відсутня після одного або декількох очних оглядів, повторний огляд може проводитись не щороку, а кожні 2 роки. Так, в осіб із добре контрольованим діабетом 2 типу не було виявлено ризику розвитку значної ретинопатії протягом трьох років після очного обстеження, результати якого були в межах норми [26]. Частішого обстеження в офтальмолога потребують пацієнти з прогресуючою ретинопатією.
Вагітність часто асоційована зі швидким прогресуванням ДР при встановленні діабету 1 і 2 типу [27]. Жінки, в яких розвинувся гестаційний ЦД, не потребують очного огляду під час вагітності, тому що в цей період не мають підвищеного ризику розвитку ДР [28]. Жінки з уже наявним діабетом 1 або 2 типу, які планують завагітніти, мають пройти обстеження в офтальмолога та отримати консультацію щодо ризику розвитку та прогресування ДР. Під час вагітності необхідно проходити огляд очей протягом першого триместру з подальшими візитами залежно від ступеня тяжкості ретинопатії [12, 29]. Також слід пам’ятати, що у вагітних швидке здійснення жорсткого глікемічного контролю в умовах ретинопатії може бути пов’язане з погіршенням ретинопатії [12]. У хворих на ЦД регулярне спостереження, раннє виявлення та лікування зорової ретинопатії дають можливість запобігти втраті зору через ДР до 98% [30].
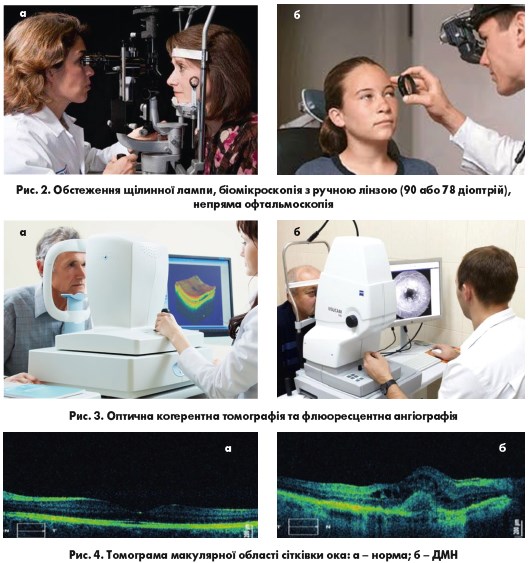 Обстеження проводить офтальмолог, який має досвід у діагностиці ДР. Якщо вона буде виявлена, рекомендується оперативне лікування. Комплексна оцінка лікарем-офтальмологом складатиметься з розширеного обстеження щілинної лампи, зокрема біомікроскопії з ручною лінзою (90 або 78 діоптрій) (рис. 2), непрямої офтальмоскопії та тестування, що може включати оптичну когерентну томографію та флюоресцентну ангіографію (рис. 3).
Обстеження проводить офтальмолог, який має досвід у діагностиці ДР. Якщо вона буде виявлена, рекомендується оперативне лікування. Комплексна оцінка лікарем-офтальмологом складатиметься з розширеного обстеження щілинної лампи, зокрема біомікроскопії з ручною лінзою (90 або 78 діоптрій) (рис. 2), непрямої офтальмоскопії та тестування, що може включати оптичну когерентну томографію та флюоресцентну ангіографію (рис. 3).
Світлини із зображенням сітківки для дистанційної консультації експертів мають великий потенціал для надання скринінгу в ситуаціях, коли пацієнт проживає в місцевості, де доступ до кваліфікованіх фахівців із проблем зору відсутній. Якісні світлини очного дна допомагають виявити більшість клінічно значущих ознак ДР. Інтерпретацію зображень має проводити досвідчений лікар. Водночас світлини із зображенням сітківки не є заміною комплексного огляду очей, який треба проводити принаймні на початку діагностики ДР та надалі з певним інтервалом, як рекомендує лікар-офтальмолог. Результати очних оглядів мають бути задокументовані та передані спеціалісту з охорони здоров’я.
Хоча оптимізація рівнів глюкози в крові, АТ та ліпідів у сироватці крові в поєднанні з відповідним плановим розширеним оглядом очей може суттєво знизити ризик втрати зору від ускладнень ДР, у значної частини хворих на діабет розвиваються ДМН або проліферативні зміни, які потребують втручання (табл. 4.) [3].
Діабетичний макулярний набряк
ДМН – найбільш поширена причина зниження зору в пацієнтів із ЦД. Унаслідок структурних змін в ендотелії судин сітківки відбувається порушення гематоретинального бар’єра, підвищення проникності судинної стінки і накопичення рідини в міжклітинному просторі сітківки [7].
Здавлювання клітин інтраретинальною речовиною призводить до поступової загибелі нейронів і незворотного погіршення зору [14]. Традиційно фокальна ЛФ була стандартним методом лікування очей із клінічно значущим набряком макули (КЗНМ), що визначається як набряк сітківки, розташований на відстані або в межах 500 мкм від центру макули, або набряк області диска. Дослідницькою групою з вивчення ефективності ранньої терапії ДР (ETDRS) показано, що лікування КЗНМ фокальною лазерною фотокоагуляцією значно знижувало ризик подальшої втрати зору (рис. 4).
Лікування базується на наявності ЦДМН або набряку в центральному підполі сітківки діаметром 1 мм. Інтравітреальна терапія препаратами, які нейтралізують VEGF, сьогодні вважається стандартом у лікуванні очей із ЦДМН. Є три речовини анти-VEGF, які зазвичай використовують у терапії осіб із ЦДМН – бевацизумаб, ранібізумаб та афліберцепт. За останніми даними Клінічно-дослідницької мережі ДР (DRCRN), для очей із ЦДМН та хорошим рівнем гостроти ≥20/40 кожен засіб анти-VEGF ефективно покращує гостроту зору. Однак у пацієнтів із ЦДМН та нижчим рівнем гостроти, ≤20/50, більш ефективним виявився афліберцепт [4, 38]. Більшість пацієнтів потребують майже щомісячного прийому інтравітреальної терапії анти-VEGF-препаратами протягом перших 12 міс лікування, з подальшим зменшенням кількості ін’єкцій для підтримки ремісії від ЦДМН.
Сьогодні вивчається кілька нових методів терапії ретинопатії; вони спрямовані на альтернативні шляхи лікування ЦДМН, забезпечують стійку інтравітреальну терапію фармакологічними препаратами або дають можливість використовувати пероральні чи місцеві неінвазивні засоби. Інтравітреальна стероїдна терапія при ЦДМН була оцінена в декількох дослідженнях. Ураховуючи гірший результат інтравітреальної терапії стероїдами у великому дослідженні DRCRN, а також розвиток таких побічних явищ, як катаракта та глаукома, на тлі вживання стероїдів, проти анти-VEGF препаратів, вищезгадані засоби рідко застосовують як терапію першої лінії при ЦДМН.
Рекомендації щодо лікування:
- Слід негайно направити пацієнтів із будь-яким рівнем макулярного набряку, тяжкою непроліферативною ДР (попередника ПДР) або з будь-якою формою ПДР до офтальмолога з досвідом лікування ДР (рівень доказовості А).
- Лазерна фотокоагуляційна терапія зменшує ризик зниження зору в пацієнтів із ПДР високого ризику та, у деяких випадках, тяжкою НПДР (рівень доказовості А).
- Внутрішньокісткові ін’єкції інгібітору фактору росту ендотелію судин показані при центральному ураженні ДМН, що виникає під фовеальним центром і може загрожувати зору при читанні (рівень доказовості А).
- Наявність ретинопатії не є протипоказанням до терапії ацетилсаліциловою кислотою (АСК) для кардіопротекції, оскільки АСК не збільшує ризик крововиливу в сітківку (рівень доказовості А).
Проліферативна діабетична ретинопатія
Дослідження ДР продемонструвало, що панретинальна ЛФ (ПЛФ) знижує ризик втрати зору в очах, уражених ПДР [39]. Найбільш позитивний результат спостерігався в пацієнтів з основними ознаками високого ризику розвитку ПДР, що складаються з неоваскуляризації диску, яка перевищує або дорівнює чверті площі диску, будь-якої неоваскуляризації диску з крововиливом у склоподібне тіло або з неоваскуляризацією сітківки, що більше або дорівнює половині розміру диску.
Однак більшість спостережень виявили, що швидка регресія неоваскуляризації сітківки відбувається в пацієнтів, які отримують інтравітреальну анти-VEGF-терапію при ЦДМН, що зробило ці засоби альтернативним лікуванням ПДР. У рандомізованому дослідженні, проведеному DRCRN, порівнювали інтравітреальний ранібізумаб із ПЛФ для покращення результатів гостроти зору в пацієнтів із ПДР. Статистично достовірної різниці гостроти зору між групами ранібізумабу та ПЛФ протягом 2 років не було [40]. Однак середні показники гостроти зору в згаданий період були кращими в групі ранібізумабу.
ЦД – дуже серйозне і поширене в усьому світі захворювання, асоційоване зі смертністю, зумовленою мікро- та макросудинними ускладненнями, зокрема з боку органів зору. Одним із таких ускладнень є ДР, яка стає все більш важливою причиною втрати зору. При правильному скринінгу, хорошому контролі глюкози та артеріального тиску і ранньому втручанні як з хірургічною, так і фармакологічною терапією у багатьох пацієнтів можна уникнути серйозної втрати гостроти зору. Для офтальмолога стратегія ведення має бути адаптована для кожного пацієнта, щоб максимізувати збереження зору й мінімізувати побічні ефекти, виходячи з унікальних проявів кожного пацієнта та прогресування ДР.
Література
- Diabetic Retinopathy: A Position Statement by the American Diabetes Association Diabetes Care 2017 Mar; 40(3): 412-418. https://doi.org/10.2337/dc16-2641
- Маньковський Б.М. Нові терапевтичні можливості профілактики та лікування діабетичної ретинопатії. Науковий симпозіум: Діабетична ретинопатія при ЦД 2 типу: Мультидисциплінарний підхід до діагностики та лікування. 30.04.2020 р.
- Вітовська О.П. Діабетична ретинопатія – грізне ускладнення цукрового діабету: стан проблеми в Україні, сучасні підходи до діагностики та лікування. Науковий симпозіум: Діабетична ретинопатія при ЦД 2 типу: Мультидисциплінарний підхід до діагностики та лікування. 30.04.2020 р.
- Хайтович М.В. Сучасні напрями фармакологічної корекції діабетичної ретинопатії. Науковий симпозіум: Діабетична ретинопатія при ЦД 2 типу: Мультидисциплінарний підхід до діагностики та лікування. 30.04.2020 р.
- Abdhish R Bhavsar, MD; Chief Editor: Romesh Khardori, MD, PhD, FACP. Diabetic Retinopathy. May 19, 2020.
- Leske M.C., Wu S.-Y., Hennis A. et al.; Barbados Eye Study Group. Hyperglycemia, blood pressure, and the 9-year incidence of diabetic retinopathy: the Barbados Eye Studies. Ophthalmology 2005;112:799-805 pmid: 15878059CrossRefPubMedWeb of ScienceGoogle Scholar.
- Chew E.Y., Davis M.D., Danis R.P. et al. Action to Control Cardiovascular Risk in Diabetes Eye Study Research Group. The effects of medical management on the progression of diabetic retinopathy in persons with type 2 diabetes: the Action to Control Cardiovascular Risk in Diabetes (ACCORD) Eye Study. Ophthalmology 2014;121:2443-2451 pmid: 25172198 CrossRefPubMedGoogle Scholar.
- UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS33). Lancet 1998;352:837-853 pmid: 9742976CrossRefPubMedWeb of ScienceGoogle Scholar.
....
51. Diabetes Control and Complications Trial Research Group. Progression of retinopathy with intensive versus conventional treatment in the Diabetes Control and Complications Trial. Ophthalmology 1995; 102:647–661CrossRefPubMedWeb of ScienceGoogle Scholar
Повний список літератури знаходиться в редакції.
Підготувала Юлія Золотухіна
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 2 (50), 2020 р.