8 вересня, 2020
Коморбідна депресія на тлі ішемічної хвороби серця: ефективність венлафаксину
 На даний час депресивні розлади є однією із провідних медико-соціальних проблем. ВООЗ порівнює депресію з епідемією, що охопила людство. Депресивні розлади займають перше місце серед причин втрати працездатності в економічно розвинених країнах. Депресія часто зустрічається при різних станах: артеріальній гіпертензії (АГ), ішемічній хворобі серця (ІХС), інсульті, хронічних захворюваннях легень, онкопатології, цукровому діабеті (ЦД), синдромі набутого імунодефіциту, хворобі Паркінсона, а також у разі втрати зору і слуху. При цьому пацієнти, що страждають на депресію на тлі будь-якого іншого захворювання, мають виразніші симптоми як депресії, так і супутньої патології та важче пристосовуються до хвороби порівняно з тими, хто не має коморбідної депресії.
На даний час депресивні розлади є однією із провідних медико-соціальних проблем. ВООЗ порівнює депресію з епідемією, що охопила людство. Депресивні розлади займають перше місце серед причин втрати працездатності в економічно розвинених країнах. Депресія часто зустрічається при різних станах: артеріальній гіпертензії (АГ), ішемічній хворобі серця (ІХС), інсульті, хронічних захворюваннях легень, онкопатології, цукровому діабеті (ЦД), синдромі набутого імунодефіциту, хворобі Паркінсона, а також у разі втрати зору і слуху. При цьому пацієнти, що страждають на депресію на тлі будь-якого іншого захворювання, мають виразніші симптоми як депресії, так і супутньої патології та важче пристосовуються до хвороби порівняно з тими, хто не має коморбідної депресії.
Встановлено, що ІХС та інсульт є чинниками ризику розвитку депресії у літньому віці [26]. Проте існує і зворотний зв’язок: депресія достовірно підвищує ризик виникнення транзиторних ішемічних атак та інсульту, і ця кореляція не залежить від інших факторів ризику, включно з АГ і ЦД [21, 49]. При обстеженні 10547 жінок віком 47‑52 роки без гострих порушень мозкового кровообігу (ГПМК) в анамнезі було виявлено, що депресія асоційована із дворазовим підвищенням вірогідності виникнення інсульту протягом найближчих 12 років [27]. У дослідженні за участю 80 574 жінок віком 54‑79 років без ГПМК в анамнезі наявність депресії була пов’язана зі зростанням імовірності розвитку інсульту протягом найближчих шести років зі співвідношенням ризиків 1,29 [39].
Депресія являє собою незалежний чинник ризику розвитку серцево-судинних захворювань (ССЗ) [18, 32, 47]. Зокрема, депресія є предиктором розвитку ІХС у здорових людей [25]. Для молодих осіб віком 23‑35 років, які мають високі (≥16) бали за шкалою депресії Центру епідеміологічних досліджень США, характерна достовірно більша вірогідність появи АГ порівняно з такими із низьким показником (≤7) [33].
Наявність депресії у хворих на ССЗ ускладнює їхній перебіг [18, 22, 23, 49]. На додаток, депресія визначає якість життя пацієнтів з ІХС, і цей зв’язок не залежить від тяжкості перебігу хвороби [20]. При оцінці якості життя 503 хворих на стенокардію за допомогою сіетлівського опитувальника через 18 місяців після перенесеного інфаркту міокарда (ІМ) в осіб із депресією спостерігалися достовірно нижчі бали порівняно з такими без депресії [34]. Обстеження 5038 пацієнтів із верифікованим діагнозом ІХС та/або АГ показало, що при виявленні під час первинного огляду клінічних ознак депресії ризик смерті через ССЗ збільшується в 1,64 рази, а загальної летальності – в 1,82 рази [38].
Депресія є чинником ризику несприятливого прогнозу у пацієнтів із гострим коронарним синдромом [29]. За різними даними, поширеність депресивних симптомів протягом року після перенесеного ІМ становить від 22,7 до 25,5% [28, 49]. При цьому всі категорії депресивних симптомів після перенесеного ІМ, незалежно від тривалості й характеру, пов’язані з вищими рівнями повторної госпіталізації та смертності, частішими приступами стенокардії, більшими фізичними обмеженнями і гіршою якістю життя порівняно з пацієнтами без депресії [40]. Депресивні симптоми у постінфарктному періоді є предикторами відновлення працездатності [37]. Депресія після перенесеного ІМ незалежно корелює зі зростанням смертності від усіх причин на 22% і ризику серцево-судинних (СС) подій на 13% [31]. Таким чином, депресія є фактором ризику підвищеної летальності в осіб з ІХС.
Через високу поширеність депресивних розладів у загальномедичній і, особливо, кардіологічній практиці заслуговують на увагу питання терапії депресій поза психіатричною мережею [1, 3, 12, 13]. На сьогодні накопичені переконливі дані щодо використання антидепресантів при лікуванні кардіологічних хворих. Найбільш значущими дослідженнями у цьому напряму є SADHART і ENRICHD [15, 24, 42, 45].
На сучасному етапі розробки й удосконалення методів лікування депресії велику увагу приділено участі моноамінних нейротрансмітерів у патогенезі захворювання та особливостям впливу на ці ланки новостворених психотропних антидепресивних препаратів [44, 46]. Фармакологічна дія різних класів антидепресантів зумовлена різноманітними механізмами їхньої взаємодії з тими чи іншими рецепторами головного мозку й участю у різних обмінних процесах. Пошук тимоаналептиків, які взаємодіють як із серотонінергічними, так і з норадренергічними рецепторами, тобто з подвійним механізмом дії, привів до створення нового класу антидепресантів – селективних інгібіторів зворотного захоплення серотоніну й норадреналіну (СІЗЗСН). Поява антидепресантів із подвійним механізмом дії супроводжувалася підвищенням ефективності лікування депресивних станів і дозволила досягти ремісії у 45% хворих [11, 46, 48].
Одним із СІЗЗСН є венлафаксин – перший тимоаналептик третього покоління. В багатьох дослідженнях він оцінюється як «еталонний» у групі цих сполук [9, 30, 41]. Венлафаксин та його основний метаболіт О-дезметилвенлафаксин є потужними інгібіторами зворотного захоплення серотоніну і норадреналіну та слабкими інгібіторами зворотного захоплення дофаміну. Як основний препарат, так і його зазначений метаболіт знижують β-адренергічну реактивність. Венлафаксин не впливає на мускаринові, холінергічні, гістамінові, α1-адренергічні, опіоїдні, бензодіазепінові, оренциклідинові й N-метил-α-аспартатні рецептори головного мозку. При цьому співвідношення моноамінового перенесення (серотонін/норадреналін) венлафаксином дорівнює 30 (порівняно з 9,4 у іншого СІЗЗСН дулоксетину). Це свідчить про значне переважання серотонінергічного ефекту в дії венлафаксину, схожого за силою із СІЗЗС. Групою авторитетних експертів у галузі психофармакотерапії було показано, що венлафаксин можна розглядати як один із найефективніших антидепресантів [35].
На сьогодні накопичені переконливі дані про дозозалежність терапевтичного ефекту венлафаксину. За широкого діапазону лікувальної дії венлафаксин послідовно включає у спектр своєї нейрохімічної активності серотонінергічні, норадренергічні й дофамінергічні рецептори [2]. При порівнянні ефективності венлафаксину та антидепресантів із групи СІЗЗС у метааналізі 34 рандомізованих подвійних сліпих досліджень, що включали 8 тис. осіб із депресивними розладами різного ступеня виразності, були встановлені статистично достовірні переваги венлафаксину як препарату для досягнення ремісії [36].
Окрім того, до особливостей венлафаксину слід віднести високу селективність його фармакологічної дії, що зумовлює сприятливий профіль переносимості й безпеки [4, 8, 17]. Також відзначено високу ефективність препарату при широкому спектрі соматогенних і постінсультних депресій [9, 43].
Клінічні дослідження венлафаксину виконували переважно в умовах психіатричного стаціонара. Щодо використання препарату в пацієнтів кардіологічного профілю, даних у доступній літературі замало. Лише у незначній кількості закордонних публікацій зустрічаються відомості про лікування депресії у хворих віком від 60 років із супутніми ССЗ. Слід зазначити, що в цих роботах автори не приділяли особливої уваги вивченню впливу препарату на основні гемодинамічні показники, хоча при застосуванні венлафаксину у психіатричній практиці у низці випадків відзначено зміни частоти серцевих скорочень і рівня АТ [8].
Таким чином, сучасна тактика ведення пацієнтів з ІХС потребує нової стратегії – своєчасного виявлення депресивних розладів і обґрунтованого використання у лікувальному процесі не тільки препаратів соматичної дії, але й психофармакотерапії. У кардіологічній практиці застосування психотропних засобів, зокрема антидепресантів, є непростим клінічним завданням для терапевтів і кардіологів.
Було проведене дослідження, мета якого полягала в оцінці терапевтичної ефективності й безпеки венлафаксину в пацієнтів з ІХС і супутніми депресивними розладами.
Матеріали й методи дослідження
Загалом обстежено 52 пацієнти, з них 40 (76,9%) чоловіків і 12 (23,1%) жінок віком від 30 до 75 років (середній вік – 64,2±5,6 року) зі стабільною стенокардією I‑III функціонального класу (ФК), госпіталізованих у кардіологічну клініку Військово-медичного клінічного центру Західного регіону (м. Львів). Усі включені хворі дали письмову згоду на участь у дослідженні.
Критеріями виключення були:
- період вагітності та лактації у жінок;
- коморбідність депресивного епізоду з гострим психотичним станом;
- тяжкий ступінь АГ (АТ ≥180/115 до початку терапії);
- будь-які клінічно значущі декомпенсовані захворювання нирок, печінки, дихальної СС-систем;
- органічні захворювання центральної нервової системи;
- гіперчутливість до досліджуваних препаратів.
У пацієнтів, які приймали будь-які психотропні препарати до початку дослідження, проводили 7-денний період «відміни» (wash out).
Пацієнти були розподілені на три групи:
- Учасники першої групи (n=17) отримували традиційну стандартизовану терапію з флуоксетином у дозі 20‑40 мг/добу;
- Хворим другої групи (n=20) було призначено традиційне стандартизоване лікування з венлафаксином по 75‑150 мг/добу;
- Пацієнти третьої групи (контрольна, n=15) отримували традиційну стандартизовану терапію без додаткового призначення антидепресантів.
Флуоксетин був обраний як препарат порівняння з антидепресантів групи СІЗЗС, що найчастіше виписується хворим. На етапі включення не було виявлено достовірних відмінностей між групами за віком, статтю, наявністю асоційованих соматичних захворювань, чинників ризику СС-ускладнень і психосоціальних факторів. Фармакотерапію ІХС здійснювали відповідно до клінічних рекомендацій із використанням основних груп препаратів (антиангінальних, антигіпертензивних, гіполіпідемічних, антитромботичних).
Тривалість дослідження становила вісім тижнів. Анкетування пацієнтів проводили на початку терапії, через 7 днів, 4 і 8 тижнів від ініціювання лікування. У ці ж дні протягом всього періоду спостереження реєстрували всі небажані явища (НЯ) із зазначенням їхньої тяжкості, часу виникнення і тривалості.
Ефективність дії антидепресантів оцінювали за ступенем редукції балів згідно з госпітальною шкалою депресії і тривоги HADS (HADS) відносно оцінки лікування за такими градаціями: редукція балів до 20% – «незначний», 21‑50% – «помірний», 51‑80% – «добрий» і 81‑100% – «значний» ефект (включно із «практичним одужанням»). Зниження сумарного показника за HADS до ≤6 означало повне досягення ремісії. Збереження бальної оцінки тяжкості депресії за HADS на попередньому рівні або збільшення сумарного значення розцінювали як відсутність ефекту або «погіршення» стану.
Завершили дослідження 50 пацієнтів. Один хворий вибув через відмову продовжувати лікування, ще один – у зв’язку з розвитком НЯ на 3-й день терапії.
Для первинного скринінгу депресії та тривоги, а також спостереження у динаміці застосовували шкалу HADS й опитувальник депресії Бека (BDI). Рівень тривоги аналізували за шкалою особистісної (ОТ) і ситуативною тривожності (СТ) Спілбергера –Ханіна.
Добове моніторування артеріального тиску (АТ) із визначенням середніх показників систолічного (САТ) і діастолічного АТ (ДАТ) проводили апаратом «АВРМ‑04» (Meditech Ltd, Угорщина). У дослідженні використовували пакети прикладних програм Statistica for Windows v. 8.0 (StatSoft Inc, США, 2012) відповідно до рекомендацій з обробки результатів медико-біологічних досліджень.
Результати дослідження та обговорення
За сумою балів зідно з HADS і BDI до початку лікування легкий ступінь депресивних розладів зареєстрований у 20 (38,5%) пацієнтів, помірний – у 27 (51,9%), тяжкий – у 5 (9,6%), тобто у більшості хворих депресія була легкого і помірного ступеня тяжкості.
Через вісім тижнів терапії у всіх групах відзначене достовірне зниження частоти нападів стенокардії, а також кількості споживання сублінгвального нітрогліцерину на тиждень. У 1-й групі число нападів стенокардії на тиждень зменшилося на 35,3%, у 2-й – на 40% (для обох р<0,05), у 3-й – на 26,7% (р>0,05). Частка споживання сублінгвального нітрогліцерину на тиждень знизилася у всіх досліджуваних групах: у 1-й – на 29,4% (р>0,05), у 2-й – на 35% (р<0,05), у 3-й – на 26,7% (р>0,05).
У пацієнтів із депресією початковий рівень офісного САТ становив 152,4±5,7 мм рт. ст., ДАТ – 91,5±3,8 мм рт. ст., тоді як через вісім тижнів – 132,7±4,3 і 78,2±3,0 мм рт. ст. відповідно. Достовірне зниження показників САТ і ДАТ виявили у загальній групі хворих (p=0,007) та окремо у 1-й і 2-й (p=0,017 і p=0,028 відповідно). У 3-й групі рівень САТ і ДАТ змінився недостовірно (p=0,241), що свідчить про вплив депресії на регуляторні процеси при АГ.
Слід зазначити, що більшість пацієнтів у 1-й (58,8%) і 2-й (60%) групах систематично приймали гіполіпідемічні препарати, тоді як у 3-й групі – лише 26,6%. Відмову основної частки хворих у 3-й групі застосовувати гіполіпідемічні засоби можна пояснити низькою прихильністю до лікування через збереження депресії.
Ефективність венлафаксину була вищою, ніж флуоксетину: середній сумарний бал виразності депресії за HADS зменшився на 85,9% при лікуванні венлафаксином і на 64,2% – флуоксетином. Вже до кінця 1-го тижня використання венлафаксину спостерігалася позитивна відповідь на терапію: зменшення депресії було на рівні «незначного» ефекту, але наближалося до 20% ступеня редукції розладів, що межує з «помірним» поліпшенням. Очевидне «помірне» покращання (редукція оцінки за HADS на 33,2%) було встановлене до 14-го дня лікування; між 21-м і 28-м днями терапевтичний ефект досягав діапазону «доброго» зі зниженням бальних значень за HADS на ≥50%. Вже до 8-го тижня вплив лікування венлафаксином наближався до «значного» (до 76,7% редукції тяжкості симптомів депресії). У 13 із 20 хворих (65% випадків), які закінчили курс лікування венлафаксином, депресія повністю редукувала, і спостерігався «вихід» у ремісію (загальний бал за HADS ≤6).
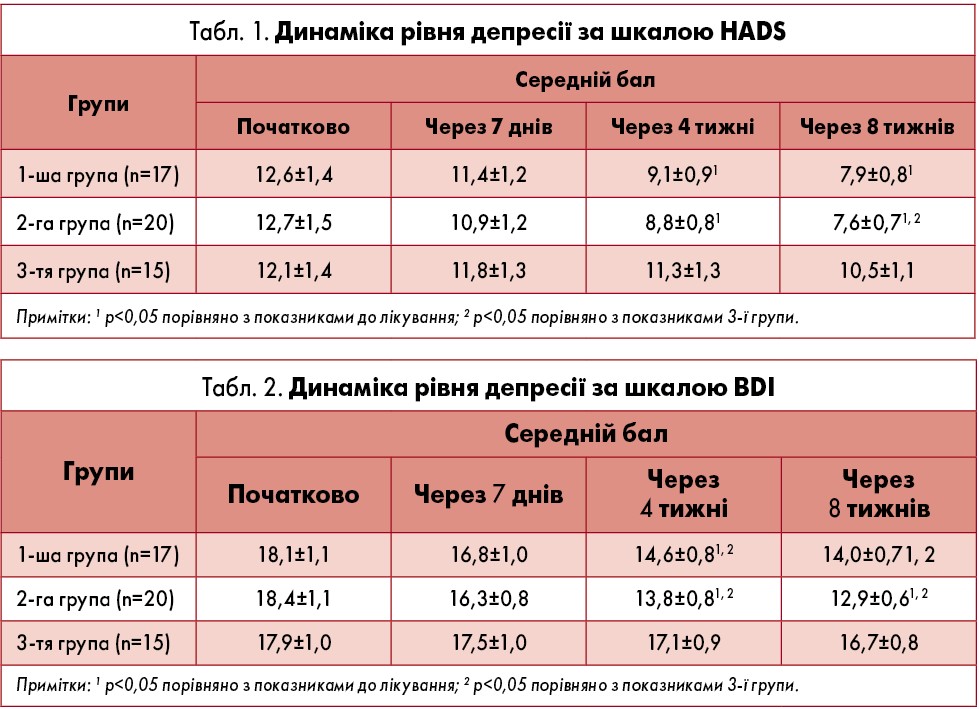
Початково не було виявлено достовірних відмінностей між групами за показниками депресії та тривоги. У 1-й і 2-й групах на тлі лікування спостерігали достовірне зниження ступеня депресії. Так, середній сумарний бал депресії за HADS порівняно з вихідним рівнем зменшився на 4-й тиждень терапії: у 1-й групі – на 27,8% (р=0,044), у 2-й – на 30,7% (р=0,027). Далі антидепресивна активність препаратів зростала, і до 8-го тижня лікування сумарний бал депресії за HADS у 1-й групі зменшився на 37,3% (р=0,007), у 2-й – на 40,2% (р=0,004). У 3-й групі на 4-й тиждень терапії відзначили зниження показників депресії за HADS і BDI на 6,6 і 4,5% (для обох р>0,05) відповідно, а на 8-й тиждень –13,2 і 6,7% (для обох р>0,05) відповідно (табл. 1).
Середній бал депресії за BDI на 4-й тиждень лікування щодо вихідного рівня у 1-й і 2-й групах зменшився на 19,3% (р=0,015) і 25% (р=0,002) відповідно, що можна розцінити як помірний антидепресивний ефект. До 8-го тижня терапії середній показник депресії у групах приймання антидепресантів достовірно відрізнявся від контрольної (табл. 2).
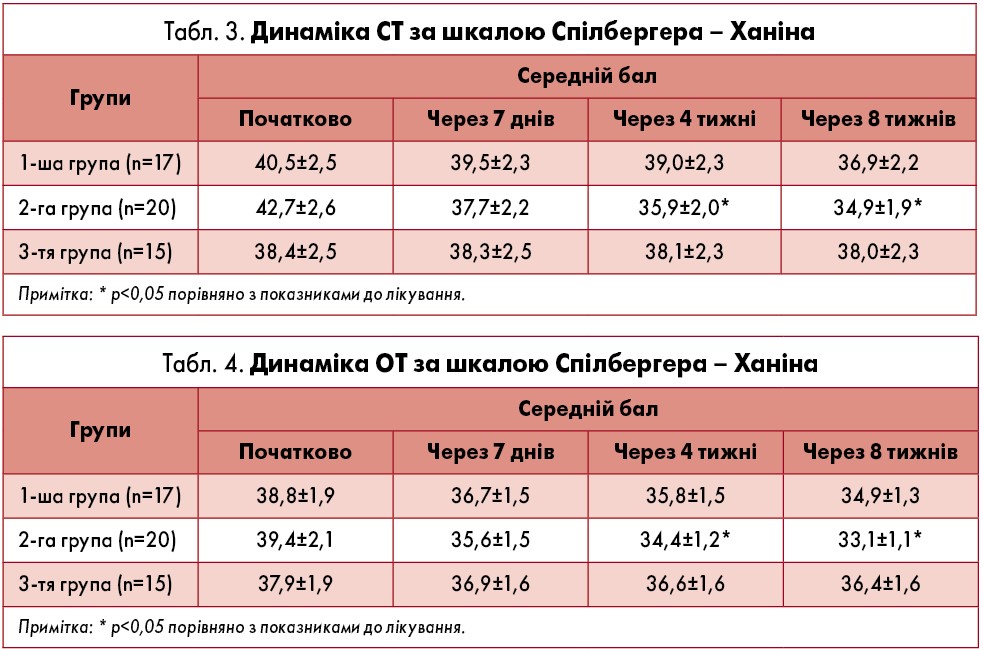
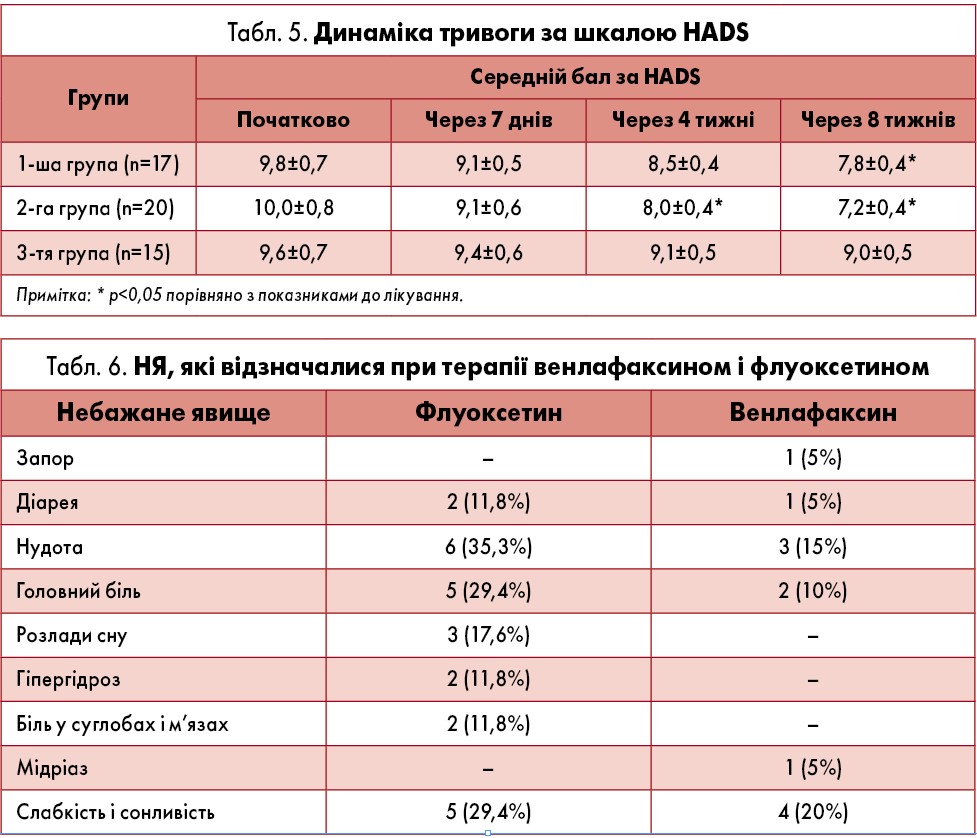
У 2-й групі виявили достовірне зниження ступеня СТ і ОТ через чотири тижні лікування порівняно з вихідним рівнем – на 15,9% (р=0,045) і 12,7% (р=0,046) відповідно, через вісім тижнів – на 18,3% (р=0,02) і 16% (р=0,014) відповідно (табл. 3, 4). Також у 2-й групі достовірно зменшився середній бал тривоги за HADS, починаючи з 4-го тижня лікування – на 20% (р=0,031), через вісім тижнів – на 28% (р=0,003) (табл. 5). Достовірного зниження показників тривожності у 1-й і 3-й групах не спостерігали.
Результати проведеного дослідження дозволяють дійти висновку про вищу антидепресивну активність сучасного антидепресанту групи СІЗЗСН венлафаксину порівняно із представником групи СІЗЗС флуоксетином. Венлафаксин проявив себе як препарат із задовільною переносимістю. Лише один пацієнт вибув із дослідження через мідріаз. НЯ було нетяжке, проте хворий відмовився від продовження терапії та коригування дози. У 6 (30%) пацієнтів зареєстрували 12 випадків НЯ (табл. 6), проте їхній зв’язок із прийманням венлафаксину оцінювали як «імовірний» лише у трьох випадках, а в інших – як «передбачуваний». Аналіз інтенсивності НЯ показав, що у 8 (66,7%) випадках НЯ були слабкими, у 4 (33,3%) – помірними. У більшості випадків жодних заходів щодо терапії не вживали, проте в 5 (41,7%) дозу препарату було зменшено.
Найбільшу питому вагу серед НЯ мали нудота і седація, які в основній кількості випадків було виявлено в перші два тижні терапії. Сонливість зазвичай спостерігалася на 1-му тижні лікування, що відображає певну седативну дію препарату в перші дні терапії. У більшості випадків (80%) НЯ були минучими. Вони розвивалися у 1-й тиждень терапії при застосуванні дози 150 мг/добу і надалі, в міру продовження терапії, редукувалися. Важливо зауважити, що такі НЯ, як затримка сечовипускання, зниження АТ, сухість у роті, блювання, судоми, ортостатизм, які властиві переважно трициклічним антидепресантам, при лікуванні венлафаксином не зустрічалися.
При терапії флуоксетином НЯ були переважно легкого або помірного ступеня, всі хворі продовжували лікування.
Таким чином, венлафаксин добре переносився, рідкісні НЯ, пов’язані з його прийманням, були виражені слабо або помірно і розвивалися здебільшого у перші два тижні лікування. Вони не потребували припинення терапії та не впливали на режим її проведення.
Висновки
Поліпшення психологічного і психічного стану пацієнтів, редукція симптомів депресії за призначення антидепресивної терапії сприять підвищенню прихильності хворих на ІХС до лікування, правильній оцінці свого соматичного стану, регулярному прийманню необхідних базисних препаратів.
На тлі тривалої антидепресивної терапії виявлено достовірне зниження частоти ангінозних нападів та використання короткодіючих нітратів. Антигіпертензивні препарати спільно з антидепресантами мали більшу ефективність. Включення антидепресантів у схеми терапії ІХС не тільки приводить до редукції симптомів депресії, але й сприяє зниженню ризику СС-ускладнень.
Венлафаксин чинить виразну тимоаналептичну дію і має збалансований характер впливу на симптоматику тривоги, з помірним седативним ефектом на 1-му тижні терапії. Особливо важливою є здатність препарату достатньо швидко редукувати депресивні розлади будь-якої тяжкості, а також широке коло коморбідних депресії тривожних порушень.
Лікарський засіб із виразною антидепресивною активністю збалансованої дії венлафаксин на сучасному етапі розвитку психофармакотерапії може бути віднесений до активних антидепресантів як високоефективний представник третього покоління цього класу психотропних сполук. Завдяки широкому спектру і глибині антидепресивної дії, а також задовільній переносимості, венлафаксин можна рекомендувати як препарат вибору при лікуванні ССЗ, перебіг якої ускладнений депресією.
Таким чином, можна дійти наступних висновків:
- Впровадження у кардіологічну практику сучасних антидепресантів надало терапевтам та кардіологам унікальну можливість проводити лікування депресій у хворих на ССЗ при мінімальній участі психіатрів.
- Венлафаксин є сучасним ефективним і безпечним антидепресантом потрійної дозозалежної дії, який може бути рекомендований як препарат вибору при терапії депресивних і тривожних розладів. З огляду на високу поширеність афективних проявів, це зумовлює доцільність його широкого застосування як на госпітальному етапі, так і в амбулаторній практиці.
- Венлафаксин в адекватних дозах має сприятливий кардіальний профіль, який проявляється у значному зменшенні внеску психологічних факторів у реалізацію кардіальних симптомів. Це позитивно впливає на клінічний перебіг ІХС і низку чинників СС-ускладнень за тривалий період спостереження.
- Проведене дослідження характеризує венлафаксин як високоефективний дозозалежний антидепресант пролонгованої дії зі сприятливою переносимістю, що дозволяє рекомендувати його включення у комплексну терапію осіб з ІХС і депресивними розладами як науково обґрунтований терапевтичний вибір. Рекомендована початкова доза венлафаксину становить 75 мг/добу.
Список літератури знаходиться в редакції
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (70) 2020 р.