12 грудня, 2020
Тикагрелор vs клопідогрель у хворих на гострий коронарний синдром, яким провели черезшкірне коронарне втручання в умовах реальної клінічної практики
Дані шведського реєстру коронарної ангіографії й ангіопластики
У чинних європейських й американських настановах віддано перевагу тикагрелору порівняно з клопідогрелем для лікування пацієнтів із гострим коронарним синдромом (ГКС) (ESC/EACTS: Neumann F. J. et al., 2018; ACC/AHA: Levine G. N. et al., 2016). Ці рекомендації базуються на даних дослідження PLATO (Study of Platelet Inhibition and Patient Outcomes), у якому було продемонстровано, що застосування тикагрелору сприяє вираженішому зниженню ризику виникнення судинної смерті, нефатального інфаркту міокарда (ІМ) чи інсульту (комбінована первинна кінцева точка) порівняно з клопідогрелем. Тикагрелор став дедалі популярнішим у всьому світі як антагоніст рецепторів P2Y12 (ESC/EACTS: Neumann F. J. et al., 2018; ACC/AHA: Levine G. N. et al., 2016; Angeras O. et al., 2016). Однак із часу оприлюднення результатів випробування PLATO (2009) з’явилися нові спостережні дослідження ефективності тикагрелору та клопідогрелю в невідібраних популяціях пацієнтів із ГКС. Результати цих випробувань є суперечливими.
Деякі звіти спостережень у постмаркетинговому періоді підтвердили дані PLATO (Sahlen A. et al., 2016; Peyracchia M. et al., 2020; Ahn J. et al., 2020), а за результатами інших досліджень тикагрелор не перевершує клопідогрель за ефективністю (Zocca P. et al. 2017; Olier I. et al., 2018; Alexopoulos D. et al., 2016; Turgeon R. et al., 2020). Ця невідповідність оживила дискусію про валідність випробування PLATO в умовах реальної клінічної практики та стала обґрунтуванням для роботи шведських дослідників S. Völz, P. Petursson, J. Odenstedt і співавт. «Тикагрелор не перевершує клопідогрель у пацієнтів із ГКС, яким провели черезшкірне коронарне втручання: звіт шведського реєстру коронарної ангіографії й ангіопластики» (Ticagrelor is Not Superior to Clopidogrel in Patients With Acute Coronary Syndromes Undergoing PCI: A Report from Swedish Coronary Angiography and Angioplasty Registry, SCAAR). Метою вчених було дослідити, чи є терапія тикагрелором ефективнішою й безпечнішою порівняно з лікуванням клопідогрелем у невідібраній популяції пацієнтів із ГКС, яким провели черезшкірне коронарне втручання (ЧКВ).
Пропонуємо до вашої уваги огляд цього випробування (з повною версією публікації можна ознайомитися за посиланням http://ahajournals.org).
Методи та матеріали
Було використано матеріали бази даних SCAAR (Шведський реєстр коронарних ангіографій та ангіопластики) з 5 лікарень в окрузі Вестра-Йоталанд на заході Швеції, що становить ≈20% від загального реєстру SCAAR.
Вивчено й узагальнено інформацію про всі процедури ЧКВ у період між 2005 і 2015 роком щодо нестабільної стенокардії / ІМ з елевацією сегмента ST (STEMI) та без неї (Non-STEMI). Діагнози було встановлено відповідно до критеріїв, визначених Європейським кардіологічним товариством (ESC/EACTS: Neumann F. J. et al., 2018).
Базові характеристики пацієнтів і методи лікування
До дослідження залучили 15 097 пацієнтів; 12 168 (80,6%) отримували клопідогрель, 2929 (19,4%) – тикагрелор. 27% з усіх хворих становили жінки, 30% учасників мали вік >75 років. STEMI діагностовано в 44% хворих, 16% страждали на цукровий діабет. Не виявлено статистично значимої різниці між групами клопідогрелю та тикагрелору за віком, статтю, рівнем кліренсу креатину, індексом маси тіла, наявністю цукрового діабету, оклюзією коронарних судин і виконанням аспірації тромбу під час ЧКВ. Схожим виявилося відсоткове співвідношення курців.
Серед хворих, які отримували тикагрелор, спостерігалася більша частка тих, хто переніс ІМ і кому були проведені ЧКВ і шунтування коронарних артерій (попередньо). У цій групі пацієнтів більше застосовували бівалірудин, менше – антагоніст рецептора глікопротеїну тромбоцитів (GP) 2b/3a. Ці хворі частіше були повністю реваскуляризовані, а також у них ширше застосовували стенти, що елюють ліки. Пацієнти, котрі отримували клопідогрель, частіше мали гіперліпідемію. Більша частка учасників цієї групи перенесла ГКС без елевації сегмента ST і кардіогенний шок, а також їм частіше проводилася аортальна балонна контрапульсація. 4515 (30%) пацієнтам ЧКВ було проведено після переходу від клопідогрелю до тикагрелору як препарату вибору в лютому 2012 року.
Клінічні результати
Первинна кінцева точка
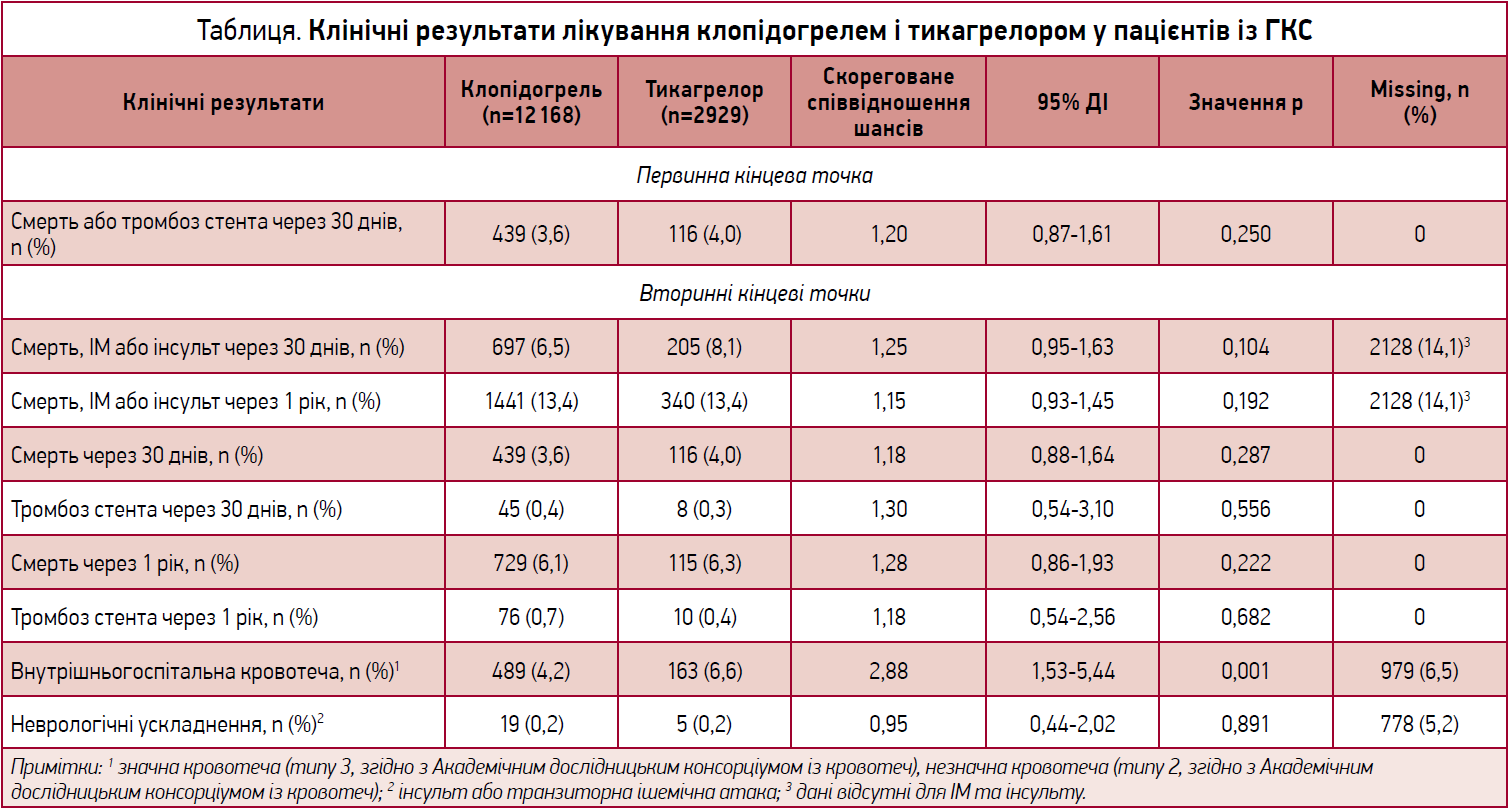
Первинний результат оцінювали через 30 днів після госпіталізації. За місяць було зафіксовано 555 несприятливих подій, із них 53 (9,5%) – тромбози стентів. Лікування тикагрелором не асоціювалося з нижчим ризиком для первинної кінцевої точки (скореговане співвідношення шансів (aOR) 1,20; 95% довірчий інтервал (ДІ) 0,87-1,61; p=0,250) (табл.).
Вторинні кінцеві точки
У період із 2000 по 2015 рік рівень загальної смертності за 30 днів (aOR 1,01; 95% ДІ 0,97-1,06; p=0,514) і через 1 рік (aOR 1,02; 95% ДІ 0,99-1,06; p=0,174) не змінився.
Ризик летальності через 30 днів (aOR 1,18; 95% ДІ 0,88-1,64; p=0,287) і через рік (aOR 1,28; 95% ДI 0,86-1,93; p=0,222) не відрізнявся між групами клопідогрелю та тикагрелору. Не було різниці й у частоті виникнення тромбозів стента через 30 днів (aOR 1,30; 95% ДІ 0,54-3,10; p=0,556). Дані про внутрішньолікарняні кровотечі та внутрішньолікарняні неврологічні ускладнення відсутні в 1757 (11,6%) пацієнтів. Ризик появи внутрішньогоспітальних кровотеч був вищим у разі застосування тикагрелору (aОR 2,88; 95% ДІ 1,53-5,44; p=0,001).
Кількість неврологічних ускладнень під час госпіталізації була схожою в обох когортах (aOR 0,95; 95% ДІ 0,44-2,02; p=0,891). Середній час спостереження становив 1633±1048 днів (діапазон – 0-3692) у всій вибірці. Пацієнти, котрі отримували клопідогрель, мали довший середній час спостереження (1918±963 дні, діапазон – 0-3692), ніж хворі, котрі отримували тикагрелор (454±280 днів, діапазон – 0-1179). За весь час спостереження померли 2618 (17,3%) осіб. Дослідники не виявили значимої різниці у віддаленій смертності між 2 групами (скореговане співвідношення ризиків (aНR) 1,07; 95% ДІ 0,89-1,29; p=0,437) (рис.).
Рис. Порівняльний аналіз груп лікування клопідогрелем і тикагрелором
Також не було значимої різниці між групами щодо розвитку віддалених основних несприятливих серцево-судинних (СС) подій (смерть, ІМ або інсульт) (aHR 1,08; 95% ДІ 0,91-1,28; p=0,400). Не виявлено взаємозв’язку між ефективністю застосування антагоністів P2Y12 і віком, статтю, наявністю цукрового діабету, STEMI/Non-STEMI, призначенням інгібітора GP 2b/3a (всі p>0,05).
Обговорення
Серед 15 097 осіб із ГКС, яким було проведено ЧКВ у період із січня 2005 по січень 2015 року в Швеції, лікування тикагрелором не асоціювалося з меншим ризиком смертності та появою тромбозу стентів. Однак пацієнти, котрі отримували тикагрелор, мали вищий ризик внутрішньолікарняних кровотеч. Ці висновки відрізняються від результатів дослідження PLATO, а отже, постають важливі питання для обговорення.
Результати цього випробування відповідають висновкам кількох інших спостережних досліджень.
У роботі, проведеній на базі даних реєстру ЧКВ Британського товариства серцево-судинних втручань, вивчався вплив антагоністів рецепторів P2Y12 на смертність від усіх причин через 1 рік у хворих зі STEMI, щодо котрих було застосовано первинне ЧКВ (Olier I. et al., 2018). За результатами не виявлено різниці смертності між групами тикагрелору чи клопідогрелю. Автори повідомили про поліпшення результатів у хворих, які отримували прасугрель, порівняно з клопідогрелем і тикагрелором.
У популяції голландських пацієнтів із ГКС тикагрелор збільшував ризик комбінованої кінцевої точки – смерті від усіх причин, ІМ, інсульту чи великої кровотечі через 1 рік від моменту госпіталізації (Zocca P. et al., 2017). Хоча тикагрелор не асоціювався з перевагами щодо ішемічних кінцевих точок, ризик серйозних кровотеч був майже втричі вищим у хворих, які отримували цей препарат.
Нещодавно опубліковані дані канадського аналізу, де показано, що тикагрелор не перевершує клопідогрель за ефективністю запобігання основним несприятливим СС подіям у пацієнтів із ГКС, яким проведено ЧКВ (Turgeon R. D. et al., 2020).
В обсерваційному дослідженні SWEDEHEART (Sahlen A. et al., 2016) повідомлено, що терапія тикагрелором асоціюється з нижчою смертністю від усіх причин, але з вищим ризиком кровотечі. Проте тут оцінювали лише виживання після виписки з лікарні (тобто з аналізу було виключено 1434 випадки внутрішньолікарняних летальних випадків). У цій роботі включено всі випадки смерті від моменту госпіталізації до кінця періоду спостереження. Автори стверджують, що такий підхід є доречнішим для оцінки валідності випробування PLATO щодо смертності від усіх причин в умовах реальної клінічної практики.
Результати випробування також підтверджуються даними кількох рандомізованих контрольованих досліджень (РКД). У РКД ARTEMIS (Affordability and Real-World Antiplatelet Treatment Effectiveness After Myocardial Infarction Study: Wang T. Y. et al., 2019) оцінили кількість оплачених рецептів на антагоністи рецепторів P2Y12 й основні несприятливі СС події у хворих, яким було виписано ці ліки. Серед >11 000 осіб з ІМ із понад 300 різних лікарень США вищу прихильність виявлено до тикагрелору, але це не зумовило клінічної користі.
Крім того, в дослідженні TOPIC (Timing of Platelet Inhibition after ACS: Cuisset T. et al., 2017) була вивчена деескалація антагоніста рецептора P2Y12 (від тикагрелору до клопідогрелю) в сучасній популяції хворих на ГКС. Ризик комбінованої клінічної точки (серцево-судинна смерть, незапланована госпіталізація, термінова реваскуляризація, інсульт, кровотеча) протягом 1 року був нижчим у пацієнтів, які перейшли з тикагрелору на клопідогрель. Відмінність зумовлена частотою кровотеч без різниці в ішемічних кінцевих точках.
Розбіжності між висновками дослідження PLATO та результатами цього випробування можна пояснити деякими особливостями. Тоді як у PLATO понад ⅓ хворих лікувалися консервативно, всім пацієнтам у цьому дослідженні було проведено ЧКВ. Хворі в PLATO були молодшими (зазвичай чоловіки), що підтверджує добре відомі розбіжності між РКД і невідібраною популяцією пацієнтів (Steg P. G. et al., 2007). З огляду на встановлені предиктори кровотечі (Moscucci M. et al., 2003; Kinnaird T. et al., 2003) невідібрана за визначеними критеріями когорта хворих у цьому дослідженні могла бути схильнішою до кровотеч під впливом потужного антитромбоцитарного агента. Ще одним простим, але потужним посередником для послаблення ефективності тикагрелору поза РКД може бути більший рівень побічних явищ (задишка, кровотеча).
Крім того, як і багато медичних новинок після виходу на ринок, тикагрелор спричинив значне економічне навантаження на ресурси охорони здоров’я. У регіоні, де проводилося дослідження, ці фінансові витрати щороку сягають додаткових 2 млн євро порівняно з клопідогрелем. Звісно, шведська практика не обов’язково відображає серцево-судинну допомогу в інших країнах, але сукупність доказів, що існують на сьогодні, неоднозначно підтверджує економічну рентабельність тикагрелору.
Автори визнають, що спостережний дизайн дослідження створює ризик залишкового змішування. Проте статистичні моделі базувалися на інструментальному аналізі змінних, який є одним із найкращих методів усунення як відомих, так і невідомих факторів, які впливають на результати спостереження. Крім того, більшість відомих змінних, пов’язаних із характеристиками пацієнта та процедурними деталями, віддавали перевагу тикагрелору.
Хоча доступні дані не давали змоги диференціювати серцеву та несерцеву смерть, смертність є надійною кінцевою точкою. Дослідники не могли врахувати тривалість лікування антитромбоцитарними засобами та можливий перехід між групами, оскільки ця інформація не передається до реєстру.
Висновки
У цьому обсерваційному дослідженні терапія тикагрелором не перевершувала лікування клопідогрелем у пацієнтів із ГКС, які перенесли ЧКВ, за ефективністю, що супроводжувалося підвищеним ризиком кровотечі. Переваги тикагрелору, що продемонстровано в дослідженні PLATO, можуть бути нерелевантними в умовах реальної клінічної практики.
Коментар експерта
Результати обсерваційного дослідження на базі даних реєстру SCAAR (Völz S. et al., 2020) спричинили в медичній спільноті активне обговорення. Експертну думку щодо цього висловив доктор Brian A. Bergmark у ґрунтовному матеріалі «Порівняння тикагрелору та клопідогрелю в реальній клінічній практиці: розетський камінь чи труднощі перекладу?» (з оригінальною версією публікації можна ознайомитися за посиланням http://ahajournals.org).
Пацієнти з ГКС мають підвищений ризик додаткових ішемічних подій (Sabatine M. S. et al., 2018; Bonaca M. P. et al., 2015; Sabatine M. S. et al., 2017; Schwartz G. G. et al., 2018). Шляхи модифікації цих ризиків ми отримуємо з результатів РКД, що демонструють ефективність і безпеку кількох типів втручань у пацієнтів із попереднім ІМ (включно з антитромботичними засобами) (CURE Trial Investigators, 2001; Mega J. L. et al., 2012; Wallentin L. et al., 2009; Wiviott S. D. et al., 2007), гіполіпідемічною терапією (Sabatine M. S. et al., 2017; Schwartz G. G. et al., 2018; Cannon C. P. et al., 2015; Cannon C. P. et al., 2005) та реваскуляризацією (Mehta S. R. et al., 2018).
Частина підвищеного ризику після ГКС зумовлена саме причиною ураження, хоча багато повторюваних подій не пов’язані з індексом ушкодження ГКС, судиною чи навіть судинним руслом (Scirica B. M. et al., 2020). Ця різниця набуває особливої актуальності у випадку пацієнтів, яким проводять ЧКВ, оскільки в них існує ризик нецільових уражень, а також є ймовірність ускладнень, пов’язаних зі стентами (особливо їх тромбозом).
Що стосується антитромбоцитарної терапії, то у великих РКД PLATO (Wallentin L. et al., 2009) та TRITON-TIMI 38 (Wiviott S. D. et al., 2009) було продемонстровано більшу ефективність інгібіторів P2Y12 третього покоління тикагрелору та прасугрелю порівняно з клопідогрелем у пацієнтів із ГКС, які отримували аспірин. У PLATO було залучено 18 624 хворих на ГКС, які були рандомізовані в групи, що отримували тикагрелор 90 мг 2 р/день, проти тих, які застосовували клопідогрель 75 мг/день. Спостереження тривало 12 міс. Частота основних несприятливих СС подій була на 16% нижчою в пацієнтів, яким призначили тикагрелор, включаючи нижчий рівень смертності від усіх причин. Однак частота кровотеч у цій групі була вищою.
Що стосується підгрупи пацієнтів із ГКС, які перенесли планове ЧКВ, у групі тикагрелору відзначалося зниження смертності від усіх причин на 19% і зменшення кількості тромбозів стента на 36%.
У дослідженні TRITON-TIMI 38, у якому 99% хворих перенесли ЧКВ (95% установлено стент), ризик виникнення тромбозу стента зменшився на 52% при застосуванні прасугрелю.
Найвища ефективність і прийнятний профіль безпеки тикагрелору та прасугрелю, продемонстровані в цих випробуваннях, зумовили те, що стосовно більшості пацієнтів із ГКС (включно з тими, хто переніс ЧКВ) клініцисти віддають перевагу призначенню цих препаратів порівняно з клопідогрелем (ESC: Ibanez B. et al., 2017; ESC/EACTS: Neumann F. J. et al., 2018; ACC/AHA: Levine G. N. et al., 2016). Хоча великі РКД – механізм, за допомогою котрого можна оцінити ефективність і безпеку одного втручання порівняно з іншим, вони, очевидно, не дають відповіді на всі запитання, що стосуються використання цих препаратів у повсякденній практиці. Так, у дослідженнях терапії СС захворювань зазвичай беруть участь білошкірі чоловіки віком 60 років із Північної Америки та Західної Європи, що зумовлює питання стосовно генералізації запропонованих методів лікування для різних груп населення та клінічних сценаріїв (Tahhan A. S. et al., 2020).
Окрім того, соціальні фактори, як-от економічна доцільність, виходять за рамки дослідження, призначеного для розуміння ефективності та безпеки лікарського засобу чи терапевтичної стратегії в конкретній групі пацієнтів із певним захворюванням. З огляду на це дані з реальної практики мають можливість надати важливе допоміжне уявлення про те, як внутрішньо обґрунтовані висновки того чи іншого РКД перевести в зовнішній світ.
Отже, які підсумки можна підбити за результатами обсерваційного дослідження S. Völz і співавт. з урахуванням даних рандомізованих випробувань? Як цей аналіз допомагає перевести наявну інформацію про ефективність і безпеку тикагрелору та клопідогрелю в реальну практику? По-перше, SCAAR – всеосяжний реєстр, який дає змогу досить докладно описати перехід від клопідогрелю до тикагрелору в широкій системі охорони здоров’я. З першого місяця виходу на ринок тикагрелору в березні 2012 року минуло лише 2 міс після того, як цей лікарський засіб став препаратом вибору серед інгібіторів P2Y12. Таке спостереження дає всі підстави наголошувати на швидкому переведенні керівних принципів і рішень на рівні системи охорони здоров’я в реальну медичну допомогу на рівні пацієнтів у таких системах, як шведська, а отже, це свідчить про важливість аналізів, як-от дослідження S. Völz і співавт. По-друге, хоча це дослідження керується демографічними показниками, схожими на оригінальне випробування PLATO, є важлива різниця у віці учасників. Тільки ≈15% пацієнтів, які брали участь у PLATO, мали вік >75 років, тоді як когорта літніх хворих у зазначеному дослідженні складала майже 30%. Середній вік учасників становить ≈68 років, що відображає сучасний демографічний розподіл серед хворих на СС хвороби в Північній Америці та Європі. У цій категорії осіб можуть бути важливі відмінності щодо ризику кровотеч і розвитку ішемічних подій порівняно з PLATO.
Кількісний рівень кровотеч складно порівняти, враховуючи оцінку цих несприятливих подій лише в межах стаціонарного лікування, але абсолютні показники смертності від усіх причин та її склад, а також ризик розвитку ІМ або інсульту за 1 рік є вищими в аналізі SCAAR (аніж у PLATO). Важливе обмеження – відсутність даних про припинення лікування. Навіть у РКД спостерігалися суттєві показники відмови від прийому тикагрелору (Wallentin L. et al., 2009; Steg P. et al., 2019).
Доречно відзначити низькі показники встановлення стентів, що елюють ліки, проведення внутрішньокоронарної візуалізації та повної реваскуляризації, що рекомендовані сучасними настановами. Враховуючи, що ці підходи продемонстрували клінічну користь (Mehta S. R. et al., 2019; Neumann F. J. et al., 2018; Hong S. J. et al., 2015; Tonino P. A. et al., 2015), доцільно припустити, що в сучасну епоху користь від потужної антитромбоцитарної терапії може бути менш очевидною, ніж це було в минулому. Такі припущення, звичайно, є спекулятивними, але оптимізовані ЧКВ швидко розвиваються, тому нерозумно очікувати, що ці зміни не вплинуть на залишковий ризик, а отже, на абсолютну користь додаткової медикаментозної терапії в майбутньому.
Постає питання щодо дослідження S. Völz і співавт.: чи існує пряме клінічне застосування його висновків? Оскільки наведені результати є обсерваційними, вони вразливі до значних невимірних факторів. Однак ці спостереження – важливе нагадування клініцистам про те, що багато пацієнтів, з якими їм доводиться мати справу в щоденній практиці, не підходять під чітко визначені рамки популяцій і клінічних сценаріїв, які досліджуються в РКД. Отже, необхідне ретельно обґрунтоване й орієнтоване на пацієнта рішення. Зокрема, отримані результати зумовлюють появу значимих питань щодо терапевтичної стратегії у хворих старшого віку.
S. Völz і співавт. проаналізували переваги й недоліки використання тикагрелору та клопідогрелю в реальній клінічній практиці Швеції, зробивши важливі спостереження щодо поточного ведення пацієнтів із ГКС, яким провели ЧКВ; вони висунули низку гіпотез, які потребують подальшого вивчення. Отже, комплексні набори даних, як-от реєстр SCAAR, надають безцінний інформаційний ресурс, оскільки ми прагнемо інтегрувати дані РКД у реальне життя пацієнтів.
Підготувала Наталія Нечипорук
Медична газета «Здоров’я України 21 сторіччя» № 21 (490), 2020 р.