13 грудня, 2020
Тромбоемболія легеневої артерії як окремий випадок венозної тромбоемболії
Тактика ведення пацієнтів із ТЕЛА
Після підтвердження діагнозу ТЕЛА постає питання щодо обрання тактики ведення пацієнта, методу лікування, але насамперед слід пригадати класифікацію ТЕЛА, оскільки саме вона визначає вибір тактики.
Якщо звернутися до джерел різних років, можна знайти багато класифікацій. Існувала класифікація ТЕЛА залежно від обсягу ураження: надмасивна (головного стовбура), обструкція 75-100%; масивна (головних гілок), обструкція 50-75%; немасивна (середніх гілок), обструкція 15-50%; дрібних гілок, обструкція <15%. На жаль, ця класифікація мало допомагає в обранні тактики, оскільки швидко визначити обсяг ураження легеневих артерій без додаткових обстежень неможливо, а отже, при критичному стані гемодинаміки вона не дає змоги швидко визначити тактику.
У 1983 р. розглядалася класифікація залежно від тяжкості ураження: тяжка (легеневий стовбур, головні гілки легеневої артерії); середньотяжка (дольові сегментарні гілки); легка (дрібні гілки). Проте й ця класифікація виявилася недосконалою з тієї самої причини.
У 2000 р. ESC було запропоновано розрізняти види ТЕЛА залежно від клініки: масивна (характеризується шоком, гіпотензією); субмасивна (перебігає з ознаками дисфункції правого шлуночка); немасивна (без виражених ознак правошлуночкової недостатності). Певною мірою ця класифікація допомагає лікарю швидко обрати метод лікування.
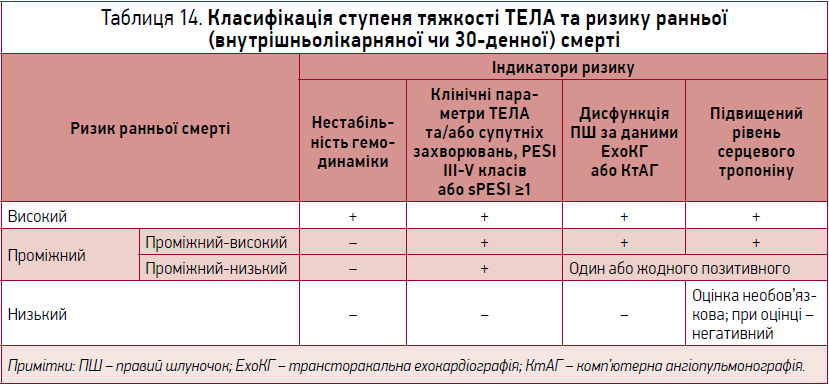
Із 2014 р. ESC рекомендовано клінічну класифікацію тяжкості епізоду гострої ТЕЛА на базі оцінки ризику (30-денної) смертності, пов’язаної з ТЕЛА (табл. 14).
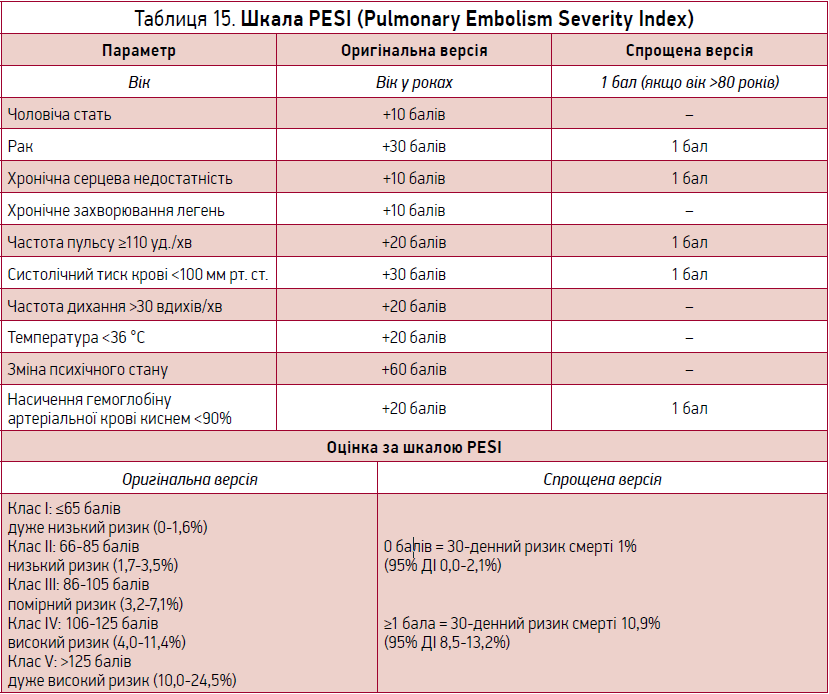
Як бачимо, крім клінічних параметрів, інструментально підтверджених даних про наявність/відсутність дисфункції правого шлуночка та рівня серцевого тропоніну, необхідна оцінка за шкалою PESI чи sPESI (спрощеною шкалою) (табл. 15).
Основне значення шкали PESI полягає в надійній ідентифікації пацієнтів із низьким ризиком 30-денної смертності (PESI I та II класів). В одному рандомізованому дослідженні низький показник PESI був використаний як головний критерій включення в амбулаторне лікування ТЕЛА [19].
Оцінивши стан гемодинаміки та ризик 30-денної смерті, підходимо до обрання тактики ведення пацієнта (рис. 4).
Рис. 4. Тактика ведення пацієнта з ТЕЛА з урахуванням ризику смертності (за рекомендаціями ESC 2019)
Примітка: * враховувати й критерії Hestia.
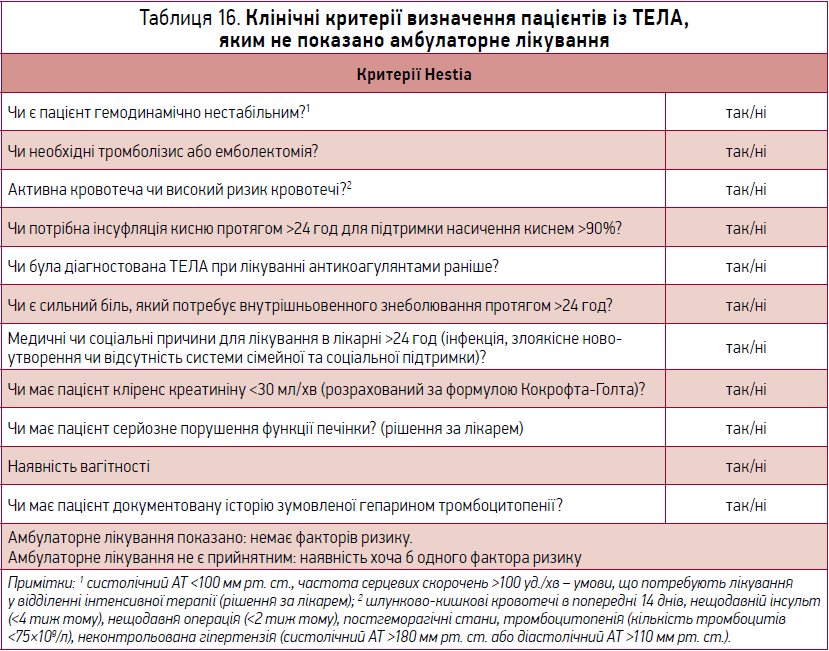
Критерії Hestia (табл. 16) згадувались і в ESC 2014 р., але з приміткою щодо недостатньої валідизації. В ESC 2019 р. їх наведено в додаткових таблицях.
В ESC 2019 р. також зазначені ознаки дисфункції правого шлуночка за ехокардіографічними критеріями (рис. 5).
Як бачимо, пацієнти з низьким ризиком і можливістю адекватного виконання наданих рекомендацій після обстеження можуть бути виписані на амбулаторне лікування. За даними одного дослідження, частка таких пацієнтів у Харкові становила 9,8% [15].
 Рис. 5. Графічне зображення трансторакальних ехокардіографічних параметрів при оцінці перевантаження тиском правого шлуночка
Рис. 5. Графічне зображення трансторакальних ехокардіографічних параметрів при оцінці перевантаження тиском правого шлуночка
Примітки: ПШ – правий шлуночок; ЛШ – лівий шлуночок; МШП – міжшлуночкова перетинка; НПВ – нижня порожниста вена; A’ – пікова пізня діастолічна (під час скорочення передсердь) швидкість на трикуспідальному клапані; AcT – час прискорення доплерівського потоку правого шлуночка; Ао – аорта; E’ – пікова рання діастолічна швидкість на трикуспідальному клапані при тканинній доплерографії; IVC – нижня порожниста вена; LA – ліве передсердя; RA – праве передсердя; RiHTh – тромб правого серця (чи тромби); LV – лівий шлуночок; RV – правий шлуночок; S’ – пікова систолічна швидкість на трикуспідальному клапані при тканинній доплерографії; TRPG – пік систолічного градієнта на трикуспідальному клапані.
Лікування
Тепер розглянемо наступне запитання, що постає перед практичним лікарем при виявленні пацієнта з ТЕЛА. Які методи лікування застосувати, де та як довго має лікуватися такий пацієнт?
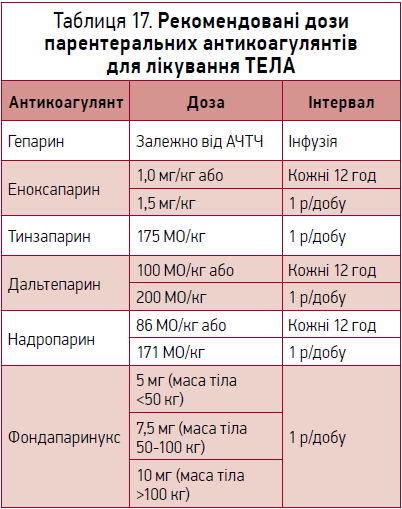
З огляду на рекомендації ESC 2019 р. усі пацієнти з ТЕЛА, незалежно від ризику смерті, повинні отримувати антикоагулянти. В умовах стаціонару щодо хворих із високим ризиком смерті перевага має віддаватися парентеральному введенню НМГ, або фондапаринуксу, або нефракціонованому гепарину. Зважаючи на зручність застосування, на практиці перевага віддається НМГ. У рекомендаціях ESC 2014 р. наводилися рекомендовані дозування деяких парентеральних антикоагулянтів. У рекомендаціях ESC 2019 р. вибір парентерального антикоагулянта залишається за лікарем (табл. 17).
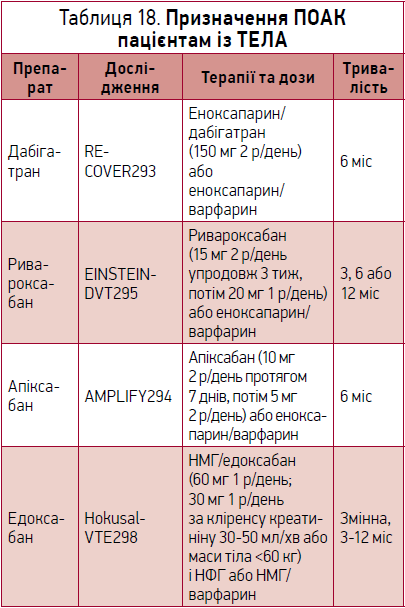
Щодо пацієнтів із низьким і проміжним ризиком перевага має віддаватися прямим оральним антикоагулянтам (ПОАК): дабігатрану, апіксабану, едоксабану та ривароксабану. За відсутності протипоказань і за винятком окремих коморбідних станів ПОАК мають перевагу над антагоністами вітаміну К (АВК). Рекомендовані дози ПОАК були апробовані в низці досліджень (табл. 18).
АВК можуть призначатися вагітним, оскільки безпечність ПОАК для них не вивчалася.
Що стосується онкологічних хворих, то слід зазначити, що отримано позитивні результати стосовно двох ПОАК: едоксабану та ривароксабану. В європейських й американських рекомендаціях 2019 р. зазначено, що за результатами досліджень едоксабан і ривароксабан не поступаються за ефективністю НМГ, але ризик кровотеч дещо більший. Саме тому щодо таких пацієнтів (насамперед це стосується хворих із раком шлунково-кишкового тракту) перевага має віддаватися НМГ. Також онкохворим можуть призначатися нефракціонований гепарин або фондапаринукс.
Отже, всім пацієнтам із ТЕЛА негайно слід призначати антикоагулянтну терапію. Подальша тактика лікування залежить від ризику смерті.
Хворі з високим ризиком мають перебувати у відділеннях реанімації. Їм призначаються оксигенотерапія (під контролем сатурації), помірна інфузія (низький серцевий викид пов’язаний насамперед із недостатністю правого шлуночка), для стабілізації артеріального тиску призначаються симпатоміметики (певну перевагу має норепінефрин), можуть призначатися вазодилататори. За рефрактерного колапсу чи в разі зупинки кровообігу може використовуватися екстракорпоральна серцево-легенева підтримка в поєднанні з хірургічною емболектомією. Проте основним патогенетичним методом лікування пацієнтів із високим ризиком залишається тромболітична терапія. Дози тромболітичних препаратів наведено в таблиці 19.
Винятково хірургічні методи лікування ТЕЛА найчастіше використовуються в разі критичного стану, при протипоказаннях для тромболітичної терапії, а відтерміновані (після стабілізації стану) – при масивних ураженнях.
Слід зазначити, що тенектеплази немає в рекомендаціях, оскільки час дії цього лікарського засобу обмежений; його ефективність у разі венозного тромбозу буде меншою порівняно з іншими тромболітиками. Проте відомі випадки використання тенектеплази практичними лікарями як метод відчаю за явищ шоку та відсутності можливості негайного призначення іншого тромболітичного лікарського засобу чи застосування хірургічних методів.
За відсутності критичного стану для зменшення спазму судин (зумовлених вивільненням тромбоксану А2 та серотоніну), а також для зниження тиску в малому колі кровообігу в низці випадків практичні лікарі призначають спазмолітичні препарати. На жаль, ця данина застарілим рекомендаціям пов’язана іноді з банальною неможливістю екстрено застосувати найдієвіші методи діагностики та лікування.
Профілактика ВТЕ
Зрозуміло, що краще не припускати появи ВТЕ, ніж проводити лікування в критичному стані, тому завжди потрібно пам’ятати про необхідність і методи профілактики ВТЕ.
В основі профілактики лежить призначення ПОАК або НМГ чи фондапаринуксу пацієнтам із високим ризиком ТЕЛА. Оскільки ризик появи ТЕЛА для хворих різного профілю вже обговорювався вище, зупинимося лише на деяких особливостях профілактики.
Вагітним і породіллям, які вигодовують грудним молоком, не призначають ПОАК, тому схема призначення антикоагулянтної терапії може бути такою:
- I триместр – перевага може бути віддана АВК. У разі госпіталізації терапія АВК може бути продовжена, але зазвичай АВК замінюють на НМГ;
- II-III триместри – перевага віддається АВК;
- із 36-го тижня – заміна АВК на НМГ або нефракціонований гепарин;
- за 36 год до планового розродження перехід на нефракціонований гепарин, інфузію котрого слід припинити за 4-6 год до пологів і відновити (при кровотечі) через 4-6 год після пологів.
Під час вигодовування грудним молоком можуть призначатися АВК.
За неможливості призначення НМГ й АВК іноді призначають ацетилсаліцилову кислоту, хоча її ефективність недостатня, а ризик кровотеч збільшується.
Хворим онкологічного профілю профілактику ВТЕ проводять як парентеральними антикоагулянтами, так і тими самими ПОАК, які призначаються для лікування ТЕЛА цій групі пацієнтів.
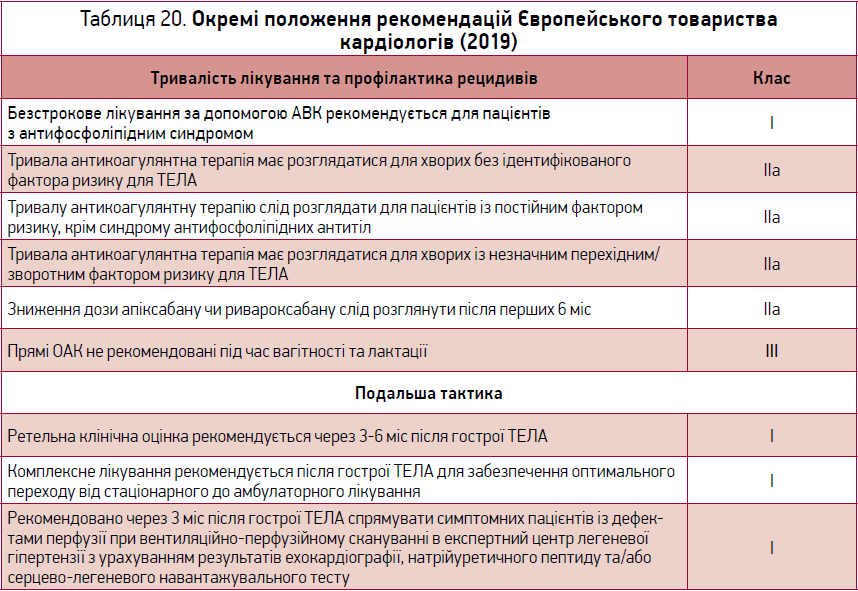
Тривалість фармакологічної профілактики ВТЕ залежить від наявності факторів ризику ВТЕ та закінчується за їх відсутності. Тривалість профілактики ВТЕ для окремих груп пацієнтів згідно з рекомендаціями ESC 2019 р. наведено в таблиці 20.
Серед інших методів профілактики в арсеналі профілактики ТГВ також залишаються призначення при відповідних показаннях компресійних панчох і встановлення кава-фільтрів. Але ці вузькопрофільні питання можна знайти у відповідних рекомендаціях, тому ми не зупинятимемося на них детально.
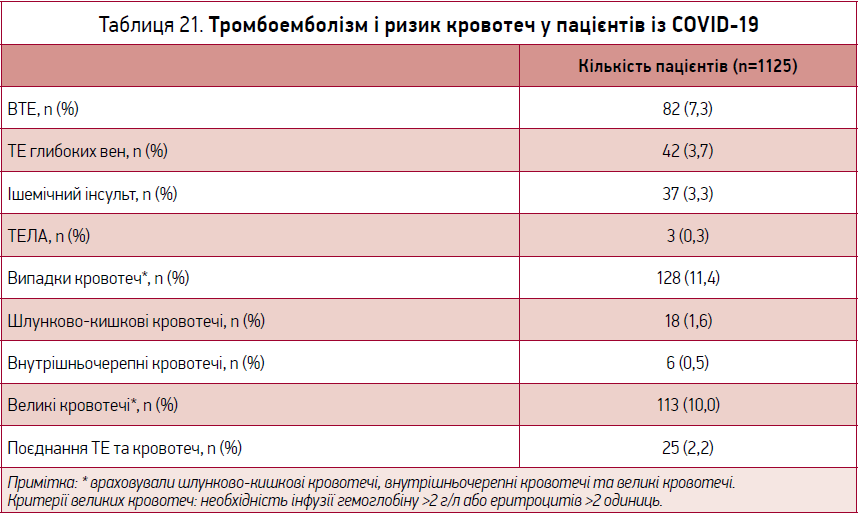
Наостанок зазначимо, що на сьогодні доведено участь COVID‑19 у розвитку тромбоемболічних ускладнень. У виступі Yutao Guo (Китай) на Європейському конгресі кардіологів у 2020 р. наведено дані про кількість хворих із порушенням згортання крові та ризиком кровотеч (табл. 21), які мають COVID‑19, а також такі висновки:
- пацієнти з COVID‑19 мали високий ризик розвитку тромбоемболічних ускладнень і кровотеч, а також смертності;
- застосування антикоагулянтів, особливо парентеральних, істотно знижує ризик наслідків тромбоемболії, кровотеч і смерті;
- наявність фібриляції передсердь спричиняла системну тромбоемболію в пацієнтів із COVID‑19;
- дисфункція печінки була незалежним фактором ризику як тромбоемболізму (ТЕ), так і великих кровотеч.
Отже, при захворюванні на COVID‑19 показана профілактика ВТЕ. Сьогодні й досі ще дискутуються методи та дози лікарських засобів, не виключена можливість призначення ПОАК або прямих антикоагулянтів із метою профілактики в дозах, які перевищують загальноприйняті в 1,5-2 рази.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 21 (490), 2020 р.