4 січня, 2021
Порівняння тикагрелору та клопідогрелю в пацієнтів старечого віку з гострим коронарним синдромом: інформація з реєстру SWEDEHEART
 Від моменту публікації у 2009 р. результатів дослідження PLATO (Platelet Inhibition and Patient Outcomes) [1] у чинних європейських [2, 3] й американських настановах [4, 5] із лікування інфаркту міокарда (ІМ) рекомендовано застосовувати замість клопідогрелю комбінацію ацетилсаліцилової кислоти (АСК) із тикагрелором (якщо він не протипоказаний). У дослідженні PLATO тикагрелор (порівняно з клопідогрелем), який використовувався в термін до 12 міс після гострого коронарного синдрому (ГКС), продемонстрував однозначну перевагу з позиції зниження частоти досягнення комбінованої кінцевої точки (смерть унаслідок судинних причин, ІМ або інсульт). Окрім того, на тлі лікування тикагрелором знижувалася смертність через будь-які причини (на 1,4%). Завдяки цим переконливим доказам та однозначним рекомендаціям тикагрелор почав широко застосовуватися після ІМ [6].
Від моменту публікації у 2009 р. результатів дослідження PLATO (Platelet Inhibition and Patient Outcomes) [1] у чинних європейських [2, 3] й американських настановах [4, 5] із лікування інфаркту міокарда (ІМ) рекомендовано застосовувати замість клопідогрелю комбінацію ацетилсаліцилової кислоти (АСК) із тикагрелором (якщо він не протипоказаний). У дослідженні PLATO тикагрелор (порівняно з клопідогрелем), який використовувався в термін до 12 міс після гострого коронарного синдрому (ГКС), продемонстрував однозначну перевагу з позиції зниження частоти досягнення комбінованої кінцевої точки (смерть унаслідок судинних причин, ІМ або інсульт). Окрім того, на тлі лікування тикагрелором знижувалася смертність через будь-які причини (на 1,4%). Завдяки цим переконливим доказам та однозначним рекомендаціям тикагрелор почав широко застосовуватися після ІМ [6].
У дослідженні PLATO зменшення частоти ішемічних подій супроводжувалося підвищенням ризику значимої кровотечі, пов’язаної з проведенням аорто-коронарного шунтування (3,8% при застосуванні клопідогрелю порівняно з 4,5% при прийомі тикагрелору). Одним з найважливіших факторів, асоційованих з вищим ризиком кровотечі, є похилий вік [7-10]. У дослідженні PLATO медіана віку пацієнтів становила 62 роки, тобто вони були більше ніж на 10 років молодшими, ніж хворі цього профілю в повсякденній клінічній практиці [11, 12]. У реальності лікарям часто доводиться мати справу з пацієнтами похилого та старечого віку, які порівняно з молодшими хворими мають більшу кількість супутніх захворювань та часто – більше факторів ризику розвитку кровотечі (як-от знижена ниркова функція, анемія та запалення). Отже, в невідібраній популяції пацієнтів з ІМ ризик кровотечі на тлі потужнішої антитромбоцитарної терапії може бути набагато вищим. Протягом останніх років частота значимих кровотеч зросла. Так, упродовж першого року після виписки зі стаціонару вони з’являються у 4,8% хворих, тоді як смертність пацієнтів не знизилася [7]. Одна з можливих причин цього явища може полягати в тому, що «компроміс» між зниженням частоти ішемічних подій та підвищенням ризику виникнення кровотеч не дає користі пацієнтам похилого та старечого віку.
Мета цього дослідження – порівняння клінічних наслідків на тлі застосування тикагрелору чи клопідогрелю в пацієнтів віком ≥80 років, у яких було діагностовано ІМ.
Методи
Загальнонаціональна когорта з реєстру SWEDEHEART
Дані про всіх хворих було отримано із загальнонаціонального реєстру SWEDEHEART [13], до якого включають усіх послідовних пацієнтів, госпіталізованих до кардіологічних відділень із симптомами, що вказують на ГКС. Наразі інформацію до цього реєстру вносять фахівці всіх шведських лікарень (n=72), які надають медичну допомогу при гострій кардіологічній патології. У реєстрі зібрано відомості про >100 змінних, що стосуються вихідних характеристик хворих, медикаментозного лікування на момент госпіталізації, терапії в стаціонарі, ускладнень та лікарських препаратів, призначених при виписці (http://www.ucr.uu.se/swedeheart).
Наша мета полягала в тому, щоби змоделювати прагматичне цільове дослідження, покликане порівняти ефект тикагрелору та клопідогрелю (так само, як це було зроблено в дослідженні PLATO, але в популяції осіб старечого віку) [14].
Отже, до цього дослідження було залучено всіх послідовних пацієнтів віком ≥80 років, які були живі на момент виписки з лікарні та перенесли ІМ, уперше зареєстрований у реєстрі SWEDEHEART у період з 1 січня 2010 р. по 31 грудня 2017 р. Цей період охоплював час появи в розпорядженні лікарів тикагрелору, який став доступним у другій половині 2011 р. Хворих виключали з дослідження, якщо вони отримували лікування клопідогрелем або тикагрелором перед госпіталізацією щодо ІМ, мали потребу у призначенні прямих оральних антикоагулянтів чи антагоністів вітаміну К, попередню кровотечу в анамнезі, серйозну кровотечу під час перебування в стаціонарі (що потребувала проведення гемотрансфузії або операції) чи рівень гемоглобіну <100 г/л (<10 г/дл). Із цього випробування також були виключені пацієнти з діагнозами чи станами, що роблять менш імовірним призначення їм потужнішого антитромбоцитарного препарату (наприклад, деменція, діаліз тощо).
Вплив препаратів
Вважалося, що хворі приймали тикагрелор або клопідогрель, якщо дані про відпуск їм цих препаратів з аптеки були зафіксовані у Шведському реєстрі лікарських засобів протягом 2 тижнів після виписки зі стаціонару. Якщо ці дані були недоступні (n=553; 3,9%), але в реєстрі SWEDEHEART містився запис про призначення препарату на момент виписки, використовувалася остання інформація.
Визначення наслідків
Основні наслідки, які аналізувалися як окремо, так і в комбінації, включали смерть, повторну госпіталізацію щодо ІМ, інсульт і кровотечу, що з’явилися протягом 365 днів із дати виписки. Дані про ці кінцеві точки були отримані на підставі аналізу кодів МКХ із національного реєстру пацієнтів і життєвого статусу з популяційного реєстру. Новий ІМ у перші 4 тижні після виписки визначався як нова реєстрація у SWEDEHEART і як новий діагноз у реєстрі хворих. Остання дата спостереження – 31 грудня 2017 р.
Результати
Досліджувана популяція – віком ≥80 років
Загалом до випробування було залучено 14 005 пацієнтів віком ≥80 років, які залишилися живими після виписки зі стаціонару, де перебували щодо ІМ; з них у 4428 (31,6%) було діагностовано ІМ з елевацією сегмента ST (STEMI), в решти – ІМ без елевації сегмента ST (NSTEMI). Більшості хворих призначався клопідогрель (n=8434; 60,2%), меншій частині – тикагрелор (n=5571; 39,8%). У період із 2010 по 2017 р. частота застосування тикагрелору зросла від 0 до 72,5%. Пацієнти, котрим призначався тикагрелор, були молодші за віком і мали меншу кількість супутніх захворювань на момент обстеження, проте після корекції із застосуванням зважених показників зворотної імовірності лікування (inverse probability treatment weighting, IPTW) вихідні характеристики хворих виявилися збалансованими.
Результати дослідження в пацієнтів віком ≥80 років
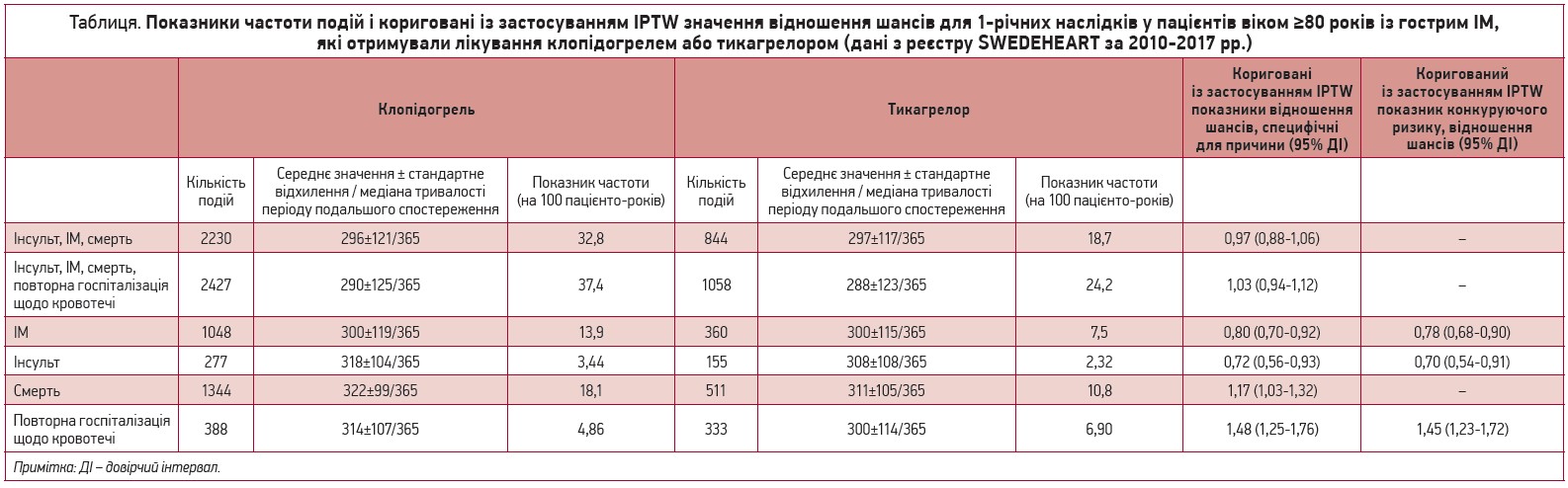
За некоригованого аналізу хворі, котрі отримували лікування тикагрелором, мали достовірно меншу частоту розвитку комбінованих ішемічних подій або досягнення комбінованої кінцевої точки, що включала ішемічні події / кровотечу (табл.).
Серед хворих, які отримували лікування тикагрелором, показники частоти розвитку ІМ, інсульту та настання смерті були нижчими, проте частота повторної госпіталізації щодо кровотечі в них була вищою.
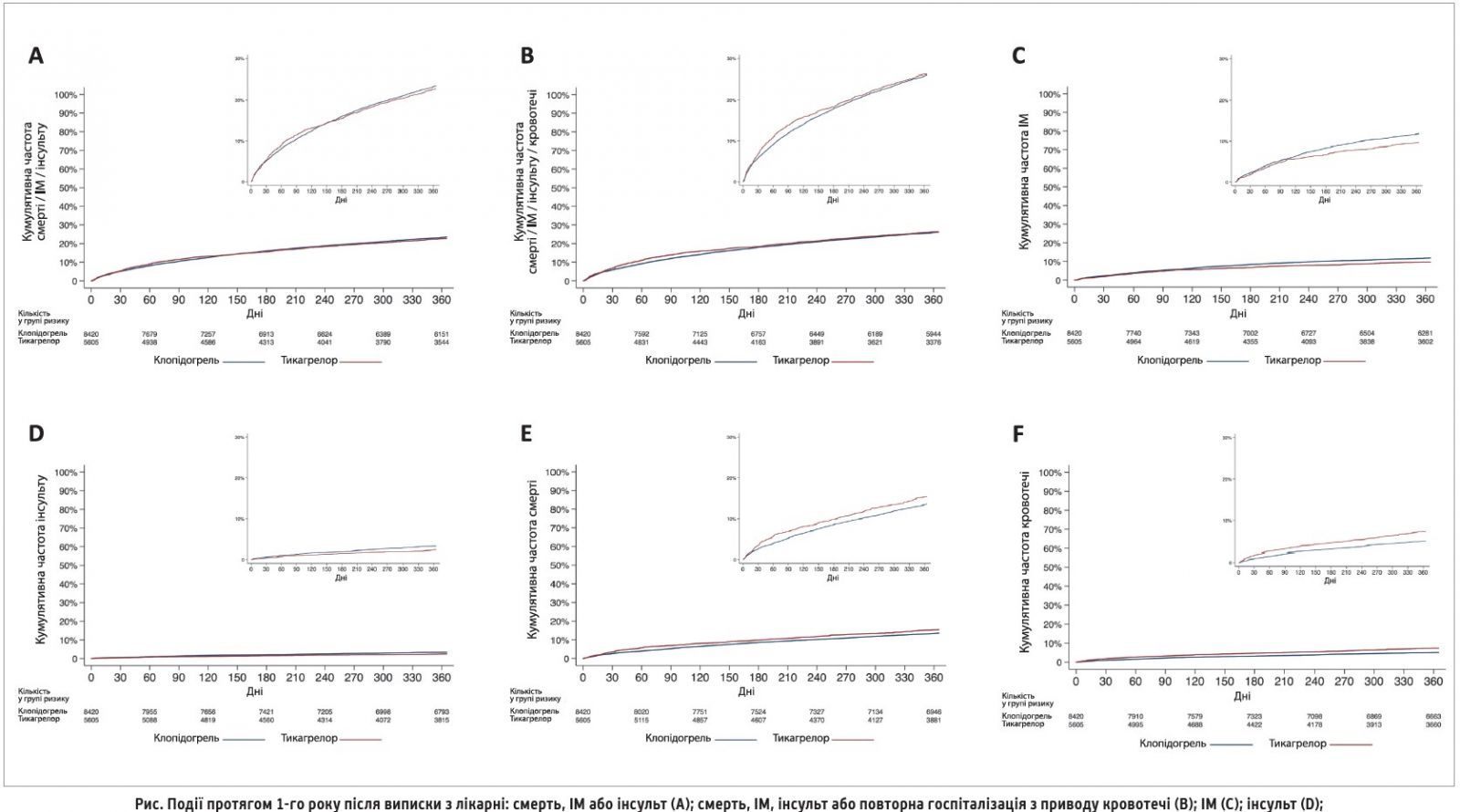
В основному аналізі, що проводився із застосуванням методу регресії Кокса (IPTW) із введеними пропущеними значеннями, на тлі застосування тикагрелору порівняно з терапією клопідогрелем не відзначалося значимого зниження частоти досягнення ні комбінованої кінцевої точки ішемічних подій, ні комбінованої кінцевої точки «ішемічні події / кровотеча» (рис.).
Протягом одного року пацієнти, котрих лікували тикагрелором, мали на 20% нижчий ризик появи нового ІМ (відношення шансів (ВШ) 0,80; 95% ДІ 0,70-0,92) та на 28% нижчий ризик розвитку інсульту (ВШ 0,72; 95% ДІ 0,56-0,93) порівняно із хворими, котрі отримували клопідогрель. Однак пацієнти, які приймали тикагрелор, мали на 17% вищий ризик смерті (ВШ 1,17; 95% ДІ 1,03-1,32) та на 48% вищий ризик повторної госпіталізації щодо кровотечі (ВШ 1,48; 95% ДІ 1,25-1,76), ніж ті хворі, котрі отримували клопідогрель.
Порівняння ефектів лікування серед пацієнтів віком <80 років
У когорті хворих віком <80 років 38,2% осіб (n=22 415) отримували лікування клопідогрелем, а 61,8% (n=36 256) – тикагрелором.
Результати аналізу (IPTW) повних випадків продемонстрували зниження ризику ІМ на 18% (ВШ 0,82; 95% ДІ 0,75-0,91), зниження ризику інсульту на 18% (ВШ 0,82; 95% ДІ 0,60-0,98) та зниження ризику смерті на 15% (ВШ 0,85; 95% ДІ 0,76-0,96), але на 32% вищий ризик кровотеч (ВШ 1,32; 95% ДІ 1,18-1,47). Загалом відзначалося зниження на 17% імовірності досягнення комбінованої кінцевої точки ішемічних подій (ВШ 0,83; 95% ДІ 0,77-0,89), але щодо комбінованої кінцевої точки ішемічних подій і кровотечі значимої різниці між двома препаратами не спостерігалося (ВШ 0,95; 95% ДІ 0,89-1,01).
Обговорення
У цьому дослідженні встановлено, що в пацієнтів старечого віку (≥80 років) з ІМ, які отримували терапію тикагрелором, не відзначалося нижчого ризику досягнення комбінованої кінцевої точки (смерть, повторна госпіталізація щодо ІМ або інсульту). Хоча ризик тільки інсульту чи лише ІМ був нижчим, ризик кровотечі та смерті – вищим порівняно із хворими, які отримували терапію клопідогрелем. Ці результати вказують, що чинні рекомендації слід обережно застосовувати щодо пацієнтів старечого віку; в них не можна очікувати показників ефективності та безпеки, аналогічних тим, які були наявні у клінічних дослідженнях. Однак за понад 7 років періоду випробування відбулося значне збільшення частоти призначення тикагрелору; наприкінці 2017 р. ≈¾ хворим старечого віку під час виписки зі стаціонару після ІМ був призначений саме тикагрелор, а не клопідогрель. Отже, існує потреба у проведенні рандомізованого дослідження з оцінки ефектів потужнішої антитромбоцитарної терапії в популяції осіб старечого віку.
Ефективність і безпека тикагрелору та прасугрелю в пацієнтів старечого віку були предметом вивчення в інших випробуваннях. Це питання є важливим, оскільки приблизно 35% усіх хворих з ІМ мають вік ≥75 років [18], а в пацієнтів старечого віку спостерігається багато причин, які зумовлюють підвищений ризик кровотечі [7-10, 19], що може зменшити переваги терапії, наявні в молодших хворих. У двох невеликих дослідженнях (одному рандомізованому й одному нерандомізованому) порівнювали застосування потужних інгібіторів P2Y12 з використанням клопідогрелю в осіб похилого та старечого віку. Під час випробування POPular AGE [20], що проводилося в Нідерландах, 1003 пацієнти віком >70 років із ГКС без елевації сегмента ST були рандомізовані для застосування клопідогрелю чи тикагрелору/прасугрелю (на вибір лікаря-дослідника) протягом 12 міс. У групі тикагрелору/прасугрелю більшість хворих отримували тикагрелор (95%). Ризик кровотечі був на 29% нижчим на тлі терапії клопідогрелем порівняно з терапією тикагрелором/прасугрелем (ВШ 0,71; 95% ДІ 0,54-0,94; p=0,03), тоді як лікування клопідогрелем не було менш ефективним з позиції зниження частоти досягнення комбінованої кінцевої точки, що об’єднувала ішемічні події та кровотечі. Те, що тикагрелор і прасугрель асоційовані з вищим ризиком кровотечі, не є дивним: це було очевидним при порівнянні клопідогрелю з тикагрелором у дослідженні PLATO та з прасугрелем у випробуванні TRITON-TIMI‑38. Ці результати очікувані, адже як тикагрелор, так і прасугрель характеризуються набагато швидшим і стабільним початком дії на тромбоцитарні рецептори аденозинтрифосфату P2Y12, що супроводжується негайним інгібуванням агрегації тромбоцитів. У виконаному в Німеччині нерандомізованому реєстровому дослідженні [21] ефект тикагрелору порівняно з клопідогрелем був оцінений в 1087 пацієнтів віком ≥75 років з ІМ з елевацією сегмента ST (вік 54% із них становив ≥80 років). Половина хворих отримувала тикагрелор, інша половина – клопідогрель. Підібрані за ступенем ризику аналізи продемонстрували, що порівняно з клопідогрелем тикагрелор був асоційований зі зниженням на 31% ризику досягнення комбінованих кінцевих точок ішемічних подій (ВШ 0,69; 95% ДІ 0,49-0,97) без різниці в частоті кровотечі чи смерті. Проте частота позагоспітальних кровотеч була надзвичайно низькою (0,4% у групі клопідогрелю порівняно з 1,8% – тикагрелору); це свідчить про те, що не всі епізоди кровотеч були зафіксовані. Це набагато нижче за показник річного ризику позагоспітальних кровотеч, що складає 4,8%, про який повідомлялося в інших реальних клінічних даних [22].
Наше випробування на сьогодні є найбільшим дослідженням, у якому порівнювали клінічні результати в осіб старечого віку, котрі отримували лікування тикагрелором і клопідогрелем. Кількість пацієнтів, дані про яких були зібрані протягом декількох років клінічної практики, дозволили виконати аналіз як в осіб похилого та старечого віку, так і в молодих людей. Отже, стало можливим оцінити та підтвердити перевагу тикагрелору серед осіб більш молодого віку, в яких на тлі його застосування відзначалося зниження ризику смерті на 15%, ІМ – на 18%, інсульту – на 18%, але водночас – підвищення ризику кровотеч на 32%. Ці результати отримані у хворих віком <80 років; отже, вони узгоджуються з результатами дослідження PLATO [1], медіана віку учасників якого складала 62 роки. Це також вказує, що наша методологія оцінки результатів у цих популяціях є адекватною.
Ми спробували розробити дизайн випробування, що максимально нагадував би клінічне дослідження, відібравши осіб з низьким ризиком кровотечі. За винятком віку, який є фактором ризику кровотеч, з нього були виключені пацієнти з анемією, попередньою кровотечею в анамнезі чи кровотечею, що з’явилася в період перебування в стаціонарі. Також на момент госпіталізації усі залучені до цього дослідження хворі не приймали тикагрелор або клопідогрель. Проте, незважаючи на ці жорсткі критерії відбору, ризик кровотечі був вищим серед пацієнтів, які отримували лікування тикагрелором.
Наші результати дещо відрізняються від даних дослідження PLATO, в якому не було виявлено ознак впливу віку на лікування [23]. Важливо підкреслити, що хворі, яких залучають до клінічних досліджень, дуже відрізняються від пацієнтів у реальній світовій клінічній практиці [24]. Не всі люди старечого віку є однаковими; на ризик кровотечі впливає декілька інших факторів [25], але похилий та старечий вік асоціюються з високою реактивністю тромбоцитів і підвищеним ризиком тромботичних ускладнень [26, 27].
Саме тому перед отриманням більшої кількості доказів з рандомізованих досліджень у людей похилого та старечого віку може бути доречним використання індивідуалізованішого підходу до призначення антитромбоцитарної терапії [28].
Отже, це обсерваційне дослідження свідчить, що тикагрелор слід обережно застосовувати щодо пацієнтів старечого віку (≥80 років), оскільки це може бути асоційоване з підвищеним ризиком смерті та кровотеч. Існує потреба в проведенні рандомізованого випробування з адекватною потужністю, що оцінить ефекти потужних антитромбоцитарних препаратів саме в популяції осіб старечого віку.
КЛІНІЧНІ ПЕРСПЕКТИВИ
Що нового?
◆ У цьому обсерваційному аналізі даних шведського загальнонаціонального реєстру ІМ (SWEDEHEARТ) ми встановили, що пацієнти віком ≥80 років можуть мати інше співвідношення користі та ризику при лікуванні тикагрелором порівняно з клопідогрелем після перенесеного ІМ.
◆ Зокрема, ми виявили, що хворі віком ≥80 років мали на 17% вищий ризик смерті та на 48% вищий ризик кровотечі, якщо під час виписки з лікарні після перенесеного ІМ їм призначався тикагрелор порівняно з клопідогрелем, тоді як ризик нового ІМ був нижчим на 20%, а ризик інсульту – нижчим на 28%.
Якими є клінічні наслідки?
◆ Вибір комбінації АСК з інгібітором P2Y12 (клопідогрелем або тикагрелором) слід здійснювати з обережністю в пацієнтів віком ≥80 років, які можуть мати співвідношення користі та ризику, що відрізняється від такого в осіб молодшого віку.
◆ Для підтвердження цих результатів необхідно провести рандомізоване клінічне дослідження за участю людей старечого віку.
Роботу було представлено у формі абстракту в рамках цьогорічного Конгресу Європейського товариства кардіологів (29 серпня – 1 вересня).
Стаття друкується в скороченні.
Список літератури знаходиться в редакції.
Szummer K., Montez-Rath M., Alfredsson J. et al. Comparison between ticagrelor and clopidogrel in elderly patients with an acute coronary syndrome: insights from the SWEDEHEART registry. Circulation. 2020 Sep 1. doi: 10.1161/CIRCULATIONAHA.120.050645. Online ahead of print.
Переклала з англ. Інга Боброва
Медична газета «Здоров’я України 21 сторіччя» № 22 (491), 2020 р.