15 грудня, 2015
Клиническая эффективность цефподоксима при инфекциях дыхательных путей
Внебольничные респираторные инфекции, в частности острый средний отит (ОСО), синусит и тонзиллофарингит, являются одними из наиболее частых причин обращения к врачам общей практики. На эти заболевания приходится более 50% всех консультаций в педиатрической практике и более 75% амбулаторных назначений антибиотиков (S.M. Shappert, 1992). Наиболее значимыми бактериальными возбудителями ОСО и синусита являются Streptococcus pneumoniae, Haemophilus influenzae и Moraxella catarrhalis, а тонзиллофарингита – Streptococcus pyogenes. Поскольку к началу лечения, как правило, нет микробиологического подтверждения бактериальной этиологии инфекции, эмпирическая антибиотикотерапия должна назначаться с учетом основных возбудителей. Однако рост антибиотикорезистентности бактерий, особенно S. pneumoniae к пенициллинам и макролидам, вызывает обеспокоенность по поводу эффективности традиционных препаратов выбора для эмпирической терапии респираторных инфекций. Это побудило к поиску альтернативных эффективных методов лечения. Одной из альтернатив может быть пероральный цефалоспорин III поколения цефподоксим. В этой статье рассмотрены данные о его клинической и бактериологической эффективности в лечении бактериального ОСО, синусита и тонзиллофарингита.
Острый средний отит
Быстрое эффективное лечение ОСО необходимо не только для облегчения симптомов, но и для предотвращения, насколько это возможно, долгосрочных последствий, таких как необратимое повреждение среднего уха и потеря слуха.
В настоящее время основным клинически значимым бактериальным возбудителем ОСО считается S. pneumoniae, поэтому в качестве препарата первой линии предлагается использовать амоксициллин. Однако следует принимать во внимание и возможную роль H. influenzae, особенно в случае рефрактерного к терапии отита. Есть основания полагать, что в связи с более широким применением вакцинации против пневмококковой инфекции гемофильная палочка может выходить на первый план как возбудитель ОСО. Таким образом, для достижения высокой бактериологической и клинической эффективности и предотвращения развития резистентности для лечения ОСО необходимо выбирать антибиотики, активные как в отношении S. pneumoniae (чувствительных к пенициллину штаммов и штаммов с промежуточным уровнем устойчивости), так и H. influenzae.
Результаты исследований in vitro показали, что цефподоксим – пероральный цефалоспорин с широким спектром антибактериальной активности – может быть хорошим выбором для лечения бактериального отита, а также синусита, имеющего похожую этиологию. Цефподоксим активен как в отношении чувствительных к пенициллину штаммов S. pneumoniae с минимальной подавляющей концентрацией (МПК90) от <0,06 мг/л до <0,25 мг/л, так и штаммов с умеренной устойчивостью (МПК90 1-2 мг/л). Он также показал хорошую активность в отношении H. influenzae (включая штаммы, продуцирующие β-лактмазы) с МПК90 от <0,03 мг/л до 0,13 мг/л. В исследовании, проведенном в США (B. Fulton, C.M. Perry, 2001), цефподоксим продемонстрировал in vitro более высокую активность в отношении S. pneumoniae, чем цефаклор, цефуроксим, цефпрозил, цефиксим и лоракарбеф. Кроме того, следует отметить хорошие фармакодинамические и фармакокинетические характеристики цефподоксима при ОСО, поскольку эффективная концентрация этого антибиотика в жидкости среднего уха детей достигается при применении рекомендуемых доз.
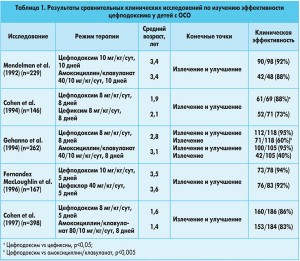
Клинические исследования подтверждают, что цефподоксим является эффективным средством для лечения бактериального отита у детей. В таблице 1 суммированы результаты пяти многоцентровых рандомизированных исследований, сравнивавших клиническую эффективность цефподоксима с амоксициллином/клавуланатом, цефиксимом и цефаклором, с участием в общей сложности 1202 детей. Продолжительность лечения цефподоксимом колебалась от 5 до 10 дней. В трех испытаниях цефподоксим оказался как минимум так же клинически эффективен, как препарат сравнения. В двух других исследованиях лечение цефподоксимом продемонстрировало значительно более высокую клиническую эффективность и частоту излечения, чем при применении цефиксима или амоксициллина/клавуланата.
Также были изучены результаты альтернативных методов оценки эффективности антибиотиков при ОСО, таких как «тест чувствительности in vivo» (исследование жидкости, полученной при тимпаноцентезе до и через несколько дней после лечения) и ретроспективный анализ случаев терапевтической неудачи. Эти методы подтвердили хорошую бактериологическую эффективность цефподоксима в отношении H. influenzae и пенициллинчувствительных штаммов S. pneumoniae (J. Klein, 1993; R. Dagan et al., 1996 и др.).
Меньшая кратность приема цефподоксима (2 раза в сутки) по сравнению с амоксициллином/клавуланатом или цефаклором (3 раза в сутки) является его дополнительным преимуществом.
Острый синусит
Лечение острого синусита затрудняется сложностью установления возбудителя. Если при ОСО отбор проб жидкости среднего уха с использованием тимпаноцентеза в некоторых странах является рутинной процедурой, то отбор проб из околоносовых пазух с помощью пункции является болезненной и редкой процедурой. Следовательно, при остром синусите предположительно бактериальной природы лечение назначается обычно эмпирически.
При выборе антибиотика следует учитывать наиболее вероятных возбудителей, региональные данные по резистентности и фармакокинетический профиль препарата.
Амоксициллин/клавуланат в настоящее время считается препаратом первой линии для терапии острого бактериального синусита. Однако рост распространенности резистентных штаммов среди основных возбудителей острого синусита указывает на необходимость поиска эффективных альтернатив.
Поскольку структура бактериальной этиологии острого синусита аналогична той, которая наблюдается при ОСО, цефподоксим, демонстрирующий хорошую активность in vitro против S. pneumoniae и H. influenzae, может быть приемлемой альтернативой для лечения этого заболевания.
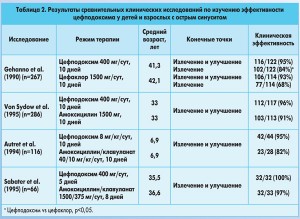
Клинические исследования показывают, что лечение цефподоксимом как минимум не уступает по клинической эффективности терапии амоксициллином или амоксициллином/клавуланатом у взрослых и детей. Частота клинического излечения у взрослых пациентов с острым синуситом была значительно выше после 10-дневного курса лечения цефподоксимом по сравнению с цефаклором (табл. 2).
Тонзиллофарингит
Самой частой бактериальной причиной острого тонзиллофарингита является β-гемолитический стрептококк группы А. Тонзиллофарингит, вызванный этим патогеном, в большинстве стран считается абсолютным показанием к назначению антибиотикотерапии, которая призвана предотвратить гнойные осложнения и отдаленные серьезные последствия, такие как ревматизм или гломерулонефрит. Но, к сожалению, только по клиническим признакам достаточно сложно установить инфекцию, вызванную пиогенным стрептококком, поскольку его признаки в целом неспецифичны и неотличимы от вирусных инфекций даже для опытных клиницистов. Поэтому для подтверждения диагноза тонзиллофарингита, вызванного β-гемолитическим стрептококком группы А, и принятия решения относительно антибиотикотерапии рекомендуется проведение антигенного экспресс-теста или микробиологического исследования.
Традиционно препаратами выбора для лечения тонзиллофарингита, вызванного β-гемолитическим стрептококком группы А, являются пероральные пенициллины (с длительностью курса 10 дней) в связи с их доказанной эффективностью, узким спектром антибактериальной активности и хорошей переносимостью. Но, несмотря на то что они эффективны у большинства пациентов с тонзиллофарингитом, частота терапевтической неудачи может достигать 10-30% (M.E. Pichichero, 1995), хотя возбудитель остается при этом восприимчивым к бета-лактамной терапии. Возможными причинами такого явления могут быть плохой комплайенс и смешанная колонизация с другими микроорганизмами, которые разрушают β-лактамазы, например S. aureus, H. influenzae или M. catarrhalis. Таким образом, более предпочтительными являются антибиотики, которые обладают высокой активностью против β-гемолитического стрептококка группы А, устойчивы к действию β-лактамаз и эффективны при более коротких схемах лечения. Макролиды являются одной из альтернатив, однако в ряде стран наблюдается повышенная распространенность устойчивости к макролидам, что следует учитывать при выборе препарата.
Цефподоксим показал высокую активность in vitro в отношении S. pyogenes с МПК90 <0,06 мг/л.
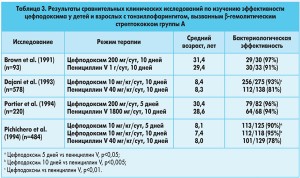
Клинические исследования продемонстрировали, что лечение цефподоксимом 200 мг в сутки в течение 5-10 дней по крайней мере столь же эффективно в эрадикации β-гемолитического стрептококка группы А, как стандартный 10-дневный курс терапии пенициллином у взрослых пациентов и детей. В педиатрических исследованиях (табл. 3) частота эрадикации после 5- или 10-дневного курса цефподоксима была значительно выше, чем при лечении пенициллином V в течение 10 дней.
Учитывая тот факт, что плохой комплайенс является важным фактором риска микробиологической неэффективности при тонзиллофарингите, вызванном β-гемолитическим стрептококком группы А, цефподоксим, курс лечения которым составляет 5-10 дней, может быть подходящим вариантом при данном заболевании.
Выводы
Цефподоксим обладает высокой активностью in vitro против бактериальных патогенов, отвечающих за развитие распространенных инфекций дыхательных путей, таких как ОСО, острый синусит и тонзиллофарингит. Клинические исследования показали, что цефподоксим по крайней мере столь же эффективен, как стандартные антибиотики первой линии для каждого из этих показаний. Как и в случае других антибиотиков широкого спектра действия, существует риск роста устойчивости микроорганизмов, если препараты используются чрезмерно или нерационально. Однако при грамотном использовании цефподоксим можно рассматривать как адекватный выбор для эмпирической терапии внебольничных бактериальных инфекций дыхательных путей, особенно в тех регионах, где наблюдается устойчивость к традиционным противомикробным препаратам.
Подготовлено по материалам статьи Cohen R. Clinical efficacy of cefpodoxime in respiratory tract infection (Journal of Antimicrobial Chemotherapy).
Список литературы находится в редакции.
Перевод с англ. Натальи Мищенко


