14 травня, 2021
Рак стравоходу: сучасний погляд на проблему
 4 лютого позначений як Всесвітній день боротьби проти раку. У зв’язку з цим представник Всесвітньої організації охорони здоров’я (ВООЗ) Андре Ільбаві в цифрах охарактеризував стан цієї актуальної проблеми людства. Так, за прогнозом, на рак рано чи пізно захворіває кожен 5-й житель світу. Від онкопатології помирає кожен 8-й чоловік і кожна 11-та жінка. 70% випадків смерті від злоякісних новоутворень припадають на країни з низьким і середнім рівнем доходу. Рак став другою провідною причиною смерті в світі. (Перше місце, за даними ВООЗ, посідають серцево-судинні захворювання.) Відзначено, що, по суті, рак – це вже проблема кожної сім’ї. На сьогодні спостерігається погіршення онкологічної ситуації на тлі пандемії COVID‑19, що зумовлено спрямуванням усіх ресурсів системи охорони здоров’я на боротьбу з вірусною інфекцією. При цьому у хворих на рак підвищений ризик тяжкого перебігу COVID‑19 та смерті від нього [1].
4 лютого позначений як Всесвітній день боротьби проти раку. У зв’язку з цим представник Всесвітньої організації охорони здоров’я (ВООЗ) Андре Ільбаві в цифрах охарактеризував стан цієї актуальної проблеми людства. Так, за прогнозом, на рак рано чи пізно захворіває кожен 5-й житель світу. Від онкопатології помирає кожен 8-й чоловік і кожна 11-та жінка. 70% випадків смерті від злоякісних новоутворень припадають на країни з низьким і середнім рівнем доходу. Рак став другою провідною причиною смерті в світі. (Перше місце, за даними ВООЗ, посідають серцево-судинні захворювання.) Відзначено, що, по суті, рак – це вже проблема кожної сім’ї. На сьогодні спостерігається погіршення онкологічної ситуації на тлі пандемії COVID‑19, що зумовлено спрямуванням усіх ресурсів системи охорони здоров’я на боротьбу з вірусною інфекцією. При цьому у хворих на рак підвищений ризик тяжкого перебігу COVID‑19 та смерті від нього [1].
Серед різних онкологічних захворювань дещо відокремлено перебуває рак стравоходу. З одного боку, ця патологія не посідає перші місця у структурі захворюваності та смертності (це відповідно сьоме та шосте місця серед усіх неопластичних процесів). З іншого – це один з агресивних видів раку, що призводить до смерті, зазвичай, протягом одного року після виявлення. За статистикою, виживаність пацієнтів зі злоякісним ураженням стравоходу протягом п’яти років становить менше 25% [2]. Це зумовлено майже завжди запізнілою діагностикою, оскільки на ранніх стадіях рак стравоходу, як правило, має безсимптомний перебіг чи неспецифічні симптоми диспепсії.
Виділяють два основних гістологічних підтипи раку цієї локалізації: плоскоклітинний рак стравоходу (ПКРС) та аденокарцинома стравоходу (АКС). Слід зазначити, що у пацієнтів з будь-яким із цих гістологічних підтипів має місце поганий прогноз. Так, за даними одного з останніх досліджень, проведених у США, у 23 804 (42%) пацієнтів АКС була діагностована як слабо диференційована 3 ступеня, а у 13 919 пацієнтів ПКРС був ідентифікований як помірно диференційований 2 ступеня (39,5%). Найпоширенішою стадією була IV для АКС (36,9%) і ПКРС (26,8%) [3].
Клінічні особливості перебігу раку стравоходу пов’язані з анатомічною здатністю органа до розтягування. Тому пацієнт починає відчувати дисфагію лише коли діаметр просвіту стравоходу скорочується менше 14 мм. Спочатку утруднюється ковтання густої їжі, потім – напіврідкої, а врешті-решт – рідини та слини. Іноді може виникати біль у грудній клітці з іррадіацією в спину. Таке неухильне прогресування дисфагії вказує на прогресування злоякісного новоутворення. Через те пацієнти звертаються до лікаря лише за значного поширення пухлини. Вважають, що в середньому тривалість анамнезу хвороби (від перших проявів до звернення за медичною допомогою) становить від 2 до 4 міс.
Надалі в клінічній картині майже завжди спостерігають схуднення пацієнта, навіть при збереженні хорошого апетиту. Стискання поворотного гортанного нерва може призводити до парезу голосових зв’язок і захриплості голосу, а також гикавки чи паралічу діафрагми. Плевральний випіт злоякісної природи і метастази в легенях викликають задишку.
Зміни тканини пухлинного вузла, що виступає у просвіт стравоходу, можуть супроводжуватися ковтанням з болем (одинофагією), блюванням з домішкою крові, а також меленою, розвитком залізодефіцитної анемії, аспірацією, кашлем. Формування фістул між стравоходом і трахеобронхіальним деревом спричиняє розвиток пневмонії, абсцесу легені. Можуть проявлятися ознаки стиснення верхньої порожнистої вени, асцит пухлинного генезу, біль у кістках. Для раку стравоходу характерне лімфогенне поширення через внутрішні югулярні, шийні, надключичні, медіастинальні, черевні лімфатичні вузли. Метастазування, як правило, відбувається в легені, печінку, іноді – в більш віддалені ділянки, зокрема, в кістки, серце, головний мозок, надниркові залози, нирки, очеревину [4].
Фахівці підкреслюють, що рання діагностика відіграє ключову роль у лікуванні раку стравоходу. Через відсутність якісної діагностики та лікування захворювання на ранніх стадіях у країнах із низьким і середнім рівнем доходу смертність від раку значно вища, ніж в економічно розвинутих країнах.
Підвищити ефективність виявлення захворювання дозволяє впровадження в практику сучасних ендоскопічних технологій, таких як NBI-ендоскопія (narrow band imaging – зображення у вузькому спектрі світла) [5] або конфокальна лазерна ендомікроскопія [6]. З метою неінвазивної діагностики ранньої стадії раку стравоходу вивчають біомаркери крові [7]. Водночас основним методом діагностики пухлини залишається морфологічний.
2000 р. була опублікована стаття про класифікацію шлунково-кишкових епітеліальних новоутворень за висновками семінару, проведеного в 1998 р. у Відні (Австрія) [8]. Існують певні відмінності у поглядах західноєвропейських і японських патоморфологів на гістологічні критерії ранньої стадії раку. Різні підходи призводять до відмінностей у виявленні новоутворень і веденні пацієнтів. Однією з тем в цьому обговоренні був ПКРС. На наступних семінарах польські, німецькі та японські патоморфологи оцінювали точність діагнозу ПКРС і з’ясовували значимість відмінностей з наслідками для клінічної практики [9]. Висловлено думку, що «західний» підхід може призводити до дефектів ранньої діагностики з невиправданим відстроченням початку лікування пацієнтів з ПКРС. Водночас використання японських критеріїв у країнах Європи, де поширеність раку стравоходу нижча, ніж у Японії, європейські фахівці розцінюють як шлях до гіпердіагностики і необґрунтованого початку лікування.
З моменту обговорення гістологічних критеріїв ранньої стадії ПКРС минуло понад 20 років, але хвороба не здається. Тому важливо зрозуміти, чи пов’язано це з інертністю західноєвропейських фахівців щодо прийняття більш жорстких установок морфологічної діагностики раку стравоходу. Розуміння реальних поглядів в аспекті морфологічних норм має принципове значення для діагностики цього захворювання.
Відома низка досліджень, результати яких свідчать про те, що можна досягти 80% виживаності пацієнтів, якщо виявляти рак стравоходу на ранній стадії [10]. Водночас звичний посил до значення часу встановлення діагнозу має неоднозначне трактування. Стійкий зв’язок між коротшим часом до верифікації діагнозу й успішним результатом лікування при таких злоякісних новоутвореннях ще не доведений. Так, у ретроспективному когортному дослідженні за участю 3613 пацієнтів із симптомами раку стравоходу з’ясовано, що при довшому часі до встановлення діагноз не був пов’язаний із можливістю радикального видалення пухлини (відношення шансів 0,997; 95% довірчий інтервал – ДI – 0,994-1,001) та п’ятирічною загальною виживаністю (відношення ризиків – ВР – 0,999; 95% ДІ 0,997-1,001) або п’ятирічною виживаністю без ознак захворювання (ВР 0,999; 95% ДІ 0,998-1,001) [11]. Можливо, це пов’язано із дисфагією, на тлі якої протягом кількох місяців розвивається кахексія, і хворі зазвичай помирають від аліментарного виснаження. Іншою причиною смерті від раку стравоходу є широке та раннє метастазування: у середостіння, навколостравохідний простір, у верхній відділ малого чепця [4].
Чоловіки хворіють на рак стравоходу частіше, ніж жінки, у співвідношенні 5-10:1 (8,6:1 в Україні); пік захворюваності припадає на 50-60 років, хворі віком понад 70 років становлять 40%. Епідеміологія раку стравоходу означена географічною поширеністю за гістологічними формами. З двох його основних гістологічних типів АКС більш поширена у «західних» країнах, ПКРС частіше спостерігається у «східних» популяціях. Вважають, що за цим можуть стояти різні етіологічні чинники та генетичні детермінанти [12, 13]. Утім загальновизнано, що незалежно від гістологічного типу раку стравоходу його скринінг неефективний, патологія діагностується, зазвичай, на пізній стадії та належить до найбільш агресивних за перебігом злоякісних новоутворень людини з несприятливим результатом лікування.
За результатами проведеного нами аналізу матеріалів Національного канцер-реєстру України встановлено, що за 2014-2019 рр. загальноукраїнський показник захворюваності на рак стравоходу коливався від мінімального 4,2 до максимального 4,9, у середньому становлячи 4,5 на 100 тис. населення (рис. 1). Захворюваність на рак стравоходу та смертність від нього в різних регіонах України у 2019 р. представлено на рисунку 2. Загалом отримані нами дані збігаються з основними тенденціями, які характеризують особливості перебігу раку стравоходу. Зокрема, захворюваність, смертність, гендерний і віковий розподіл повністю відповідають таким оцінки тягаря раку стравоходу в Європі [14]. Істотний внесок в онкологічну захворюваність зумовлений збільшенням кількості населення України старших вікових груп, ризик захворювання яких у 5-7 разів перевищує такий в осіб молодшого віку.
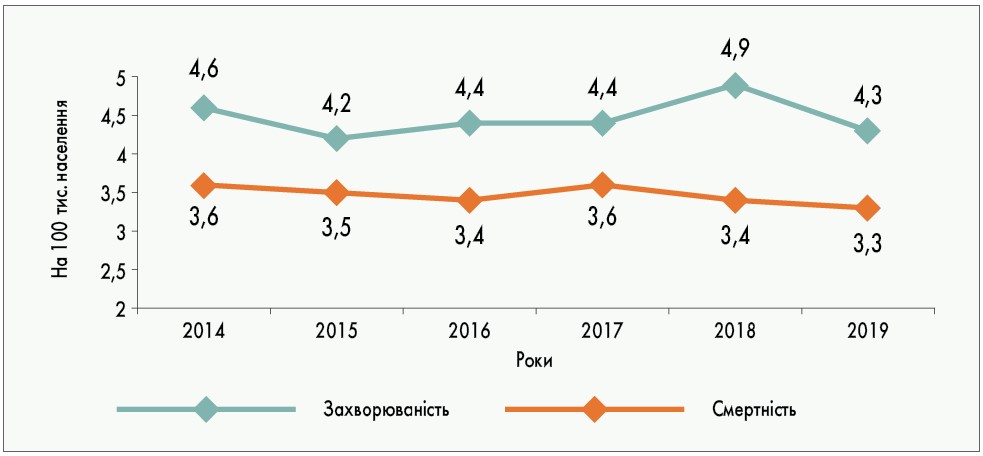 Рис. 1. Динаміка захворюваності та смертності від раку стравоходу в Україні
Рис. 1. Динаміка захворюваності та смертності від раку стравоходу в Україні
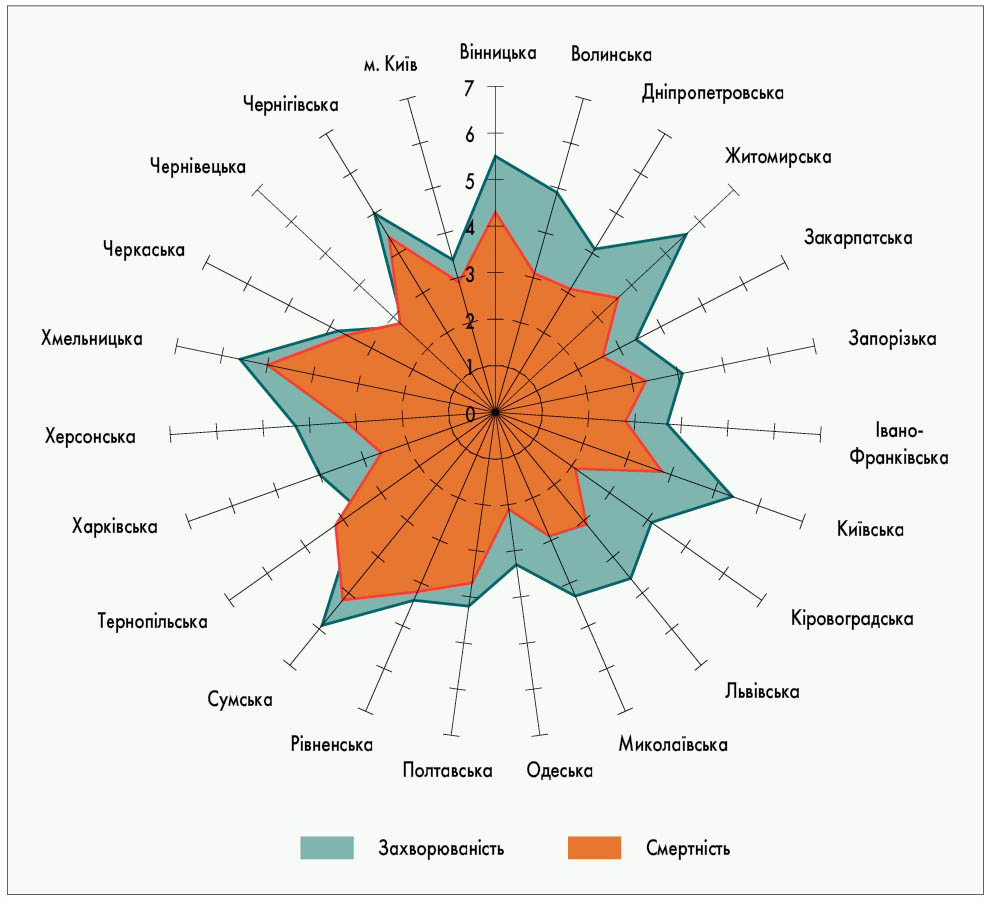 Рис. 2. Захворюваність на рак стравоходу та смертність від нього у різних регіонах України у 2019 р.
Рис. 2. Захворюваність на рак стравоходу та смертність від нього у різних регіонах України у 2019 р.
В основі структурно-морфологічних змін слизової оболонки стравоходу лежить гастроезофагеальна рефлюксна хвороба (ГЕРХ), тому в профілактичному напрямі вирішення проблеми раку стравоходу насамперед слід приділяти увагу медикаментозному лікуванню ГЕРХ і стравоходу Барретта, зокрема, за допомогою інгібіторів протонної помпи (ІПП). Оцінка ризиків, що пов’язані з тривалим застосуванням ІПП при цих станах, висвітлена у рекомендаціях Американської гастроентерологічної асоціації на підставі думки експертів і відповідних публікацій з PubMed, Embase і Кокранівської бібліотеки (до липня 2016 р.) [15].
Необхідно звернути увагу на такі практичні поради з цих рекомендацій. Пацієнти зі стравоходом Барретта та симптоматичною ГЕРХ тривалий час мають приймати ІПП. Пацієнтам з безсимптомним перебігом стравоходу Барретта слід розглянути можливість тривалого застосування ІПП. Дозу ІПП при довгих курсах треба періодично переглядати, щоб можна було призначити найнижчу ефективну дозу. Пацієнти, що приймають ІПП протягом тривалого часу, не повинні регулярно використовувати пробіотики для запобігання інфекції; підвищувати споживання кальцію, вітаміну B12 або магнію понад рекомендовану добову норму; перевіряти або контролювати мінеральну щільність кісток, рівень креатиніну сироватки, магнію або вітаміну B12, якщо в них немає додаткових показань для цього. Крім того, збільшується кількість досліджень, що підтверджують можливості ІПП як хіміосенсибілізаторів для лікування та профілактики раку різної локалізації [16]. Такі висновки базуються на тому, що всі види раку мають кисле мікросередовище, яке є основною причиною хіміорезистентності, оскільки кисле мікросередовище призводить до протонування лікарських засобів, блокуючи їх за межами ракових клітин. ІПП забезпечують буферизацію мікросередовища. Це підвищує ефективність лікарських препаратів та дозволяє вбивати ракові клітини шляхом підвищення внутрішньоклітинного закислення. Отже, ІПП чекає нове майбутнє.
Необхідно звернути увагу на зміну можливостей лікування пацієнтів із раком стравоходу. Кілька років тому як хірургічну операцію розглядали переважно часткову езофагектомію, яку важко переносять пацієнти. Сучасні ендоскопічні операції дозволяють зберігати стравохід, забезпечуючи оздоровлення його слизової оболонки шляхом локальної резекції. Фіксація клітинних і структурних порушень слизової оболонки стравоходу незалежно від наявності стромальної інвазії вимагає активного втручання з боку лікарів, що значно підвищує шанси пацієнтів на збереження і збільшення тривалості їх життя.
Свого часу було висловлено пропозицію про необхідність проведення консенсусної зустрічі між японськими і західноєвропейськими патоморфологами, а також ендоскопістами для розроблення загального підходу з номенклатури і тактики ведення таких пацієнтів [17]. Накопичено достатній досвід для визначення чітких позицій з низки питань, що стосуються ранньої діагностики раку стравоходу. Такий консенсус необхідний для забезпечення своєчасного лікування та збільшення виживаності хворих на рак стравоходу. Сьогодні зможемо зберегти життя багатьом нашим пацієнтам, якщо налагодимо тісну співпрацю між клініцистами, ендоскопістами та патоморфологами.
Список літератури знаходиться в редакції.
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 2 (69) 2021 р.



