15 червня, 2021
Потенциал инулина в терапевтической практике
Значение микрофлоры кишечника в поддержании здоровья человека и возможность ее нормализации с помощью полезных бактерий были впервые отмечены И. И. Мечниковым более века назад. В последние годы терапевтические подходы, направленные на поддержание и восстановление микробиоты (применение пробиотиков, пребиотиков, синбиотиков и метабиотиков), вызывают все больший интерес как исследователей, так и практических врачей (табл. 1).
 Термин «пребиотики» был впервые применен G. Gibson (1995). В основе концепции пребиотик – неперевариваемый пищевой ингредиент, способный улучшать состояние здоровья человека посредством избирательной стимуляции роста и/или активности одного или ограниченного количества видов бактерий в толстой кишке [2]. С этого времени было предложено много вариантов определений. Так, M. Roberfroid (2007) дополнил определение следующим образом: пребиотики – избирательно ферментируемые кишечными микроорганизмами ингредиенты пищи, специфически меняющие состав и/или активность микрофлоры, что ведет к улучшению самочувствия и здоровья человека [3]. В августе 2017 года экспертами Международной научной ассоциации пробиотиков и пребиотиков (International Scientific Association for Probiotics and Prebiotics) предложено новое определение термина: пребиотик – субстрат, который селективно используется микроорганизмами хозяина, что обеспечивает пользу для его здоровья [4].
Термин «пребиотики» был впервые применен G. Gibson (1995). В основе концепции пребиотик – неперевариваемый пищевой ингредиент, способный улучшать состояние здоровья человека посредством избирательной стимуляции роста и/или активности одного или ограниченного количества видов бактерий в толстой кишке [2]. С этого времени было предложено много вариантов определений. Так, M. Roberfroid (2007) дополнил определение следующим образом: пребиотики – избирательно ферментируемые кишечными микроорганизмами ингредиенты пищи, специфически меняющие состав и/или активность микрофлоры, что ведет к улучшению самочувствия и здоровья человека [3]. В августе 2017 года экспертами Международной научной ассоциации пробиотиков и пребиотиков (International Scientific Association for Probiotics and Prebiotics) предложено новое определение термина: пребиотик – субстрат, который селективно используется микроорганизмами хозяина, что обеспечивает пользу для его здоровья [4].
К пребиотикам предъявляются достаточно строгие требования: они не должны подвергаться гидролизу пищеварительными ферментами человека, а также абсорбироваться в верхних отделах пищеварительного тракта, при этом должны селективно стимулировать один вид или определенную группу микроорганизмов, резидентных для толстой кишки.
Подавляющее большинство пребиотических веществ – это углеводы, которые не перевариваются пищеварительными ферментами человека, но могут служить питательным субстратом для полезных бактерий, обитающих в толстой кишке. Некоторые из них (например, олигосахариды) можно найти в натуральных продуктах. Примерами пребиотиков являются инулин, фруктоолигосахариды, галактоолигосахариды, олигосахариды сои и сложные полисахариды, которые состоят из пищевых волокон. Наиболее изученные в мире пребиотические волокна – инулин и олигофруктоза.
Открытие инулина связывают с именем немецкого фармаколога, выделившего в 1800-е углевод растений из корней девясила (Inula helenium), получивший название «инулин». Инулин уже давно используется в качестве подсластителя для пациентов с сахарным диабетом (СД).
Инулин – это естественный запасной углевод, который встречается в более чем 30 000 растений. В отличие от крахмала (широко распространенного резервного полисахарида растений) инулин представляет собой полимер D-фруктозы, содержащий до 27-35 остатков фруктозы в фуранозной форме и один остаток глюкозы. Основными источниками инулина являются клубни топинамбура и георгины, корни цикория, одуванчика лекарственного, артишока и др. Так, содержание инулина в топинамбуре и цикории составляет около 70%, в клубнях георгины, корнях одуванчика, пастернаке, луке-порее – 15%, репчатом луке – 2-6%, спарже – 10-15%, девясиле – 9-12%, банане – 0,58-1,09%, пшеничной и рисовой муке – 1-4% [5]. В растениях инулин находится в виде смеси олиго- и полисахаридов фруктозы в диапазоне от 2 до 100 ед., зависит от вида и возраста растений, а также метода экстракции [6].
Физико-химические и функциональные свойства инулина связаны со степенью полимеризации (DP), а также наличием разветвлений в структуре. Так, существуют инулины низкомолекулярные (средняя DP составляет 10 и ниже) и высокомолекулярные (средняя DP – 20 и выше до 35). Свойства низкомолекулярных и высокомолекулярных инулинов существенно различаются. Низкомолекулярные инулины слегка сладковаты и хорошо растворяются в холодной воде, а высокомолекулярные имеют нейтральный вкус и с трудом растворяются даже при кипячении. Общеизвестным является такой факт: чем выше DP, тем выше биологическая активность инулина [3].
Механизмы взаимодействия пребиотиков с организмом хозяина представлены в табл. 2.
Механизмы реализации благоприятных эффектов инулина и других пребиотиков на организм хозяина изучаются уже более трех десятилетий; эти исследования продолжаются. Выделяют прямые и непрямые эффекты инулина. Прямое влияние – это непосредственные эффекты потребления пребиотика инулина на здоровье хозяина. Так, исследования in vitro и in vivo продемонстрировали устойчивость инулина к соляной кислоте желудочного сока и пищеварительным ферментам желудочно-кишечного тракта человека [7]. Так, β-связь этих молекул не расщепляется α-глюкозидазами кишечника, в связи с чем они не перевариваются и достигают толстой кишки, где утилизируются микроорганизмами (бактериальная ферментация инулина и стимулирующее влияние на рост бифидофлоры) [8]. Так, в экспериментальном исследовании [9] отмечено, что диета, обогащенная инулином или олигофруктозой, способствует увеличению микробной массы в толстой кишке, снижению рН кишечного содержимого, увеличению числа молочнокислых бактерий и снижению количества колиформных микроорганизмов. В другом исследовании установлено, что пребиотический индекс инулина (т. е. прирост числа бифидобактерий в единице объема содержимого толстой кишки (КОЕ/г) на единицу (г) принятого вещества) составляет 4,00±0,82×108 [8].
В отличие от других пребиотиков, например лактулозы, снижающей образование бутирата и пропионата в толстой кишке в пользу ацетата, инулин является источником эндогенной масляной кислоты, выделяющейся при ферментировании инулина бутиратпродуцирующими бактериями. Так, в образцах фекалий, полученных от лиц, употреблявших в пищу инулин, отмечалось повышенное содержание важнейшей бутиратпродуцирующей бактерии Faecalibacterium prausnitzii [10]. Установлено, что введение инулина способно снизить воспаление кишечника [11], а также предотвратить образование предраковых и опухолевых очагов в толстой кишке путем стимуляции апоптоза колоноцитов [12].
Отмечено, что использование инулина в качестве заменителя жира и сахара приводит к снижению калорийности потребляемой пищи [13]. Инулин также известен своей антиоксидантной активностью [14] и противовоспалительным (защитным) действием. По данным исследований, также было установлено, что инулин снижает риск возникновения остеопороза (за счет повышения всасывания кальция в толстой кишке); снижает вероятность развития СД [8].
Применение в клинической медицине
Кишечный микробиоценоз представляет собой высокоорганизованную систему, реагирующую качественными и количественными сдвигами на различные условия жизнедеятельности, здоровья и болезни. Нормофлора человека выполняет различные жизненно важные функции, в т. ч. обеспечивает процессы переваривания и всасывания, синтез витаминов, аминокислот, ферментов, оказывает подавляющее действие на патогенную микрофлору, обеспечивает иммунорегулирующую функцию и антиинфекционную защиту, принимает участие в синтезе иммуноглобулинов и в морфогенезе иммунной системы [15]. Микрофлора толстого кишечника считается биогенным фактором, в значительной степени определяющим состояние организма [16].
Данные биомедицинских исследований позволили установить связь дисбиотических нарушений микробиоценоза желудочно-кишечного тракта с широким спектром заболеваний. В исследовании Ю. А. Слащовой [17] показано, что развитие экспериментального антибиотик-ассоциированного дисбиоза в организме животных приводит к нарушению гомеостаза в толстой кишке, которое выражается в изменении состава микробиоты и смещении прооксидантно-антиоксидантного баланса колоноцитов.
Продемонстрировано, что негативные изменения микробиоты кишечника посредством снижения детоксикационной функции индигенной флоры ведут к увеличению функциональной нагрузки на печень. Получены данные о влиянии алкоголя на состав микробиоты кишечника [18]. Установлена решающая роль метаболита этанола (ацетальдегида) в нарушении барьерной функции кишечника [19].
В исследовании Л. П. Кнышовой [20] изучены изменения кишечной микробиоты при экспериментальной хронической алкоголизации. Отмечено, что хроническая алкогольная интоксикация приводит к изменению качественного и количественного состава биоценоза кишечника, характеризующегося смещением равновесия в сторону патогенной флоры, сокращением сахаролитической микробиоты – Lactobacterium spp., Bifidobacterium spp. на 2-4 порядка, увеличением протеолитической микрофлоры ‒ Enteroccocus spp., Staphylococcus spp. на 3-4 порядка (с увеличением активности аэробов на высоте алкогольобусловленной интоксикации). Обнаружено появление типичных представителей дисбиотических процессов – Candida spp. и Proteus spp. Этому соответствовало увеличение экспрессии провоспалительных цитокинов (интерлейкина (ИЛ)-1β и ИЛ‑6 в плазме крови более чем в 2 раза, незначительное повышение фактора некроза опухоли).
Пребиотики действуют путем модуляции профиля микробиоты кишечника и служат в качестве субстрата для производства метаболически активных веществ (в частности короткоцепочечных жирных кислот). Известно, что по мере нормализации моторики нормализуется и микрофлора кишечника, с другой стороны, восстановление активности и количества микрофлоры может способствовать улучшению моторики [21].
В исследовании Т. Д. Звягинцевой и соавт. [22] изучена терапевтическая эффективность инулина (по 1 саше (6 г) 2 р/день перед приемом пищи) у больных с синдромом раздраженного кишечника с запорами. Длительность исследования составила 3-4 нед. Установлено, что лечение эффективно уменьшает частоту и интенсивность клинических симптомов, улучшает транзит кишечного содержимого, повышает частоту стула и смягчает его консистенцию, улучшает качество жизни пациентов с запорами (наряду с хорошей переносимостью терапии).
Продемонстрировано, что дисгомеостаз магния может оказывать влияние на сосудистый тонус, эндотелиальную функцию, липидный обмен, агрегацию тромбоцитов, систему коагуляции и проводящую систему сердца, что обуславливает актуальность данной проблемы для практического здравоохранения [23]. Особенно это важно на начальных стадиях заболевания, поскольку позволяет предупредить или замедлить появление сосудистых осложнений. Отмечено, что инулин улучшает усвояемость магния, способствует снижению артериального давления у пациентов с гиперлипидемией [23].
Влияние на липидный обмен
В исследовании in vivo [19] установлено, что при переходе на диету с большим количеством жира разнообразие кишечной микробиоты существенно уменьшается, в частности, уменьшается количество представителей филума Bacteroidetes, а количество представителей филума Firmicutes возрастает, что ассоциируется с увеличением уровней холестерина липопротеинов низкой плотности (ХС ЛПНП), триглицеридов и снижением холестерина липопротеинов высокой плотности (ХС ЛПВП). Добавление к питанию Lactobacillus rhamnosus приводило к восстановлению уровней бактерий филумов Bacteroidetes и Firmicutes. Продемонстрирована прямая ассоциация между уровнем Ruminococcus (Clostridium кластер XIVa) и уровнем триглицеридов в крови [24], а также между числом бактерий Dorea и общим холестерином (ОХС) и ХС ЛПНП, количеством Enterococcus и уровнем ХС ЛПВП [19]. Установлено, что количество Bifidobacterium longum прямо коррелирует с уровнем ХС ЛПВП [25]. Предполагается, что некоторые молочнокислые бактерии снижают всасывание холестерина в кишечнике [26].
Wu и соавт. [27] провели систематический обзор 9 исследований по оценке влияния инулиноподобных фруктанов на показатели липидного обмена в крови. Продемонстрировано, что у пациентов с гиперлипидемией употребление с пищей инулиноподобных фруктанов до 17 г/сут приводило к существенному улучшению липидного профиля в крови, что, соответственно, способствует снижению сердечно-сосудистого риска. Отмечено, что улучшение липидного профиля при добавлении инсулиноподобных фруктанов во многом зависело от вида диеты, на фоне которой проводилась терапия, и патофизиологического состояния пациентов.
Продемонстрировано, что фруктаны инулиноподобного типа улучшают липидный профиль за счет ряда механизмов [28]:
- снижение экспрессии генов печеночных ферментов, ответственных за синтез липидов de novo;
- повышение активности фермента липопротеинлипазы в мышцах;
- увеличение продукции короткоцепочечных жирных кислот;
- изменение продукции полиаминов, увеличивающих синтез сатиогенного пептида;
- изменение уровня глюкозы в крови и инсулинемии;
- увеличение фекальной экскреции солей желчных кислот и холестерина;
- увеличение популяции Bifidobacterium.
Ожирение и СД
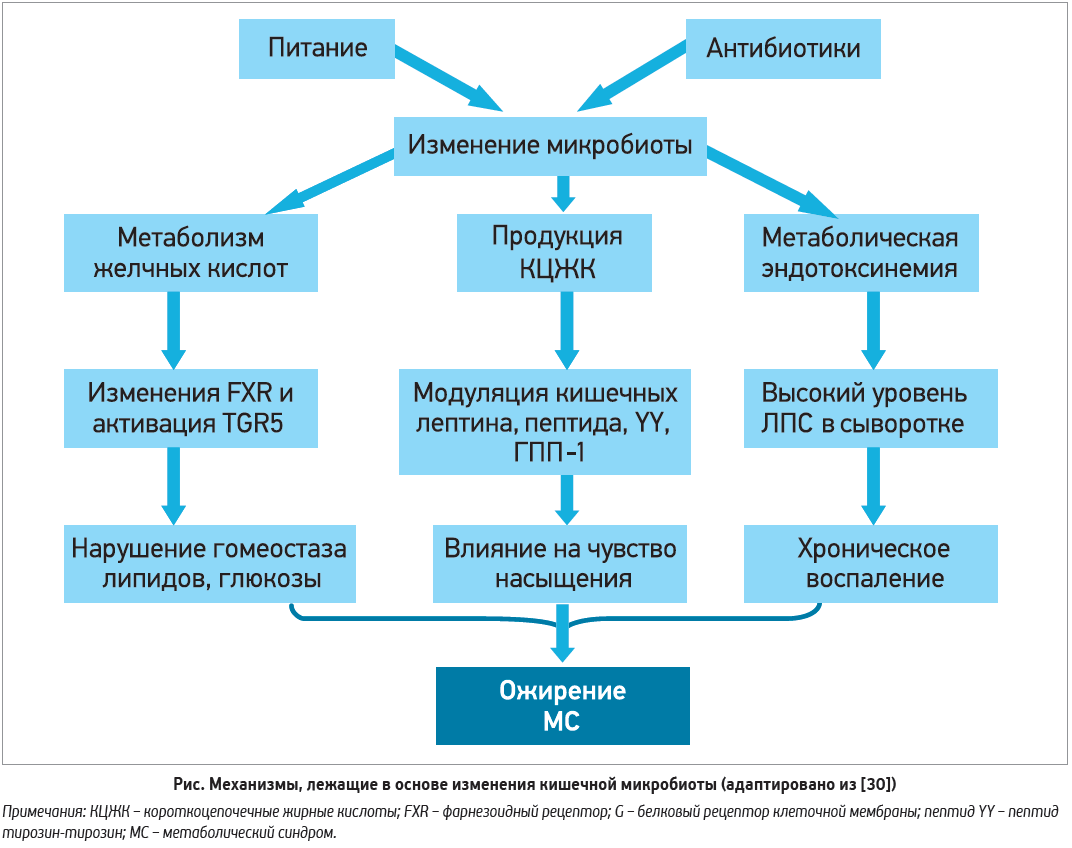
В развитии метаболических нарушений важную роль играет системное воспаление (рис.) [29]. Установлено, что при ожирении увеличивается содержание липополисахарида (ЛПС), являющегося составной частью клеточной стенки грамотрицательных бактерий и мощным фактором вирулентности. ЛПС из клеток толстого кишечника транспортируется в кровеносное русло с помощью хиломикронов или через межклеточные промежутки в стенке кишечника; путем образования комплекса CD14 с Toll-подобным рецептором‑4 макрофагов и клеток эндотелия вызывает выброс провоспалительных цитокинов: ИЛ‑1, ИЛ‑6, фактора некроза опухоли [30]. Это ведет к развитию хронического системного воспаления, снижению чувствительности к инсулину, увеличению липогенеза в печени, активации воспаления в жировой ткани [31].
Существует ряд механизмов, объединяющих ожирение и эндотоксемию. Один из них ассоциируется со способностью диеты с высоким содержанием жиров вызывать гибель грамотрицательной флоры и высвобождением большого количества ЛПС. Другой механизм связывают со способностью избыточного потребления жиров повышать содержание хиломикронов в кишечнике, что способствует увеличению ЛПС [31].
Одной из главных функций кишечной микрофлоры является расщепление пищевых волокон, конечным продуктом ферментации которых являются короткоцепочечные жирные кислоты – уксусная, пропионовая, масляная. Короткоцепочечные жирные кислоты являются субстратами для многих тканей: участвуют в глюконеогенезе в печени, служат основным источником энергии для колоноцитов, являются лигандами G-протеинсвязывающих рецепторов (GPR‑41, GPR‑43, GPR109А) [31]. Установлено, что при ожирении наблюдается уменьшение числа бутиратпродуцирующих бактерий, содержания короткоцепочечных жирных кислот, лакто- и бифидобактерий.
Микрофлора кишечника активно участвует в метаболизме желчных кислот путем преобразования части первичных желчных кислот, поступивших в кишечник с желчью, во вторичные желчные кислоты, которые активируют секрецию глюкагоноподобного пептида‑1 (ГПП‑1), действуя на мембранные рецепторы желчных кислот (TGR‑5-рецепторы), что способствует увеличению толерантности к глюкозе, возрастанию потребления энергии бурой жировой тканью и скелетными мышцами, предотвращая развитие инсулинорезистентности и ожирения [32].
В нескольких исследованиях было оценено влияние пребиотиков на состав кишечной микрофлоры. В эксперименте добавление к питанию инулина приводило к увеличению Bifidobacterium и снижению C. perfringens [33]. В исследовании на мышах с индуцированным ожирением прием пребиотика привел к уменьшению Firmicutes и увеличению Bacteroidetes, а также к увеличению A. muciniphila, чья популяция отрицательно коррелирует с ожирением. Исследования у человека также показали стимулирующий эффект пребиотиков на рост Bifidobacterium, Lactobacillus и F. prausnitzii [34]. Путем увеличения и изменения состава кишечной микрофлоры пребиотики оказывают множество положительных эффектов, таких как стимуляция роста бифидо- и лактобактерий, снижение рН содержимого кишечника, регуляция физиологической деятельности кишечника, продукция КЦЖК, угнетение образования фактора некроза опухоли, ИЛ‑8, лейкотриенов [35].
В исследовании Ю. В. Козыренко [36], включавшем пациентов с СД 2 типа, установлены нарушения микробиоценоза кишечника со снижением количества бифидо- и лактобактерий, типичных Е. coli, увеличением количества дрожжеподобных грибов рода Candida, проявляющиеся симптомами кишечной диспепсии (чаще в виде запоров, диареи или смены запоров диареей, астеноневротическим синдромом и симптомами гиповитаминоза). Автором показано, что 4-недельное применение препарата на основе инулина в комплексной терапии обострения хронического панкреатита у больных СД 2 типа с выявленным дисбиозом кишечника приводило к купированию клинических симптомов у большего количества пациентов и восстановлению экосистемы кишечника у 93% пациентов (в группе плацебо – у 73%). Отмечено, что добавление препарата на основе инулина к комплексной терапии больных СД 2 типа приводило к существенному гипохолестеринемическому эффекту (снижению уровня ОХС на 11% и триглицеридов на 21%) и положительному влиянию на углеводный обмен (снижение показателей постпрандиальной глюкозы крови на 12,5%, HbA1c – на 8%).
Выводы
Таким образом, влияние на микробиоту кишечника является перспективным направлением в лечении и профилактике различных заболеваний. В этом направлении перспективными препаратами, влияющими на микробиоту, являются пребиотики. К наиболее изученным пребиотикам относится инулин. Продолжающиеся исследования пребиотиков постоянно расширяют показания к их применению. Результаты исследований демонстрируют, что добавление инулина к традиционной терапии ряда заболеваний желудочно-кишечного тракта, МС и др. может способствовать повышению эффективности терапевтических схем, а также позволяет с высокой эффективностью проводить коррекцию и профилактику нарушений микробиоценоза.
Список литературы находится в редакции.